Hans-Jörg Assion, Dortmund, Thomas Aubel, Essen, Göran Hajak, Bamberg, Stephan Heres, München, René Hurlemann, Oldenburg, Kai-Uwe Kühn, Bonn, Karolina Leopold, Berlin, Dan Rujescu, Wien, Nenad Vasic, Göppingen, Thomas Wobrock, Groß-Umstadt, und Stefan Leucht, München
Antipsychotisch wirksame Substanzen werden in allen Phasen der Therapie von Patienten mit Schizophrenie sowohl in der Akut- als auch in der Erhaltungstherapie und zur Rezidivprophylaxe erfolgreich eingesetzt [5, 17, 30]. Allerdings treten trotz Therapie bei den meisten Betroffenen Rückfälle der Erkrankung auf [38]. Als ein wichtiger Grund für Rezidive gilt die mangelnde Adhärenz der Patienten, zu der komplexe und oft nicht auf die Patienten abgestimmte Therapieregimes, mangelnde Krankheitseinsicht, ungenügende soziale Unterstützung, Nebenwirkungen und schlechte Symptomkontrolle beitragen [8, 34].
Vergleichsstudien unterschiedlichen Designs inklusive prospektiver randomisierter kontrollierter Studien (RCT) konnten im Hinblick auf die Erhaltungstherapie und Rezidivprophylaxe mindestens eine klinische Gleichwertigkeit von oralen und Depotformulierungen nachweisen [20, 21]. Die Ergebnisse einer neueren Studie, in der Behandlungszentren und nicht Patienten randomisiert worden waren, zeigen sogar, dass mit Depotantipsychotika behandelte Patienten später hospitalisiert werden müssen als herkömmlich therapierte Patienten [19]. Weitere Vorteile der Depottherapie betreffen unter anderem die Reduktion der täglichen Auseinandersetzung mit der Medikation und die Vermeidung von Einnahmelücken, nicht zuletzt in der kritischen Phase, wenn Patienten frühzeitig aus der stationären in die ambulante Behandlung entlassen werden. Doch trotz vergleichbarer Wirksamkeit mit oralen Medikamenten bieten Ärzte in Deutschland nur circa einem Drittel der geeigneten Patienten eine Therapie mit Depotantipsychotika an [15]. Zudem lehnen die Patienten selbst nicht selten eine Therapie mit Depotinjektionen ab, wobei deren Akzeptanz mit der Erfahrung der Patienten mit dieser Darreichungsform zunimmt [16]. Letztlich werden in den meisten Ländern einschließlich Deutschland höchstens 10 % der Patienten mit Schizophrenie auf Depotantipsychotika eingestellt [26, 36, 39].
Risperidon, ein kombinierter Serotonin-5-HT2A- und Dopamin-D2-Rezeptor-Antagonist, ist ein 1994 auf dem Markt eingeführtes, akut und prophylaktisch wirksames atypisches Antipsychotikum mit bekanntem Nebenwirkungsprofil [28]. Im Vergleich zu anderen Antipsychotika der zweiten Generation weist Risperidon Vorteile im Hinblick auf Körpergewicht und metabolische Veränderungen auf; etwas häufiger werden extrapyramidale Nebenwirkungen und ein Prolactinanstieg beschrieben [22]. Risperidon war bisher in oraler Formulierung und seit 2002 als langwirksame Risperidon-Mikrosphären-Injektion verfügbar. Nach Injektion oder oraler Einnahme wird Risperidon zum pharmakologisch wirksamen Hauptmetaboliten 9-Hydroxyrisperidon (Paliperidon) umgewandelt, dessen erwünschte und unerwünschte Wirkungen weitgehend denen der Muttersubstanz Risperidon ähneln. Paliperidon ist als orale sowie als Depotformulierung mit monatlicher oder 3-monatlicher Anwendung verfügbar. Weitere verfügbare, atypische langwirksame Depotantipsychotika existieren für Aripiprazol und Olanzapin.
Mit Risperidon ISM® (OKEDI®, Laboratorios Farmacéuticos ROVI, S.A., Madrid, Spanien), einer mittels In-situ-Mikropartikel-Technologie entwickelten Depotformulierung von Risperidon, steht nun ein neues atypisches Depotantipsychotikum für die Therapie von Patienten mit Schizophrenie zur Verfügung, das eine unmittelbare mit einer langanhaltenden Freisetzung von Risperidon über vier Wochen verbindet. Der folgende Beitrag geht auf die pharmakokinetischen Besonderheiten und Möglichkeiten des klinischen Einsatzes von Risperidon ISM® bei Patienten mit Schizophrenie ein, die im Rahmen des klinischen Studienprogramms, u. a. in der PRISMA-III-Studie (Study to evaluate the efficacy and safety of risperidone in situ microparticle [ISM]® in patients with acute schizophrenia) untersucht wurden.
In-situ-Mikropartikel-Technologie
Bei Risperidon ISM® handelt es sich um eine spezielle Formulierung von Risperidon. Die Galenik basiert auf der innovativen ISM®-Technologie zur Verkapselung von Arzneimitteln [23]. Sie erlaubt die Freisetzung des Wirkstoffs in zwei Phasen – zum einen unmittelbar nach Injektion, zum anderen verlängert über circa vier Wochen – bei gleichzeitig einfacher Zubereitung und Anwendung. Das Depotsystem beruht auf der Bildung einer Polymermatrix in situ nach parenteraler Verabreichung.
Risperidon ISM® ist als Kit mit zwei Spritzen erhältlich. Dabei enthält eine Spritze Risperidon-Mikropartikel und Polylactid-co-Glycolid (PLGA) als festes Pulver, die andere das Lösungsmittel Dimethylsulfoxid (DMSO). Für die Zubereitung der Injektionssuspension werden die Bestandteile der beiden Spritzen vermischt. Nach intramuskulärer Injektion der Suspension und Kontakt mit Körperflüssigkeiten bildet sich eine feste biologisch abbaubare Polymermatrix, die den Wirkstoff enthält. Das Polymer mit den Mikropartikeln wird durch Hydrolyse während vier Wochen zu Kohlendioxid und Wasser abgebaut. Während dieses Prozesses wird der Arzneistoff retardiert und anhaltend freigesetzt.
Pharmakokinetik
Risperidon wird nach der Injektion des Arzneimittels durch zwei Mechanismen freigesetzt. Die ISM®-Technologie ermöglicht es, dass sich ein Teil des Wirkstoffs Risperidon in DMSO löst und direkt mit diesem Lösungsmittel unverzüglich freigesetzt wird. In der Phase-II-Studie wurde gezeigt, dass therapeutische Plasmaspiegel bereits zwei Stunden nach der Injektion erreicht werden [2]. Gleichzeitig fällt an der Injektionsstelle das Polymer im Muskelgewebe aus und bildet eine stabile, biologisch abbaubare Matrix. Aus dieser Matrix diffundieren Risperidon-Mikropartikel langsam in das umliegende Gewebe. Zusätzlich wird die Polymermatrix durch Hydrolyse abgebaut. Im Zuge des Abbauprozesses kommt es zu einer fortgesetzten, retardierten Abgabe des Wirkstoffs.
Die Bioverfügbarkeit von Risperidon ISM® im Vergleich zu oralem Risperidon wurde in einer offenen Studie untersucht (NCT03527186) [40]. Eingeschlossen waren 81 stabile, ambulant behandelte, erwachsene Patienten mit Schizophrenie gemäß Diagnostic and Statistical Manual of Mental Disorders, Fifth Edition (DSM-5) und mäßiger Krankheitsschwere. Vor dem Screening hatten die Patienten über mindestens vier Wochen als Erhaltungstherapie einmal täglich 4 mg Risperidon oral erhalten, ebenso mindestens eine Woche vor Verabreichung von Risperidon ISM®. Die Gabe von Risperidon ISM® i. m. erfolgte vier Mal in 4-wöchentlichen Abständen. Talspiegel und Fluktuationen des pharmakologisch aktiven Anteils des Wirkstoffs (Summe aus Muttersubstanz Risperidon und Metabolit 9-Hydroxyrisperidon) waren nach Injektion von Risperidon ISM® mit denjenigen nach oraler Einnahme vergleichbar, während Spitzenspiegel im Steady State, Fläche unter der Plasmakonzentrations-Zeit-Kurve (AUC) und mittlere Plasmakonzentrationen etwas höher lagen (Abb. 1). Da die Steady-State-Konzentration im gleichen Konzentrationsbereich des Risperidon-Wirkstoffs aufrechterhalten wird, der mit der oralen Behandlung erreicht wird, kann eine direkte Umstellung von oralem Risperidon auf Risperidon ISM® 24 Stunden nach der letzten oralen Dosis erfolgen. Eine Loading-Dose oder orale Supplementierung ist im Rahmen der Umstellung auf Risperidon ISM® nicht erforderlich.
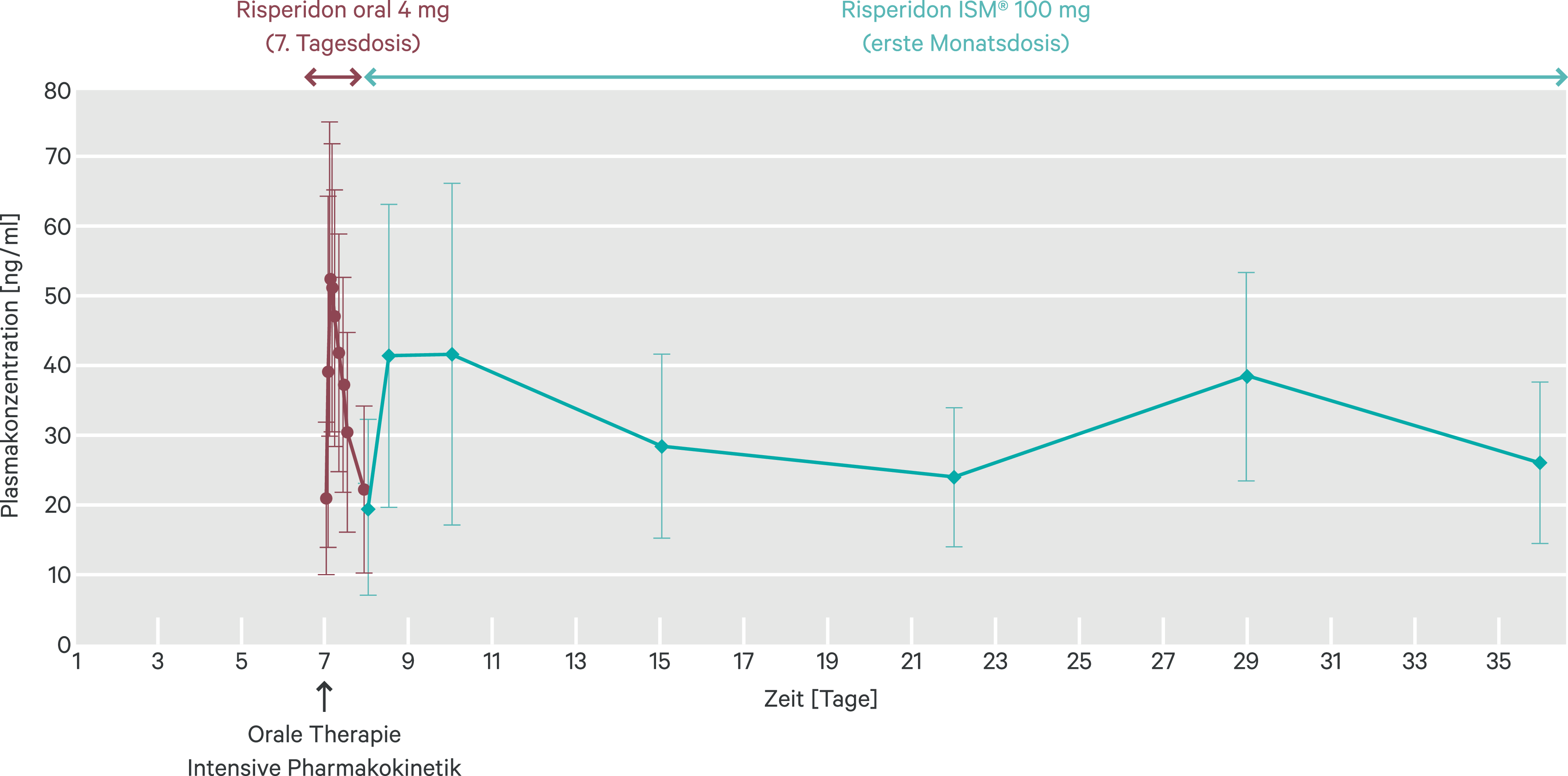
Abb. 1. Mittlere (± SD) Plasmakonzentrationen des Risperidon-Wirkstoffs im zeitlichen Verlauf während der oralen Behandlung mit 4 mg Risperidon (7. Dosis) und nach Umstellung auf Risperidon ISM® 100 mg (ab Tag 8). ISM: In-situ-Mikropartikel. Abbildung modifiziert aus [40] mit freundlicher Genehmigung von Dovepress.
Klinische Daten
PRISMA-Studienprogramm
Das klinische Studienprogramm PRISMA zu Risperidon ISM® umfasste zwei Studien der Phase I [7, 31] und je eine multizentrische Phase-II- und Phase-III-Studie (Tab. 1) [2, 9]. An die Doppelblindphase der Phase-III-Zulassungsstudie PRISMA-3 schloss sich eine einjährige offene Extensionsphase (Open-label extension [OLE]) an, deren Ergebnisse ebenfalls bereits veröffentlicht sind [10].
Tab. 1. Risperidon-ISM®-Studienprogramm mit Patienten
|
Studie |
PRISMA-1 (Phase I) [31] |
PRISMA-2 (Phase II) [2] |
PRISMA-3 (Phase III) [9] |
OLE [10] |
|
Autoren |
Llaudó J et al. |
Anta LA et al. |
Correll CU et al. |
Filts Y et al. |
|
ClinicalTrial.gov Identifier |
NCT01788774 |
NCT02086786 |
NCT03160521 |
NCT03870880 |
|
Patientenpopulation |
Schizophrenie oder schizoaffektive Störung |
Schizophrenie |
Akute Exazerbation einer Schizophrenie |
Nach Studienende PRISMA-3: mit Risperidon ISM® oder Placebo vorbehandelte Patienten (n = 174); zusätzlich: mit Risperidon oral vorbehandelte Patienten (n = 41) |
|
Patienten [n] |
36 |
67 |
438 |
215 |
|
Primärer Endpunkt |
AUC vor und nach Injektion |
Spitzenplasma-Konzentration (Cmax) für den aktiven Bestandteil |
Mittlere Veränderung des PANSS-Gesamtscores bis Tag 85 Post-Baseline |
Mittlere Veränderung des PANSS-Gesamtscores bis Tag 365 Post-Baseline |
|
Dauer |
75 Tage |
120 Tage |
12 Wochen |
12 Monate |
|
Studienmedikament |
Risperidon ISM® 50 mg, 75 mg, 100 mg (einmalige Injektion) |
Risperidon ISM® 75 mg alle 4 Wochen |
Risperidon ISM® 75 mg oder 100 mg alle 4 Wochen |
Risperidon ISM® 75 mg oder 100 mg alle 4 Wochen |
|
Kontrollgruppe |
Nein |
Nein |
Placebo |
Nein |
AUC: Area under the curve (Fläche unter der Plasmakonzentrations-Zeit-Kurve), ISM: In-situ-Mikropartikel, OLE: Open-label extension (offene Verlängerungsstudie), PANSS: Positiv- und Negativsyndromskala
Insgesamt waren mehr als 750 Patienten im Alter zwischen 18 und 65 Jahren in das Studienprogramm eingeschlossen. Tabelle 1 zeigt einen Überblick über das Studienprogramm zu Risperidon ISM®.
Phase-III-Studie PRISMA-3
PRISMA-3 war eine internationale, multizentrische 1 : 1 : 1-randomisierte, doppelblinde und Placebo-kontrollierte Studie der Phase III, in der die Wirksamkeit und Sicherheit von Risperidon ISM® in zwei Dosierungen (75 mg und 100 mg alle 28 Tage) bei Patienten mit Schizophrenie untersucht wurde [9]. Eingeschlossen werden konnten erwachsene Patienten im Alter von 18 bis 65 Jahren mit akut exazerbierter Schizophrenie (Positiv- und Negativsyndrom-Skala [PANSS]-Gesamtscore 80−120 und Score ≥ 4 Punkte für ≥ 2 definierte Positivsymptome) nach DSM-5. Die Patienten waren nach der Clinical Global Impression – Severity Scale (CGI-S) mäßig bis schwer erkrankt und mussten zuvor klinisch signifikant auf ein anderes Antipsychotikum als Clozapin angesprochen haben. Ausgeschlossen waren unter anderem Patienten mit einer anderen psychiatrischen Begleiterkrankung oder einer anderen instabilen Erkrankung. Die Studiendauer betrug 12 Wochen; danach konnten die Patienten an einer offenen Verlängerungsstudie über ein Jahr teilnehmen.
Primärer Wirksamkeitsendpunkt war die mittlere Veränderung des PANSS-Gesamtscores zwischen Baseline und Behandlungsende an Tag 85 oder am Tag der letzten Untersuchung. Wichtigster sekundärer Wirksamkeitsendpunkt war die mittlere Veränderung des CGI-S-Scores zwischen dem Beginn und dem Ende der Behandlung. Weitere Endpunkte betrafen unter anderem den mittleren Score der Clinical Global Impression – Improvement Scale (CGI-I) und die Gesamtansprechrate zum Endpunkt (definiert als Abfall des PANSS-Gesamtscores ≥ 30 % gegenüber dem Ausgangswert oder ein CGI-I-Score von 1 oder 2).
Wirksamkeit von Risperidon ISM®
Die Ergebnisse dieser Zulassungsstudie zeigen, dass die Therapie mit Risperidon ISM® mit einer raschen Reduktion schwerer bis mäßiger psychotischer Symptome bei Patienten mit akut exazerbierter Schizophrenie einhergeht. Die vordefinierten primären und sekundären Endpunkte wurden mit Risperidon ISM® in beiden Dosierungen erreicht. Die mittlere Veränderung im PANSS-Gesamtscore unterschied sich am Studienende in beiden Dosierungen signifikant gegenüber Placebo (–13,0; 95%-Konfidenzintervall [KI] –17,3 bis –8,8; p < 0,0001 und –13,3; 95%-KI –17,6 bis –8,9; p < 0,0001) (Abb. 2). Ebenso unterschieden sich die mittleren Veränderungen der PANSS-Positiv- und -Negativsyndromskalen-Scores sowie die mittleren Scores der CGI-I und CGI-S bis zum Studienende signifikant von Placebo (p < 0,0001). Bei Patienten mit einem Ausgangswert des PANSS-Gesamtscores ≥ 95 war die Effektstärke mit insgesamt über 0,7 hoch, bei der 100-mg-Dosis mit 0,87 sogar sehr hoch (vgl. Netzwerk-Metaanalyse von Huhn et al., 2019 [17]). Die hohe Effektstärke spricht dafür, dass Risperidon ISM® nicht nur zur Erhaltungstherapie, sondern bereits noch in der Akutphase eingesetzt werden kann.

Abb. 2. Veränderung des mittleren PANSS-Scores unter Risperidon ISM® vs. Placebo; signifikanter Unterschied bei ISM® 100 mg vs. Placebo ab Tag 8. ISM® (*p < 0,01, **p < 0,001, ***p < 0,0001). ISM: In-situ-Mikropartikel; LS: least squares (kleinste Quadrate); PANSS: Positiv- und Negativsyndrom-Skala; SE: standard error (Standardfehler). Modifiziert aus [9].
Der Unterschied zwischen Placebo und Risperidon ISM® im PANSS-Gesamtscore und Gesamtansprechen erreichte bereits ab Tag 8 (100 mg) bzw. Tag 15 (75 mg) statistische Signifikanz gegenüber Placebo. Die Unterschiede im PANSS erreichten bei beiden Dosierungen auf der Positivsyndrom-Skala ab Tag 8 und auf der Negativsyndrom-Skala ab Tag 15 gegenüber Placebo statistische Signifikanz, ab Tag 8 ebenso der Score der allgemeinen Psychopathologie in der 100-mg-Dosierung und der CGI-I-Score.
Beinahe dreimal so viele Patienten sprachen auf Risperidon ISM® an wie auf Placebo (59,7 % bei 75-mg-Dosierung vs. 20,5 % mit Placebo [absoluter Unterschied: 39,2 %], p < 0,0001). Für beide Dosierungen lag die Number needed to treat (NNT) bei 3.
Sicherheit und Verträglichkeit von Risperidon ISM®
Unerwünschte Ereignisse waren unter Risperidon ISM® meist leicht (67,8 %) oder mäßig (28,0 %) ausgeprägt und denjenigen unter oralen Risperidon-Formulierungen vergleichbar. Häufigste Nebenwirkungen waren erhöhte Prolactin-Spiegel, Kopfschmerzen, Hyperprolaktinämie und Gewichtszunahme. Schwerwiegende unerwünschte Ereignisse traten bei fünf Patienten (3,4 %) unter Placebo, bei zwei Patienten (1,4 %) unter Risperidon ISM® 75 mg und fünf Patienten (3,4 %) unter Risperidon ISM® 100 mg auf. Neue oder unerwartete Sicherheitssignale im Vergleich zu anderen Risperidon-Formulierungen waren nicht zu verzeichnen. Tabelle 2 zeigt eine Zusammenfassung der unter der Therapie aufgetretenen unerwünschten Ereignisse bei Patienten, die mindestens eine Dosis der Studienmedikation erhalten hatten (Sicherheitspopulation).
Tab. 2. Nebenwirkungen unter Risperidon ISM® vs. Placebo bei Patienten mit ≥ 1 TEAE
|
TEAE [n (%)] |
Placebo (n = 147) |
Risperidon ISM® 75 mg (n = 144) |
Risperidon ISM® 100 mg (n = 146) |
|
Alle Patienten |
32 (21,8) |
60 (41,7) |
77 (52,7) |
|
Hyperprolaktinämiea |
1 (0,7) |
8 (5,6) |
13 (8,9) |
|
Schmerzen an der Injektionsstelle |
3 (2,0) |
5 (3,5) |
4 (2,7) |
|
Alaninaminotransferase erhöht |
1 (0,7) |
2 (1,4) |
4 (2,7) |
|
Prolactin im Blut erhöht |
0 (0) |
13 (9,0) |
21 (14,4) |
|
Gewichtszunahme |
2 (1,4) |
5 (3,5) |
6 (4,1) |
|
Akathisie |
2 (1,4) |
5 (3,5) |
11 (7,5) |
|
Schwindel |
4 (2,7) |
4 (2,8) |
5 (3,4) |
|
Dystonie |
1 (0,7) |
4 (2,8) |
3 (2,1) |
|
Kopfschmerzen |
4 (2,7) |
9 (6,3) |
5 (3,4) |
|
Somnolenz |
2 (1,4) |
4 (2,8) |
8 (5,5) |
|
Schlaflosigkeit |
1 (0,7) |
3 (2,1) |
4 (2,7) |
ISM: In-situ-Mikropartikel, TEAE: unter Therapie aufgetretenes unerwünschtes Ereignis (treatment-emergent adverse event) − Beschreibung gemäß MedDRA-Version 20.0; aufgeführt sind TEAE, die bei ≥ 2 % der mit Risperidon ISM® behandelten Patienten auftraten.
aAls UE wurde ein Anstieg der Prolactin-Spiegel im Plasma betrachtet (sowohl für Hyperprolaktinämie als auch für erhöhte Prolactinwerte im Blut), wenn mindestens eines der folgenden Kriterien zutraf: Werte > 1000 mIU/l bei drei aufeinander folgenden Messungen nach Randomisierung, auch ohne Nachweis klinischer Symptome oder Werte > 530 mIU/l bei Vorliegen klinischer Symptome einer Hyperprolaktinämie (z. B. Kopfschmerz, Libidominderung, Oligo-Amenorrhö). Tabelle aus [9].
PRISMA-3-Langzeitphase
In der offenen, multizentrischen Langzeitphase wurden Patienten der PRISMA-3-Studie weiter über 12 Monate mit Risperidon ISM® behandelt [10]. Patienten der Verum-Gruppe behielten ihre jeweilige Dosierung bei (n = 119), während Patienten, die Placebo erhalten hatten, in der Langzeitstudie randomisiert mit 75 mg oder 100 mg Risperidon ISM® behandelt wurden (n = 55). Zusätzlich wurde eine Gruppe Patienten mit Schizophrenie eingeschlossen, die nach einer stabilen Erhaltungstherapie mit oralem Risperidon 4–6 mg/Tag über mindestens 4 Wochen de novo Risperidon ISM® in einer Dosierung von 75 mg (bei Vorbehandlung mit 4 mg oralem Risperidon) oder von 100 mg (bei Vorbehandlung mit > 4–6 mg oralem Risperidon) erhielten (n = 41) (Abb. 3).
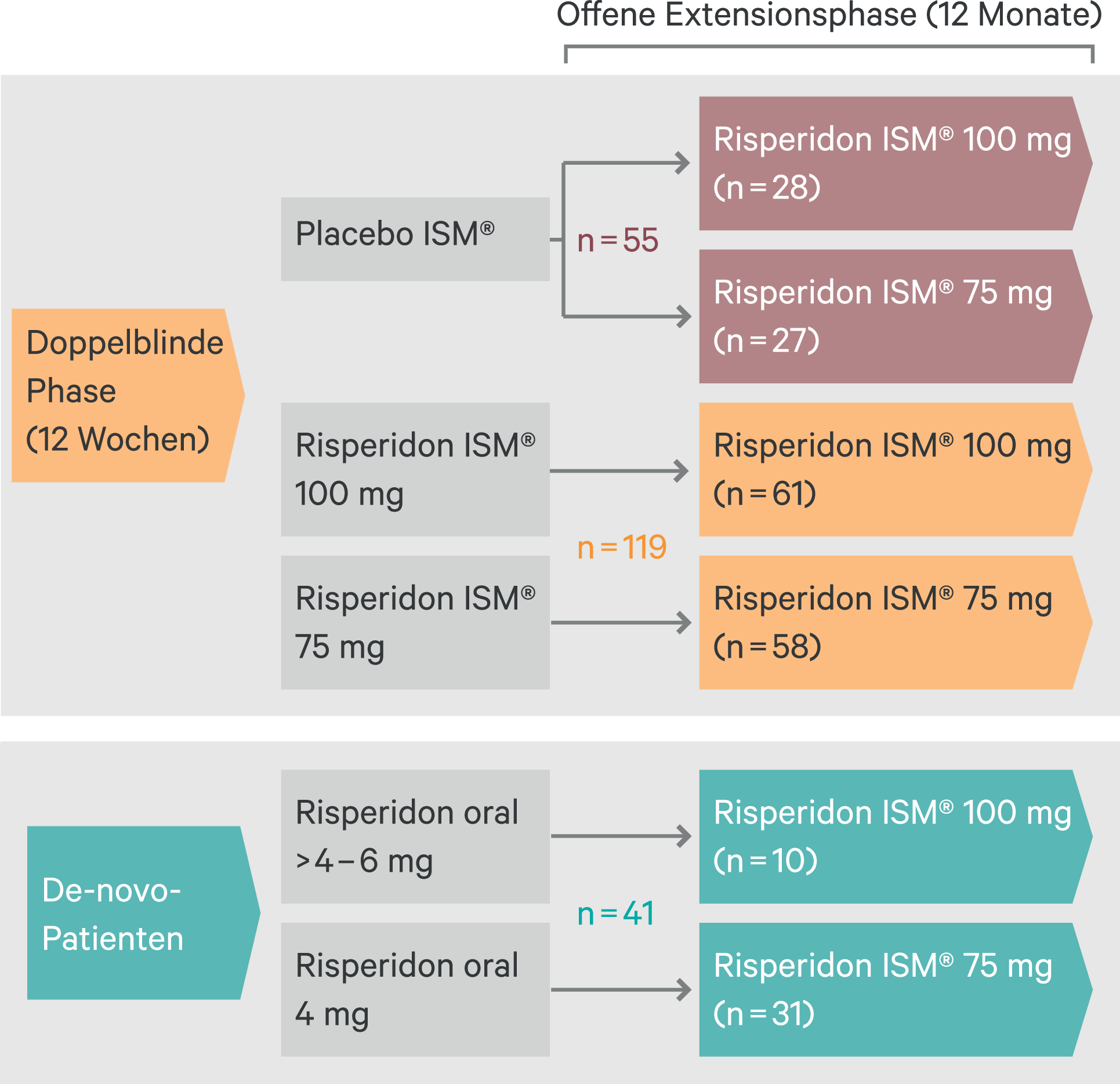
Abb. 3. Design der PRISMA-3-Extensionsphase [10]. ISM: In situ microparticles. Abbildung modifiziert aus [10].
Unter Risperidon ISM® verbesserte sich der mittlere PANSS-Gesamtscore ± SD in allen drei Behandlungsgruppen zwischen Baseline und Studienendpunkt nach 12 Monaten. Dabei war der Effekt in der Gruppe der zuvor mit Placebo behandelten Patienten und zu Beginn der Depottherapie stärker ausgeprägt; im weiteren Verlauf stellte sich ein Deckeneffekt ein. Nach rund sechs Monaten Therapie waren die mittleren PANSS-Gesamtscores in allen drei Behandlungsgruppen auf vergleichbarem niedrigem Niveau. Bei oral mit Risperidon vorbehandelten Patienten war keine wesentliche Veränderung zu verzeichnen (Abb. 4A).
Die mittleren Scores der CGI-S-waren im Verlauf denjenigen der PANSS vergleichbar. Nach ungefähr vier Monaten Therapie mit Risperidon ISM® waren die mittleren CGI-S-Scores der drei Patientengruppen auf gleichem niedrigem Niveau (Abb. 4B).

Abb. 4. PRISMA-3-Extensionsphase: Mittlerer PANSS (SD)-Gesamtscore (A) und CGI-S (SD)-Score (B) bei instabilen, stabilisierten und stabilen Patienten, die mit Risperidon ISM® (75 und 100 mg gepoolt) behandelt wurden. CGI–S: Clinical Global Impression – Severity Scale; PANSS: Positiv- und Negativsyndrom-Skala; SD: Standardabweichung; ISM: In-situ-Mikropartikel. Abbildung modifiziert aus [10].
Parallel zur Reduktion der PANSS-Gesamt- und CGI-S-Scores verbesserten sich sowohl bei Placebo- als auch bei Risperidon-ISM®-vorbehandelten Patienten die Scores für die PANSS-Positivsyndrom-, Negativsyndrom- und Psychopathologie-Subskalen. Dagegen blieben diese Scores bei zuvor oral mit Risperidon behandelten Patienten nahezu konstant (Tab. 3).
Tab. 3. PRISMA-3-Extensionsphase: Wirksamkeit von Risperidon ISM® zum Studienendpunkt [10]
|
Parameter |
Placebo-vorbehandelte Patienten (n = 55) |
Risperidon-ISM®-vorbehandelte Patienten (n = 114) |
Oral mit Risperidon vorbehandelte Patienten |
|
PANSS-Scores, Veränderung gegenüber Baseline, Mittelwert (SD) |
|||
|
–20,9 (14,40) |
–9,8 (13,88) |
–1,8 (8,60) |
|
–6,3 (5,05) |
–3,0 (5,10) |
–0,9 (3,16) |
|
–3,7 (4,58) |
–2,2 (3,62) |
–0,4 (3,43) |
|
–10,9 (7,95) |
–4,6 (7,37) |
–0,5 (5,26) |
|
CGI-S, Veränderung gegenüber Baseline, Mittelwert (SD) |
|||
|
–1,1 (0,96) |
–0,4 (0,87) |
0,0 (0,48) |
|
CGI-I Mittelwert (SD) |
|||
|
2,4 (1,05) |
2,9 (1,19) |
3,6 (1,11) |
|
Responder, % Patienten (95%-KI) |
|||
|
69,1 (55,2–80,9) |
45,4 (36,2–54,8) |
12,2 (4,1–26,2) |
CGI-I: Clinical Global Impression-Improvement Scale; CGI-S: Clinical Global Impression – Severity Scale; KI: Konfidenzintervall; ISM: In-situ-Mikropartikel; PANSS: Positiv- und Negativsyndrom-Skala; SD: Standardabweichung. a Anteil an Patienten in Prozent, die ein Gesamtansprechen zum Studienendpunkt erreichten, definiert als Reduktion des PANSS-Gesamtscores gegenüber dem Ausgangswert ≥ 30 % oder ein CGI-I-Score von mindestens 2 (sehr verbessert). Tabelle modifiziert aus [20].
Die Gesamtrückfallrate – definiert als Anstieg des PANSS-Gesamtscores ≥ 30 % gegenüber den Ausgangswerten, stationäre Wiederaufnahme des Patienten wegen psychotischer Symptome oder Anwendung zusätzlicher Antipsychotika nach ursprünglicher Stabilisierung – betrug über alle Studiengruppen hinweg 10,7 %, in den Gruppen nach Vorbehandlung mit Risperidon ISM® 11,8 % und nach Vorbehandlung mit oralem Risperidon 14,6 % (Tab. 4). Nach Vortherapie mit Placebo, d. h. bei Patienten, die zu Beginn der Extensionsphase höhere PANSS-Werte aufwiesen und zunächst mit Risperidon ISM® stabilisiert wurden, betrug die Rückfallrate 5,5 %. Insgesamt mussten neun Patienten (4,2 %) wegen psychotischer Symptome erneut stationär aufgenommen werden [10].
Tab. 4. Rückfallraten unter Langzeittherapie mit Risperidon ISM®
|
Placebo-vorbehandelte Patienten (n = 55) |
Risperidon-ISM®-vorbehandelte Patienten (n = 119) |
Oral mit Risperidon vorbehandelte Patienten (n = 41) |
Alle Patienten (n = 215) |
|
|
Rezidiv, n (%), 95 % KIa |
3 (5,5) 1,1−15,1 |
14 (11,8) 6,6−19,0 |
6 (14,6) 5,6−29,2 |
23 (10,7) 6,9−15,6 |
|
PANSS-Anstieg vs. Baseline, n (%) |
0 |
10 (8,4) |
4 (9,8) |
14 (6,5) |
|
Rehospitalisierung aufgrund psychotischer Symptome, n (%) |
2 (3,6) |
4 (3,4) |
3 (7,3) |
9 (4,2) |
|
Zusätzlicher Antipsychotika-Bedarf nach Stabilisierung, n (%) |
1 (1,8) |
5 (4,2) |
3 (7,3) |
9 (4,2) |
a Exaktes Clopper-Pearson-Konfidenzintervall. KI: Konfidenzintervall; PANSS: Positiv- und Negativsyndromskala. Tabelle modifiziert aus [20].
Nebenwirkungen waren in der Langzeittherapie unter Risperidon ISM® ebenfalls meist leicht (26,0 %) oder mäßig (12,1 %) ausgeprägt; therapiebedingt waren Kopfschmerzen (12,1 %), Hyperprolaktinämie (9,8 %), Asthenie (5,1 %), Gewichtszunahme (4,2 %), Schlaflosigkeit (4,2 %) und Akathisie (3,7 %) am häufigsten zu beobachten [10]. Extrapyramidal-motorische Störungen (EPS) waren bei insgesamt 4,2 % der Patienten zu verzeichnen [10], scheinen jedoch seltener als unter anderen Depotantipsychotika in vergleichbaren 1-Jahresstudien aufzutreten [6, 12, 18, 33] – unter Berücksichtigung der eingeschränkten Beurteilbarkeit indirekter Vergleiche. Dabei nahmen die mittleren Scores in EPS-Symptomskalen im Verlauf nur wenig zu [10]. Im Mittel lediglich numerisch kleine Anstiege waren bei den metabolischen Parametern Glucose (mittlere Veränderung ± SD unter beiden Dosierungen: 0,39 ± 1,97 mmol/l) und Gesamtcholesterin (0,13 ± 0,95 mmol/l) bis zum Studienende zu verzeichnen. Das Körpergewicht der Patienten nahm innerhalb eines Jahres verhältnismäßig wenig um durchschnittlich etwa 1 kg zu. Die Veränderungen dieser Parameter sind für die meisten Patienten klinisch wahrscheinlich wenig relevant, könnten jedoch für manche wegen der relativ hohen Varianz klinische Relevanz erreichen. Beim QTc-Intervall zeigte sich ein kleiner Dosiseffekt mit einer Verlängerung zum Studienende um 1,8 ± 22,99 ms unter 100 mg Risperidon ISM® gegenüber der Baseline (377,3 ± 27,03 ms) [10]. 15 (7 %) Patienten beendeten die Studie vorzeitig aufgrund von schwerwiegenden unerwünschten Ereignissen, wobei bei 7 (3,3 %) Patienten ein Zusammenhang mit Risperidon ISM® angenommen wurde. Die Häufigkeit von Therapieabbrüchen war niedriger oder vergleichbar mit anderen Studien mit Paliperidon oder Risperidon über 12 Monate [6, 11, 33].
Therapie mit Risperidon ISM® von Patienten mit Schizophrenie
Risperidon ISM® ist von der Europäischen Arzneimittel-Agentur (EMA) zur Behandlung von erwachsenen Patienten mit Schizophrenie zugelassen, bei denen Verträglichkeit und Wirksamkeit von oralem Risperidon nachgewiesen ist [25]. Die Behandlung mit Risperidon ISM® kann Patienten nach der Akutphase in der postsymptomatischen Remissionsphase weiter stabilisieren und als Erhaltungstherapie bzw. Rezidivprophylaxe fortgeführt werden [3]. Dabei ist der Einsatz von Risperidon ISM® sowohl im Rahmen der Erstmanifestation als auch bei Exazerbation oder Rezidiv möglich [25] sowie bei Patienten, deren Adhärenz mit der oralen Therapie nicht ausreichend sichergestellt ist.
Dosierung und Anwendung von Risperidon ISM®
Die Zubereitung der Injektionssuspension erfolgt mittels zweier miteinander verbundener Spritzen [25], was anfangs etwas Zeit und Übung benötigen kann. Vor der ersten Anwendung sollten Verträglichkeit und Ansprechen auf Risperidon bekannt sein oder zunächst in einer Titrationsphase bestätigt werden. Risperidon ISM® wird 4-wöchentlich als intramuskuläre Injektion tief gluteal oder deltoidal verabreicht [25]. Bei Injektion in den Deltamuskel sollte zwischen den beiden Oberarmen, bei der Injektion in den Gluteus zwischen den beiden Gesäßhälften abgewechselt werden [24, 25]. Die übliche Erhaltungsdosis beträgt 75 mg alle vier Wochen und kann auf 100 mg Risperidon ISM® gesteigert werden [25]. Eine Tagesdosis von 3 mg Risperidon oral ist ungefähr mit 75 mg Risperidon ISM® alle vier Wochen äquivalent, eine Tagesdosis von 4 mg oder höher Risperidon oral mit 100 mg Risperidon ISM®. Die Dosis kann gegebenenfalls bis zu drei Tage vor Ende des 4-wöchigen Dosierungsintervalls verabreicht werden. Wird die Injektion um eine Woche verzögert, nimmt die Risperidon-Talkonzentration im Plasma um 50 % gegenüber dem zeitgerechten Zeitpunkt der Injektion ab [25].
Therapiemanagement
Häufigste Nebenwirkung von Risperidon ISM® ist die durch den Dopamin-D2-Antagonismus induzierte Hyperprolaktinämie, die zu Hypogonadismus führen und unter anderem mit Menstruationsstörungen, Erektionsstörungen und Libidominderung einhergehen kann. Liegen Anzeichen möglicherweise Prolactin-assoziierter Störungen vor, wird eine Überwachung des Prolactin-Spiegels empfohlen. Vorsicht ist bei vorbestehender Hyperprolaktinämie oder prolactinabhängigen Tumoren geboten [25], zum Beispiel bei Patientinnen mit vorbestehendem Mammakarzinom [37]. Bezüglich der Akathisie liegen keine Empfehlungen zum Management unter Risperidon ISM® vor. Einer Übersichtsarbeit zufolge hat sich bei Akathisie unter Antipsychotika die Umstellung auf Wirkstoffe wie Olanzapin, Clozapin oder Quetiapin klinisch bewährt, ist aber nicht immer möglich. Andere Optionen umfassen die Gabe eines Betarezeptorblockers, eines noradrenergen und spezifisch serotonergen Antidepressivums oder eines Benzodiazepins [14].
Mit der Anwendung von Risperidon bei Schwangeren liegen keine oder nur sehr begrenzte Erfahrungen vor. Tierexperimentelle Studien haben eine Reproduktionstoxizität gezeigt. Risperidon ISM® sollte während der Schwangerschaft daher nicht angewendet werden, es sei denn, dies ist eindeutig erforderlich [24, 25]. Da Risperidon und seine Metaboliten wahrscheinlich in die Muttermilch ausgeschieden werden, kann ein Risiko für das gestillte Kind nicht ausgeschlossen werden. Für die Entscheidung bezüglich Therapieabbruch/-unterbrechung sind Nutzen und Risiken unter Berücksichtigung des Nutzens des Stillens für das Kind und des Nutzens der Therapie für die Frau abzuwägen [25].
Bei der Anwendung von Risperidon ISM® bei älteren Patienten ist Vorsicht geboten. Vor der Anwendung muss zuverlässig sichergestellt werden, dass eine orale Tagesdosis von ≥ 3 mg Risperidon vertragen wird. Im Allgemeinen ist die empfohlene Risperidon-Dosis für ältere Patienten mit normaler Nierenfunktion identisch mit der für erwachsene Patienten mit normaler Nierenfunktion [25].
Umstellung auf Risperidon ISM®
Die Umstellung auf Risperidon ISM® als Depotantipsychotikum ist frühzeitig, d. h. circa eine Woche nach Exazerbation der Schizophrenie unter der Vortherapie ohne Zusatzmedikation und direkt ohne Überlappungsphase möglich. Die Injektion von Risperidon ISM® sollte 24 Stunden nach Einnahme der letzten oralen Risperidon-Dosis erfolgen. Die Art der Umstellung hängt maßgeblich davon ab, ob der betreffende Patient zuvor mit Risperidon oral behandelt worden war bzw. ob ein Ansprechen auf Risperidon anamnestisch bekannt ist (Tab. 5).
Tab. 5. Umstellung auf Risperidon ISM® [25]
|
Vortherapie |
Umstellungsstrategie |
|
Ansprechen und Verträglichkeit von Risperidon bekannt |
|
|
Risperidon oral, Patient stabil (leichte/mittelschwere Symptome) |
Direkte Umstellung auf Risperidon ISM® ohne Titration |
|
Risperidon-Mikrosphären |
Direkte Umstellung auf 4-wöchentlich Risperidon ISM® ohne Boosterinjektion, Latenzphase oder simultane orale Medikation |
|
Andere Antipsychotika außer Risperidon |
Mindestens 6 Tage Titration mit oralem Risperidon zur Bestätigung des Ansprechens und der Verträglichkeit; dann Umstellung auf Risperidon ISM® |
|
Ansprechen und Verträglichkeit von Risperidon nicht bekannt |
|
|
Keine Risperidon-Vortherapie |
Zunächst Verträglichkeit und Ansprechen auf orales Risperidon bestätigen (Dauer der Titrationsphase mindestens 14 Tage); dann Umstellung auf Risperidon ISM® |
Ist die individuelle Verträglichkeit von Risperidon bereits bekannt, kann sofort von Risperidon oral oder Risperidon-Mikrosphären auf Risperidon ISM® umgestellt werden. Bei Wechsel von einem anderen Antipsychotikum und bei zuvor nie mit oralem Risperidon behandelten Patienten ist Risperidon über zunächst mindestens 6 bzw. 14 Tage oral zu testen [25]. Bei verspäteter Depotgabe ist eine einfache Weiterführung der Therapie möglich, da therapeutische Plasmaspiegel erneut innerhalb von zwei Stunden erreicht werden [25].
Zur Umstellung von Risperidon ISM® auf andere Risperidon- oder Paliperidon-Depotformulierungen liegen bisher keine klinischen Erfahrungen vor. Die Kosten der SGA-Depot-Antipsychotika, einschließlich Risperidon ISM®, bewegen sich in einer vergleichbaren Größenordnung.
Diskussion
Risperidon ISM® stellt eine neue, kurz- und langwirksame Depotformulierung des atypischen Antipsychotikums Risperidon für die Therapie erwachsener Patienten mit Schizophrenie dar. Risperidon ISM® war in der Placebo-kontrollierten Zulassungsstudie in beiden Dosierungen (75 mg und 100 mg alle vier Wochen) im Hinblick auf die klinische Gesamt-, Positiv- und Negativsymptomatik sowie den klinischen Gesamteindruck wirksam [9]. Die Ansprechrate nach 12 Wochen (60 %) ist mit der mittleren Ansprechrate oraler Antipsychotika in randomisierten kontrollierten Studien von 51 % vergleichbar – Letztere allerdings ausgewertet im Rahmen einer Netzwerk-Metaanalyse von Studien einer kürzeren Studiendauer von etwa sechs Wochen [29]. Die 1-Jahres-Rezidivrate unter Risperidon ISM® (10,7 %) ist ebenfalls mit den aus Metaanalysen von anderen (Depot-)Antipsychotika bekannten Rezidivraten vergleichbar [21, 27, 30]. Die Zulassungsstudie war jedoch nicht darauf angelegt, einen Unterschied der Rezidivraten von Risperidon ISM® und oralem Risperidon zu belegen. Eine Besonderheit stellt der durch die In-situ-Mikropartikel-Galenik bedingte frühe Wirkungseintritt von Risperidon ISM® dar. Dessen Dynamik ist mit derjenigen von oralem Risperidon [32, 35] vergleichbar. Nach Risperidon-Mikrosphären-Injektionen dagegen setzt eine signifikante Freisetzung des Wirkstoffs erst nach drei Wochen ein, sodass hier in der akuten Erkrankungsphase ein weiteres Antipsychotikum verabreicht werden muss [13].
Wie bei anderen Risperidon-Präparaten ist Hyperprolaktinämie auch bei Risperidon ISM® die häufigste Nebenwirkung. Bei Patienten mit vorbestehender Hyperprolaktinämie, Anzeichen einer Prolactin-assoziierten Störung oder eines Prolactin-abhängigen Tumors sollte der Prolactin-Spiegel überwacht werden oder ggf. ein anderer Wirkstoff gewählt werden.
Für die Therapie mit Risperidon ISM® ist kein komplexeres Therapieregime notwendig. Daher kommen für die Behandlung auch Patienten mit Adhärenz- oder kognitiven Problemen in Frage sowie Patienten, zu denen nur ein kurzer psychiatrischer Kontakt aufgebaut werden konnte.
Fazit
- Risperidon ISM® wird zur Behandlung von Schizophrenie bei Erwachsenen angewendet, bei denen die Verträglichkeit und Wirksamkeit von oralem Risperidon nachgewiesen ist.
- Die neue Depotformulierung von Risperidon besitzt ein breites Anwendungsspektrum. Es kann noch in der Akutphase verabreicht werden, ebenso wie für die Erhaltungstherapie und Rezidivprophylaxe.
- Für die Therapie stehen mit 75 mg und 100 mg zwei Risperidon-Dosierungen zur Verfügung, bei anamnestisch bekanntem Ansprechen und vorbekannter Verträglichkeit ist eine direkte Umstellung auf das Depotantipsychotikum möglich.
Interessenkonflikte
Dr. Thomas Aubel hat von Otsuka, Janssen-Cilag, ROVI und Recordati Honorare für Berater- und Vortragstätigkeiten erhalten.
Prof. Dr. Stephan Heres hat von ROVI, TEVA, KYE, Lundbeck/Otsuka und Johnson & Johnson Honorare für Berater- und Vortragstätigkeiten erhalten.
Prof. Dr. Dr. René Hurlemann hat von ROVI und Lundbeck/Otsuka 5 Honorare für Berater- und Vortragstätigkeiten erhalten.
Prof. Dr. Kai-Uwe Kühn hat von ROVI, Idorsia, Otsuka, Medical Tribune Honorare für Berater- und Vortragstätigkeiten erhalten.
PD Dr. med. habil. Karolina Leopold hat von Janssen-Cilag, Lundbeck, Recordati, ROVI und Otsuka Honorare für Berater- und Vortragstätigkeiten erhalten.
Prof. Dr. Nenad Vasic hat von Otsuka, ROVI, Janssen-Cilag und Lundbeck Honorare für Berater- und Vortragstätigkeiten erhalten.
Prof. Dr. med. Hans-Jörg Assion hat von ROVI und Janssen-Cilag Honorare für Berater- und Vortragstätigkeiten erhalten.
Prof. Dr. Dr. Göran Hajak hat von Gedeon Richter, Idorsia, Janssen-Cilag, Recordati, ROVI, Sanofi-Aventis, Bristol-Meyers, FEO, Georg Thieme, Heel, Hexal, Hikma, Jazz, Lundbeck, Medfora, Medice, Medical Tribune, Medscape, MedTrix, Neuraxpharm, Pfizer, Prosomno, Repha, Sanofi-Aventis und Schwabe Honorare für Berater- und Vortragstätigkeiten erhalten.
Prof. Dr. Thomas Wobrock hat von ROVI, Otsuka/Lundbeck, Janssen-Cilag und Recordati Honorare für Berater- und Vortragstätigkeiten erhalten.
Prof. Dr. med. Dan Rujescu hat von AC Immune, Roche, ROVI, Gerot Lannacher, Janssen-Cilag und Pharmgenetix Honorare für Berater- und Vortragstätigkeiten erhalten.
Prof. Dr. med Stefan Leucht hat von Alkermes, Angelini, Eisai, Gedeon Richter, Janssen, Lundbeck, Lundbeck Institute, Merck Sharp and Dome, Otsuka, Recordati, ROVI, Sanofi Aventis, TEVA, Medichem, Mitsubishi Honorare für Berater- und Vortragstätigkeiten erhalten sowie 20 Drittmittel vom Bundesministerium für Bildung und Forschung, der DFG und der EU.
Literatur
1. Alphs L, Bossie CA, Sliwa JK, Ma YW, et al. Onset of efficacy with acute long-acting injectable paliperidone palmitate treatment in markedly to severely ill patients with schizophrenia: post hoc analysis of a randomized, double-blind clinical trial. Ann Gen Psychiatry 2011;10:12.
2. Anta L, Llaudo J, Ayani I, Martinez J, et al. A phase II study to evaluate the pharmacokinetics, safety, and tolerability of risperidone ISM multiple intramuscular injections once every 4 weeks in patients with schizophrenia. Int Clin Psychopharmacol 2018;33:79–87.
3. Bodatsch M, Kuhn J. Stadiengerechte Therapiestrategien in der Schizophreniebehandlung. Arzneimitteltherapie 2016;34:146–53.
4. Bossie CA, Sliwa JK, Ma YW, Fu DJ, et al. Onset of efficacy and tolerability following the initiation dosing of long-acting paliperidone palmitate: post-hoc analyses of a randomized, double-blind clinical trial. BMC psychiatry 2011;11:79.
5. Ceraso A, Lin JJ, Schneider-Thoma J, Siafis S, et al. Maintenance treatment with antipsychotic drugs for schizophrenia. Cochrane Database Syst Rev 2020;8:CD008016.
6. Citrome L, Cucchiaro J, Sarma K, Phillips D, et al. Long-term safety and tolerability of lurasidone in schizophrenia: a 12-month, double-blind, active-controlled study. Int Clin Psychopharmacol 2012;27:165–76.
7. ClinicalTrials.gov. Pharmacokinetics, Safety, and Tolerance Study of Single Dose Administration of Risperidone ISM®. https://clinicaltrials.gov/ct2/show/NCT01320410 (Zugriff am 23.02.2022).
8. Correll CU, Citrome L, Haddad PM, Lauriello J, et al. The use of long-acting injectable antipsychotics in schizophrenia: Evaluating the evidence. J Clin Psychiatry 2016;77:1–24.
9. Correll CU, Litman RE, Filts Y, Llaudo J, et al. Efficacy and safety of once-monthly risperidone ISM® in schizophrenic patients with an acute exacerbation. NPJ Schizophr 2020;6:37.
10. Filts Y, Litman RE, Martinez J, Anta L, et al. Long-term efficacy and safety of once-monthly risperidone ISM® in the treatment of schizophrenia: Results from a 12-month open-label extension study. Schizophr Res 2022;239:83–91.
11. Fleischhacker WW, Gopal S, Lane R, Gassmann-Mayer C, et al. A randomized trial of paliperidone palmitate and risperidone long-acting injectable in schizophrenia. Int J Neuropsychopharmacol 2012;15:107–18.
12. Gopal S, Vijapurkar U, Lim P, Morozova M, et al. A 52-week open-label study of the safety and tolerability of paliperidone palmitate in patients with schizophrenia. J Psychopharmacol 2011;25:685–97.
13. Harrison TS, Goa KL. Long-acting risperidone: a review of its use in schizophrenia. CNS Drugs 2004;18:113–32.
14. Hasan A, Leucht S. Erkennen und behandeln von Antipsychotika-Nebenwirkungen. InFo Neurologie + Psychiatrie 2022;24:43–55.
15. Heres S, Hamann J, Kissling W, Leucht S. Attitudes of psychiatrists toward antipsychotic depot medication. J Clin Psychiatry 2006;67:1948–53.
16. Heres S, Schmitz FS, Leucht S, Pajonk FG. The attitude of patients towards antipsychotic depot treatment. Int Clin Psychopharmacol 2007;22:275–82.
17. Huhn M, Nikolakopoulou A, Schneider-Thoma J, Krause M, et al. Comparative efficacy and tolerability of 32 oral antipsychotics for the acute treatment of adults with multi-episode schizophrenia: a systematic review and network meta-analysis. Lancet 2019;394:939–51.
18. Kane JM, Sanchez R, Perry PP, Jin N, et al. Aripiprazole intramuscular depot as maintenance treatment in patients with schizophrenia: a 52-week, multicenter, randomized, double-blind, placebo-controlled study. J Clin Psychiatry 2012;73:617–24.
19. Kane JM, Schooler NR, Marcy P, Correll CU, et al. Effect of long-acting injectable antipsychotics vs usual care on time to first hospitalization in early-phase schizophrenia: A randomized clinical trial. JAMA Psychiatry 2020;77:1217–24.
20. Kirson NY, Weiden PJ, Yermakov S, Huang W, et al. Efficacy and effectiveness of depot versus oral antipsychotics in schizophrenia: synthesizing results across different research designs. J Clin Psychiatry 2013;74:568–75.
21. Kishimoto T, Hagi K, Kurokawa S, Kane JM, et al. Long-acting injectable versus oral antipsychotics for the maintenance treatment of schizophrenia: a systematic review and comparative meta-analysis of randomised, cohort, and pre-post studies. Lancet Psychiatry 2021;8:387–404.
22. Komossa K, Rummel-Kluge C, Schwarz S, Schmid F, et al. Risperidone versus other atypical antipsychotics for schizophrenia. Cochrane Database Syst Rev 2011:CD006626.
23. Kranz H, Bodmeier R. A novel in situ forming drug delivery system for controlled parenteral drug delivery. Int J Pharm 2007;332:107–14.
24. Laboratorios Farmacéuticos Rovi. Okedi® Fachinformation. Aktueller Stand.
25. Laboratorios Farmaceuticos ROVI SA. Fachinformation OKEDI®, Stand: Mai 2022.
26. Laux G. Verordnung von typischen und atypischen Antipsychotika (FGA, SGA) nach Versorgungs-Sektoren. Psychopharmakotherapie 2016;23:67–72.
27. Leucht C, Heres S, Kane JM, Kissling W, et al. Oral versus depot antipsychotic drugs for schizophrenia – a critical systematic review and meta-analysis of randomised long-term trials. Schizophr Res 2011;127:83–92.
28. Leucht S, Cipriani A, Spineli L, Mavridis D, et al. Comparative efficacy and tolerability of 15 antipsychotic drugs in schizophrenia: a multiple-treatments meta-analysis. Lancet 2013;382:951–62.
29. Leucht S, Leucht C, Huhn M, Chaimani A, et al. Sixty years of placebo-controlled antipsychotic drug trials in acute schizophrenia: Systematic review, Bayesian meta-analysis, and meta-regression of efficacy redictors. Am J Psychiatry 2017;174:927–42.
30. Leucht S, Tardy M, Komossa K, Heres S, et al. Antipsychotic drugs versus placebo for relapse prevention in schizophrenia: a systematic review and meta-analysis. Lancet 2012;379:2063–71.
31. Llaudo J, Anta L, Ayani I, Martinez J, et al. Phase I, open-label, randomized, parallel study to evaluate the pharmacokinetics, safety, and tolerability of one intramuscular injection of risperidone ISM at different dose strengths in patients with schizophrenia or schizoaffective disorder (PRISMA-1). Int Clin Psychopharmacol 2016;31:323–31.
32. Mousavi SG, Rostami H, Sharbafchi MR, Boroujeni AS, et al. Onset of action of atypical and typical antipsychotics in the treatment of acute psychosis. J Res Pharm Pract 2013;2:138–44.
33. Naber D, Peuskens J, Schwarzmann N, Goltz M, et al. Subjective well-being in schizophrenia: a randomised controlled open-label 12-month non-inferiority study comparing quetiapine XR with risperidone (RECOVER). Eur Neuropsychopharmacol 2013;23:1257–69.
34. Oehl M, Hummer M, Fleischhacker WW. Compliance with antipsychotic treatment. Acta Psychiatr Scand Suppl 2000;(407):83–6.
35. Raedler TJ, Schreiner A, Naber D, Wiedemann K. Early onset of treatment effects with oral risperidone. BMC psychiatry 2007;7:4.
36. Reymann S, Schoretsanitis G, Egger ST, Mohonko A, et al. Use of long-acting injectable antipsychotics in inpatients with schizophrenia spectrum disorder in an academic psychiatric hospital in Switzerland. J Pers Med 2022;12:441.
37. Riecher-Rössler A, Schmid C, Bleuer S, Birkhäuser M. Hyperprolactinämie unter Antipsychotika: Pathophysiologische Grundlagen, klinische Bedeutung und praktisches Vorgehen. Gynäkol Endokrinologie 2009;7:171–82.
38. Taylor M, Jauhar S. Are we getting any better at staying better? The long view on relapse and recovery in first episode nonaffective psychosis and schizophrenia. Ther Adv Psychopharmacol 2019;9:2045125319870033.
39. Verdoux H, Pambrun E, Tournier M, Bezin J, et al. Antipsychotic long-acting injections: A community-based study from 2007 to 2014 of prescribing trends and characteristics associated with initiation. Schizophr Res 2016;178:58–63.
40. Walling DP, Hassman HA, Anta L, Ochoa L, et al. The steady-state comparative bioavailability of intramuscular risperidone ISM and oral risperidone: An open-label, one-sequence study. Drug Des Devel Ther 2021;15:4371–82.
Prof. Dr. Hans-Jörg Assion, LWL-Klinik Dortmund im LWL PsychiatrieVerbund Westfalen, Marsbruchstraße 179, 44287 Dortmund-Aplerbeck, E-Mail: hans-joerg.assion@lwl.org
Dr. Thomas Aubel, Abteilung für Psychiatrie, Evangelische Kliniken Essen-Mitte gGmbH, Henricistraße 92, 45136 Essen, E-Mail: t.aubel@kem-med.com
Prof. Dr. Göran Hajak, Klinik für Psychiatrie und Psychotherapie, Klinikum Bamberg, Sozialstiftung Bamberg, Buger Straße 80, 96049 Bamberg, E-Mail: goeran.hajak@sozialstiftung-bamberg.de
Prof. Dr. Stephan Heres, kbo-Klinik für Psychiatrie und Psychotherapie Nord – Schwabing. Kölner Platz 1, 80804 München. E-Mail: stephan.heres@kbo.de
Prof. Dr. Dr. René Hurlemann, Universitätsklinik für Psychiatrie und Psychotherapie, Fakultät 6 für Medizin- und Gesundheitswissenschaften, Carl von Ossietzky Universität Oldenburg, Ammerländer Heerstraße 114–118, 26129 Oldenburg, E-Mail: rene.hurlemann@uol.de
Prof. Dr. Kai-Uwe-Kühn, LVR-Klinik Bonn. Kaiser-Karl-Ring 20, 53111 Bonn, E-Mail: kai-uwe.kuehn@lvr.de
Priv.-Doz. Dr. med. habil. Karolina Leopold, Vivantes Klinikum Am Urban und Vivantes Klinikum im Friedrichshain, Kliniken für Psychiatrie, Psychotherapie und Psychosomatik mit FRITZ am Urban & soulspace, Charité – Universitätsmedizin Berlin, Klinik und Poliklinik für Psychiatrie und Psychotherapie, Universitätsklinikum Carl Gustav Carus, Dresden, E-Mail: karolina.leopold@vivantes.de
Prof. Dr. Dr. Stefan Leucht (korrespondierender Autor), Klinik und Poliklinik für Psychiatrie und Psychotherapie, Ismaninger Straße 22, 81675 München, E-Mail: stefan.leucht@lrz.tum.de
Prof. Dr. Dan Rujescu, Klinische Abteilung für Allgemeine Psychiatrie, Universitätsklinik für Psychiatrie und Psychotherapie, Universitätsklinikum AKH Wien, Spitalgasse 23, 1090 Wien, Österreich, E-Mail: dan.rujescu@meduniwien.ac.at
Prof. Dr. Nenad Vasic, Klinik für Psychiatrie und Psychotherapie, Klinikum Christophsbad, Faurndauer Straße 6–28, 73035 Göppingen, E-Mail: nenad.vasic@christophsbad.de
Prof. Dr. Thomas Wobrock, Zentrum für Seelische Gesundheit, Kreiskliniken Darmstadt-Dieburg, Krankenhausstraße 7, 64823 Groß-Umstadt, Klinik für Psychiatrie und Psychotherapie, Universitätsmedizin Göttingen, E-Mail: t.wobrock@kreiskliniken-dadi.de
Risperidone ISM® – an innovative long-acting formulation for the treatment of schizophrenia
Risperidone ISM® (OKEDI®), a new long-acting formulation of the atypical antipsychotic risperidone manufactured using in situ microparticle technology, has been available in Germany since April 2022, in Austria since February 2023. Effective plasma levels are achieved as early as 2 hours after IM injection without loading dose or oral supplementation with risperidone. The results of the phase III PRISMA-3 study (n = 438) show that therapy with risperidone ISM® is associated with a significant reduction in severe to moderate psychotic symptoms (mean positive and negative syndrome scale [PANSS] total score) as well as in Clinical Global Impression Improvement (CGI-I) scores with a high effect size (p < 0.0001). The difference from placebo in PANSS total score, positive syndrome score, and overall response reached statistical significance from day 8 (100-mg dose) and day 15 (75 mg), respectively. Adverse events were mostly mild (67.8 %) or moderate (28.0 %) and comparable to those seen with oral risperidone. In the open-label extension study, patients who had completed the phase III study patients pre-treated either with risperidone ISM® or placebo (n = 174) received risperidone ISM® for 12 months. In addition, a group of patients was treated with risperidone ISM® 75 mg or 100 mg de novo (n = 41). Thereby, the mean PANSS total score improved in all treatment groups to the endpoint, most significantly in placebo or risperidone ISM® pre-treated patients. Thus, the new atypical depot antipsychotic risperidone ISM® is suitable for early treatment of patients subsequent to acute phase schizophrenia as well as for maintenance therapy and relapse prophylaxis. The prerequisite for use is that the efficacy and tolerability of risperidone or paliperidone are known; if necessary, individual oral tolerability should be tested prior to administration of risperidone ISM®. Patients may particularly benefit from risperidone ISM® who have had problems in the past with the up-dosing of antipsychotic treatment as well as patients with adherence issues.
Keywords: schizophrenia, risperidone, depot antipsychotic, in situ microparticle
Psychopharmakotherapie 2023; 30(03):72-81
