Julia Pieper, Bonn
Es werden zwei Typen der bipolaren Erkrankung unterschieden: Beim Typ I treten sowohl manische als auch depressive Phasen im Wechsel auf, während Typ II vor allem durch depressive Episoden in Verbindung mit hypomanischen Phasen gekennzeichnet ist. Betroffene Patienten sind in ihrem Alltag eingeschränkt, ihre Lebensqualität ist häufig beeinträchtigt. Behandlungsoptionen sind kaum vorhanden und mit unerwünschten Wirkungen wie kardiometabolischen Entgleisungen oder extrapyramidal-motorischen Störungen (EPMS) verbunden.
Mit Lumateperon wurde 2020 in den USA ein neuartiges Antipsychotikum für die Behandlung der Schizophrenie zugelassen. Die Substanz hat ein eigenes Rezeptorprofil: Lumateperon wirkt als potenter Serotonin-5-HT2A-Antagonist, hat zudem partialagonistische Wirkung an präsynaptischen Dopamin-D2-Rezeptoren und wirkt antagonistisch an postsynaptischen D2-Rezeptoren. Außerdem fungiert die Substanz als D1-Rezeptor-abhängiger Glutamat-Modulator und Serotonin-Wiederaufnahmehemmer. Ein Vorteil ist, dass Lumateperon kaum an histaminerge oder muskarinerge Rezeptoren bindet. Damit treten typische Nebenwirkungen kaum bis gar nicht auf (z. B. kardiometabolisch).
In einer aktuellen Phase-III-Studie wurde nun die Wirksamkeit und Sicherheit bei Patienten mit einer depressiven Episode im Zusammenhang mit einer bipolaren Erkrankung untersucht.
Design der Studie
Es wurde eine 6-wöchige Placebo-kontrollierte Doppelblindstudie in sechs verschiedenen Ländern durchgeführt. In die Studie eingeschlossen wurden Patienten, die sich im Rahmen einer bipolaren Erkrankung Typ I oder II in einer mindestens als mittelschwer eingestuften depressiven Episode befanden. Diese durfte nicht länger als sechs, musste aber seit mindestens zwei Wochen bestehen. In einer 1 : 1-Randomisierung erhielten die Teilnehmer entweder einmal täglich 42 mg Lumateperon peroral als Kapsel oder ein Placebo. Endpunkte waren Änderungen an Tag 43 auf der Montgomery-Åsberg Depression Rating Scale (MADRS; primärer Endpunkt) sowie der Clinical Global Impressions Scale–Bipolar Version–Severity Scale (CGI-BP-S; wesentlicher sekundärer Endpunkt).
Ergebnisse
Von 377 behandelten Patienten beendeten 333 die 6-wöchige Behandlungsdauer. 79,8 % der eingeschlossenen Patienten hatten eine Bipolar-I-Erkrankung. Der mittlere MADRS-Score vor Therapie lag bei 30,5, der mittlere CGI-BP-S-Depression-Subscore bei 4,6. Die Behandlung mit Lumateperon reduzierte den MADRS-Score signifikant (Tab. 1), erste Effekte traten schon ab Tag 8 auf und hielten bis zum Ende des Beobachtungszeitraums an. Bei beiden Typen der Bipolarstörung war Lumateperon dem Placebo signifikant überlegen, sowohl in Bezug auf den MADRS-Score (Abb. 1) als auch beim CBI-BP-S-Gesamtscore und Subscore für Depression.
Lumateperon wurde gut vertragen: Schläfrigkeit und Übelkeit waren die einzig relevanten Nebenwirkungen. EPMS traten nur bei einem Patienten mit EPMS in der Vorgeschichte auf. Es gab keine relevanten Veränderungen der kardiometabolischen oder endokrinologischen Parameter.
Tab. 1. Ergebnisse zur Wirksamkeit von Lumateperon im Vergleich zu Placebo [nach Calabrese et al.]
|
Lumateperon |
Placebo |
Effekt |
|
|
MADRS-Gesamtscore (prim. Endpunkt) |
–16,7 (SD 0,69) |
–12,1 (SD 0,68) |
p < 0,0001 |
|
CGI-BP-S-Gesamtscore |
–3,5 (SD 0,17) |
–2,5 (SD 0,17) |
p < 0,0001 |
|
CGI-BP-S-Depressions-Subscore |
–1,8 (SD 0,09) |
–1,3 (SD 0,09) |
p < 0,0001 |
|
MADRS-Ansprechrate |
51,1 % |
36,7 % |
p < 0,001 |
|
MADRS-Remissionsrate |
39,9 % |
33,5 % |
p = 0,018 |
KI: Konfidenzintervall; SD: Standardabweichung; MADRS: Montgomery-Åsberg Depression Rating Scale; CGI-BP-S: Clinical Global Impressions Scale–Bipolar Version–Severity Scale
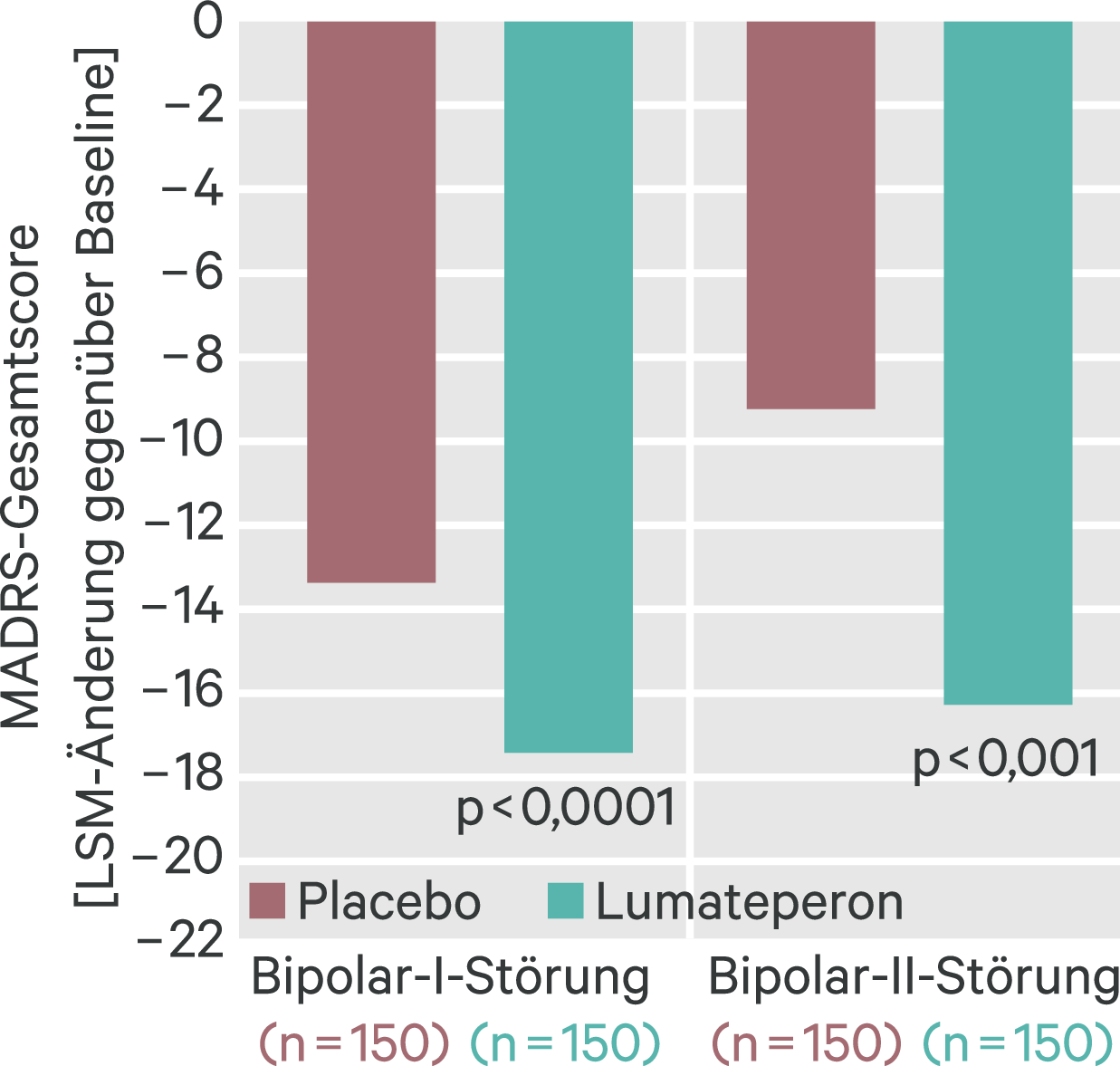
Abb. 1. Wirksamkeit von Lumateperon auf die Depressionssymptome in Abhängigkeit vom Typ der Bipolarstörung [nach Calabrese et al.]; MADRS: Montgomery-Asberg Depression Rating Scale
Einschränkungen der Studie sind die kurze Studiendauer und der Ausschluss bestimmter Patientengruppen (z. B. therapieresistente Patienten). Die Effektivität weiterer Dosierungen von Lumateperon wurde in dieser Studie nicht untersucht.
Es stand in der PPT
Schizophrenie: Wirksamkeit von Lumateperon in der Akuttherapie. Psychopharmakotherapie 2020;27:165–6.
Positiver Ausblick
Lumateperon verbessert depressive Symptome bei Patienten mit schweren depressiven Episoden bei bipolarer Erkrankung signifikant bei einem überschaubaren Nebenwirkungsprofil.
Die Ergebnisse der vorliegenden Studie scheinen das Vorhaben der entsprechenden Indikationserweiterung zu unterstützen. Besonders für Patienten mit Typ-II-Erkrankung dürfte Lumateperon eine interessante Alternative sein, da aktuell nur Quetiapin für diese Indikation zugelassen ist, was eine höhere Rate an unerwünschten Wirkungen aufweist.
Quelle
Calabrese JR, et al. Efficacy and safety of lumateperone for major depressive episode associated with bipolar I or bipolar II disorder: a phase 3 randomized placebo-controlled trial. Am J Psychiatry published online Sep 23, 2021; doi: 10.1176/appi.ajp.2021.20091339.
Psychopharmakotherapie 2021; 28(06):274-285
