Jürgen Fritze, Frankfurt am Main, Claudia Riedel, Angelika Escherich, Peggy Beinlich, Karl Broich und Thomas Sudhop, Bonn
Die Hintergründe dieses Projekts wurden in diesem Journal im Beitrag zu Thrombozytenaggregationshemmern [4] bzw. Psychostimulanzien [5] detailliert dargestellt und werden deshalb hier nur zusammengefasst: Der von der Bundesregierung akzeptierte „Nationale Aktionsplan für Menschen mit Seltenen Erkrankungen“ des Nationalen Aktionsbündnisses für Menschen mit Seltenen Erkrankungen (NAMSE) empfiehlt unter anderem, eine „Studie zur Erfassung des Umfangs des Off-Label-Use bei Seltenen Krankheiten anhand der Daten nach §303a ff. SGB V […]“ durchzuführen. Darüber hinaus zielt das Projekt darauf, dem Gemeinsamen Bundesausschuss (G-BA) erstmals Informationen über Art und Häufigkeit von Off-Label-Use zumindest der am häufigsten verordneten Wirkstoffe für das Verfahren gemäß §35c Absatz 1 Sozialgesetzbuch V (SGB V) zu liefern.
Untersuchte Arzneimittel
In dieser Untersuchung wurden die Antidementiva (inklusive Nootropika) Donepezil, Galantamin, Memantin, Nicergolin, Piracetam und Rivastigmin analysiert. Die Anwendungsgebiete der verschiedenen Antidementiva unterscheiden sich – zum Teil auch zwischen verschiedenen Fertigarzneimitteln unterschiedlicher Hersteller – und sind nachfolgend auszugsweise dargestellt.
Donepezil:
- Indiziert zur symptomatischen Behandlung der leichten bis mittelschweren Alzheimer-Demenz.
Galantamin:
- Indiziert zur symptomatischen Behandlung leichter bis mittelschwerer Demenz vom Alzheimer-Typ.
Memantin:
- Indiziert zur Behandlung von Patienten mit moderater bis schwerer Alzheimer-Demenz.
Nicergolin:
- Als unterstützende Maßnahme bei Hirnleistungsstörungen im Alter (hirnorganisches Psychosyndrom) mit den Leitsymptomen: Einschränkung der Konzentrationsfähigkeit, der Merkfähigkeit, der Gesamtorientierung sowie Schlafstörungen.
Piracetam:
- Zur symptomatischen Behandlung von chronischen hirnorganisch bedingten Leistungsstörungen im Rahmen eines therapeutischen Gesamtkonzepts bei demenziellen Syndromen mit der Leitsymptomatik: Gedächtnisstörungen, Konzentrationsstörungen, Denkstörungen, vorzeitige Ermüdbarkeit und Antriebs- und Motivationsmangel, Affektstörungen. Zur primären Zielgruppe gehören Patienten mit demenziellem Syndrom bei primär degenerativer Demenz, Multiinfarktdemenz und Mischformen aus beiden. Bevor die Behandlung mit Piracetam begonnen wird, sollte geklärt werden, ob die Krankheitserscheinungen nicht auf einer spezifisch zu behandelnden Grunderkrankung beruhen.
- Zur adjuvanten Behandlung von Myoklonus-Syndromen kortikalen Ursprungs.
- Zur unterstützenden Behandlung von Kindern mit Lese-/Rechtschreibstörungen (Legasthenie), die nicht durch eine intellektuelle Retardierung (Minderbegabung), mangelnde Schulbildung oder unzureichende familiäre/soziale Verhältnisse erklärt werden können.
Rivastigmin:
- Zur symptomatischen Behandlung der leichten bis mittelschweren Alzheimer-Demenz.
- Zur symptomatischen Behandlung der leichten bis mittelschweren Demenz bei Patienten mit idiopathischem Parkinson-Syndrom.
Altersgrenzen
Für Donepezil, Galantamin, Memantin, Nicergolin und Rivastigmin war aufgrund der Formulierung in den Fachinformationen ein Mindestalter von 18 Jahren vorauszusetzen („... wird nicht zur Anwendung bei Kindern und Jugendlichen empfohlen“ o.Ä.). Piracetam ist bereits für Kinder ab dem 8. Lebensjahr zugelassenen („Für Kinder ab 8 Jahren und Jugendliche gelten zur unterstützenden Behandlung von Lese-/Rechtschreibstörungen folgende Dosierungsrichtlinien ...“).
Methoden der Datenanalyse
Die Methodik wurde in diesem Journal bereits detailliert dargestellt [4, 5]: Grundlage bilden die Daten nach §§303aff. SGB V der Jahre 2010 und 2011, also die Abrechnungsdaten der gesetzlichen Krankenkassen. Die darin enthaltenen Pharmazentralnummern (PZN) der verordneten Arzneimittel wurden in die ATC-Codes der Wirkstoffe übersetzt. Die Pseudonymisierung der Patienten erlaubte den Versichertenbezug über längere Zeiträume. Die als Freitext formulierten Anwendungsgebiete gemäß Fachinformation wurden mit Codes der amtlichen ICD-10-GM-Codes operationalisiert. Weitere den In-Label-Use definierende Kriterien (z.B. Anwendungseinschränkungen und Kontraindikationen) konnten nicht gewürdigt werden, weil das spezifisch entwickelte Auswertungsskript auf die Analyse verschiedenster Wirkstoffe anwendbar sein musste, um den vorgegebenen Zeitrahmen zur Fertigstellung des Projekts beim Deutschen Institut für Medizinische Dokumentation und Information (DIMDI) nicht zu gefährden.
Für alle gesetzlich Versicherten, denen Antidementiva gemäß den ATC-Codes N06BX03, N06DA02, N06DA03, N06DA04, N06DX01 bzw. N06DX13 mindestens einmal verordnet worden waren, wurden sämtliche in diesem Beobachtungszeitraum übermittelte ICD-10-GM-Codes erfasst. Als In-Label-Use wurden diejenigen pseudonymisierten Patienten identifiziert, bei denen mindestens einmal im zweijährigen Beobachtungszeitraum mindestens eine der im Datensatz übermittelten Diagnosen einer der zugelassenen Diagnosen gemäß Operationalisierung entsprach, als Off-Label-Use jene Versicherten, bei denen keine Diagnose den zugelassenen Indikationsdiagnosen entsprach. Um Mängel der Operationalisierung zu kompensieren, wurde gegebenenfalls ein In-Label-Use rekonstruiert. Die Rekonstruktionen konnten nur semiquantitativ erfolgen, weil im Beobachtungszeitraum von acht Quartalen derselbe Sachverhalt von unterschiedlichen Ärzten mit unterschiedlichen und damit über die Zeit wechselnden Codes kodiert worden sein konnte. Die Auswahl, Interpretation und Bewertung mutmaßlich beabsichtigter Off-Label-Indikationen konnte nur durch manuelle Sichtung jeder einzelnen Diagnose gemäß medizinischer Plausibilität erfolgen.
Um Off-Label-Use in Form eines Verstoßes gegen mögliche Altersbeschränkungen näherungsweise erkennen zu können, erfolgten die Zählungen differenziert nach den Altersgruppen „<1 Jahr“, „1 bis <14 Jahre (Kinder)“, „14 bis <18 Jahre (Jugendliche)“ und „Erwachsene nach Dekaden“, sodass die Altersgrenze acht Jahre für Piracetam nicht gewürdigt werden konnte.
Der In-Label-Use der Antidementiva wurde mit den in Tabelle 1 präsentierten Codes operationalisiert.
Tab. 1. ICD-10-GM-Codes, die zur Operationalisierung eines In-Label-Use der analysierten Antidementiva verwendet wurden
|
ICD-Code |
Donepezil |
Galantamin |
Memantin |
Nicergolin |
Piracetam |
Rivastigmin |
|
F00.- Demenz bei Alzheimer-Krankheit (G30.-†) |
+ |
+ |
+ |
+ |
+ |
+ |
|
F01.- Vaskuläre Demenz |
+ |
+ |
||||
|
F02.3 Demenz bei primärem Parkinson-Syndrom (G20†) |
+ |
|||||
|
F03 Nicht näher bezeichnete Demenz |
+ |
+ |
||||
|
F04 Organisches amnestisches Syndrom, nicht durch Alkohol oder andere psychotrope Substanzen bedingt |
+ |
+ |
||||
|
F81.0 Lese- und Rechtschreibstörung |
+ |
|||||
|
G20.- Primäres Parkinson-Syndrom |
+ |
|||||
|
G25.3 Myoklonus |
+ |
|||||
|
G30.- Alzheimer-Krankheit (F00.-*) |
+ |
+ |
+ |
+ |
+ |
+ |
Aus Gründen des Datenschutzes wurde für alle Einzeldiagnosen (ICD-Codes) mit einer Versichertenzahl zwischen 1 und 30 vom DIMDI eine Anzahl von „30“ ausgewiesen, um sicherzustellen, dass keine Re-Identifikation der Versicherten erfolgen kann. In diesen Fällen wurden zur Kompensation jeweils Spannweiten mit einem hypothetischen Minimum, bei dem n=1 versicherte Person pro Gruppe angenommen wurden, und einem Maximum, bei dem hypothetisch n=30 angenommen wurden, errechnet und in den Auswertungen in Form eines Intervalls mit jeweils unterer und oberer Grenze angegeben.
Zum identifizierten Off-Label-Use bei seltenen Krankheiten erfolgten explorative, unsystematische Literaturrecherchen in Pubmed.
Ergebnisse
Jeweils weit mehr als 99% der Versicherten waren im Beobachtungszeitraum ausschließlich ambulant behandelt worden (Tab. 2). Zwischen Piracetam einerseits und den anderen Antidementiva andererseits bestanden aufgrund der Zulassung zu erwartende Unterschiede in der Verteilung des Alters (Abb. 1). Das weibliche Geschlecht überwog mit bis zu zwei Dritteln (Tab. 2). Das Mindestalter (Tab. 2) wurde unter Donepezil, Galantamin, Memantin, Nicergolin und Rivastigmin in ähnlichem Umfang (insgesamt gemäß Datenschutzregelung bei 10 bis 300 Patienten) unterschritten. Für Piracetam konnte die untere Altersgrenze von acht Jahren nicht geprüft werden, weil die Standarddatenbankabfrage diese Grenze nicht enthielt.
Tab. 2. Verordnung von Antidementiva: Synopse der Ergebnisse
|
Donepezil |
Galantamin |
Memantin |
Nicergolin |
Piracetam |
Rivastigmin |
|
|
Total |
114096 |
64436 |
151954 |
17659 |
131046 |
80959 |
|
Ausschließlich ambulant |
99,90% |
99,91% |
99,91% |
99,92% |
99,91% |
99,89% |
|
Anteil weiblich min |
64,5% |
65,5% |
64,4% |
61,1% |
57,5% |
59,0% |
|
Anteil weiblich max |
64,4% |
65,3% |
64,4% |
60,9% |
57,4% |
58,9% |
|
OLU vor Rekonstruktion |
27,7% |
25,8% |
34,6% |
68,8% |
65,5% |
18,2% |
|
OLU nach Rekonstruktion |
28% |
26% |
35% |
50% |
62% |
18% |
|
Alter<18 Jahre min |
0,002% |
0,003% |
0,001% |
0,011% |
0,252% |
0,002% |
|
Alter<18 Jahre max |
0,053% |
0,093% |
0,039% |
0,337% |
0,318% |
0,074% |
|
Orphan-Diseases |
Keine |
Keine |
||||
|
F02.0* (Demenz bei Pick-Krankheit) G31.0†) (frontotemporale Demenzen) |
+ |
+ |
+ |
+ |
||
|
Chorea Huntington (G10) |
+ |
OLU: Off-Label-Use, min/max gemäß Datenschutzregelung
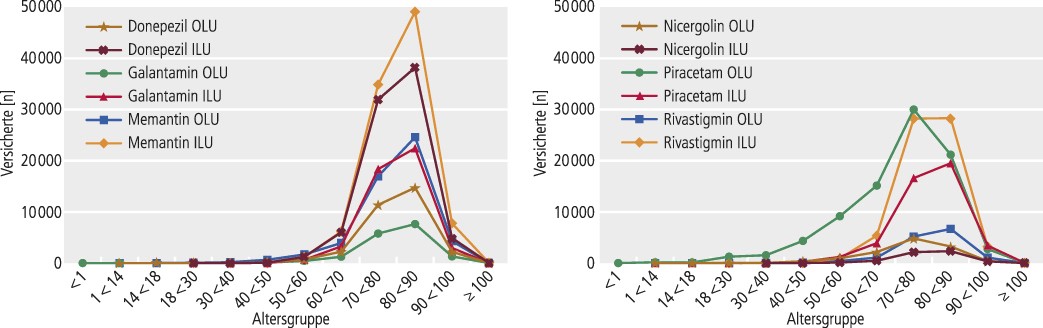
Abb. 1. Verordnung von Donepezil, Galantamin, Memantin, Nicergolin, Piracetam und Rivastigmin nach Altersgruppen. ILU: In-Label-Use; OLU: Off-Label-Use
Unter den Diagnosen, die den In-Label-Use operationalisieren, wurde der unspezifische Code F03 (nicht näher bezeichnete Demenz) am häufigsten genannt (Tab. 3). Als seltene Krankheiten, denen der Off-Label-Use möglicherweise gegolten haben konnte, wurden für die drei Cholinesterasehemmer und Memantin frontotemporale Demenzen, möglicherweise auch in Verbindung mit amyotropher Lateralsklerose (G12.2) identifiziert, für Memantin auch Chorea Huntington (Tab. 2 und 3). Bei den zugelassenen Anwendungsgebieten von Piracetam spielten Myoklonien und hier auch die bei der Operationalisierung unberücksichtigten Codes G40.3 (generalisierte idiopathische Epilepsie und epileptische Syndrome) und G40.4 (sonstige generalisierte Epilepsie und epileptische Syndrome), denen auch myoklonische Syndrome subsumiert sind, quantitativ keine Rolle (<1 %).
Bei der Aufklärung des apparenten Off-Label-Use (Tab. 3 und Tab. 4) ergab sich, dass für Nicergolin und Piracetam Rekonstruktionen vorzunehmen waren, weil organische affektive Störungen, sonstige näher bezeichnete organische psychische Störungen, organische Persönlichkeitsstörungen und organische Psychosyndrome nach Schädelhirntrauma und – zusätzlich für Nicergolin – die „leichte kognitive Störung“ (mild cognitive impairment, MCI) als vom zugelassenen Anwendungsgebiet „Hirnleistungsstörungen im Alter (hirnorganisches Psychosyndrom)“ umfasst interpretiert werden, also einem In-Label-Use entsprechen konnten. Dadurch reduzierte sich die Rate des Off-Label-Use bei Nicergolin auf näherungsweise 50%, die von Piracetam auf etwa 62%. Für die anderen Antidementiva ergab sich kein Rekonstruktionsbedarf.
Tab. 3. In den In-Label-Use- (ILU) und Off-Label-Use-Gruppen (OLU) genannte, den In-Label-Use operationalisierende Diagnosen (fett) sowie die identifizierten seltenen Krankheiten (fett-kursiv), bei denen die Antidementiva mutmaßlich zielgerichtet im Wege des Off-Label-Use eingesetzt wurden (infolge im Beobachtungszeitraum wechselnder Kodierungen übersteigt die Zahl der Nennungen die Gruppengrößen)
|
ICD-Code |
ICD-Titel 2010/2011 |
Donepezil ILU |
Donepezil OLU |
Galantamin |
Galantamin |
Memantin ILU |
Memantin OLU |
Nicergolin ILU |
Nicergolin OLU |
Piracetam ILU |
Piracetam OLU |
Rivastigmin |
Rivastigmin OLU |
|
F00.0 |
Demenz bei Alzheimer-Krankheit, mit frühem Beginn (Typ 2) |
9,04% |
8,89% |
8,02% |
2,89% |
2,40% |
7,27% |
||||||
|
F00.1 |
Demenz bei Alzheimer-Krankheit, mit spätem Beginn (Typ 1) |
58,53% |
58,63% |
54,33% |
16,12% |
14,91% |
47,16% |
||||||
|
F00.2 |
Demenz bei Alzheimer-Krankheit, atypische oder gemischte Form |
19,78% |
22,69% |
21,98% |
5,67% |
5,34% |
17,88% |
||||||
|
F00.9 |
Demenz bei Alzheimer-Krankheit, nicht näher bezeichnet |
28,69% |
29,10% |
30,13% |
8,67% |
8,02% |
23,90% |
||||||
|
F01.0 |
Vaskuläre Demenz mit akutem Beginn |
1,37% |
1,51% |
1,65% |
2,02% |
1,49% |
1,78% |
2,05% |
1,69% |
1,43% |
1,99% |
||
|
F01.1 |
Multiinfarkt-Demenz |
2,99% |
3,42% |
3,37% |
4,16% |
3,81% |
4,47% |
5,27% |
5,65% |
3,27% |
4,47% |
||
|
F01.2 |
Subkortikale vaskuläre Demenz |
3,44% |
3,89% |
3,75% |
4,59% |
4,03% |
4,30% |
7,89% |
5,49% |
3,88% |
5,01% |
||
|
F01.3 |
Gemischte kortikale und subkortikale vaskuläre Demenz |
7,12% |
8,73% |
8,40% |
10,01% |
8,45% |
8,82% |
11,08% |
9,12% |
7,81% |
10,63% |
||
|
F01.8 |
Sonstige vaskuläre Demenz |
6,85% |
7,52% |
7,24% |
7,44% |
8,09% |
7,64% |
8,30% |
8,50% |
6,93% |
7,91% |
||
|
F01.9 |
Vaskuläre Demenz, nicht näher bezeichnet |
12,66% |
14,61% |
13,62% |
15,58% |
14,68% |
15,18% |
18,30% |
19,12% |
12,43% |
14,73% |
||
|
F02.0 |
Demenz bei Pick-Krankheit |
0,55% |
0,52% |
0,51% |
0,57% |
0,46% |
0,42% |
0,28% |
0,63% |
0,80% |
|||
|
F02.2 |
Demenz bei Chorea Huntington |
0,26% |
|||||||||||
|
F02.3 |
Demenz bei primärem Parkinson-Syndrom |
1,73% |
3,04% |
1,80% |
2,74% |
2,04% |
2,50% |
1,53% |
1,48% |
0,33% |
16,65% |
||
|
F02.8 |
Demenz bei anderenorts klassifizierten Krankheitsbildern |
1,53% |
1,65% |
1,54% |
1,69% |
1,50% |
1,51% |
1,08% |
0,24% |
3,06% |
2,32% |
||
|
F03 |
Nicht näher bezeichnete Demenz |
69,15% |
69,41% |
70,07% |
70,27% |
70,37% |
64,51% |
62,66% |
66,87% |
67,13% |
69,57% |
||
|
F04 |
Organisches amnestisches Syndrom, nicht durch Alkohol oder andere psychotrope Substanzen bedingt |
0,29% |
0,34% |
0,25% |
0,27% |
0,31% |
0,77% |
0,26% |
|||||
|
F06.3 |
Organische affektive Störungen |
5,59% |
2,91% |
6,98% |
3,56% |
6,25% |
3,23% |
3,05% |
1,09% |
3,02% |
1,09% |
7,59% |
4,07% |
|
F06.7 |
Leichte kognitive Störung |
5,09% |
6,11% |
4,78% |
6,29% |
3,45% |
4,59% |
8,79% |
7,12% |
8,55% |
7,94% |
5,53% |
6,53% |
|
F06.9 |
Nicht näher bezeichnete organische psychische Störung aufgrund einer Schädigung oder Funktionsstörung des Gehirns oder einer körperlichen Krankheit |
8,19% |
8,38% |
8,70% |
9,36% |
9,57% |
9,65% |
14,06% |
7,96% |
12,34% |
7,42% |
9,06% |
8,90% |
|
F07.0 |
Organische Persönlichkeitsstörung |
10,54% |
6,80% |
11,03% |
7,44% |
12,13% |
7,39% |
7,83% |
4,39% |
7,92% |
3,40% |
11,05% |
7,75% |
|
F07.2 |
Organisches Psychosyndrom nach Schädelhirntrauma |
0,35% |
0,44% |
0,36% |
0,24% |
0,41% |
0,56% |
0,25% |
0,58% |
0,60% |
0,40% |
0,50% |
|
|
F81.0 |
Lese- und Rechtschreibstörung |
0,07% |
|||||||||||
|
G10 |
Chorea Huntington |
0,08% |
0,49% |
||||||||||
|
G12.2 |
Motoneuron-Krankheit |
0,09% |
0,09% |
0,16% |
0,17% |
0,10% |
0,18% |
||||||
|
G20.0 |
Primäres Parkinson-Syndrom mit fehlender oder geringer Beeinträchtigung |
0,43% |
0,65% |
0,41% |
0,30% |
0,46% |
0,48% |
0,25% |
0,52% |
0,31% |
2,16% |
||
|
G20.00 |
Primäres Parkinson-Syndrom mit fehlender oder geringer Beeinträchtigung: Ohne Wirkungsfluktuation |
1,61% |
2,17% |
1,59% |
1,88% |
1,83% |
1,80% |
1,96% |
1,16% |
1,98% |
0,97% |
8,63% |
|
|
G20.01 |
Primäres Parkinson-Syndrom mit fehlender oder geringer Beeinträchtigung: Mit Wirkungsfluktuation |
0,31% |
0,34% |
0,27% |
0,20% |
0,34% |
0,26% |
0,37% |
0,18% |
1,82% |
|||
|
G20.1 |
Primäres Parkinson-Syndrom mit mäßiger bis schwerer Beeinträchtigung |
0,52% |
0,70% |
0,50% |
0,55% |
0,61% |
0,56% |
0,51% |
0,25% |
3,13% |
|||
|
G20.10 |
Primäres Parkinson-Syndrom mit mäßiger bis schwerer Beeinträchtigung: Ohne Wirkungsfluktuation |
2,10% |
2,87% |
2,00% |
2,65% |
2,46% |
2,37% |
2,11% |
0,91% |
2,13% |
0,98% |
13,50% |
|
|
G20.11 |
Primäres Parkinson-Syndrom mit mäßiger bis schwerer Beeinträchtigung: Mit Wirkungsfluktuation |
0,87% |
1,54% |
0,79% |
1,24% |
1,07% |
1,24% |
0,67% |
0,25% |
0,97% |
0,48% |
9,23% |
|
|
G20.2 |
Primäres Parkinson-Syndrom mit schwerster Beeinträchtigung |
0,11% |
0,10% |
0,06% |
0,77% |
||||||||
|
G20.20 |
Primäres Parkinson-Syndrom mit schwerster Beeinträchtigung: Ohne Wirkungsfluktuation |
0,39% |
0,55% |
0,45% |
0,46% |
0,46% |
0,45% |
0,24% |
0,13% |
3,09% |
|||
|
G20.21 |
Primäres Parkinson-Syndrom mit schwerster Beeinträchtigung: Mit Wirkungsfluktuation |
0,26% |
0,61% |
0,29% |
0,20% |
0,33% |
0,43% |
0,23% |
0,09% |
3,73% |
|||
|
G20.9 |
Primäres Parkinson-Syndrom, nicht näher bezeichnet |
0,72% |
1,07% |
0,76% |
0,98% |
0,88% |
0,92% |
0,28% |
0,84% |
0,43% |
4,50% |
||
|
G20.90 |
Primäres Parkinson-Syndrom, nicht näher bezeichnet: Ohne Wirkungsfluktuation |
6,53% |
8,66% |
6,34% |
7,82% |
7,66% |
8,10% |
6,65% |
3,82% |
6,77% |
3,26% |
28,96% |
|
|
G20.91 |
Primäres Parkinson-Syndrom, nicht näher bezeichnet: Mit Wirkungsfluktuation |
0,39% |
0,56% |
0,37% |
0,50% |
0,39% |
0,48% |
0,35% |
0,16% |
3,01% |
|||
|
G25.3 |
Myoklonus |
0,14% |
0,16% |
0,17% |
0,13% |
0,96% |
0,24% |
||||||
|
G30.0 |
Alzheimer-Krankheit mit frühem Beginn |
9,94% |
9,79% |
8,86% |
2,63% |
2,73% |
7,95% |
||||||
|
G30.1 |
Alzheimer-Krankheit mit spätem Beginn |
58,70% |
59,31% |
54,74% |
16,37% |
14,77% |
47,37% |
||||||
|
G30.8 |
Sonstige Alzheimer-Krankheit |
17,12% |
20,07% |
18,73% |
4,56% |
4,49% |
15,25% |
||||||
|
G30.9 |
Alzheimer-Krankheit, nicht näher bezeichnet |
41,84% |
41,66% |
43,41% |
12,28% |
11,73% |
33,72% |
||||||
|
G31.0 |
Umschriebene Hirnatrophie |
1,86% |
1,62% |
1,90% |
1,61% |
1,81% |
1,44% |
1,89% |
0,83% |
1,75% |
0,68% |
2,06% |
2,18% |
|
G31.1 |
Senile Degeneration des Gehirns, anderenorts nicht klassifiziert |
1,24% |
1,05% |
1,24% |
1,11% |
1,49% |
1,03% |
1,71% |
0,87% |
1,54% |
0,74% |
1,23% |
0,88% |
|
G31.82 |
Lewy-Körper-Demenz |
0,62% |
0,90% |
0,56% |
0,68% |
0,41% |
0,33% |
0,19% |
2,70% |
1,62% |
Tab. 4. Synopse einiger möglicher den Off-Label-Use von Nicergolin und Piracetam motivierenden ICD-10-GM-Codes und ihren Anteilen in den Gruppen (aus illustrativen Gründen werden auch die anderen Antidementiva gezeigt)
|
ICD-Code |
ICD-Titel 2010/2011 |
Donepezil ILU |
Donepezil OLU |
Galantamin ILU |
Galantamin OLU |
Memantin ILU |
Memantin OLU |
Nicergolin ILU |
Nicergolin OLU |
Piracetam ILU |
Piracetam OLU |
Rivastigmin ILU |
Rivastigmin OLU |
|
G43.0 |
Migräne ohne Aura |
0,32% |
0,23% |
0,23% |
0,19% |
0,29% |
0,28% |
0,58% |
1,16% |
0,50% |
1,03% |
0,33% |
|
|
G43.1 |
Migräne mit Aura |
0,21% |
0,15% |
0,24% |
0,21% |
0,19% |
0,19% |
0,90% |
0,42% |
1,03% |
0,23% |
0,30% |
|
|
G43.9 |
Migräne, nicht näher bezeichnet |
1,44% |
1,47% |
1,36% |
1,53% |
1,28% |
1,46% |
2,34% |
4,51% |
2,02% |
3,97% |
1,38% |
1,49% |
|
G44.2 |
Spannungskopfschmerz |
1,33% |
1,12% |
1,25% |
1,23% |
1,06% |
1,00% |
3,58% |
5,19% |
2,37% |
3,54% |
1,12% |
1,12% |
|
H34.8 |
Sonstiger Netzhautgefäßverschluss |
0,78% |
0,75% |
0,83% |
0,68% |
0,82% |
0,85% |
0,67% |
1,07% |
1,07% |
0,92% |
0,78% |
0,69% |
|
H81.0 |
Ménière-Krankheit |
0,57% |
0,46% |
0,51% |
0,32% |
0,47% |
0,48% |
0,73% |
1,32% |
0,89% |
1,54% |
0,54% |
0,31% |
|
H81.1 |
Benigner paroxysmaler Schwindel |
1,00% |
0,91% |
1,07% |
1,00% |
0,88% |
0,94% |
1,47% |
2,51% |
1,53% |
2,14% |
1,05% |
1,05% |
|
H81.2 |
Neuropathia vestibularis |
0,38% |
0,35% |
0,38% |
0,25% |
0,29% |
0,38% |
0,86% |
0,65% |
1,26% |
0,38% |
0,25% |
|
|
H81.3 |
Sonstiger peripherer Schwindel |
0,72% |
0,61% |
0,64% |
0,74% |
0,63% |
0,61% |
1,20% |
2,54% |
1,33% |
1,71% |
0,66% |
0,78% |
|
H81.4 |
Schwindel zentralen Ursprungs |
1,35% |
1,22% |
1,45% |
1,38% |
1,50% |
1,48% |
3,42% |
4,09% |
3,43% |
3,66% |
1,39% |
1,34% |
|
H81.8 |
Sonstige Störungen der Vestibularfunktion |
0,28% |
0,16% |
0,28% |
0,21% |
0,24% |
0,26% |
0,36% |
0,44% |
0,73% |
0,27% |
||
|
H81.9 |
Störung der Vestibularfunktion, nicht näher bezeichnet |
1,30% |
1,16% |
1,24% |
1,05% |
1,21% |
1,19% |
2,27% |
3,01% |
2,40% |
2,96% |
1,15% |
1,06% |
|
H91.2 |
Idiopathischer Hörsturz |
0,70% |
0,59% |
0,72% |
0,84% |
0,62% |
0,67% |
0,67% |
2,02% |
1,17% |
3,42% |
0,67% |
0,58% |
|
H93.1 |
Tinnitus aurium |
4,08% |
3,98% |
4,23% |
4,04% |
3,42% |
3,72% |
7,58% |
12,44% |
6,85% |
13,56% |
3,80% |
3,98% |
|
H93.2 |
Sonstige abnorme Hörempfindungen |
0,76% |
0,71% |
0,82% |
0,68% |
0,72% |
0,71% |
0,69% |
1,35% |
0,94% |
1,24% |
0,77% |
0,76% |
|
R42 |
Schwindel und Taumel |
12,58% |
12,27% |
12,42% |
12,46% |
12,25% |
12,70% |
21,18% |
22,95% |
19,61% |
20,30% |
12,76% |
12,29% |
ILU: In-Label-Use gemäß Operationalisierung; OLU: Off-Label-Use gemäß Operationalisierung
Donepezil, Galantamin, Rivastigmin und Memantin wurden wahrscheinlich mit etwa 28%, 26%, 18% bzw. 35% off Label verordnet bei Indikationen aus einem breiten Spektrum hirnorganischer psychischer Störungen, hier insbesondere vaskulären Demenzen, aber auch der sogenannten leichten kognitiven Störung. Jenseits der leichten kognitiven Störung konnte Off-Label-Use bezüglich des Schweregrads der manifesten Demenz nicht gewürdigt werden, weil die ICD-Codes für Schweregrade (U51.-) nicht in Verbindung mit den operationalisierenden Codes erfasst werden konnten und im Verhältnis zu letzteren nur bei einem Bruchteil der Patienten genutzt wurden (Abb. 2); Memantin wurde tendenziell und übereinstimmend mit der Zulassung eher bei höheren Schweregraden eingesetzt. Auffällig war die Dominanz der „nicht näher bezeichneten Demenz“ (F03) (in vergleichbarem Maße auch bei In-Label-Use) als Symptom eines allgemeinen Trends zu unspezifischem Kodieren (Tab. 3); formallogisch lässt sich mit diesem unspezifischen Code In-Label-Use nicht rechtfertigen. Es war nicht auszuschließen, dass sich hinter Code F03 In-Label-Use verbarg, gleichzeitig aber konnte F03 („nicht näher bezeichnete Demenz“) bei denjenigen Patienten kodiert worden sein, bei denen ein den In-Label-Use operationalisierender Code genannt worden war, sodass eine Aufklärung unmöglich war. Auffällig war auch, wie häufig in der In-Label-Gruppe Diagnosen kodiert worden waren, die formallogisch mit den zugelassenen Anwendungsgebieten nicht kompatibel waren (Tab. 3), was also nur durch Diagnosewechsel erklärbar war.
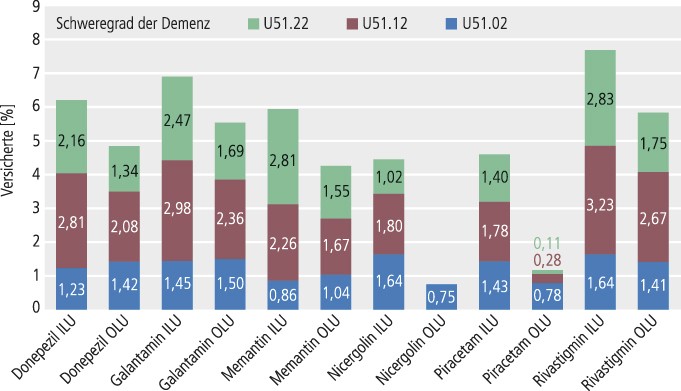
Abb. 2. Behandlung mit Antidementiva: Schweregrade; U51.02: Keine oder leichte kognitive Funktionseinschränkung: MMSE: 24–30 Punkte, U51.12: Mittlere kognitive Funktionseinschränkung: MMSE: 17–23 Punkte, U51.22: Schwere kognitive Funktionseinschränkung: MMSE: 0–16 Punkte (nur bei einem Bruchteil der Patienten wurde die Möglichkeit, mittels Codes aus dem Bereich U51.- den Schwergrad der kognitiven Beeinträchtigung abzubilden, genutzt)
Nicergolin und Memantin wurden wahrscheinlich mit etwa 50% bzw. 62% off Label verordnet, primär bei Indikationen aus einem breiten Spektrum von Krankheiten, die traditionell mit Durchblutungsstörungen in Verbindung gebracht werden, wie zum Beispiel Hörsturz und Tinnitus (Tab. 4). Es war nicht zu ermessen, welchem Anteil eine – durch Nicht-Kodieren der eigentlich indizierenden zugelassenen Nebendiagnose – unvollständige Kodierung oder unscharfe Kodierungen zugrunde lag. Somit musste offen bleiben, in welchem Umfang diese gefundenen Indikationen den Off-Label-Use aufklärten.
Formallogisch kann nicht davon ausgegangen werden, nur die in der OLU-Gruppe vorkommenden oder häufigeren Diagnosen kämen als Motiv für einen Off-Label-Use in Frage, denn beispielsweise eine Komorbidität in der ILU-Gruppe kann sehr wohl in der OLU-Gruppe den Off-Label-Use initiiert haben.
Für überzufällig häufige somatische Komorbiditäten wurden keine eindeutigen Signale (im Sinne der Pharmakovigilanz) gefunden (Tab. 5). Übelkeit und Erbrechen waren konform mit den Erwartungen unter Memantin, Nicergolin und Piracetam etwas seltener. Bei der Interpretation der Unterschiede zwischen den Wirkstoffen (Tab. 5) müssen unter anderem die Altersunterschiede als konfundierende Variable berücksichtigt werden. Bei den psychischen Komorbiditäten (Tab. 6) imponierten unspezifisch kodierte Depressionen mit einer Rate von 22% bis 24% ohne bedeutsame Unterschiede zwischen den Wirkstoffen. Mit welcher Rationalität Codes zu somatoformen Störungen neben den indizierenden Diagnosen kodiert worden waren, erlaubte die Datenbasis nicht zu klären.
Tab. 5. Häufigkeiten (Auszug) von ICD-Codes zur somatischen Komorbidität (die Anteile der Codes zu Neubildungen wurden aufsummiert, obwohl sie nicht durchgehend disjunkt sind. Unspezifische Codes werden berichtet, wenn sie im entsprechenden Code-Bereich am häufigsten genannt wurden
|
ICD-Code |
ICD-Titel 2010/2011 |
Donepezil ILU |
Donepezil OLU |
Galantamin ILU |
Galantamin OLU |
Memantin ILU |
Memantin OLU |
Nicergolin ILU |
Nicergolin OLU |
Piracetam ILU |
Piracetam OLU |
Rivastigmin ILU |
Rivastigmin OLU |
|
C00 bis C97 |
„Bösartige Neubildungen“ |
29,83% |
25,15% |
28,89% |
22,56% |
29,62% |
27,32% |
19,48% |
24,86% |
33,66% |
31,07% |
30,50% |
20,03% |
|
D46.9 |
Myelodysplastisches Syndrom, nicht näher bezeichnet |
0,25% |
0,11% |
0,22% |
0,22% |
0,21% |
0,27% |
0,17% |
0,28% |
||||
|
D61.9 |
Aplastische Anämie, nicht näher bezeichnet |
0,15% |
0,21% |
0,16% |
0,17% |
0,18% |
0,17% |
0,14% |
0,13% |
||||
|
D69.61 |
Thrombozytopenie, nicht näher bezeichnet: Nicht als transfusionsrefraktär bezeichnet |
0,74% |
0,81% |
0,74% |
0,73% |
0,81% |
0,84% |
0,70% |
0,86% |
0,66% |
0,88% |
0,74% |
|
|
D70.1 |
Arzneimittelinduzierte Agranulozytose und Neutropenie |
||||||||||||
|
D70.3 |
Sonstige Agranulozytose |
0,09% |
0,08% |
0,11% |
0,09% |
0,11% |
0,17% |
||||||
|
E03.9 |
Hypothyreose, nicht näher bezeichnet |
9,05% |
8,11% |
8,58% |
8,31% |
8,66% |
7,69% |
9,63% |
8,83% |
8,58% |
8,03% |
9,03% |
8,48% |
|
E11.90 |
Nicht primär insulinabhängiger Diabetes mellitus (Typ-2-Diabetes): Ohne Komplikationen: Nicht als entgleist bezeichnet |
26,51% |
27,01% |
27,46% |
28,61% |
28,64% |
29,01% |
28,89% |
24,44% |
30,85% |
24,51% |
27,42% |
28,17% |
|
E66.99 |
Adipositas, nicht näher bezeichnet: Body-Mass-Index (BMI) nicht näher bezeichnet |
4,98% |
5,50% |
5,05% |
5,83% |
4,92% |
5,70% |
6,56% |
8,38% |
6,51% |
7,94% |
5,22% |
5,38% |
|
E78.0 |
Reine Hypercholesterinämie |
26,23% |
24,16% |
25,41% |
23,07% |
23,95% |
22,84% |
27,96% |
27,36% |
25,74% |
24,94% |
25,41% |
24,24% |
|
E78.1 |
Reine Hypertriglyzeridämie |
1,17% |
1,01% |
1,09% |
0,96% |
1,15% |
1,27% |
1,93% |
1,73% |
1,44% |
1,53% |
1,15% |
1,28% |
|
E78.2 |
Gemischte Hyperlipidämie |
8,90% |
8,44% |
9,33% |
8,73% |
8,79% |
8,67% |
11,14% |
9,78% |
11,37% |
10,09% |
9,33% |
8,88% |
|
E78.5 |
Hyperlipidämie, nicht näher bezeichnet |
20,62% |
19,62% |
20,68% |
19,77% |
19,89% |
19,48% |
23,84% |
23,01% |
23,35% |
22,02% |
19,92% |
19,54% |
|
E79.0 |
Hyperurikämie ohne Zeichen von entzündlicher Arthritis oder tophischer Gicht |
13,50% |
14,14% |
13,59% |
13,80% |
14,17% |
14,75% |
20,80% |
21,17% |
16,61% |
14,23% |
13,94% |
14,89% |
|
H35.9 |
Affektion der Netzhaut, nicht näher bezeichnet |
1,35% |
1,08% |
1,35% |
1,19% |
1,15% |
1,17% |
1,78% |
2,06% |
1,68% |
1,85% |
1,38% |
1,16% |
|
H36.0 |
Retinopathia diabetica |
2,59% |
2,44% |
2,66% |
2,62% |
2,69% |
2,88% |
3,62% |
3,32% |
3,61% |
3,10% |
2,63% |
2,69% |
|
H40.1 |
Primäres Weitwinkelglaukom |
5,45% |
5,05% |
5,63% |
5,16% |
5,26% |
5,13% |
7,59% |
7,17% |
6,86% |
6,35% |
5,46% |
4,88% |
|
H40.2 |
Primäres Engwinkelglaukom |
0,65% |
0,48% |
0,63% |
0,56% |
0,63% |
0,57% |
0,55% |
0,69% |
0,79% |
0,72% |
0,70% |
0,51% |
|
H40.9 |
Glaukom, nicht näher bezeichnet |
5,97% |
5,54% |
6,31% |
5,72% |
6,05% |
5,91% |
7,52% |
6,97% |
7,32% |
6,45% |
6,17% |
5,59% |
|
I10.00 |
Benigne essenzielle Hypertonie: Ohne Angabe einer hypertensiven Krise |
39,43% |
36,89% |
40,53% |
37,05% |
39,59% |
35,80% |
42,04% |
33,39% |
42,15% |
32,10% |
42,24% |
38,60% |
|
I10.90 |
Essenzielle Hypertonie, nicht näher bezeichnet: Ohne Angabe einer hypertensiven Krise |
65,14% |
64,42% |
66,38% |
65,88% |
65,75% |
64,99% |
69,57% |
66,25% |
68,80% |
61,71% |
64,97% |
64,99% |
|
I25.9 |
Chronische ischämische Herzkrankheit, nicht näher bezeichnet |
23,44% |
23,32% |
25,11% |
25,41% |
25,59% |
24,83% |
29,43% |
23,82% |
30,51% |
23,67% |
24,28% |
23,41% |
|
I35.0 |
Aortenklappenstenose |
2,44% |
2,40% |
2,52% |
2,37% |
2,43% |
2,27% |
2,87% |
1,72% |
2,61% |
1,85% |
2,34% |
2,41% |
|
I50.9 |
Herzinsuffizienz, nicht näher bezeichnet |
16,16% |
17,31% |
17,17% |
17,98% |
19,19% |
18,52% |
17,73% |
11,66% |
18,39% |
11,17% |
17,11% |
17,30% |
|
J44.99 |
Chronische obstruktive Lungenkrankheit, nicht näher bezeichnet: FEV1 nicht näher bezeichnet |
6,64% |
6,67% |
6,78% |
7,60% |
6,92% |
7,12% |
8,88% |
8,30% |
8,75% |
7,71% |
6,45% |
7,35% |
|
K21.0 |
Gastroösophageale Refluxkrankheit mit Ösophagitis |
10,13% |
9,72% |
10,18% |
10,81% |
10,59% |
10,18% |
13,61% |
14,77% |
13,11% |
12,95% |
11,15% |
9,36% |
|
K59.0 |
Obstipation |
10,41% |
9,73% |
11,37% |
10,47% |
14,31% |
11,83% |
11,43% |
6,86% |
10,93% |
6,28% |
15,49% |
10,80% |
|
K71.9 |
Toxische Leberkrankheit, nicht näher bezeichnet |
0,27% |
0,30% |
0,27% |
0,19% |
0,24% |
0,31% |
0,33% |
0,35% |
0,26% |
0,22% |
||
|
K76.9 |
Leberkrankheit, nicht näher bezeichnet |
3,44% |
3,41% |
3,38% |
3,54% |
3,42% |
3,49% |
4,60% |
4,86% |
4,12% |
4,29% |
3,64% |
3,54% |
|
L89.14 |
Dekubitus 2. Grades: Kreuzbein |
1,23% |
1,08% |
1,24% |
1,35% |
1,56% |
1,23% |
0,65% |
1,00% |
0,27% |
1,65% |
1,03% |
|
|
L89.24 |
Dekubitus 3. Grades: Kreuzbein |
0,32% |
0,16% |
0,36% |
0,23% |
0,48% |
0,34% |
0,31% |
0,10% |
0,46% |
0,22% |
||
|
L89.99 |
Dekubitus, Grad nicht näher bezeichnet: Sonstige und nicht näher bezeichnete Lokalisationen |
1,77% |
1,68% |
2,15% |
1,90% |
2,75% |
2,18% |
0,76% |
0,27% |
1,31% |
0,43% |
2,46% |
1,38% |
|
M15.9 |
Polyarthrose, nicht näher bezeichnet |
6,46% |
6,39% |
6,58% |
6,42% |
6,20% |
6,19% |
8,25% |
7,47% |
7,30% |
6,35% |
5,89% |
6,47% |
|
M16.9 |
Koxarthrose, nicht näher bezeichnet |
11,68% |
11,34% |
12,26% |
12,01% |
11,48% |
11,09% |
15,15% |
13,96% |
13,77% |
11,99% |
11,32% |
10,83% |
|
M17.9 |
Gonarthrose, nicht näher bezeichnet |
17,36% |
17,24% |
17,58% |
17,38% |
16,80% |
17,04% |
21,51% |
22,02% |
20,75% |
19,29% |
16,54% |
15,87% |
|
M81.99 |
Osteoporose, nicht näher bezeichnet: Nicht näher bezeichnete Lokalisationen |
13,90% |
13,65% |
14,48% |
13,83% |
14,08% |
13,65% |
16,17% |
14,63% |
14,93% |
11,83% |
13,71% |
13,29% |
|
N18.3 |
Chronische Nierenkrankheit, Stadium 3 |
8,47% |
8,13% |
8,60% |
8,06% |
9,36% |
8,24% |
8,41% |
4,89% |
8,76% |
4,60% |
9,00% |
8,76% |
|
N19 |
Nicht näher bezeichnete Niereninsuffizienz |
6,90% |
6,86% |
6,93% |
6,93% |
7,47% |
7,30% |
7,34% |
5,32% |
7,08% |
4,60% |
7,31% |
6,88% |
|
N40 |
Prostatahyperplasie |
15,29% |
15,10% |
15,17% |
14,85% |
14,99% |
15,16% |
19,19% |
16,50% |
19,88% |
16,39% |
19,24% |
14,19% |
|
R00.1 |
Bradykardie, nicht näher bezeichnet |
2,62% |
2,23% |
2,49% |
2,20% |
2,24% |
2,02% |
2,18% |
1,91% |
2,33% |
1,60% |
2,49% |
2,18% |
|
R11 |
Übelkeit und Erbrechen |
6,04% |
5,46% |
6,85% |
6,05% |
5,76% |
5,19% |
5,34% |
4,06% |
5,33% |
4,03% |
7,52% |
6,28% |
|
R15 |
Stuhlinkontinenz |
16,03% |
12,76% |
16,74% |
13,28% |
20,49% |
14,46% |
11,26% |
2,68% |
12,73% |
3,12% |
19,58% |
13,83% |
|
R26.8 |
Sonstige und nicht näher bezeichnete Störungen des Ganges und der Mobilität |
11,27% |
10,33% |
11,00% |
10,45% |
12,12% |
10,32% |
11,14% |
5,87% |
11,19% |
5,62% |
14,57% |
11,47% |
|
S72.00 |
Schenkelhalsfraktur: Teil nicht näher bezeichnet |
2,23% |
1,91% |
2,57% |
2,34% |
2,85% |
2,14% |
1,34% |
0,45% |
1,60% |
0,65% |
2,58% |
2,35% |
|
S72.9 |
Fraktur des Femurs, Teil nicht näher bezeichnet |
1,22% |
1,08% |
1,42% |
1,24% |
1,40% |
1,25% |
0,78% |
0,32% |
0,85% |
0,40% |
1,38% |
1,36% |
|
Z92.1 |
Dauertherapie (gegenwärtig) mit Antikoagulanzien in der Eigenanamnese |
10,84% |
12,05% |
10,66% |
11,81% |
11,35% |
12,50% |
11,85% |
9,90% |
12,92% |
10,31% |
11,77% |
12,92% |
|
Z95.0 |
Vorhandensein eines implantierten Herzschrittmachers oder eines implantierten Kardiodefibrillators |
5,19% |
5,21% |
5,13% |
5,34% |
5,37% |
5,50% |
5,16% |
3,50% |
5,75% |
3,72% |
5,47% |
5,72% |
|
Z96.1 |
Vorhandensein eines intraokularen Linsenimplantats |
13,08% |
12,35% |
13,43% |
12,33% |
12,12% |
12,09% |
16,86% |
16,24% |
16,01% |
13,88% |
12,83% |
11,27% |
|
Z96.6 |
Vorhandensein von orthopädischen Gelenkimplantaten |
9,05% |
8,37% |
9,24% |
9,11% |
8,67% |
8,55% |
10,41% |
9,02% |
9,48% |
7,67% |
9,37% |
8,51% |
ILU: In-Label-Use gemäß Operationalisierung; OLU: Off-Label-Use gemäß Operationalisierung
Tab. 6. Häufigkeiten (Auszug) von ICD-Codes zur psychischen Komorbidität
|
ICD-Code |
ICD-Titel 2010/2011 |
Donepezil ILU |
Donepezil OLU |
Galantamin ILU |
Galantamin OLU |
Memantin ILU |
Memantin OLU |
Nicergolin ILU |
Nicergolin OLU |
Piracetam ILU |
Piracetam OLU |
Rivastigmin ILU |
Rivastigmin OLU |
|
F32.0 |
Leichte depressive Episode |
3,51% |
2,85% |
3,65% |
2,80% |
3,06% |
2,61% |
3,92% |
3,04% |
3,54% |
3,07% |
3,78% |
3,06% |
|
F32.1 |
Mittelgradige depressive Episode |
9,25% |
7,19% |
9,32% |
7,59% |
8,12% |
6,37% |
7,76% |
6,82% |
8,25% |
7,10% |
10,15% |
7,73% |
|
F32.2 |
Schwere depressive Episode ohne psychotische Symptome |
4,94% |
4,58% |
5,14% |
5,55% |
4,49% |
3,91% |
4,49% |
4,05% |
4,17% |
3,80% |
5,75% |
5,34% |
|
F32.3 |
Schwere depressive Episode mit psychotischen Symptomen |
1,16% |
1,02% |
1,20% |
1,19% |
1,10% |
0,85% |
0,80% |
0,59% |
0,84% |
0,66% |
1,36% |
1,29% |
|
F32.8 |
Sonstige depressive Episoden |
4,48% |
4,35% |
4,46% |
4,37% |
4,16% |
3,97% |
5,87% |
4,76% |
4,88% |
3,91% |
4,57% |
4,05% |
|
F32.9 |
Depressive Episode, nicht näher bezeichnet |
23,29% |
22,80% |
23,66% |
23,48% |
21,98% |
21,87% |
24,69% |
23,04% |
23,83% |
21,57% |
24,72% |
23,26% |
|
F33.0 |
Rezidivierende depressive Störung, gegenwärtig leichte Episode |
1,11% |
0,94% |
1,16% |
0,85% |
0,94% |
0,82% |
1,11% |
1,55% |
1,07% |
1,07% |
1,20% |
0,90% |
|
F33.1 |
Rezidivierende depressive Störung, gegenwärtig mittelgradige Episode |
3,24% |
2,68% |
3,43% |
2,75% |
3,01% |
2,59% |
3,56% |
3,08% |
2,96% |
3,18% |
3,69% |
2,97% |
|
F33.2 |
Rezidivierende depressive Störung, gegenwärtig schwere Episode ohne psychotische Symptome |
2,23% |
2,41% |
2,37% |
3,24% |
2,08% |
2,09% |
2,73% |
2,85% |
1,99% |
2,03% |
2,74% |
2,98% |
|
F33.3 |
Rezidivierende depressive Störung, gegenwärtig schwere Episode mit psychotischen Symptomen |
0,64% |
0,69% |
0,74% |
0,98% |
0,59% |
0,57% |
0,25% |
0,48% |
0,44% |
0,90% |
0,69% |
|
|
F33.4 |
Rezidivierende depressive Störung, gegenwärtig remittiert |
0,54% |
0,41% |
0,59% |
0,39% |
0,43% |
0,42% |
0,48% |
0,42% |
0,45% |
0,54% |
0,43% |
|
|
F33.8 |
Sonstige rezidivierende depressive Störungen |
0,91% |
0,78% |
0,89% |
0,70% |
0,83% |
0,73% |
1,13% |
0,84% |
1,03% |
0,71% |
1,07% |
0,90% |
|
F33.9 |
Rezidivierende depressive Störung, nicht näher bezeichnet |
3,37% |
3,32% |
3,40% |
3,24% |
3,25% |
3,15% |
3,85% |
3,78% |
3,84% |
3,43% |
3,71% |
3,24% |
|
F34.1 |
Dysthymia |
2,55% |
2,51% |
2,34% |
2,29% |
2,46% |
2,66% |
4,98% |
5,89% |
3,44% |
4,21% |
2,91% |
2,62% |
|
F41.0 |
Panikstörung (episodisch paroxysmale Angst) |
1,06% |
0,88% |
1,14% |
1,01% |
0,92% |
0,81% |
0,82% |
1,73% |
1,15% |
1,51% |
1,21% |
1,07% |
|
F41.1 |
Generalisierte Angststörung |
1,97% |
1,75% |
2,05% |
2,12% |
2,01% |
1,70% |
2,58% |
2,47% |
2,40% |
2,38% |
2,35% |
2,02% |
|
F41.2 |
Angst und depressive Störung, gemischt |
2,93% |
2,57% |
3,01% |
2,75% |
2,62% |
2,35% |
4,03% |
4,97% |
3,23% |
3,89% |
3,16% |
2,75% |
|
F41.9 |
Angststörung, nicht näher bezeichnet |
2,35% |
2,20% |
2,62% |
2,11% |
2,24% |
2,05% |
2,74% |
3,09% |
2,77% |
2,76% |
2,56% |
2,23% |
|
F43.2 |
Anpassungsstörungen |
2,81% |
2,56% |
3,15% |
3,59% |
2,41% |
2,33% |
3,69% |
4,15% |
3,16% |
4,42% |
3,04% |
2,65% |
|
F45.0 |
Somatisierungsstörung |
1,71% |
1,58% |
1,61% |
1,96% |
1,33% |
1,42% |
3,47% |
4,51% |
2,62% |
3,88% |
1,51% |
1,43% |
|
F45.9 |
Somatoforme Störung, nicht näher bezeichnet |
5,92% |
5,72% |
5,85% |
5,92% |
5,23% |
5,61% |
9,45% |
11,16% |
8,33% |
10,16% |
5,74% |
5,56% |
ILU: In-Label-Use gemäß Operationalisierung; OLU: Off-Label-Use gemäß Operationalisierung
Anhand der im Arzneiverordnungsreport 2011 und 2012 für die Jahre 2010 und 2011 bereitgestellten Daten zu den zulasten der GKV verordneten definierten Tagesdosen (DDD) konnten aus den hier erhobenen Daten erstmals die mittleren Behandlungsdauern innerhalb des zweijährigen Beobachtungszeitraums näherungsweise abgeleitet werden (Abb. 3). Gemäß Definition der WHO (und der amtlichen ATC-Klassifikation) entspricht die DDD der empfohlenen durchschnittlichen Tagesdosis, die mit der tatsächlichen Tagesdosis in der Verordnungspraxis nicht exakt übereinstimmen muss, sodass die genannten Behandlungsdauern nur Näherungswerte darstellen können.
Diskussion
In diesem Projekt werden Routinedaten der Krankenkassen als Vollerfassung aller gesetzlich Krankenversicherten – anhand der Daten nach §§303a ff. SGB V – zur Frage des Off-Label-Use und für Zwecke der Pharmakovigilanz genutzt. Das Beispiel der hier dargestellten Antidementiva belegt erneut die Praktikabilität dieses Forschungsansatzes. Bei der Interpretation der Ergebnisse müssen selbstverständlich die daraus resultierenden Schwächen der Daten berücksichtigt werden.
Rekonstruktionen waren nur für Nicergolin und Piracetam notwendig, weil deren historisch gewachsene, breit formulierte Anwendungsgebiete unvollständig operationalisiert worden waren. Rekonstruktionen erlauben nur semiquantitative Schätzungen, auch infolge der Datenschutzregelung. Danach belief sich der Off-Label-Use von Nicergolin auf etwa 50%, der von Piracetam auf etwa 62%. Der Off-Label-Use der Antidementiva galt insbesondere vaskulären Demenzen, bei Nicergolin und Piracetam auch Krankheiten, die traditionell mit „Durchblutungsstörungen“ in Zusammenhang gebracht werden [8, 13]. Für die vaskulären Demenzen existieren keine zugelassenen Arzneimittel. Donepezil, Galantamin, Memantin und Rivastigmin wurden bei vaskulärer Demenz mit uneindeutigen Ergebnissen untersucht [10]. Demenzen vom Alzheimer-Typ und vaskuläre Demenzen sind nicht immer eindeutig zu differenzieren, insbesondere wenn sich die Differenzialdiagnostik auf klinische Kriterien beschränken muss. Vaskuläre Risikofaktoren sind als Risikofaktoren auch für Alzheimer-Demenzen etabliert. Bei 30 bis 60% der klinisch als Alzheimer-Demenz imponierenden Patienten finden sich vaskuläre Läsionen. Umgekehrt findet sich bei 40 bis 80% der klinisch als vaskuläre Demenz imponierenden Patienten histologisch Alzheimer-Pathologie [2]. Die verfügbaren (hier untersuchten) Antidementiva mit Zulassung bei Alzheimer-Demenzen entfalten nur symptomatische Wirkungen, beeinflussen also nicht die Krankheitsprogression. Diese Argumente mögen ihren Off-Label-Use bei vaskulären Demenzen nahelegen. Das kann aber an den besonderen Implikationen des Off-Label-Use nichts ändern.
Bei der Erwerbstätigenbefragung der DAK-Gesundheit 2014 haben bedeutsame Anteile der Befragten angegeben, unter anderem Antidementiva im Sinne eines Neuroenhancement (also ohne medizinische Indikation) off Label eingesetzt zu haben [3]. Zwar spiegelt sich das nicht erkennbar in den Verordnungen zu Lasten der gesetzlichen Krankenversicherung im Beobachtungszeitraum 2010 bis 2011 wider; indem sich der Off-Label-Use aber unter anderem wegen der Datenschutzvorgaben nur näherungsweise quantifizieren ließ, schließen die Ergebnisse nicht aus, dass Off-Label-Use zwecks Neuroenhancement auch in gewissem Umfang zu Lasten der GKV stattgefunden haben könnte.
Die Zahl der Demenzkranken in Deutschland wird auf etwa 1,5 Millionen geschätzt [1]. Es wäre unzulässig, die Zahl der mit den einzelnen Antidementiva behandelten Versicherten zu addieren, um eine Behandlungsprävalenz zu ermitteln, denn einzelne Versicherte konnten in den Jahren 2010 und 2011 mit mehreren der Wirkstoffe behandelt worden sein. Ignoriert man dies und den Anteil des Einsatzes im Wege des Off-Label-Use bei den anderen Diagnosen, dann wären höchstens etwa 560000 Versicherte behandelt worden. Damit würde die Behandlungsprävalenz mit diesen Antidementiva höchstens ein Drittel der Betroffenen erreichen.
Die Literaturdaten zur Assoziation von Demenz und Depression variieren in einem Maße (etwa 10% bis 70%), das keine Schlussfolgerungen erlaubt [9]; die hier gefundene Komorbidität bei etwa einem Viertel der Patienten fügt sich aber unschwer ein.
Dass sich bei diesen Antidementiva keine differenziell häufigen somatischen Komorbiditäten fanden, darf als Signal auf Fehlen unerwarteter Risiken im Sinne der Pharmakovigilanz gewertet werden; die Datenbasis erlaubt aber nicht, differenzielle Risiken auszuschließen. Übelkeit und Erbrechen waren konform mit den Erwartungen unter Memantin, Nicergolin und Piracetam – etwas – seltener.
Die hier erstmalig präsentierbaren durchschnittlichen Behandlungsdauern (Abb. 3) zum Beispiel im Sinne der Versorgungsqualität zu bewerten, kann nicht Gegenstand dieses Berichts sein.
Die Datenlage zu den gefundenen seltenen Krankheiten frontotemporale Demenzen bzw. Chorea Huntington ist enttäuschend. Die zwei bisherigen randomisierten Studien mit Memantin ergaben keinen Nutzen [11], die drei Cholinesterasehemmer wurden bisher nicht in randomisierten Studien untersucht [6]. Bei Chorea Huntington fehlen für Memantin randomisierte Studien und für Donepezil zeigten zwei randomisierte Studie keinen Nutzen und für Rivastigmin und Galantamin nur Pilotstudien marginale Wirkungen [7, 12].
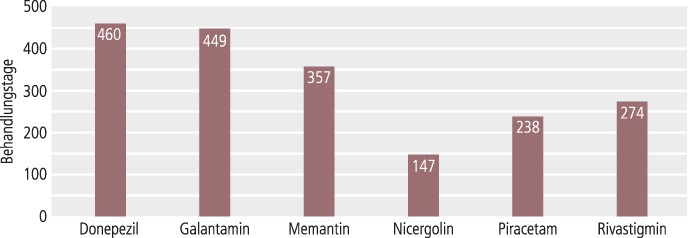
Abb. 3. Behandlungstage mit Antidementiva im Beobachtungszeitraum 2010 und 2011 auf Basis der in diesen Jahren gemäß Arzneiverordnungsreport 2011 und 2012 verordneten definierten Tagesdosen (DDD) und der in diesem Projekt ermittelten Anzahl jeweils behandelter Versicherter der gesetzlichen Krankenversicherung
Danksagung
Dem Bundesministerium für Gesundheit wird nachdrücklich für die finanzielle Unterstützung des Projekts gedankt. Herrn Prof. Dr. W. Schwerdtfeger, früherer Präsident des BfArM, wird herzlich für die Unterstützung bei der Initiierung dieses Projekts gedankt. Herrn Dr. Jochen Dreß und Herrn Dr. Michael Schopen, Deutsches Institut für Medizinische Dokumentation und Information (DIMDI), gilt besonderer Dank für die Kooperation bei der Entwicklung der Datenbankabfrageskripte und deren Anwendung.
Interessenkonflikterklärung
J.F. hat in den letzten fünf Jahren Honorare für Beratertätigkeit von Amgen, Janssen, Lilly, Lundbeck, Nestlé, Novartis, Pfizer, Roche, St. Jude Medical, 3M, Sanvartis, Teva und dem Verband der privaten Krankenversicherung e.V. erhalten.
Die anderen Autoren geben an, keine Interessenkonflikte zu haben.
Literatur
1. Alzheimer Europe, Luxembourg. EuroCoDe. Prevalence of dementia in Europe. www.alzheimer-europe.org/EN/Research/European-Collaboration-on-dementia/Prevalence-of-dementia/Prevalence-of-dementia-in-Europe (Zugriff am 28.04.2016).
2. Bowirrat A, Bisharat B, Nseir W, Omary M, Yassin M. Candidate biomarkers and CSF profiles for Alzheimer’s disease and CADASIL. Int J Brain Cognitive Sci 2015;4: 15–27.
3. DAK-Gesundheitsreport 2015. www.dak.de/dak/download/gesundheitsreport-2015-update-doping-am-arbeitsplatz-1587940.pdf (Zugriff am 05.05.2017).
4. Fritze J, Riedel C, Escherich A, Beinlich P, et al. Thrombozytenaggregationshemmer: Spektrum der Verordnung und Morbidität. Psychopharmakotherapie 2017;24:8–20.
5. Fritze J, Riedel C, Escherich A, Beinlich P, et al. Psychostimulanzien: Spektrum der Verordnung und Morbidität. Psychopharmakotherapie 2017;24:56–62.
6. Kerchner GA, Tartaglia MC, Boxer AL. Abhorring the vacuum: use of Alzheimer’s disease medications in frontotemporal dementia. Expert Rev Neurother 2011;11:709–17.
7. Li Y1, Hai S, Zhou Y, Dong BR. Cholinesterase inhibitors for rarer dementias associated with neurological conditions. Cochrane Database Syst Rev 2015;3(3):CD009444.
8. Malykh AG, Sadaie MR. Piracetam and piracetam-like drugs: from basic science to novel clinical applications to CNS disorders. Drugs 2010;70:287–312.
9. Muliyala KP, Varghese M. The complex relationship between depression and dementia. Ann Indian Acad Neurol 2010;13(Suppl 2):S69–S73.
10. Raina P, Santaguida P, Ismaila A, Patterson C, et al. Effectiveness of cholinesterase inhibitors and memantine for treating dementia: evidence review for a clinical practice guideline. Ann Intern Med 2008;148:379–97.
11. Vercelletto M, Boutoleau-Bretonnière C, Volteau C, Puel M, et al.; French research network on Frontotemporal dementia. Memantine in behavioral variant frontotemporal dementia: negative results. J Alzheimers Dis 2011;23:749–59.
12. Videnovic A. Treatment of Huntington disease. Curr Treat Options Neurol 2013;15: 424–38.
13 Winblad B, Fioravanti M, Dolezal T, Logina I, et al. Therapeutic use of nicergoline. Clin Drug Investig 2008;28:533–52.
Prof. Dr. med. Jürgen Fritze, Asternweg 65, 50259 Pulheim, E-Mail: juergen.fritze@dgn.de Dr. med. Claudia Riedel, Angelika Escherich, Peggy Beinlich, Prof. Dr. Karl Broich, Priv.-Doz. Dr. Thomas Sudhop, Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), Kurt-Georg-Kiesinger-Allee 3, 53175 Bonn
Antidementia drugs: Spectra of prescribing and morbidities
In an ongoing project supported by the Federal Ministry of Health (BMG) off-label-use of pharmaceuticals with high prescription rates is investigated in a database comprising all citizens covered by public sick funds, i. e. almost 90% of the German population. The focus is on prevalences and indications as well as on the identification of off-label-use specifically addressing rare diseases in the context of the Action Plan of the National Action League for People with Rare Diseases (NAMSE). In the years 2010 through 2011 among antidementia drugs donepezil, galantamine, memantine, nicergoline, piracetam and rivastigmine had been used off-label in 28%, 26%, 35%, 50%, 62%, and 18%, respectively, donepezil, galantamine, memantine, and rivastigmine essentially addressing vascular dementias and nicergoline and piracetam additionally addressing disorders supposedly resulting from „deficient circulation“ like tinnitus and sudden loss of hearing. Far more than 99% had exclusively been treated as outpatients. Off-label-use due to violation of age limits was rare. Beyond the diagnoses putatively underlying in- and off-label-use, respectively, there were no comorbidities specifically attributable to the antidementia drugs. Rare diseases detected as putative reasons for off-label-use included frontotemporal dementias, possibly also associated with amyotrophic lateral sclerosis, and Huntington’s chorea.
Key words: antidementia drugs, donepezil, galantamine, memantine, nicergoline, piracetam, rivastigmine, off-label-use, National Action League for People with Rare Diseases, NAMSE
Psychopharmakotherapie 2017; 24(03)
