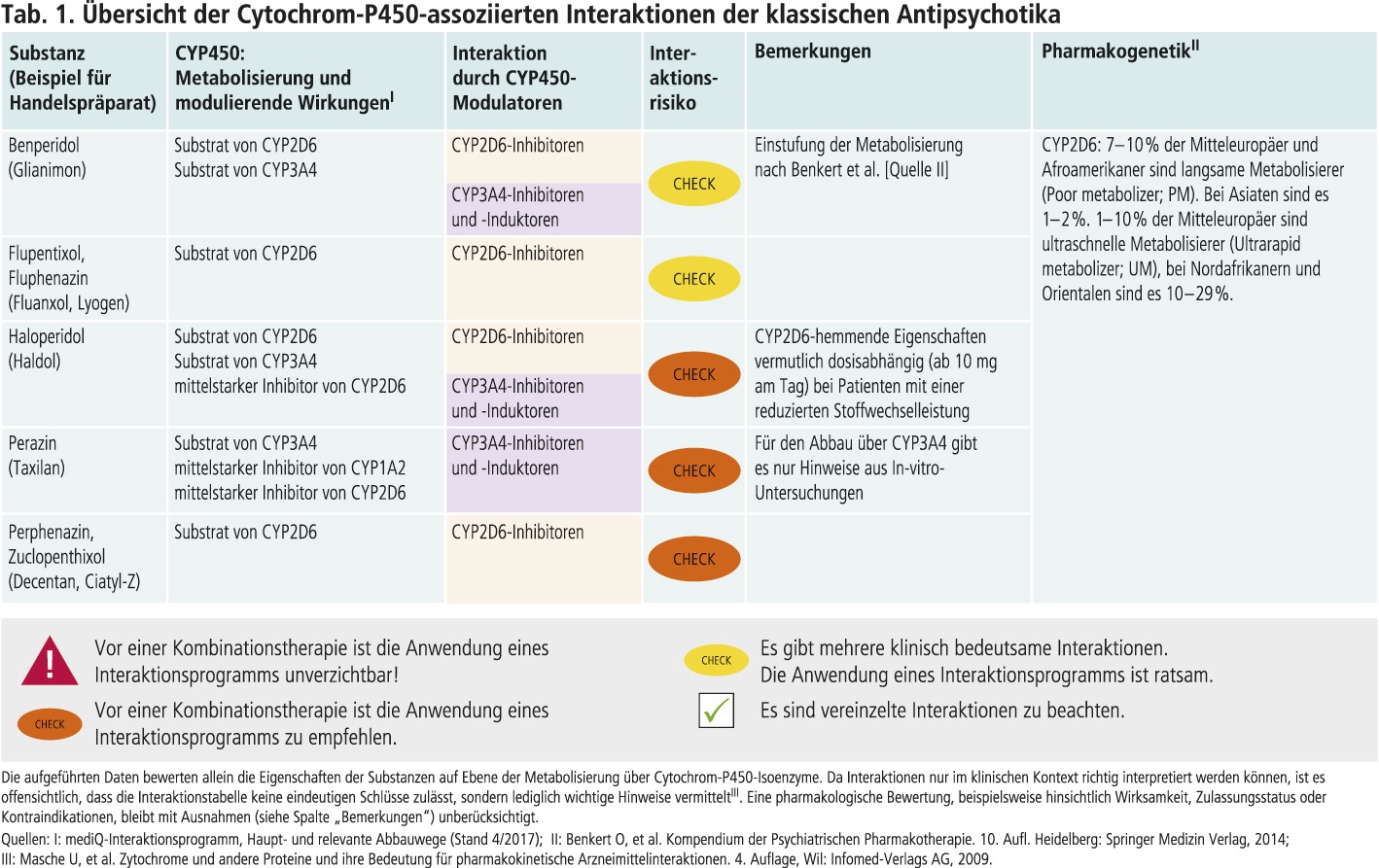
Holger Petri, Bad Wildungen*, Der Abbau klassischer Antipsychotika (syn. first-generation antipsychotics, FGA) über Cytochrom-P450(CYP)-Isoenzyme ist in unterschiedlichem Ausmaß von CYP2D6 und 3A4 abhängig. Obwohl über Jahrzehnte im klinischen Gebrauch, sind Kenntnisse über den genauen Metabolisierungsweg bei einzelnen Substanzen nicht vorhanden oder beruhen auf Ergebnissen aus In-vitro-Untersuchungen. In der Interaktionstabelle (Tab. 1) wird das Verhalten dieser Wirkstoffgruppe zu den CYP-Enzymen dargestellt.
Butyrophenone
Zu den Antipsychotika mit Butyrophenon-Struktur gehören Benperidol und Haloperidol sowie das in der psychiatrischen Pharmakotherapie nicht mehr empfohlene Bromperidol [1]. Die beiden Cytochrom-P450(CYP)-Isoenzyme 2D6 und 3A4 sind an der Metabolisierung von Haloperidol beteiligt. Der Einfluss von CYP2D6 ist dabei abhängig von der Applikationsart. CYP2D6 wird polymorph exprimiert. Personen mit einem Poor-metabolizer(PM)-Phänotyp zeigen einen stark reduzierten Stoffwechsel von CYP2D6-Substraten. Durch Dosisreduktion können zu hohe Plasmaspiegel vermieden und damit die Verträglichkeit verbessert werden. Patienten mit einem PM-Phänotyp sollten bei einer Haloperidol-Verordnung per os nur zwei Drittel der empfohlenen Dosis erhalten. Bei einer Depot-Applikation kann eine Dosisminderung um etwa zwei Drittel notwendig werden [16]. Wird die Funktionalität von CYP2D6 durch gleichzeitige Anwendung von potenten Inhibitoren dieses Isoenzyms beeinträchtigt, können die Plasmaspiegel von Haloperidol steigen. Der starke CYP2D6-Hemmer Chinidin (Abb. 1) beispielsweise verdoppelte in einer Studie mit Probanden die Plasmakonzentration von per os eingenommenem Haloperidol [19].
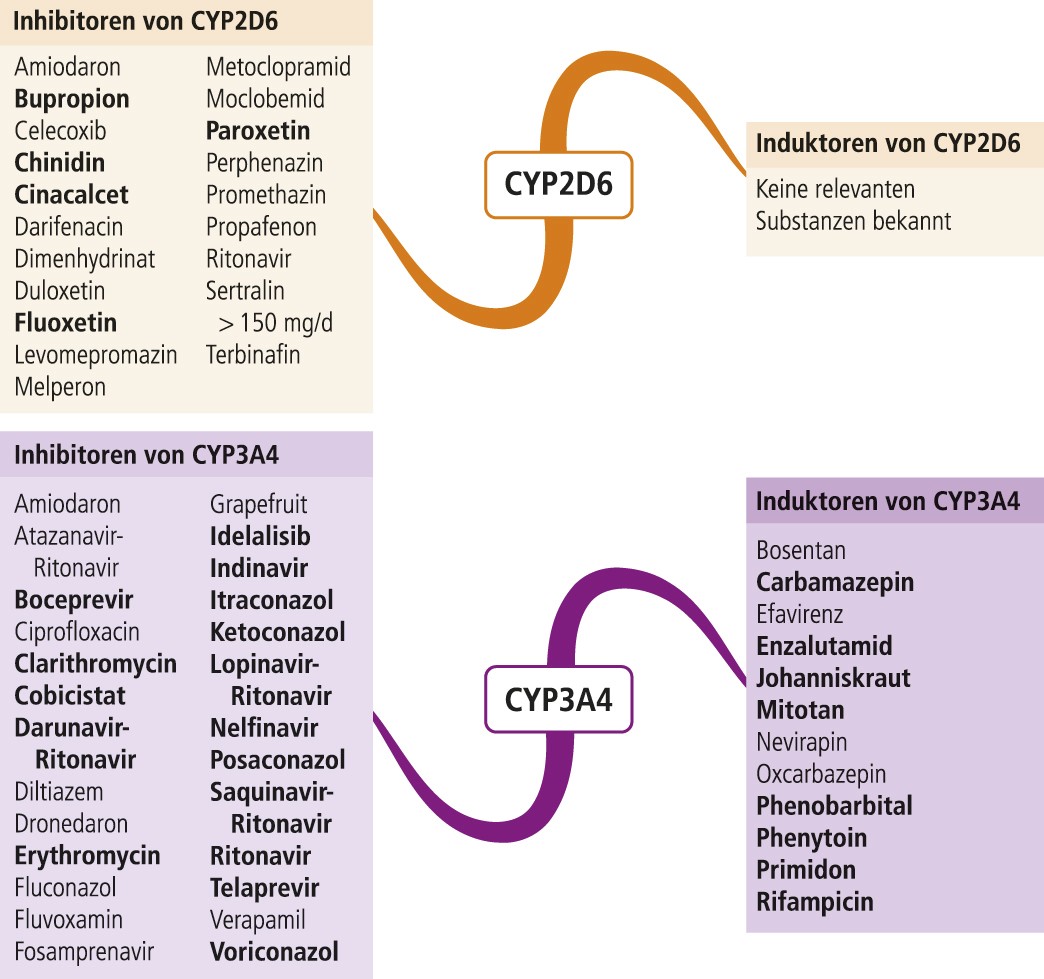
Abb. 1. Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450 (CYP) 2D6 und 3A4 (Stand: 4/2017) [Quelle: mediQ-Interaktionsprogramm]
Der starke CYP3A4-Hemmer Itraconazol (Abb. 1) erhöhte in einer klinischen Studie die AUC (Fläche unter der Konzentrations-Zeit-Kurve) von Haloperidol um 55% [17]. Starke CYP3A4-Induktoren (Abb. 1) senken dagegen die AUC-Werte. Dosisabhängig waren die durchschnittlichen Haloperidol-Konzentrationen in Kombination mit Carbamazepin bis zu 85% reduziert verglichen mit Werten vor Beginn der Induktor-Einnahme [18]. Haloperidol vermag CYP2D6 zu hemmen. Es gibt Hinweise, dass die Abbauhemmung erst ab Dosierungen von 10 mg pro Tag auftritt, besonders bei Patienten mit verminderter CYP2D6-Aktivität (Intermediate metabolizer, IM) [13]. Es wird jedoch empfohlen, Haloperidol nicht mehr höher als 10 mg/Tag zu dosieren [1]. Somit bleibt die klinische Relevanz zumindest ungeklärt.
Der Abbau von Benperidol über CYP-Enzyme ist unklar [9]. Die Fachinformation weist auf eine Wirkungsabschwächung durch Erniedrigung der Plasmakonzentration von Benperidol bei Kombination mit Antikonvulsiva wie Carbamazepin, Phenobarbital und Phenytoin sowie dem Antibiotikum Rifampicin hin [3]. Die aufgeführten Arzneistoffe sind allesamt starke CYP3A4-Induktoren (Abb. 1). Die Daten dazu stammen aus In-vitro-Untersuchungen, In-vivo-Studien liegen nicht vor. Wie bei Haloperidol ist am Metabolismus von Bromperidol neben CYP3A4 auch CYP2D6 beteiligt [4, 7]. Es kann daher angenommen werden, dass diese beiden Enzyme auch für den Abbau von Benperidol von Bedeutung sind [1].
Trizyklische Antipsychotika
Flupentixol und Fluphenazin werden unter Beteiligung von CYP2D6 abgebaut. Bei Patienten mit einem PM-Phänotyp wird empfohlen, die Flupentixol-Dosis um etwa ein Viertel zu reduzieren [16]. Der Einfluss von starken CYP2D6-Hemmern auf die Plasmaspiegel von Flupentixol kann als gering eingestuft werden. Die Fachinformation von Flupentixol enthält in Bezug auf mögliche Wechselwirkungen mit CYP2D6-Hemmern keine Hinweise [2]. Fluoxetin erhöhte in einer Doppelblindstudie die Fluphenazin-Konzentration um durchschnittlich 65% [8]. Starke CYP2D6-Hemmer sollen bei Patienten unter Fluphenazin-Therapie gemieden werden [5]. Unter Plasmaspiegelkontrolle ist im Einzelfall eine Kombination durchführbar [9].
Perazin hemmt CYP1A2 und 2D6 und kann pharmakokinetische Interaktionen mit Arzneistoffen eingehen, die über eines dieser beiden Cytochrome primär metabolisiert werden. Beispielsweise wird das Reserve-Antipsychotikum Clozapin vorzugsweise über CYP1A2 abgebaut. In einer Fallserie erhöhte Perazin die Clozapin-Konzentrationen bis zum Dreifachen der Ausgangswerte und es traten vermehrt unerwünschte Arzneimittelwirkungen auf. Perazin hemmt dosisabhängig dieses Enzym vergleichbar wie Fluvoxamin. Der empfohlene therapeutische Referenzbereich des Atypikums wurde jeweils deutlich überschritten [6, 9].
Risperidon wird über CYP2D6 zu seinem Hauptmetaboliten 9-Hydroxyrisperidon (syn. Paliperidon) verstoffwechselt. Perazin steigerte in einer klinischen Vergleichsstudie sowohl die Risperidon- als auch die Paliperidon-Plasmaspiegel. Das Risiko für das Auftreten von ZNS- und kardialen Nebenwirkungen ist hierdurch erhöht [15].
Perphenazin wird primär über CYP2D6 abgebaut [12]. Die Komedikation mit dem starken CYP2D6-Hemmer Paroxetin resultiert in einem Anstieg der maximalen Plasmakonzentrationen von Perphenazin bis zum 13-Fachen. Zentralnervöse Nebenwirkungen treten vermehrt auf. Eine Dosisreduktion bei Anwendung von Perphenazin mit potenten CYP2D6-Hemmern ist indiziert [14].
Auch der Metabolismus von Zuclopenthixol wird von der Funktionalität des polymorphen Isoenzyms CYP2D6 bestimmt. Patienten mit einem oder zwei Allelen, die nicht funktionsfähige Enzyme exprimieren, zeigen eine verminderte Clearance von Zuclopenthixol [11, 12]. Wechselwirkungen mit CYP2D6-Hemmern wie Fluoxetin erhöhen das Risiko für extrapyramidal-motorische Störungen bis hin zur Intoxikation schon bei einmaliger Gabe von i.m. injiziertem Zuclopenthixolacetat [10].
Literatur
1. Benkert O, Hippius H, et al. Kompendium der Psychiatrischen Pharmakotherapie. 10 Aufl. Heidelberg: Springer Medizin Verlag, 2014.
2. Fachinformation Fluanxol®. Stand: Januar 2014.
3. Fachinformation Glianimon®. Stand: Dezember 2014.
4. Fachinformation Impromen®. Stand Juli 2012.
5. Fachinformation Lyogen®. Stand: Juli 2015.
6. Fischer M, Unterecker S, Deckert J, et al. Elevated clozapine serum levels in combination with perazine. Psychopharmacology 2013;226:623–5.
7. Furukuri H, Kondo T, Yasui N, et al. Effects of itraconazole on the steady-state plasma concentrations of bromperidol and reduced bromperidol in schizophrenic patients. Psychopharmacology 1999;145:189–92.
8. Goff DC, Midha KK, Sarid-Segel O, et al. A placebo-controlled trial of fluoxetine added to neuroleptic in patients with schizophrenia.Psychopharmacology 1995;117:417–23.
9. Hiemke C, et al. AGNP-Konsensus-Leitlinien für therapeutisches Drug-Monitoring in der Psychiatrie: Update 2011. Psychopharmakotherapie 2012;19:91–122.
10. Hood S, et al. Severe laryngeal dystonia in a patient receving zuclopenthixol “Acuphase” and fluoxetine. Australas Psychiatry 2010;18:174–6.
11. Jaanson P, Marandi T, Kiivet RA, et al. Maintenance therapy with zuclopenthixol decanoate: associations between plasma concentrations, neurological side effects and CYP2D6 genotype. Psychopharmacology 2002;162:67–73.
12. Jerling M, Dahl ML, Aberg-Wistedt A, et al. The CYP2D6 genotype predicts the oral clearance of the neuroleptic agents perphenazine and zuclopenthixol. Clin Pharmacol Ther 1996;59:423–8.
13. LLerena A, de la Rubia A, Berecz R, et al. Relationship between haloperidol plasma concentration, debrisoquine metabolic ratio, CYP2D6 and CYP2C9 genotypes in psychiatric patiens. Pharmacopsychiatry 2004;37:69–73.
14. Ozdemir V, Naranjo CA, Herrmann N, et al. Paroxetine potentiates the central nervous system side effects of perphenazine: contribution of cytochrome P4502D6 inhibition in vivo. Clin Pharmacol Ther 1997;62:337–47.
15. Paulzen M, Haen E, Hiemke C, et al. Cytochrome P450-mediated interaction between perazine and risperidone: implications for antipsychotic polypharmacy. Br J Clin Pharmacol 2017 Feb 4 doi: 10.1111/bcp.13255.
16. Stingl JC, Brockmöller J, Viviani R. Genetic variability of drug-metabolizing enzymes: the dual impact on psychiatric therapy and regulation of brain function. Mol Psychiatry 2013;18:273–87.
17. Yasui N, Kondo T, Otani K, et al. Effects of itraconazole on the steady-stade plasma concentrations of haloperidol and its reduced metabolite in schizophrenic patients: in vivo evidence of the involvement of CYP3A4 for haloperidol metabolism. J Clin Psychopharmacol 1999;19:149–54.
18. Yasui-Furukori N, Kondo N, Mihara K, et al. Significant dose effect of carbamazepine on reduction of steady-state plasma concentration of haloperidol in schizophrenic patients. J Clin Psychopharmacol 2003;23:435–40.
19. Young D, Midha KK, Fossler MJ, et al. Effect of quinidine on the interconversion kinetics between haloperidol and reduced haloperidol in humans: implications of the involvement of cytochromeP450IID6. Eur J Clin Pharmacol 1993;44:433–8.
*Nachdruck aus Krankenhauspharmazie 2017;38:240–43.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2017; 24(03)
