Heinz Reichmann, Dresden
Das idiopathische Parkinson-Syndrom wird klinisch durch Bradykinese sowie Rigor, Tremor und posturale Instabilität charakterisiert. Neben diesen motorischen Störungen weisen Parkinson-Patienten allerdings auch nichtmotorische Symptome wie Angst, Apathie, Anhedonie, Müdigkeit (Fatigue), Depression, Demenz, aber auch Störungen des kardiovaskulären Systems, Impotenz und Inkontinenz, profuses Schwitzen, Orthostaseprobleme, Schmerz, Schlafstörungen und vieles mehr auf. Den motorischen Störungen liegt ein progressives Absterben der Dopamin-produzierenden nigrostriatalen Neuronen zugrunde. Durch diesen Dopaminmangel kommt es an den sogenannten spiny medium neurons im Mittelhirn zu einem relativen Übergewicht des glutamatergen Systems. Letzteres kann durch Amantadin und Budipin teilweise korrigiert werden, sodass diesen Arzneimitteln eine antiglutamaterge Wirksamkeit durch Hemmung der NMDA-Rezeptoren zugeschrieben wird. Zumindest für Amantadin konnte gezeigt werden, dass dies in einer Verbesserung von Dyskinesien resultiert [10]. Der Dopaminmangel wird duch eine dopaminerge Ersatztherapie ausgeglichen, das heißt durch den Einsatz von Levodopa zusammen mit einem Decarboxylase-Hemmer, dem zusätzlichen Einsatz eines Catechol-O-Methyltransferase(COMT)-Hemmers wie Entacapon oder Tolcapon oder einem Monoaminoxidase(MAO)-B-Hemmer. Diese Therapie resultiert in einer Erhöhung des Dopaminspiegels, setzt aber einen intakten Metabolismus der noch überlebenden nigralen dopaminergen Neurone voraus [5]. Unabhängig von diesem Mechanismus wirken die sogenannten Dopaminagonisten direkt an den Dopaminrezeptoren. Bekannte Beispiele hierfür sind in Deutschland Pramipexol, Ropinirol, Rotigotin und Piribedil. Diese nicht-ergolinen Dopaminagonisten sind durch eine sehr lange Plasmahalbwertszeit charakterisiert, die im Gegensatz zu dem kurz wirksamen Levodopa zu einer eher phasischen und nicht zu einer pulsatilen Stimulation der Dopaminrezeptoren führt. Im Gegensatz zum kurz wirksamen Levodopa, das durch seine pulsatile Stimulation zu motorischen Fluktuationen führt, wird dies unter den lang wirksamen Dopaminagonisten deutlich seltener gesehen. Ihr Nachteil besteht in dem Auftreten von sogenannten Impulskontrollstörungen [13], die bei etwa 5 bis 10% der Patienten nennenswerte Gefahren darstellen.
Nun ist nach zehn Jahren erstmals wieder ein neues Produkt auf den deutschen Markt gekommen, nämlich Safinamid, das durch besondere Eigenschaften charakterisiert ist.
Charakteristika von Safinamid
Safinamid ist ein Monoaminoamid, das oral in Dosierungen von 50 bzw. 100 mg appliziert wird. Es handelt sich um eine wasserlösliche Substanz. Safinamid hat zwei Wirkungsmechanismen: eine dopaminerge Wirkung durch reversible Hemmung der MAO-B und eine antiglutamaterge Wirkung durch Reduzierung der glutamatergen Überaktivität [3]. Die MAO-B-Hemmung ist im Gegensatz zu Selegilin und Rasagilin reversibel und hoch spezifisch. Es findet sich eine 1000-fach höhere Affinität für MAO-B als für die isoforme MAO-A. Es konnte gezeigt werden, dass in den angewandten Dosen eine nahezu vollständige Hemmung der MAO-B ohne eine Beeinträchtigung der MAO-A erzielt wird. Somit erhöht Safinamid die dopaminerge Stimulation. Die Blockade von aktivierten Natriumkanälen (use dependent) und eine Reduzierung der neuronalen Erregbarkeit durch Calciumkanalmodulation an den glutamatergen Neuronen führt zu einer Hemmung der abnormen Glutamat-Freisetzung [4]. Diesbezüglich unterscheidet sich Safinamid von Amantadin, das seine antiglutamaterge Wirksamkeit durch eine Blockierung der NMDA-Rezeptoren erlangt. Die Pharmakokinetik im Steady State ist bei Safinamid dosisabhängig mit einer sehr geringen interindividuellen Variabilität. Die Zeit bis zum Erreichen maximaler Plasmaspiegel beträgt etwa 2,5 Stunden; die Plasmahalbwertszeit beträgt 24 Stunden, was eine einmal tägliche Dosierung, bevorzugt morgens, erlaubt [7].
Da Safinamid nur zu einem geringen Anteil mit dem Urin ausgeschieden wird [8], haben leichte oder moderate Störungen der Nierenfunktion keinen nennenswerten Einfluss auf die Clearance von Safinamid. Bei Patienten mit Niereninsuffizienz muss somit weder eine Dosisadaptation vorgenommen werden noch auf den Einsatz von Safinamid verzichtet werden. Anders ist die Situation bezüglich Leberfunktionsstörungen. Bei schwersten Leberfunktionsstörungen sollte Safinamid nicht verwendet werden, da es bevorzugt in der Leber verstoffwechselt wird. Dabei ist allerdings das Cytochrom-System nicht beteiligt. Somit ist eine Interaktion mit anderen Arzneimitteln über diesen Weg nicht gegeben; weitere Interaktionen mit anderen Arzneimitteln sind ebenfalls nicht bekannt. Des Weiteren hat Safinamid auch keinen klinisch relevanten Einfluss auf den Tyramin-Abbau [4]. Es wurde nachgewiesen, dass auch beim Verzehr Tyramin-haltiger Nahrung unter Langzeittherapie mit Safinamid klinisch keine relevanten postprandialen Blutdruckveränderungen auftreten. Wichtig ist auch darauf hinzuweisen, dass Auswirkungen auf die QTc-Zeiten unter Safinamid geprüft und dabei keinerlei pathologischen Werte gesehen wurden.
Klinische Studien zu Safinamid
Safinamid wurde im Mai 2015 in Deutschland zur Anwendung bei Patienten unter Levodopa-Therapie zugelassen. Der Grund dafür sind drei internationale Studien, in denen Safinamid als Add-on zur Levodopa-Therapie bei 1218 Patienten getestet wurde. Die Zulassung ist somit enger gefasst als für Selegilin und Rasagilin, die auch in Monotherapie eingesetzt werden dürfen.
Die erste Studie untersuchte in 35 indischen, 10 rumänischen und 7 italienischen Prüfzentren die Wirksamkeit von Safinamid als Add-on bei Parkinson-Patienten mit motorischen Fluktuationen [1]. Diese sogenannte 016-Studie hatte als primären Endpunkt die Verlängerung der On-Zeit. Es wurden dabei männliche und weibliche Patienten im Alter von 30 bis 80 Jahren mit einem mittleren bis späten Parkinson-Stadium eingeschlossen. Die Patienten durften mit Levodopa und anderen Dopaminergika vorbehandelt worden sein. Die Patienten mussten seit mindestens drei Jahren an einem idiopathischen Parkinson-Syndrom leiden und sich im Hoehn&Yahr-Stadium I–IV während der Off-Phasen befinden. Sie sollten motorische Fluktuationen aufweisen und pro Tag zumindest 1,5 Stunden im Off sein. Dazu mussten sie fähig sein, ein Tagebuch akkurat zu führen. Das Studiendesign war so, dass eine Stabilisierungsphase für Levodopa von vier Wochen zur Optimierung der Levodopa-Dosierung genutzt wurde. Die Einnahme aller anderen Parkinson-Arzneimittel durfte fortgesetzt werden. Sechs Monate lang wurden dann 222 Patienten mit Placebo, 223 Patienten mit 50 mg Safinamid und 224 Patienten mit 100 mg Safinamid behandelt. Die Studie war doppelblind und zeigte bezüglich der primären Wirksamkeitsendpunkte, nämlich der mittleren Veränderung der täglichen On-Zeit, eine Verbesserung von 9,5 auf 11 Stunden pro Tag unter 100 mg und von 9,4 auf 10,9 Stunden pro Tag unter 50 mg Safinamid. Damit unterschieden sich die beiden Verum-Arme signifikant vom Placebo-Arm, der eine Verbesserung von 9,3 auf 10,3 Stunden nach 24-wöchiger Einnahmezeit aufwies. Parallel dazu kam es zu einer Veränderung der täglichen Off-Zeit unter 100 mg Safinamid von 5,2 auf 3,8 Stunden. Das Ergebnis für 50 mg Safinamid war nahezu gleich. Unter Placebo wurde ebenfalls eine Verbesserung von 5,2 auf 4,5 Stunden Off-Zeit beschreiben. Bezüglich der sekundären Wirksamkeitsendpunkte muss auf die Verbesserung der UPDRS-III-Werte hingewiesen werden. Hier wurde unter Placebo eine Verbesserung von 28,7 auf 23,8 Punkte beschrieben, wohingegen unter 100 mg Safinamid eine Verbesserung von 28,3 auf 21,1 Punkte beschrieben wurde, was einem p-Wert von <0,0006 (Safinamid vs. Placebo) entspricht. Die weiteren sekundären Wirksamkeitsendpunkte waren bezüglich der Clinical Global Impressions, der Aktivitäten des täglichen Lebens in der UPDRS II, der motorischen Fluktuationen in UPDRS IV sowie der Lebensqualitätsparameter gemessen mit der PDQ 39 für 100 mg Safinamid signifikant verbessert, für 50 mg Safinamid dagegen nicht signifikant verbessert.
Die zweite Untersuchung ist die Studie 018. Es handelt sich um eine Verlängerung der Studie 016 in einem Doppelblinddesign um weitere 18 Monate [2]. Sämtliche Patienten, die in der 016-Studie doppelblind Placebo erhielten, mussten diese Therapie fortsetzen, was auch für die mit 50 mg bzw. 100 mg Safinamid therapierten Patienten galt. Von den 222 initial in die 016-Studie rekrutierten Placebo-therapierten Patienten waren am Ende der 018-Studie noch 142 Patienten in der Studie verblieben, von den 223 mit 50 mg Safinamid therapierten Patienten noch 148 und von den 224 mit 100 mg Safinamid therapierten noch 150 Patienten. In die Studie wurden nur die Patienten aufgenommen, die nach der 016-Studie bereit waren, eine Fortsetzung in einem doppelblinden Design zu erlauben, sodass von den 222 Placebo-rekrutierten Patienten 175 die Studie begannen, von den 223 mit 50 mg Safinamid initiierten noch 189 und von den 224 mit 100 mg Safinamid rekrutierten Patienten noch 180 in die Studie eintraten. Aus der Studie ausgeschlossen wurden Patienten, bei denen in der 016-Studie klinisch relevante unerwünschte Wirkungen aufgetreten waren oder die in der Studie 016 eine klinisch relevante Verschlechterung der motorischen Symptome gezeigt hatten.
Als primärer Wirksamkeitsendpunkt bei dieser Studie wurde die Dyskinesia Rating Scale (DRS) im On gegenüber Baseline gewertet. Es kam dabei zu einer 31%igen Reduktion unter 50 mg Safinamid sowie zu einer 27%igen Reduktion unter 100 mg Safinamid, wohingegen unter Placebo nur eine 3%ige Reduktion des DRS-Gesamtwerts beschrieben wurde. Trotzdem wurde der primäre Endpunkt nicht erreicht, da die Signifikanz lediglich p=0,21 bzw. p=0,15 für Safinamid 50 bzw. 100 mg betrug. In einer Post-hoc-Analyse wurden die DRS-Daten von 224 Patienten, die bereits bei Aufnahme in die Studie 016 moderate bis schwere Dyskinesien aufwiesen, das heißt, einen DRS-Gesamtscore von über vier aufgewiesen hatten, post hoc analysiert. Dies war deswegen sinnvoll, weil die meisten Patienten, nämlich 74%, zur Baseline keine oder nur milde Dyskinesien aufgewiesen hatten, sodass für das Gesamtkollektiv kaum Raum für eine klinisch relevante Verbesserung gegeben war. Unter dieser Prämisse kam es bei dieser Post-hoc-Analyse unter 100 mg Safinamid pro Tag zu einer signifikanten Verbesserung des DRS-Scores (p<0,0317). Neben diesem primären Endpunkt wurde der wichtigste sekundäre Endpunkt, nämlich die Verbesserung der On-Zeit in beeindruckender Weise über die Verlängerungsperiode von 1,5 Jahren bei einer On-Zeit von 10,7 Stunden pro Tag unter 100 mg Safinamid und von 10,5 Stunden unter 50 mg Safinamid gehalten. Dieses Ergebnis ist bemerkenswert, da es zeigt, dass die erzielte Wirksamkeit von Safinamid nach sechs Monaten in der 016-Studie für weitere 1,5 Jahre in der 018-Studie gehalten werden konnte.
Die dritte (noch nicht publizierte) Studie, die sogenannte SETTLE-Studie, wurde ebenfalls als randomisierte, doppelblinde, Placebo-kontrollierte Phase-III-Studie durchgeführt, um die Effektivität und Sicherheit von 50 bzw. 100 mg Safinamid als Add-on-Therapie bei Parkinson-Patienten mit Levodopa und motorischen Fluktuationen zu untersuchen. Diese Patienten durften stabile Dosen an Dopaminagonisten, Anticholinergika und/oder Amantadin zusätzlich verwenden. Das Studiendesign der SETTLE-Studie unterschied sich von der 016-Studie dahingehend, dass eine Anfangsdosis von 50 mg Safinamid für zwei Wochen vorgeschlagen wurde und dann möglichst auf 100 mg Safinamid erhöht werden musste. Das Verhältnis der Placebo- und Safinamid-behandelten Patienten betrug 1:1, die Studiendauer war sechs Monate. In diese Studie wurden ebenfalls 30- bis 80-jährige männliche und weibliche Patienten mit der Diagnose eines idiopathischen Parkinson-Syndroms mit einer durchschnittlichen Krankheitsdauer von drei Jahren rekrutiert. In der Off-Phase sollten die Patienten einem Hoehn&Yahr-Stadium I bis IV entsprechen und mehr als 1,5 Stunden pro Tag im Off sein. Die Levodopa-Dosis musste während der letzten vier Wochen vor dem Screening stabilisiert werden. Das wichtigste Ausschlusskriterium war ein schweres spätes Parkinson-Syndrom mit erheblichen beeinträchtigenden Peak-Dose- oder biphasischen Dyskinesien oder unvorhersehbaren symptomatischen Fluktuationen. In dieser Studie konnte eine Verbesserung der On-Zeit zum Ende der sechsmonatigen Beobachtung von 9,3 auf 10,7 Stunden unter 100 mg Safinamid erreicht werden; dies war hochsignifikant (p<0,001) gegenüber der Placebo-Wirkung, unter der sich die On-Zeit von 9,1 auf 9,6 Stunden pro Tag verbesserte. Parallel dazu führten 100 mg Safinamid zu einer Verbesserung der Off-Zeit von 5,3 auf 3,8 Stunden, was ebenfalls hochsignifikant war (p<0,001), wohingegen unter Placebo eine Verbesserung der Off-Zeit von nur 5,4 auf 4,8 Stunden beschrieben wurde. Beeindruckend war auch die Verbesserung des UPDRS-III-Scores, der unter der Verum-Therapie von 22,3 auf 18,8 Punkte und unter Placebo von 23 auf 21,2 Punkte abnahm (p<0,003).
Klinischer Nutzen und potenzielle Anwendung von Safinamid
Die drei genannten Studien, die zur klinischen Zulassung in Deutschland führten, zeigen allesamt einen nennenswerten und effektiven Nutzen der Safinamid-Therapie. Es kommt zu einer Verbesserung der On-Zeit, die zumindest im Bereich der MAO-B-Hemmer bzw. COMT-Hemmer liegt und gegenüber Dopaminagonisten nicht weit abfällt. Bemerkenswert ist das Nebenwirkungsprofil von Safinamid, weil es beispielsweise bezüglich der dopaminergen Effekte zu keinem erweiterten Nebenwirkungsspektrum gegenüber Levodopa allein kommt. Es gibt erste Hinweise darauf, dass eventuell die depressive Verstimmung etwas verbessert wird.
Zusammenfassend ist Safinamid somit bei Patienten mit Fluktuationen als Add-on-Therapie zu einer stabilen Dosis von Levodopa allein oder in Kombination mit anderen Anti-Parkinson-Mitteln zugelassen. Es wird empfohlen, mit einer Startdosis von 50 mg zu beginnen und dann nach zwei Wochen auf 100 mg zu erhöhen. Sollte sich allerdings das in den Studien hervorragend niedrige Nebenwirkungsprofil auch realiter als wenig bedenklich erweisen, könnte künftig empfohlen werden, bereits mit 100 mg zu beginnen.
Klinische Empfehlungen zur Verwendung von Safinamid
Wie in der STRIDE-PD-Studie [11] gezeigt werden konnte, kommt es bei Levodopa-Dosen von mehr als 400 mg nach einigen Jahren zu Dyskinesien, während dies bei Patienten, die 400 mg oder weniger Levodopa einnehmen, in sehr viel geringer Anzahl der Fall zu sein scheint. Sharma et al. [9] konnten darüber hinaus grob vereinfacht zeigen, dass Frauen 5 mg Levodopa pro kg Körpergewicht und Männer 7 mg Levodopa pro kg Körpergewicht ohne Induktion von Dyskinesien tolerieren können. Nachdem Fahn und Kollegen in der sogenannten ELLDOPA-Studie [6] gezeigt hatten, dass Patienten leider bereits nach einem Jahr Therapie in der Mehrheit der Fälle mehr als 400 mg Levodopa benötigen, muss somit eine Alternative zur Erhöhung der Levodopa-Dosis über 400 mg gefunden werden. Leider hatte die STRIDE-PD-Studie gezeigt, dass die Idee, COMT-Hemmer zusammen mit Levodopa zu verwenden, nicht zu einer Reduktion der Dyskinesie-Rate führte. Somit ist dies die Domäne der Dopaminagonisten, deren Kombination zum Levodopa beispielsweise von Watts et al. 2010 [12] als Dyskinesie-mindernd gezeigt werden konnte. Eine neue Option bietet nun Safinamid, genauer das Hinzufügen von 100 mg Safinamid morgens. Die Patienten erreichen unter dieser Therapie, wie in den drei genannten Studien überzeugend gezeigt wurde, eine Verbesserung der On-Symptomatik und die Patienten, die bereits unter Levodopa Dyskinesien entwickelt haben, können auch diesbezüglich eine Verbesserung erwarten. Unklar ist derzeit noch, ob durch die frühe Kombination von Safinamid mit Levodopa sogar das Auftreten von Dyskinesien verhindert werden kann. Auch das Wearing-off ist somit neben der COMT-Gabe ein sicherlich naheliegendes Feld, auf dem sich das Hinzufügen von Safinamid zu Levodopa bewähren sollte. Ganz generell könnten Patienten, die leichte Dyskinesien oder erste motorische Komplikationen aufweisen, sicherlich von der Therapie mit Safinamid profitieren, wenn man den Post-hoc-Analysen Glauben schenkt. Dies muss aber in weiteren Studien erst schlüssig bewiesen werden, da sich in den Studien auch bei manchen Patienten die Dyskinesien verschlechterten.
Abbildung 1 zeigt ein Schema der Verwendung von Safinamid bei Patienten im Wearing-off bzw. unter Dyskinesien. Praktische Hinweise für die Einnahme von Safinamid beinhalten die Empfehlung, dass Patienten, die die Safinamid-Einnahme vergessen haben, erst am kommenden Morgen mit der nächsten Regeldosis weitermachen sollten. Ältere Patienten benötigen keine Dosisanpassung. Halluzinationen wurden durch das Hinzufügen von Safinamid auch bei älteren Patienten nicht beschrieben. Kontraindikationen für die Einnahme von Safinamid sind die Anwendung von MAO-A-Hemmern oder Pethidin, schwere Leberschädigungen oder Retina-Schäden. Bei der Anwendung von selektiven Serotonin-Wiederaufnahmehemmern (SSRI) sollten möglichst niedrige Dosen verwendet werden und die Einnahme von Fluoxetin und Fluvoxamin sollte ähnlich wie bei Rasagilin vermieden werden oder zumindest in der niedrigst möglichen Dosis erfolgen. Es wird auch empfohlen, bis zumindest sieben Tage zu warten, bevor man nach dem Absetzen von Safinamid mit einer SSRI-Therapie beginnt. Hinweise auf eine Auslösung von Impulskontrollstörungen gibt es bislang unter Safinamid nicht. Trotzdem ist es ratsam, da es sich doch zum Teil um ein Dopaminergikum handelt, die Patienten und Betreuer auf die Symptome einer Impulskontrollstörung hinzuweisen. Soweit bisher bekannt ist, kommt es unter Safinamid zu keinem negativen Effekt auf die Fahrtauglichkeit oder das Verwenden von Maschinen. Aber auch diesbezüglich sollten die Patienten, die Auto fahren müssen oder gefährliche Maschinen benutzen, zumindest zu Beginn der Safinamid-Therapie auf eine mögliche Beeinträchtigung hingewiesen werden. Das Sicherheitsprofil von Safinamid basiert derzeit auf der Anwendung an über 3000 Personen, von denen sicherlich mehr als 500 länger als zwei Jahre behandelt wurden. Selbst unter den oben diskutierten SSRI, Serotonin-Noradrenalin-Wiederaufnahmehemmern (SNRI), tri- und tetrazyklischen Antidepressiva und MAO-Hemmern wurde keine schwere Nebenwirkung gesehen. Ganz selten kam es zu hypertensiven Krisen, einem neuroleptischen malignem Syndrom, einem serotonergen Syndrom oder Hypotension.
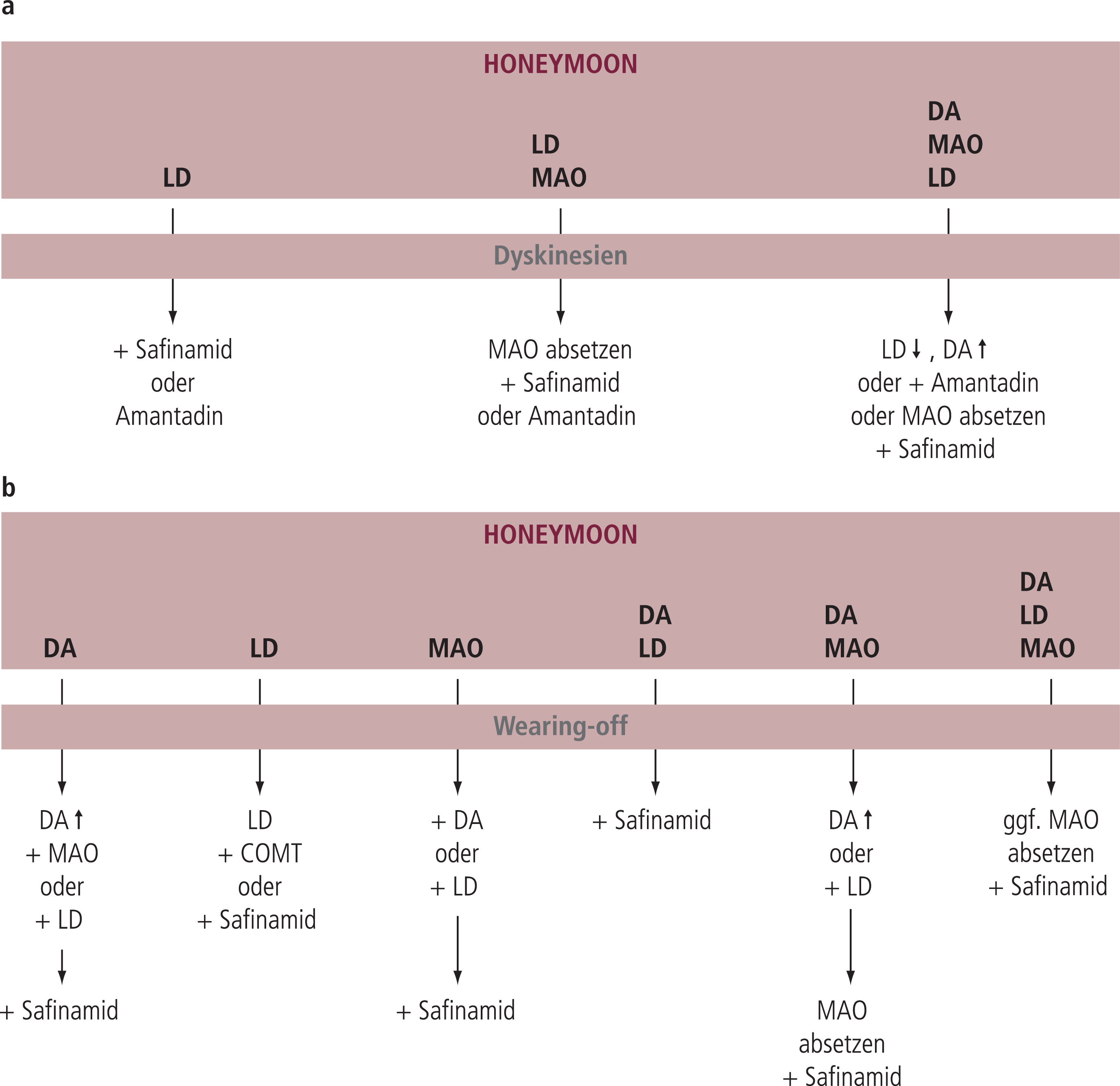
Abb. 1. Entscheidungsbaum Folgetherapie beim Auftreten von Dyskinesien [a] bzw. bei „Wearing-off“ [b] DA: Dopaminagonist; LD: Levodopa + Decarboxylasehemmer; MAO: Monoaminoxidase-(MAO-)B-Hemmer; COMT: Catechol-O-Methyltransferase-(COMT-)Hemmer; ↑: Dosis erhöhen
Nur 1,5% der mit Safinamid therapierten Patienten entwickelten schwere Dyskinesien
Zusammenfassend ist somit aus meiner Sicht Safinamid tatsächlich eine neue Therapieoption. Es unterscheidet sich in seinem dualen Wirkungsmechanismus überzeugend von den anderen bewährten Anti-Parkinson-Medikamenten. Zusätzlich besticht es durch seine einmal tägliche Applikation und insbesondere das nahezu vernachlässigbare Nebenwirkungsprofil.
Interessenkonflikterklärung
HR hat Honorare für Vorträge und die Teilnahme an einem Expertenbeirat sowie Forschungsbeihilfen erhalten von Abbott, AbbVie, Bayer Health Care, Boehringer/Ingelheim, Brittania, Cephalon, Desitin, GSK, Lundbeck, Medtronic, Merck-Serono, Novartis, Orion, Pfizer, TEVA, UCB Pharma, Valeant und Zambon.
Literatur
1. Borgohain R, Szasz J, Stanzione P, Meshram C, et al. Randomized trial of safinamide add-on to levodopa in Parkinson’s disease with motor fluctuations. Mov Disord 2014;29:229–37.
2. Borgohain R, Szasz J, Stanzione P, Meshram C, et al. Two-year, randomized, controlled study of safinamide as add-on to levodopa in mid to late Parkinson’s disease. Mov Disord 2014;29:1273–80.
3. Cassia C, Maj R, Calabresi M, Maestroni S, et al. Safinamide: from molecular targets to a new anti-Parkinson drug. Neurology 2006;67:S18–23.
4. Cattaneo C, Caccia C, Marzo A, Maj R, et al. Pressor response to intravenous tyramine in healthy subjects after safinamide, a novol neuroprotectant with selective, reversible monoamine oxidase B inhibition. Clin Neuropharmacol 2003;26:213–7.
5. Eggert KM, Oertel WH, Reichmann H. Leitlinie Parkinson-Syndrome: Diagnostik und Therapie. In: Diener HC, Weimar C (Hrsg.). Leitlinien der Deutschen Gesellschaft für Neurologie. 5. Auflage. Stuttgart: Thieme Verlag, 2012.
6. Fahn S, Oakes D, Shoulson I, Kieburtz K, et al. Levodopa and the progression of Parkinson’s disease. N Engl J Med 20014;351:2498–508.
7. Marzo A, Dal Bo L, Monti NC, Crivelli F, et al. Pharmacokinetics and pharmacodynamics of safinamide, a neuroprotectant with antiparkinsonian and anticonvulsant activity. Pharmacol Res 2004;50:77–85.
8. Onofrj M, Bonanni L, Thomas A. An expert opinion on safinamide in Parkinson’s disease. Expert Opin Investig Drugs 2008;17:1115–25.
9. Sharma JC, Vassallo M. Prognostic significance of weight changes in Parkinson’s disease: the Park-weight phenotype. Neurodegener Dis Manag 2014;4:309–16.
10. Verhagen Metmann L, Del Dotte P, van der Munckhof P, Fang J, et al. Amantadine as treatment for dyskinesias and motor fluctuations in Parkinson’s disease. Neurology 1998;50:1323–6.
11. Warren Olanow C, Kieburtz K, Rascol O, Poewe W, et al. Factors predictive of the development of Levodopa-induced dyskinesia and wearing-off in Parkinson’s disease. Mov Disord 2013;28:1064–71.
12. Watts RL, Lyons KE, Pahwa R, Sethi K, et al. Onset of dyskinesia with adjunct ropinirole prolonged-release or additional levodopa in early Parkinson’s disease. Mov Disord 2010;25:858–66.
13. Weintraub D, David AS, Evans AH, Grant JE, et al. Clinical spectrum of impulse control disorders in Parkinson’s disease. Mov Disord 2015;30:121–7.
Prof. Dr. med. Heinz Reichmann, Klinik und Poliklinik für Neurologie, Universitätsklinikum Carl Gustav Carus Dresden, Fetscherstraße 74, 01307 Dresden, E-Mail: heinz.reichmann@uniklinikum-dresden.de
Safinamide – a new treatment of Parkinson‘s disease
Safinamide offers an new option in the treatment of Parkinson’s disease (PD). In contrast to other PD medication safinamide holds a dual mode of action, i.e., it has both a dopaminergic and an anti-glutamatergic effect. Safinamide is a selective and reversible MAO-B inhibitor and regulates use-dependently the glutamatergic system. In three international pivotal studies, which are discussed in this overview, safinamide has shown significant efficacy with respect to motor function and some signal to decrease dyskinesia, as well. The tolerability is extremely good. Solely, patients with major liver insufficiency should not receive safinamide. No specific monitoring is necessary. Safinamide should be applied once daily in the morning in a dose of 100 mg.
Key words: Parkinson’s disease, safinamide, motor complications, anti-dyskinetic effect
Psychopharmakotherapie 2015; 22(05)
