Holger Petri, Bad Wildungen*
Substrate von CYP1A2 und CYP3A4
Eletriptan, Frovatriptan und Zolmitriptan werden primär über ein Cytochrom-P450(CYP)-Isoenzym abgebaut. Eletriptan ist Substrat von CYP3A4 [10]. In klinischen Studien mit dem starken CYP3A4-Hemmer Ketoconazol stieg der AUC(Area under the curve)-Wert von Eletriptan um das 5,9-Fache und die Halbwertszeit (t½) verlängerte sich von 4,8 auf 8,3 Stunden [14]. Folglich darf es nicht mit Arzneimitteln kombiniert werden, die CYP3A4 ausgeprägt hemmen, wie Clarithromycin, Itraconazol und Ritonavir (Abb. 1) [10]. Wie mit CYP3A4-Induktoren zu verfahren ist, kann der Fachinformation nicht entnommen werden. Die Veränderung der pharmakokinetischen Parameter AUC und t½ durch CYP3A4-Inhibitoren lassen jedoch erwarten, dass es zu einem signifikanten Abfall der Eletriptan-Exposition mit verminderter Wirkung kommen kann. Frovatriptan ist Substrat von CYP1A2 [4]. Bei gleichzeitiger Gabe mit dem starken CYP1A2-Hemmer Fluvoxamin steigt die Plasmakonzentration des Triptans um 27–49% [4]. Die klinische Relevanz scheint wegen der großen therapeutischen Breite von Frovatriptan aber gering zu sein [1, 4]. Polyzyklische aromatische Kohlenwasserstoffe im Tabakrauch induzieren dosisabhängig CYP1A2 [12]. Die Bioverfügbarkeit von Frovatriptan ist bei Rauchern jedoch nur wenig geringer als bei Nichtrauchern und erfordert keine Dosisanpassung [1]. Zolmitriptan ist Substrat von CYP1A2 [6]. Als maximale Tagesdosis werden bei gleichzeitiger Gabe von CYP1A2-Hemmern 5 mg Zolmitriptan empfohlen. Der über CYP1A2 gebildete aktive Metabolit N-Demethyl-Zolmitriptan wird über die Monoaminooxidase A (MAO-A) abgebaut [17]. Daher wird eine Maximaldosis von 5 mg über 24 Stunden bei Komedikation mit dem MAO-A-Hemmer Moclobemid empfohlen. Bei höheren Dosen als zweimal täglich 150 mg Moclobemid sollte Zolmitriptan nicht angewandt werden [6]. Es wäre zu erwarten, dass die Zolmitriptan-Plasmaspiegel bei Rauchern erniedrigt sind. In einer Untersuchung konnten keine pharmakokinetischen Unterschiede zwischen rauchenden und nichtrauchenden Probanden festgestellt werden. Zur Klärung der klinischen Bedeutung fordern die Autoren weitere, speziell auf diese Fragestellung ausgerichtete Untersuchungen [15].
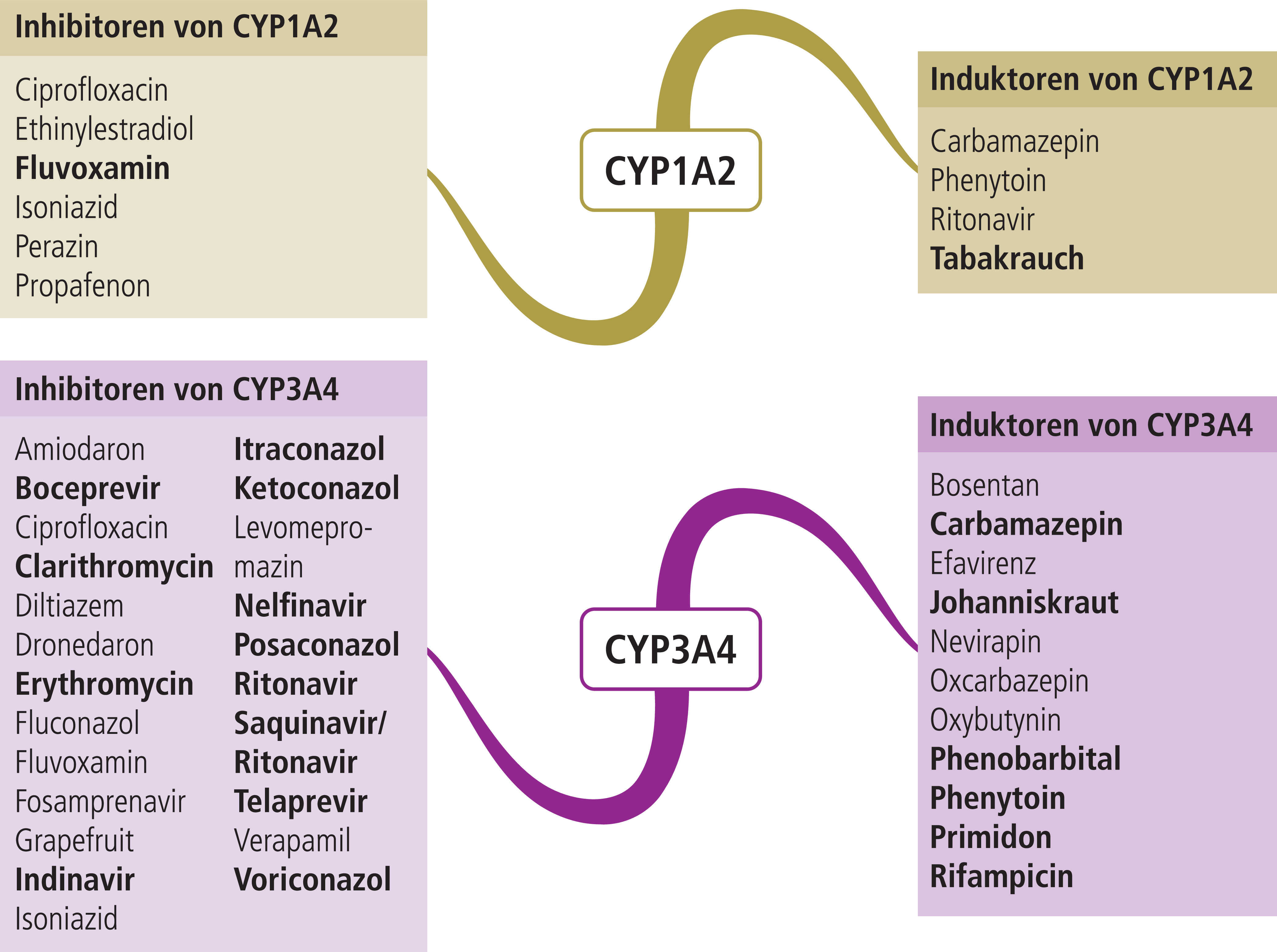
Abb. 1. Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450 1A2 und 3A4 (Stand: 08/2015) [Quelle: mediQ-Interaktionsprogramm]
MAO-A-Substrate
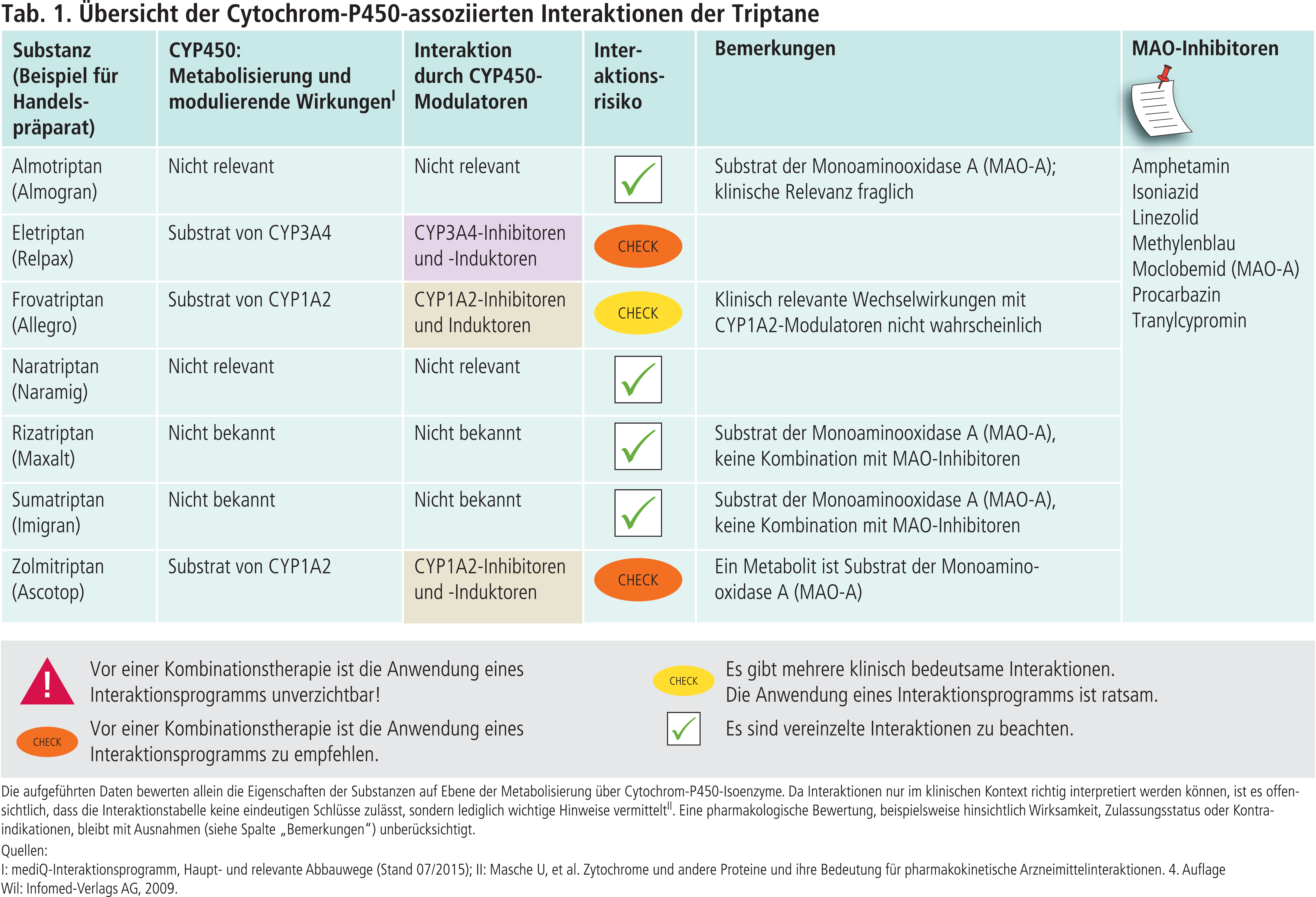
Almotriptan, Rizatriptan und Sumatriptan werden über die MAO-A abgebaut [5, 7, 8]. Während die Clearance von Almotriptan durch Moclobemid in einem Ausmaß beeinflusst wird, das keine Dosisanpassung erfordert, dürfen Rizatriptan und Sumatriptan nicht mit MAO-Hemmern zusammen verordnet werden [5, 7, 8, 13]. Tabelle 1 enthält eine Auswahl von klinisch relevanten MAO-Inhibitoren.
Naratriptan
Naratriptan wird weitgehend unverändert renal eliminiert [9]. Wechselwirkungen auf Ebene des Metabolismus sind nicht zu erwarten.
Triptane und Risiko für ein Serotonin-Syndrom?
Die US-amerikanische Arzneimittelüberwachungsbehörde FDA warnte im Jahr 2006 vor einer möglichen Wechselwirkung von Triptanen mit selektiven Serotonin-Wiederaufnahmehemmern (SSRI) und Serotonin-Noradrenalin-Wiederaufnahmehemmern (SNRI) mit dem Risiko eines lebensbedrohlichen Serotonin-Syndroms [16]. Ein Serotonin-Syndrom entsteht durch eine Hyperstimulation der 5-Hydroxytryptamin(5-HT)-Rezeptoren 5-HT1A und 5-HT2A im zentralen und peripheren Nervensystem.
Triptane sind jedoch Agonisten der 5-HT1B- und 5-HT1D-Rezeptoren [11]. Vor dem Hintergrund dieses pharmakologischen Wirkungsprofils ist es nicht plausibel, dass Triptane zu einem schwerwiegenden Serotonin-Syndrom beitragen. In einem Positionspapier der American Headache Society wird auf die mangelnde Datenlage hingewiesen [3]. Die Gefahr für ein Serotonin-Syndrom wird als so gering angesehen, dass die gemeinsame Gabe von Triptanen mit SSRI- und SNRI-Antidepressiva nicht eingeschränkt zu werden braucht. Auch für die Empfehlung, Triptane zu bevorzugen, die nicht über das MAO-A-System abgebaut werden, fehlen fundierte Daten.
Dennoch sollten Patienten, die gleichzeitig Triptane und Antidepressiva (SSRI und SNRI) einnehmen, besonders sorgfältig ärztlich begleitet werden. Bei der Auswahl eines Triptans ist die Begleitmedikation und die Verstoffwechslung zu beachten [2].
Literatur
1. Buchan P, et al. Frovatriptan: a review of drug-drug interactions. Headache 2002;42 Suppl 2:S63–73.
2. Deutsche Migräne- und Kopfschmerzgesellschaft DMKG. Medikation bei Migräne und Depression – Gefahr von ungünstigen Wechselwirkungen? Presseinformation Juni 2012.
3. Evans RW, et al. The FDA alert on serotonin syndrome with use of triptans combined with selective serotonin reuptake inhibitors or selective serotonin-norepinephrine reuptake inhibitors: American Headache Society position paper. Headache 2010;50:1089–99.
4. Fachinformation Allegro®. Stand: November 2014.
5. Fachinformation Almogran®. Stand: August 2014.
6. Fachinformation Ascotop®. Stand: November 2014.
7. Fachinformation Imigran®. Stand: Januar 2013.
8. Fachinformation Maxalt®. Stand: März 2015.
9. Fachinformation Naramig®. Stand: Mai 2013.
10. Fachinformation Relpax®. Stand: Mai 2014.
11. Gillman PK. Triptans, serotonin agonists, and serotonin syndrome (serotonin toxicity): a review. Headache 2010;50:264–72.
12. Kroon LA. Drug interactions with smoking. Am J Health-Syst Pharm 2007;64:1917–21.
13. McEnroe JD, Fleishaker JC. Clinical pharmacokinetics of almotriptan, a serotonin 5-HT(1B/1D) receptor agonist for the treatment of migraine. Clin Pharmacokinet 2005;44:237–46.
14. Tepper S, et al. Coprescription of triptans with potentially interacting medications: a cohort study involving 240,268 patients. Headache 2003;43:44–8.
15. Uemura N, et al. Bioequivalence and rapid absorption of zolmitriptan nasal spray compared with oral tablets in healthy Japanese subjects. Clin Drug Investig 2005;25:199–208.
16. US Food and Drug Administration. Information for healthcare professionals. Selective serotonin reuptake inhibitors (SSRIs), 5-hydroxytryptamine receptor agonists (triptans). 2006. www.fda.gov/drugs/drugsafety/postmarketdrugsafetyinformationforpatientsandproviders/drugsafetyinformationforheathcareprofessionals/ucm085845.htm (Zugriff am 12.08.2015).
17. Wild MJ, McKillop D, Butters CJ. Determination of the human cytochrome P450 isoforms involved in the metabolism of zolmitriptan. Xenobiotica 1999;29:847–57.
*Nachdruck aus Krankenhauspharmazie 2015;36:467–9.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2015; 22(05)
