Birgit Hecht, Stuttgart
Die multiple Sklerose ist eine immunvermittelte, chronisch entzündliche Erkrankung des zentralen Nervensystems, die bei über 80% der Patienten schubförmig beginnt. Durch immunmodulierende Basistherapeutika kann bei Patienten mit schubförmiger MS die Schubrate und die Krankheitsaktivität in der Magnetresonanztomographie (MRT) verringert werden. Langfristig verzögert eine Therapie mit Interferon beta-1a das Fortschreiten der Behinderung und die Konversion einer schubförmigen MS in eine sekundär progrediente Form.
Bei Patienten mit klinisch isoliertem Syndrom (clinically isolated syndrome, CIS) verzögerte die Gabe von Interferon beta-1a (Avonex® bzw. Rebif® [1-mal wöchentlich 22 mg]), Interferon beta-1b (Betaferon®) oder Glatirameracetat (Copaxone®) in früheren Studien die Konversion in eine klinisch manifeste MS (clinically definite MS, CDMS, zweiter Schub [oder anhaltende Behinderungsprogression]) [1–4].
Die REFLEX-Studie
In der multizentrischen, randomisierten, doppelblinden, Plazebo-kontrollierten Phase-III-Studie REFLEX (Rebif flexible dosing in early multiple sclerosis) wurde nun bei Patienten mit klinisch isoliertem Syndrom untersucht, wie sich die subkutane Gabe von Interferon beta-1a (IFN beta-1a) auf die Konversion in eine MS nach den McDonald-Kriterien (Nachweis durch zweites klinisches Ereignis oder durch klinische Daten und MRT) auswirkt [5, 6]. Eingeschlossen wurden 517 erwachsene Patienten (18–50 Jahre), die
- in den vorangegangenen 60 Tagen ein klinisches Ereignis hatten, das auf eine MS hindeutet,
- einen Behinderungsgrad entsprechend einem Wert zwischen 0 und 5 auf der Expanded Disability Status Scale (EDSS) aufwiesen und
- bei denen im T2-gewichteten MRT mindestens zwei asymptomatische Läsionen zu sehen waren (≥3 mm, davon mindestens eine ovoid, periventrikulär oder infratentoriell).
Ausgeschlossen waren Patienten, die bereits die Diagnosekriterien für eine multiple Sklerose (McDonald 2005) erfüllten oder die an einer anderen Erkrankung litten, mit der die Befunde und Symptome besser erklärt werden konnten.
Die Probanden wurden im Verhältnis 1:1:1 randomisiert. Untersucht wurden zwei Dosierungen des Interferons (1-mal wöchentlich 44 mg und die zur Therapie der MS zugelassene Dosierung von 3-mal wöchentlich 44 mg) sowie Plazebo. Die Dosis des Interferons wurde in den ersten Wochen schrittweise erhöht, bis die Zieldosis erreicht war.
Primärer Endpunkt war die Zeit bis zur Diagnose einer MS nach den McDonald-Kriterien von 2005. Die Entwicklung einer klinisch manifesten MS wurde als sekundärer Endpunkt ausgewertet. Die Beobachtungszeit betrug 24 Monate. MRT-Aufnahmen wurden zu Beginn sowie in den Monaten 3, 6, 9, 12, 15, 18 und 24 angefertigt (bis zur Konversion in eine CDMS, danach alle 6 Monate).
Ergebnisse
Innerhalb von zwei Jahren entwickelte sich bei 379 Patienten eine MS nach den McDonald-Kriterien (n=106 bzw. 129 vs. 144 für IFN beta-1a 3-mal bzw. 1-mal wöchentlich vs. Plazebo). Das Risiko, eine MS zu entwickeln, war bei Behandlung mit dem Interferon signifikant niedriger als mit Plazebo und bei 3-mal wöchentlicher Applikation des Interferons niedriger als bei 1-mal wöchentlicher Applikation (Tab. 1). Die Zeit bis zur Konversion war in den Verum-Gruppen signifikant länger als in der Plazebo-Gruppe (p=0,008 bzw. p<0,001 für IFN beta-1a vs. Plazebo, Abb. 1).
Tab. 1. Wirksamkeit von subkutanem Interferon beta-1a auf die Konversion zu einer multiplen Sklerose nach den McDonald-Kriterien (2005) in der REFLEX-Studie [5]
|
Vergleich |
Hazard-Ratio (95%-KI) |
p-Wert |
Absolute Risikoreduktion (95%-KI) [Prozentpunkte] |
|
|
IFN beta-1a 3-mal wöchentlich vs. Plazebo |
0,49 (0,38–0,64) |
<0,0001 |
23,3 (12,6–34,0) |
|
|
IFN beta-1a 1-mal wöchentlich vs. Plazebo |
0,69 (0,54–0,87) |
0,008 |
10,3 (0,2–20,4) |
|
|
IFN beta-1a 3-mal wöchentlich vs. IFN beta-1a 1-mal wöchentlich |
0,71 (0,54–0,91) |
0,009 |
13,0 (2,0–24,0) |
KI: Konfidenzintervall
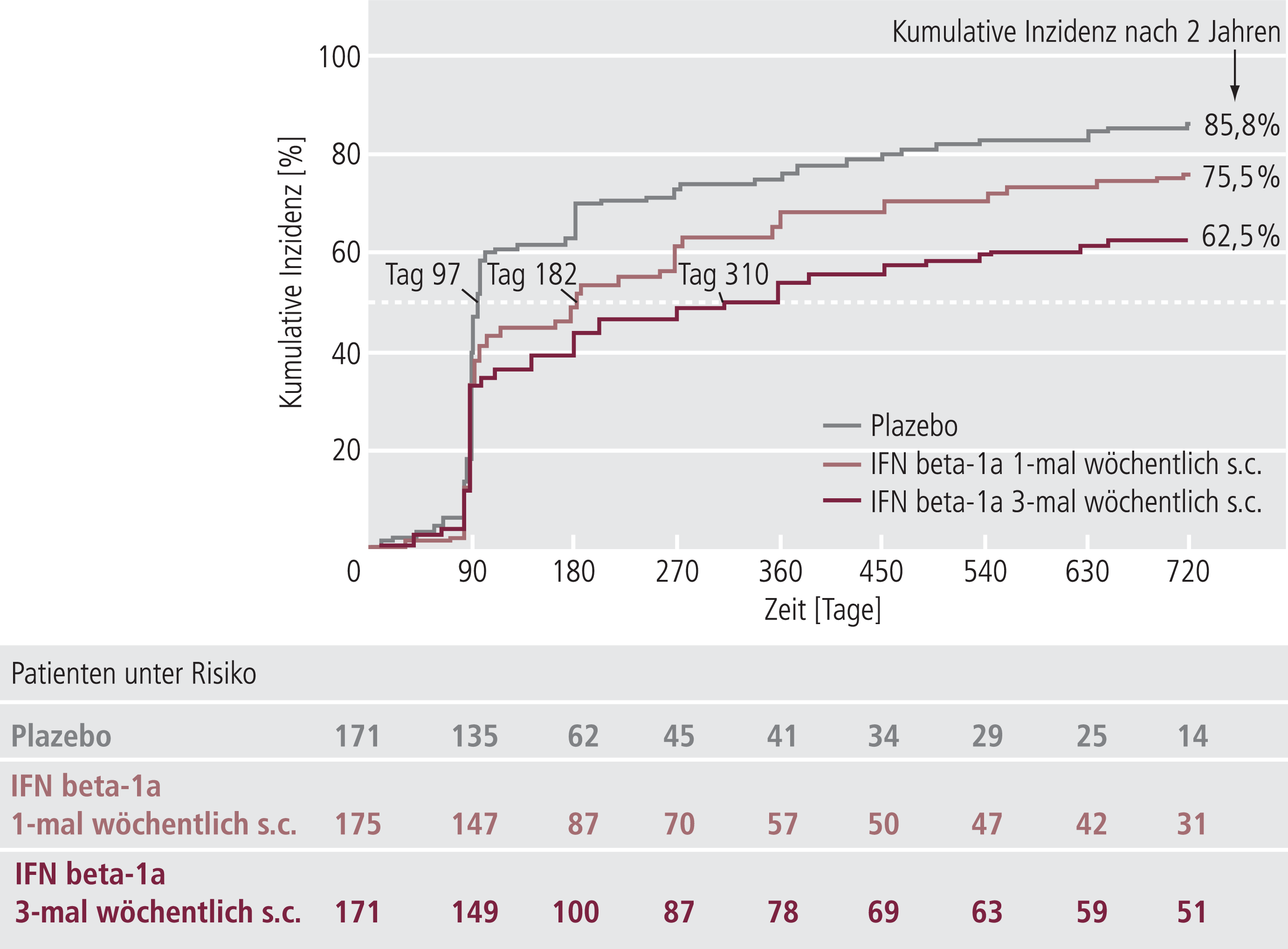
Abb. 1. Kaplan-Meier-Darstellung des primären Endpunkts der REFLEX-Studie: Konversion eines klinisch isolierten Syndroms in eine multiple Sklerose, die die Diagnosekriterien nach McDonald (2005) erfüllt [5]. IFN: Interferon; s.c.: subkutan
Die Wahrscheinlichkeit, eine klinisch manifeste MS zu entwickeln, war unter dem Interferon ebenfalls niedriger als unter Plazebo, hier zeigte sich jedoch kein Unterschied zwischen den beiden Interferon-Dosierungen (Anteil der Patienten mit Konversion 20,6 bzw. 21,6 vs. 37,5%; p<0,001 bzw. p=0,002 für 3-mal bzw. 1-mal wöchentlich IFN beta-1a vs. Plazebo).
Die mittlere Zahl der kombinierten aktiven Läsionen pro Patient und Scan, der wichtigste MRT-Parameter in dieser Studie, war in beiden Interferon-Gruppen niedriger als unter Plazebo (0,6 bzw. 1,23 vs. 2,70; jeweils p<0,0001 für IFN beta-1a 3-mal bzw. 1-mal wöchentlich vs. Plazebo). In diesem Endpunkt war die 3-mal wöchentliche Gabe der 1-mal wöchentlichen Gabe signifikant überlegen (p=0,0015).
Das Verträglichkeitsprofil von IFN beta-1a entsprach im Wesentlichen dem Bekannten. Überraschenderweise waren aber grippeartige Beschwerden bei 3-mal wöchentlicher Applikation seltener als bei 1-mal wöchentlicher Gabe (54 bzw. 71% vs. 20% [Plazebo]).
Zulassung von Interferon beta-1a beim klinisch isolierten Syndrom
Auf Basis dieser Studie wurde die Zulassung von subkutanem Interferon beta-1a (Rebif®) im Januar 2012 erweitert: Seitdem kann es nicht nur bei Patienten mit schubförmiger MS eingesetzt werden, sondern auch bei Patienten mit einem einzigen demyelinisierenden Ereignis mit aktivem Entzündungsprozess, wenn alternative Diagnosen ausgeschlossen wurden und ein hohes Risiko besteht, dass sich eine klinisch manifeste MS entwickelt [7].
Dafür, was unter einem hohen Risiko für die Entwicklung einer klinisch manifesten MS in der Praxis zu verstehen ist, gibt es keine allgemeingültige Definition. Nach Angaben in der Fachinformation kann von einem hohen Risiko ausgegangen werden, wenn im initialen MRT mindestens neun hyperintense T2-Läsionen und in einer Folgeaufnahme, die mindestens einen Monat nach der initialen Aufnahme angefertigt wird, mindestens eine neue T2-Läsion oder eine neue Gadolinium-anreichernde Läsion nachgewiesen werden [7]. Welche Erkrankungen vor Therapiebeginn ausgeschlossen werden müssen, wird in der Fachinformation nicht näher ausgeführt.
Leitlinie gibt Hinweise für die Praxis
In der neuen S2e-Leitlinie zur Diagnose und Therapie der MS [8] werden als Differenzialdiagnosen beispielhaft chronisch-infektiöse Erkrankungen (Neuro-Lues, Borreliose, HIV-Infektion), Kollagenosen, Vaskulitiden und Leukodystrophien sowie Sonderformen entzündlich demyelinisierender Erkrankungen (z.B. Neuromyelitis optica, akute disseminierte Enzephalomyelitis) genannt. Als weitere Erkrankungen mit ähnlichen Krankheitsbildern kommen Sarkoidose, zerebrovaskuläre und metabolischen Erkrankungen sowie Tumoren in Betracht.
Eine Indikation für einen Therapiebeginn nach dem ersten Schub besteht nach der der neuen Leitlinie, wenn eine intrathekale IgG-Synthese und eine subklinische Dissemination in der Magnetresonanztomographie nachgewiesen wurden und zusätzlich entweder
- ein funktionell beeinträchtigender Schub stattgefunden hat, der sich trotz Glucocorticoid-Hochdosistherapie innerhalb von zwei Monaten nur mangelhaft zurückgebildet hat, oder
- eine hohe Läsionslast besteht (≥6 Herde in der kraniellen MRT) oder
- wenn nach sechs Monaten Gadolinium-aufnehemnde Herde oder eine Zunahme der T2-Läsionen festgestellt werden.
Für die Therapie nach dem ersten Schub werden wie für die Behandlung der schubförmigen MS alle Basistherapeutika (Interferon beta-1a [s.c., i.m.], -1b, Glatirameracetat) gleichermaßen empfohlen [8].
Fazit
Zahlreiche Studien sprechen dafür, bei Patienten mit schubförmiger MS möglichst früh mit einer verlaufsmodifizierenden Basistherapie zu beginnen. Die Diagnose einer MS kann nach den aktuellen Kriterien (DGN/KKNMS-Leitlinie bzw. McDonald 2010) bei vielen Patienten bereits unmittelbar nach dem ersten Schub und mit einzeitiger Kernspintomographie gestellt werden. Doch selbst wenn diese Kriterien noch nicht erfüllt sind, ist es bei einem Teil der Patienten indiziert, mit einer immunmodulierenden Basistherapie zu beginnen – mit dem Ziel, die Entzündungsaktiviät im zentralen Nervensystem zu verringern und langfristig die Funktion der Nervenzellen zu erhalten.
Quellen
Prof. Dr. med. Ralf Gold, Bochun. MS-Presselunch „Wann beginnen, wie behandeln? Schlüsselfragen der modernen MS-Therapie“, veranstaltet von Merck Serono, Hamburg, 10. Februar 2012, Hamburg.
1. Jacobs LD, et al. Intramuscular interferon beta-1a therapy initiated during a first demyelinating event in multiple sclerosis. CHAMPS Study Group. N Engl J Med 2000;343:898–904.
2. Filippi M, et al. Interferon beta-1a for brain tissue loss in patients at presentation with syndromes suggestive of multiple sclerosis: a randomised, double-blind, placebo-controlled trial. Lancet 2004;364(9444):1489–96.
3. Kappos L, et al. Treatment with interferon beta-1b delays conversion to clinically definite and McDonald MS in patients with clinically isolated syndromes. Neurology 2006;67:1242–9.
4. Comi G, et al. Effect of glatiramer acetate on conversion to clinically definite multiple sclerosis in patients with clinically isolated syndrome (PreCISe study): a randomised, double-blind, placebo-controlled trial. Lancet 2009;374(9700):1503–11.
5. Comi G, et al. Comparison of two dosing frequencies of subcutaneous interferon beta-1a in patients with a first clinical demyelinating event suggestive of multiple sclerosis (REFLEX): a phase 3 randomised controlled trial. Lancet Neurol 2012;11:33–41.
6. European Medicines Agency. Assessment report Rebif, interferon beta-1a, Procedure No. EMEA/H/C/136/II/88/G (www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Assessment_Report_-_Variation/human/000136/WC500122183.pdf, Zugriff am 2.8.2012).
7. Fachinformation Rebif 44 Mikrogramm (Stand Januar 2012).
8. DGN/KKNMS Leitlinie zur Diagnose und Therapie der MS Online-Version, Stand: 17.07.2012 unter www.dgn.org/images/stories/dgn/leitlinien/LL_MS_Neu/dgn-kknms_ms-ll_20120717_frei.pdf (Zugriff am 30.7.2012).
Psychopharmakotherapie 2012; 19(05)
