Daniela Roesch-Ely, Heidelberg, Laura Speck, Karlsbad-Langensteinbach, Sven Ulrich, Magdeburg/Berlin, und Matthias Weisbrod, Heidelberg/Karlsbad-Langensteinbach
Schizophrenie zählt zu den schwersten psychischen Erkrankungen. Neben Symptomen wie Wahn, Halluzinationen und anderen, die als Positivsymptome zusammengefasst werden, leidet ein großer Teil der Betroffenen auch unter Negativsymptomen wie sozialem Rückzug, Affektverflachung, kognitiven Defiziten, Apathie und reduziertem Antrieb. Negativsymptome sind häufig die ersten auftretenden und die am stärksten überdauernden Symptome der Schizophrenie. Die pharmakologische Monotherapie mit konventionellen Antipsychotika und Antipsychotika der zweiten Generation zeigt für die Negativsymptomatik, im Unterschied zur Positivsymptomatik, nur eingeschränkten Behandlungserfolg [28–30].
Heute ist die pathogenetisch begründete Hypothese einer dopaminerg und noradrenerg bedingten Hypofrontalität die theoretische Grundlage bei schizophrener Negativsymptomatik [14, 28, 29]. Demzufolge kann eine Imbalance der präfrontalen und subkortikalen Dopamin- und Noradrenalinaktivität durch dopaminerge und noradrenerge Substanzen ausgeglichen werden und Versuche etwa mit serotonergen Antidepressiva scheinen weniger erfolgreich zu sein [34]. Deshalb sind pharmakologische Strategien von klinischer Relevanz, die vor allem den Dopamin- und Noradrenalinstoffwechsel in den mesokortikalen Netzwerken erhöhen. Ein vorgeschlagener Ansatz besteht in der begleitenden Therapie mit Dopaminagonisten, adjuvant zur Gabe von Antipsychotika. Die Ergebnisse einer Reihe von Fallstudien, in denen Bromocriptin (ein Dopamin-D2-Agonist) mit Haloperidol [24] oder Pergolid (ein Dopamin-D2/D1-Agonist) zusammen mit Amisulprid [33] verabreicht wurde, sowie prospektive Studien mit dem Dopamin-D2-Agonisten B-HT 920 unterstützen dies [31]. In ähnlicher Weise zeigen Patienten mit einem Schädel-Hirn-Trauma erhöhte Motivation und Ansprechen auf Belohnung unter Bromocriptin-Behandlung [32].
Eine dopaminerg und noradenerg geprägte Strategie besteht in der adjuvanten Verwendung eines irreversiblen und nichtselektiven MAO-A/B-Hemmers wie Tranylcypromin (TCP), wobei die vorwiegende Indikation dieser Arzneistoffgruppe die Depression, insbesondere therapieresistente Depression, ist. TCP ist in Deutschland der einzige pharmakopsychiatrisch verwendete Wirkstoff, mit dem das Prinzip der präfrontalen Dopamin- und Noradrenalinaktivierung mittels MAO-Hemmung umgesetzt werden kann. In Vorwegnahme dieser modernen Herangehensweise wurde bei bestimmten schizophrenen Patienten auch in Deutschland schon immer TCP eingesetzt. Das zeigt beispielsweise eine pharmakoepidemiologische Studie der LMU München und der FU Berlin für 1978 bis 1986. Von 803 TCP-Patienten wurden 66,0% wegen Depression, 15,7% wegen neurotischer Störungen, 7,8% wegen schizophrener Psychosen und 6,6% wegen einer bipolaren Störung behandelt [36]. Schon in ersten klinischen Erkundungsstudien zu MAO-Hemmern in der Psychiatrie wurden nicht nur depressive, sondern auch schizophrene Patienten einbezogen. So berichtet W. Geller 1962 in Bonn von 50 mit MAO-Hemmern behandelten Patienten, darunter 20 schizophrene Patienten. Er betont die besondere Eignung als Adjuvans zu Phenothiazinen und Thioxanthenen bei „Defektschizophrenien ohne akute Symptomatik“ [16]. Die ausschließliche Einordnung von MAO-Hemmern als antidepressive Psychopharmaka wird empirisch verworfen, wobei aber auch deren Grenzen in der Schizophreniebehandlung schon gesehen werden: „Kontraindiziert erscheinen vor allem wahnbildende Formen und Erregungszustände.“ Während aber der primäre Wirkungsmechanismus bei Depression schon als verstanden galt, wurde in einer Übersicht klinischer Studien zu MAO-Hemmern bei chronischer Schizophrenie aus dem Jahr 1980 die pharmakologische Begründung dafür noch als „obskur“ bezeichnet [7].
Adjuvantes TCP zur Antipsychotika-Therapie schizophrener Patienten mit Negativsymptomatik wurde bisher in elf klinischen Studien untersucht [4, 8–10, 19, 20, 22, 26, 35, 38, 41], die Mehrzahl in den 1960er Jahren. Der gezeigte Vorteil der Kombination gegenüber Antipsychotika allein war teilweise gering, wobei diese Studien einer explorativen Testphase hinsichtlich Dosis und Erkrankungsbild zuzuordnen sind. So wurden hohe Dosen von 60 bis 80 mg TCP verwendet [4, 35, 38] und keineswegs nur schizophrene Negativsymptomatik behandelt [20]. Aus heutiger Sicht ist weiter hervorzuheben, dass diese Ergebnisse ausschließlich aus der Ära der Antipsychotika der ersten Generation stammen. Daten zur Kombination von TCP mit Antipsychotika der zweiten Generation und unter modernen Therapieverhältnissen liegen nicht vor. In zwei neuen kontrollierten Studien mit 40 und 60 Patienten war der MAO-B-Hemmer Selegilin adjuvant zu Antipsychotika der zweiten Generation der Monotherapie mit Antipsychotika der zweiten Generation leicht überlegen. Es wurde eine stärkere Abnahme der Negativsymptomatik und des PANSS-Gesamtwertes gefunden [2, 6].
Pharmakologie von TCP
Die Hemmkonstanten des pharmakologischen Primäreffektes von TCP sind sehr niedrig (MAO-A: IC50=76 nmol/l, MAO-B: IC50=90 nmol/l, jeweils Homogenisate von Rattenhirn), was eine hochspezifische Wirkung bei Konzentrationen um 10 ng/ml (= 75 nmol/l) ausmacht [12]. Durch die MAO-Hemmung werden in verschiedenen Hirnarealen synaptisches Serotonin (163 bis 256%), Noradrenalin (171 bis 263%) und Dopamin (119 bis 206%) sowie weitere, im ZNS in viel geringerer Konzentration vorliegende Amine (sogenannte trace amines wie 2-Phenylethylamin) erhöht [15]. Verglichen mit anderen Hirnregionen wie Nucleus caudatus (119%), Nucleus accumbens (133%) und Hypothalamus (198%) war die Erhöhung von Dopamin im frontalen Kortex mit 206% am ausgeprägtesten [17]. Es sollte dabei nicht vergessen werden, dass die Konzentration von Metaboliten der Neurotransmitter gleichzeitig erheblich abnimmt. Die klinische Relevanz abnehmender Metaboliten von Neurotransmittern während der Behandlung mit MAO-Hemmern wird bisher nur im Ansatz verstanden [11].
Bei steigenden Dosen von TCP können zum pharmakologischen Primäreffekt sekundäre Wirkungen wie Noradrenalin-Wiederaufnahmehemmung und eine Amfetamin-ähnliche Wirkung der Transmitterfreisetzung hinzukommen. So betrugen die Hemmkonstanten (IC50) in Homogenisaten von Rattenhirn für die Noradrenalin-Wiederaufnahmehemmung 0,43 µmol/l (60 ng/ml) und für die Dopaminfreisetzung ≈ 10 µmol/l (ca. 1300 ng/ml) [3, 18]. Die Maximalspiegel im Plasma von Probanden, die nach ≈ 2 Stunden (tmax) gefunden werden, betragen für eine Dosis von 20 mg TCP etwa 50 bis 75 ng/ml. Sie nehmen aber wegen einer sehr kurzen Halbwertszeit (t1/2) von ≈ 2 Stunden schnell wieder Werte von nur 1 bis 10 ng/ml an und es kommt nicht zu einer Kumulation [39]. Zumindest für kurze Zeit um tmax sollte also neben MAO-Hemmung auch eine Noradrenalin-Wiederaufnahmehemmung im ZNS vorliegen, insbesondere auch da die Konzentration im Gehirn höher ist als im Plasma (bei Versuchstieren 3- bis 4-mal [12]). Schließlich ist so ab einer Dosis von 80 bis 100 mg TCP auch eine direkte Wirkung auf die Dopamin- und Noradrenalinfreisetzung abschätzbar. Eine indirekte Stimulation der Monoaminfreisetzung ist ebenfalls denkbar, denn durch MAO-Hemmung 100fach erhöhtes Phenylethylamin ist als Monoaminfreisetzer bekannt [3, 15]. Wenn auch manchmal als „endogenes Amphetamin“ bezeichnet, sind jedoch pharmakologische Unterschiede zwischen Phenylethylamin und Amfetamin evident [21].
Andere psychiatrisch verwendete MAO-Hemmer unterscheiden sich von TCP. Mit dem reversiblen und selektiven MAO-A-Hemmer Moclobemid erreicht die Erhöhung der Serotonin-Konzentration im Gehirn von Versuchstieren nur etwa 50% der von TCP und hielt auch weniger lange an. Die Dopamin-Konzentration wird nicht erhöht [13]. Der irreversible MAO-A/B-Hemmer Phenelzin hat einen geringeren Einfluss auf die Noradrenalin-Wiederaufnahmehemmung und die Dopaminfreisetzung [3].
Zusammengefasst gibt es theoretische Grundlagen und klinische Hinweise darauf, dass die adjuvante Therapie von TCP zu Antipsychotika bei schizophrenen Patienten mit überwiegender Negativsymptomatik eine klinische Besserung herbeiführen kann. Zu Nutzen und Risiken des Einsatzes in dieser Indikation gibt es aber keine neueren Daten. Anliegen dieser Arbeit war daher die Untersuchung der Sicherheit und praktischen Umsetzung der TCP-Therapie schizophrener Patienten mit überwiegender Negativsymptomatik in einem modernen therapeutischen Umfeld. Im Vordergrund stand dabei die Kombinationsfähigkeit mit Antipsychotika der zweiten Generation, das Risiko der Verschlechterung von Positivsymptomatik und die Einhaltung der notwendigen tyraminarmen Diät bei schizophrenen Patienten. Weiterhin sollten Daten zur Abschätzung des erzielten Therapieerfolgs gewonnen werden.
Patienten und Methoden
Die Studie wurde ab 2006 als retrospektive Auswertung von Patientenakten der psychiatrischen Klinik am SRH-Klinikum Karlsbad-Langensteinbach durchgeführt. Einschlusskriterien waren stationäre Behandlung, Diagnosegruppe F2X (v. a. Schizophrenie) und mindestens drei Tage Einnahme von TCP. Durch das Screening der Patientenakten sollten 100 TCP-Patienten gefunden werden, und zwar 50, die TCP auch als Entlassungsmedikation erhielten, und 50, bei denen TCP im Verlaufe der stationären Therapie wieder abgesetzt wurde. Falls die Zahl 50 in einer Gruppe nicht erreicht würde, sollte mit Patienten der anderen Gruppe auf die geplante Gesamtzahl von 100 aufgefüllt werden. Da die verwertbaren Daten in einer uneinheitlichen und komplexen Form sowie überwiegend als Freitext vorlagen, erfolgte die Erhebung der Rohdaten mit fünf in Felder strukturierten Formularen. Die Wahl- und freien Textfelder wurden entsprechend der Zielstellung und den Erwartungen zur auffindbaren Information gestaltet. Die Gliederung der Formulare und Felder war
1) Demographische Daten (18 Felder),
2) Therapiebeginn (12 Felder),
3) Vormedikation und Therapieverlauf (10 Felder),
4) Nebenwirkungen (6 Felder),
5) tyraminarme Diät (3 Felder).
Hauptfelder vor Therapiebeginn mit TCP waren beispielsweise extrapyramidal-motorische Symptome (EPS), Prolactinspiegel, Zunahme und Abnahme Körpergewicht sowie unerwünschte Arzneimittelwirkungen (UAW). Im Verlauf der Therapie mit TCP umfasste dies neben den genannten UAW weiterhin 23 Unterfelder zu möglichen neu aufgetretenen UAW. Zur tyraminarmen Diät wurden die Umsetzbarkeit und Wahrnehmung von Aufwand und Einschränkungen durch den Patienten und fremdanamnestisch (medizinisches Personal/Angehörige) sowie die Bewertung der Diät-Compliance erfasst. Zu Beginn der adjuvanten TCP-Therapie und im Therapieverlauf wurden vier Symptome der Positivsymptomatik (Halluzinationen, Wahn, Ich-Störungen, Feindseligkeit), fünf Symptome Negativsymptomatik (sozialer Rückzug, Affektverflachung, kognitive Defizite, Apathie, reduzierter Antrieb) und sieben Symptome Depression (Interessenverlust, Freudlosigkeit, Schlafstörungen, Traurigkeit, Appetitstörungen, Suizidalität, andere) erhoben. Auf eine weitere detaillierte Darstellung wird aus Platzgründen verzichtet. Nach den ersten zehn Patienten wurde die Eignung der Formulare kritisch überprüft.
Die statistische Auswertung erfolgte mit deskriptiven Methoden. Der mögliche Zusammenhang einer Besserung der Negativsymptomatik und des verwendeten Antipsychotikums, wirksam oder nicht wirksam gemäß [23], wurde anhand der Häufigkeiten mit der Chi2-Statistik ausgewertet. Sämtliche Rohdaten wurden aus den Quelldaten anonym zusammengestellt und weiterverarbeitet. Die Ethikkommission der medizinischen Fakultät der Universität Heidelberg hat dem Studienprotokoll zugestimmt.
Ergebnisse
Patienten und Vormedikation
Beim retrospektiven Screening von 2006 bis 2001 wurden die Daten von 53 Patienten mit TCP-Behandlung gefunden. Darunter war nur ein Patient (40 Jahre, männlich), bei dem TCP nach acht Wochen abgesetzt wurde (10 bis 20 mg/Tag TCP, weiterhin Risperidon und Olanzapin). Spezielle Gründe des Abbruchs von TCP wie UAW oder besonderer Therapieerfolg waren nicht erkennbar. Bei alle anderen Patienten war TCP Teil der Entlassungsmedikation. Deshalb erfolgt eine gemeinsame Auswertung aller Patienten und auf die geplante Gegenüberstellung von Therapiefortsetzern und -abbrechern wurde verzichtet. Einen Überblick der wesentlichen demographischen Daten gibt Tabelle 1.
Tab. 1. Demographische Daten von 53 Patienten der Studie zu Beginn der adjuvanten Tranylcypromin-Behandlung*
|
Geschlecht |
40 Männer, 13 Frauen |
|
Alter |
32,2 Jahre (18–56) |
|
Körpergewicht |
80,9 kg (54–117) |
|
Body-Mass-Index |
26,2 kg/m2 (18,3–38,6) |
|
Übergewicht |
Leicht: n=14; stark: n=13 |
|
Rauchen |
Raucher: n=15; |
|
Schulbildung |
Mittlere Reife: n=21; |
|
Berufsausbildung |
n=39 |
|
Zuletzt arbeitslos |
n=43 |
|
Familienstand |
Ledig: n=47; |
|
Kinder |
Ja: n=4; nein: n=33; |
|
Wohnsituation |
Allein: n=33; |
* Mittelwert (Bereich) oder Anzahl (n)
Bei der Mehrzahl der Patienten lag eine chronische Schizophrenie (F20.X) mit überwiegender Negativsymptomatik und keiner oder sehr geringer Positivsymptomatik vor (Tab. 2). Darunter befanden sich elf Patienten, für die die Erkrankung erst ein halbes Jahr manifest war. Für die meisten Patienten wurden außerdem depressive Symptome diagnostiziert, aber nur 15 Patienten mit schwerer Ausprägung. 49 Patienten wurden mit Antipsychotika der zweiten Generation vorbehandelt (Abb. 1), davon 30 mit mehr als einem Antipsychotikum gleichzeitig. Nur vier Patienten erhielten keine Antipsychotika vor TCP. Weiterhin wurde bei 48 Patienten vor TCP eine adjuvante Behandlung mit einem anderen Antidepressivum durchgeführt, in der Mehrzahl selektive Serotonin-Wiederaufnahmehemmer (SSRI; n=15), trizyklische Antidepressiva (TZA) und Venlafaxin (je n=7).
Tab. 2. Klinische Daten von 53 Patienten vor Beginn der adjuvanten Behandlung mit Tranylcypromin
|
Parameter |
Klinische Daten |
|
Primärdiagnosen (ICD-10) |
F20.X Schizophrenie (n=47), F25.X schizoaffektive Störung (n=5), |
|
Sekundärdiagnosen |
Persönlichkeitsstörungen (n=3), Substanzabhängigkeit (n=3), |
|
Erkrankungsdauer |
3,2 Jahre (0,5–16)*; 0,5 Jahre (n=11), 1 bis 2 Jahre (n=14), |
|
Stationäre Behandlungen |
0 (n=3), 1 (n=16), 2 bis 3 (n=17), >3 (n=15) |
|
Negativsymptomatik |
|
|
Schweregrad |
Keine (n=0), leicht (n=0), mittelschwer (n=21), schwer (n=32) |
|
Anzahl Symptome pro Patient |
0 (n=0), 1 (n=6), 2 (n=15), 3 (n=23), 4 (n=7), 5 (n=1) |
|
Anzahl Symptome gesamt |
Sozialer Rückzug (n=14), Affektverflachung (n=31), |
|
Positivsymptomatik |
|
|
Schweregrad |
Keine (n=37), leicht (n=3), mittelschwer (n=13), schwer (n=0) |
|
Anzahl Symptome pro Patient |
0 (n=37), 1 (n=14), 2 (n=2), 3 (n=0), 4 (n=0) |
|
Anzahl Symptome gesamt |
Halluzinationen (n=7), Wahn (n=6), Ich-Störungen (n=4), |
|
Depression |
|
|
Schweregrad |
Keine (n=11), leicht (n=1), mittelschwer (n=26), schwer (n=15) |
|
Anzahl Symptome pro Patient |
0 (n=11), 1 (n=13), 2 (n=15), 3 (n=12), 4 (n=2), 5 bis 7 (n=0) |
|
Anzahl Symptome gesamt |
Interessenverlust (n=16), Freudlosigkeit (n=31), Schlafstörungen (n=11), Traurigkeit (n=22), Appetitstörungen (n=1), Suizidalität (n=6), |
|
Empfehlung |
Rehabilitation oder nicht arbeitsfähig (n=38), arbeitsfähig oder Ausbildung in geschützter Umgebung (n=14) |
* Mittelwert (Bereich)
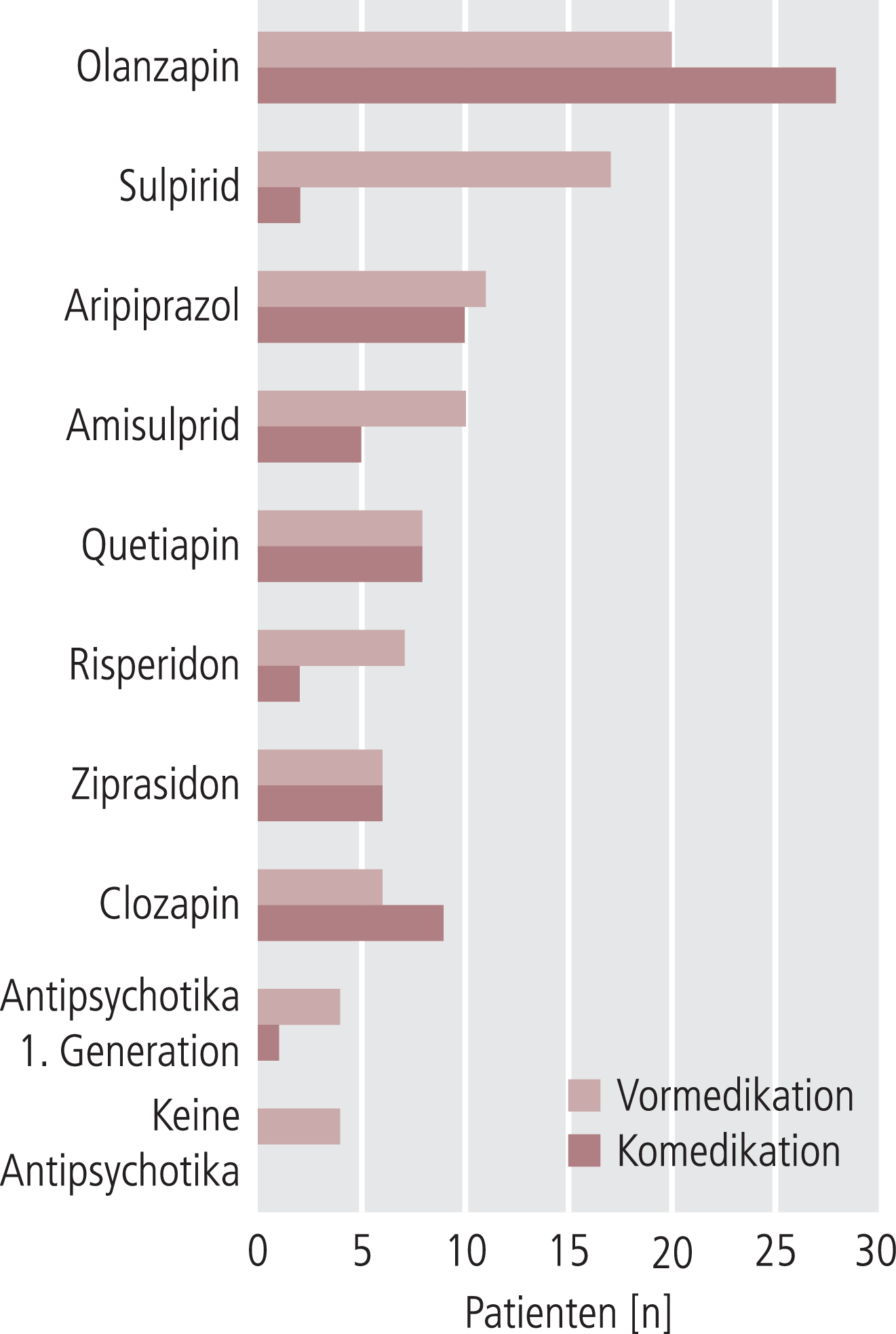
Abb. 1. Antipsychotika vor und während der adjuvanten Tranylcypromin-Behandlung schizophrener Negativsymptomatik für n=53 Patienten (AP=Antipsychotika)
Dosis von TCP und Komedikation
Die Aufdosierung von TCP dauerte im Durchschnitt 3,8 Wochen (1 bis 17). Die Entlassungsdosis betrug nach durchschnittlich 9 Wochen (1 bis 19) Therapiedauer durchschnittlich 36,0 mg/Tag (20 bis 50), wobei nur drei Patienten 50 mg/Tag TCP erhielten. Alle vor TCP verordneten Antidepressiva wurden abgesetzt, bei serotonergen Substanzen mit der notwendigen Pause. Alle Patienten erhielten während TCP Antipsychotika, in der Mehrzahl Antipsychotika der zweiten Generation (Abb. 1). Bei den vier nicht vorbehandelten Patienten wurde ein Antipsychotikum zusammen mit TCP neu verordnet. Bei 20 von 30 Patienten, die vor TCP mehr als ein Antipsychotikum gleichzeitig erhielten, wurde auf ein Antipsychotikum während TCP reduziert. Bei 15 von 19 Patienten mit einem Antipsychotikum vor TCP wurde dieses während TCP beibehalten und nur bei vier das Antipsychotikum gewechselt. Das Absetzen oder der Wechsel des Antipsychotikums stand bei einigen Patienten offensichtlich im Zusammenhang mit erhöhtem Prolactin. Demzufolge nahm die Verordnung von Sulpirid, Amisulprid und Risperidon während TCP ab und von Olanzapin und Clozapin zu. Die vor TCP verordneten Stimmungsstabilisierer (Lithium, Valproinsäure, Lamotrigin) wurden beibehalten. Kein Patient erhielt Benzodiazepine vor oder während TCP. Die somatische Komedikation umfasste Betablocker und Myrtol (je n=3), Levothyroxin und Magnesium (je n=2), Trimethoprim/Sulfamethoxazol, Dihydroergotamin, Lactulose und Pirenzepin (je n=1).
Sicherheit von adjuvantem TCP
Für keinen Patienten wurde eine Verschlechterung oder Exazerbation von Positivsymptomatik verzeichnet; für zwei Patienten lag sogar eine Verbesserung von Halluzinationen vor. Zur Umsetzbarkeit der notwendigen tyraminarmen Diät und zur Wahrnehmung von Aufwand und Einschränkungen dadurch waren den Unterlagen keine ausreichenden Informationen seitens Patienten oder fremdanamnestisch zu entnehmen. Für die sich ableitende Diät-Compliance war bei 34 Patienten ebenfalls keine Information erhältlich, für 18 wurde eine gute und für einen Patienten ein schlechte Diät-Compliance gefunden. Schwerwiegende UAW oder Interaktionen traten nicht auf, insbesondere keine Hypertonie infolge Diätfehler. Es wurden nur wenig nicht schwerwiegende UAW registriert: orthostatische Dysregulation/Hypotonie (n=1, Gabe von Dihydroergotamin), Schlafstörungen (n=1), Akathisie (n=1) sowie auch schon vor der TCP-Behandlung aufgetretene Dyskinesie oder Tremor (n=2). Das Körpergewicht von 23 Patienten nahm während der Gesamtbehandlung zu, teilweise deutlich um 5 bis 10 kg (n=6) und >10 kg (n=3).
Besserung der schizophrenen Negativsymptomatik
Bei keinem Patienten verschlechterten sich schizophrene Negativsymptomatik oder depressive Symptome. Für 23 Patienten wurde eine Besserung der Negativsymptomatik gefunden. Am häufigsten schloss das eine Verbesserung von reduziertem Antrieb ein (n=20). Die weitere Besserung auf Symptomebene betraf für die Negativsymptomatik kognitive Defizite (n=6), sozialen Rückzug (n=5), Affektverflachung (n=3) sowie Apathie (n=1).
Zur Auswertung der Besserung der depressiven Symptomatik wurden auch die Patienten herangezogen, die zu Beginn keine Angaben zur Depression hatten, aber zum Verlauf. Entsprechend wurde für 11 von 46 eine Besserung der depressiven Symptomatik gefunden. Die häufigsten gebesserten Symptome waren Freudlosigkeit (n=8) und Traurigkeit (n=6). Eine gemeinsame Auswertung der Besserung von schizophrener Negativsymptomatik und depressiver Symptome ist Abbildung 2 zu entnehmen. Für 25 Patienten (47%) wurde eine Besserung in wenigstens einem Symptom von Negativsymptomatik oder Depression gefunden. Die Häufigkeitsverteilung der Zahl gebesserter Symptome ist in Abbildung 3 dargestellt.
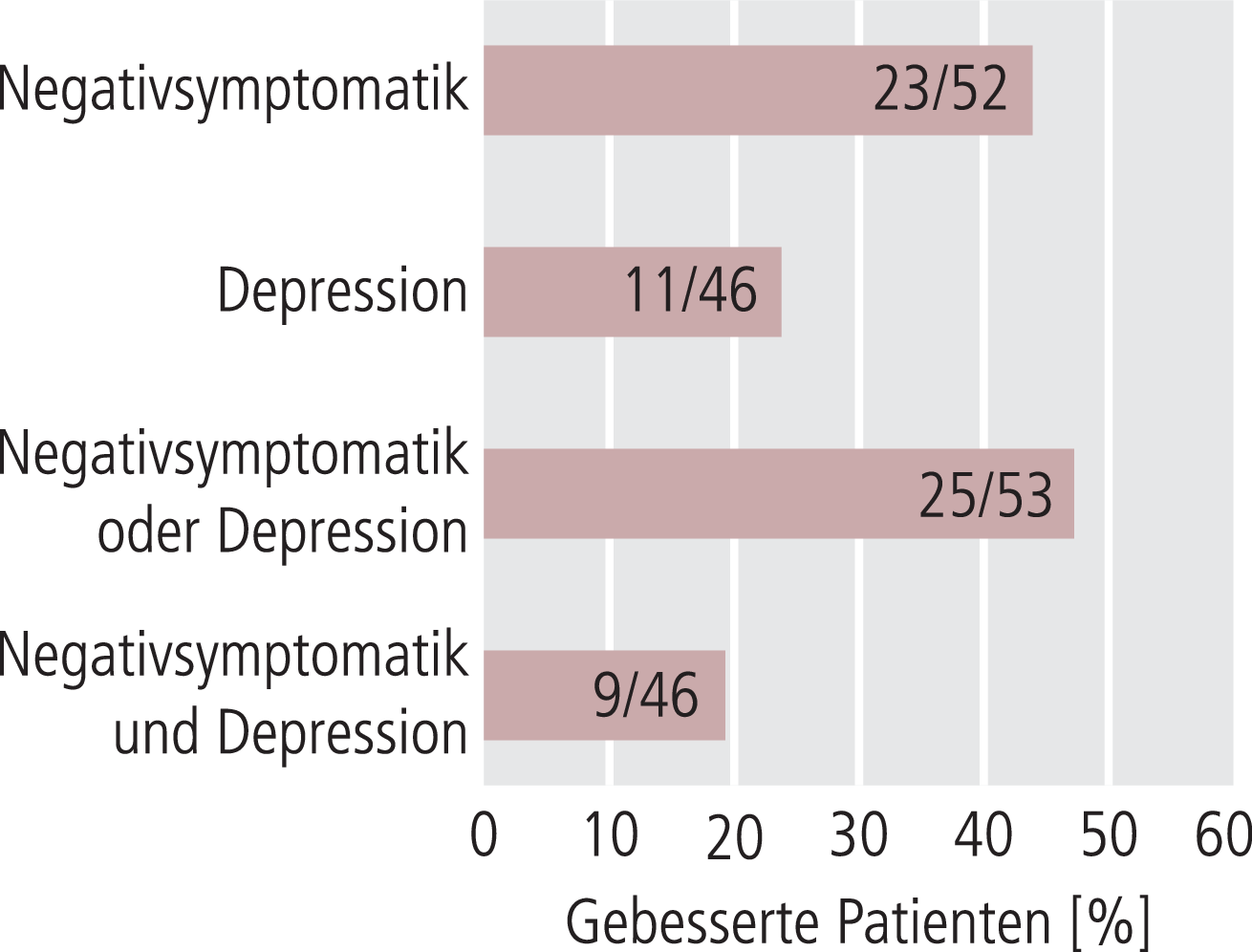
Abb. 2. Prozentualer Anteil klinisch gebesserter schizophrener Patienten (Negativsymptomatik und/oder Depression) während der adjuvanten Behandlung von 53 Patienten mit Tranylcypromin und Antipsychotika der zweiten Generation als Basistherapie
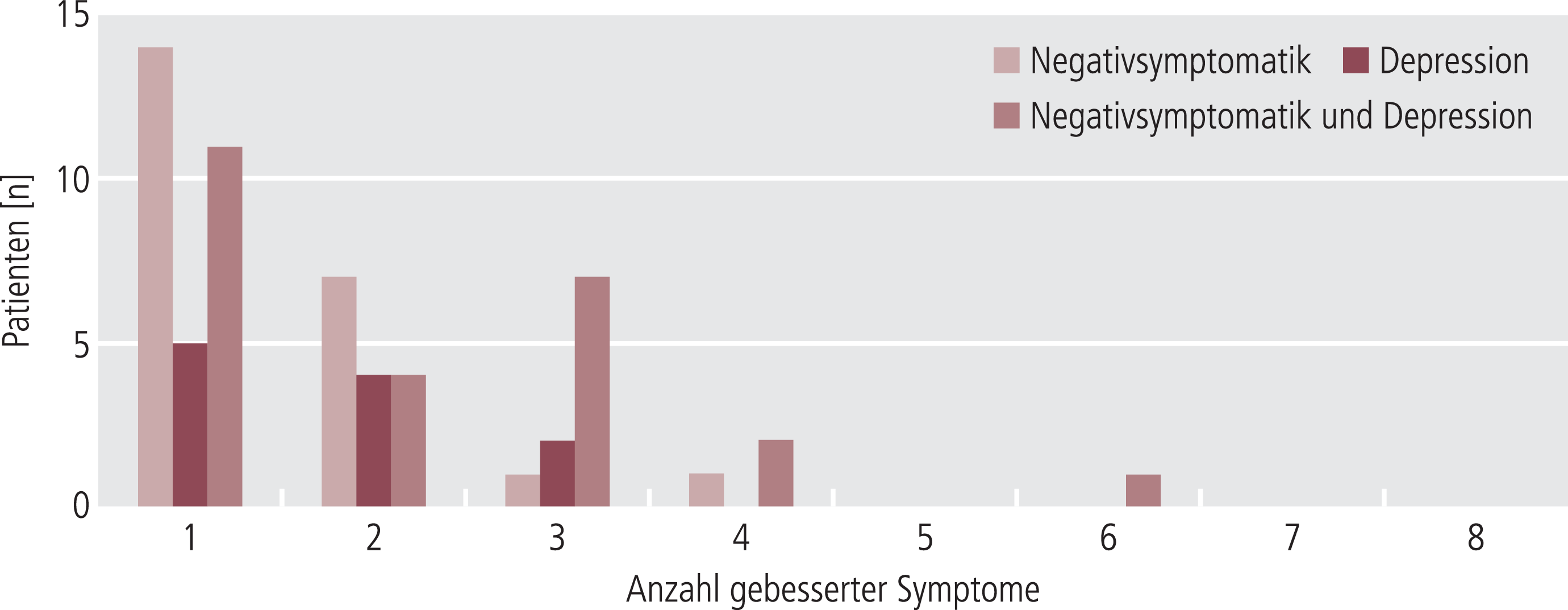
Abb. 3. Häufigkeitsverteilung gebesserter Symptome von schizophrener Negativsymptomatik und Depression während der adjuvanten Behandlung von 53 Patienten mit Tranylcypromin und Antipsychotika der zweiten Generation als Basistherapie
In einer aktuellen Metaanalyse kontrollierter Studien wurde nur für Amisulprid, Clozapin, Olanzapin und Risperidon eine Besserung der Negativsymptomatik im Vergleich mit konventionellen Antipsychotika gefunden, nicht aber für Aripiprazol, Quetiapin, Sertindol, Ziprasidon und Zotepin [23]. Eine entsprechend vorgenommene Eingruppierung der Patienten nach dem verwendeten Antipsychotikum (32 wirksame, 21 unwirksame) ergab für die Häufigkeit der Besserung der Negativsymptomatik, hier bei adjuvantem TCP, keinen signifikanten Unterschied (Chi2=1,53, p=0,216).
Diskussion
Anliegen dieser Arbeit war im Rahmen einer retrospektiven Erhebung von Patientendaten die Untersuchung der Sicherheit und praktischen Umsetzung der adjuvanten TCP-Therapie schizophrener Patienten mit überwiegender Negativsymptomatik. Im Vordergrund standen dabei die Kombinationsfähigkeit mit Antipsychotika der zweiten Generation, das Risiko der Verschlechterung von Positivsymptomatik und die Einhaltung der notwendigen tyraminarmen Diät bei schizophrenen Patienten.
Komedikation
Die Ergebnisse weisen darauf hin, dass TCP gemeinsam mit Antipsychotika der zweiten Generation sicher in der Behandlung schizophrener Patienten mit überwiegender Negativsymptomatik ist. Zur Arzneimittelsicherheit könnte auch beigetragen haben, dass die Zahl von gleichzeitig gegebenen Antipsychotika mit Beginn TCP reduziert wurde. Mit allen derzeit auf dem Markt befindlichen Antipsychotika der zweiten Generation scheint kein besonderes Potenzial für Wechselwirkungen zu bestehen. Dies ist in Übereinstimmung mit aktuellen Daten der Behandlung depressiver Patienten [1]. Mit Antipsychotika der ersten Generation wurden ebenfalls keine Interaktionen gefunden. Viele Autoren berichteten dagegen sogar über eine Abschwächung von UAW und Risiken der Monotherapien wie extrapyramidal-motorischen UAW und Depression während Antipsychotika- und dem Tyramineffekt während TCP-Gabe (Tab. 3). TCP wurde in Deutschland außerdem viele Jahre in einer fixen Kombination mit einem Antipsychotikum klinisch angewendet (10 mg TCP + 1 mg Trifluoperazin). Verdachtsfälle in der Literatur von Interaktionen zwischen TCP und Antipsychotika der zweiten Generation sind sehr selten und nicht schwerwiegend [40]. Im Unterschied zu depressiven Patienten [1, 5] und in Übereinstimmung mit früheren Studien (Tab. 3) erfolgte keine Komedikation mit Benzodiazepinen.
Für die somatische Komedikation sei hier nur die Auffälligkeit hinsichtlich Betablocker diskutiert. Diese wurden trotz Kontraindikation gemäß Fachinformation (Metoprolol, n=2) oder nicht empfohlener gemeinsamer Verordnung (Bisoprolol, n=1) zusammen mit TCP gegeben. In einer vergleichbaren Studie erhielten 7 von 32 depressiven Patienten gleichzeitig Betablocker und TCP [1]. In der Literatur wird die gute Möglichkeit der gemeinsamen Gabe gezeigt [27].
Tab. 3. Übersicht der klinischen Studien zur kombinierten Therapie von Antipsychotika mit Tranylcypromin bei Schizophrenie
|
Studie |
Design |
n |
Tagesdosis [mg] |
Patienten |
Dauer |
Ergebnis Negativsymptomatik |
Positivsymptomatik |
UAW |
Bewertung durch Autoren |
|
Kruse 1960 [22] |
Offen 1) TFP+TCP |
40 |
TFP: 20–30 TCP: 20–30 |
Im Mittel 12 Jahre erfolglos behandelt, „hard core“ |
2–3 Monate |
9 R (langsame, markante Abnahme von Apathie und Niedergeschlagenheit, verbesserte Konzentrations- und Entscheidungsfähigkeit, Zunahme von Interesse und psychomotorischer Aktivität) |
3 gebessert |
n. u. |
Gutes Ergebnis angesichts Vorgeschichte |
|
Singh 1960 [38] |
Offen 1) TFP+TCP |
25 |
TFP: 4–10 TCP: 30–80 |
14 Schizophrene: mit AP vorbehandelt, NR, Negativsymptomatik |
6 Wochen |
4 stark gebessert, 9 gebessert, 2 unverändert, 2 verschlechtert |
1 Exazerbation |
4 Hypotension (drop-out), 3 erhöhte alkal. Phosphat. (drop-out), Agitation, Insomnie, Akathisie, Müdigkeit, Miktionsstörungen, Hypotension |
Kombination ist vielversprechend |
|
Buffaloe 1961 [10] |
RCT 1) TFP+Plz 2) TFP+TCP |
20 |
TFP: 2–30 TCP: 30 |
Zuvor PhT, chronisch anerge Schizophrenie, 13–33 Jahre vorbehandelt |
5 Wochen |
Kein Unterschied zwischen 1) und 2) |
n. u. |
Kein Unterschied zw. 1) und 2) |
Kein therapeutischer Vorteil für TFP+TCP |
|
Vogt 1961 [41] |
RCT 1) TFP+Plz 2) TFP+TCP |
50 |
TFP: 40 TCP: 30 |
39 Schizophrene, >5 Jahre krank, vorbehandelt mit AP, „withdrawn“ (introvertiert) |
3 Monate |
1) 8 stark gebessert, 10 gebessert, 8 unverändert 2) 6 stark gebessert, 13 gebessert, 5 unverändert |
n. u. |
Keine schwerwiegenden UAW, TCP verstärkt EPS |
Kleiner Vorteil der Kombination möglich |
|
Barsa 1962 [4] |
Offen 1) PhT+TCP |
70 |
PhT: ? TCP: bis 60 |
2–28 Jahre hospitalisiert, > 2 Jahre erfolglos AP |
4–8 Monate |
25 R (7 Remission, 10 moderat, 8 gering), 25 NR |
20 verschlechtert (9 drop-out), reversibel nach Absetzen TCP |
Keine schweren UAW, orthostatische Dysregulation (Dosis gesenkt) |
Insgesamt vielversprechend |
|
Hordern 1962 [20] |
RCT 1) TFP+Plz 2) TFP+TCP 3) Plz+Plz |
75 |
TFP: 40 TCP: 40 |
Schizophrene, >2 Jahre hospitalisiert |
9 Wochen |
Keine signifikanten Unterschiede |
Score paranoide Inhalte: 1) 44% Verschlechterung 2) 39% Besserung 3) 38% Verschlechterung |
2) 7 Patienten: orthostatische Dysregulation mit Synkope, Kopfschmerzen, Sedierung (kein Absetzen notwendig, insgesamt mild), EPS in allen 3 Gruppen |
Besserung 2) >3) signifikant, Besserung 1) >3) nicht signifikant (Ärztescore Schizophrenie-bezogener Faktoren), Ergebnis teilweise gegenläufig für Schwesternscore Funktionalität der Patienten |
|
Schiele 1963 [35] |
RCT 1) TFP+Plz 2) TFP+TCP |
60 |
TFP: 30–40 TCP: 60 |
Weniger lange therapieresistent, 12 gar nicht vorbehandelt |
2 Monate |
Starke Besserung in 1) und 2), kein signifikanter Unterschied, Trend für Vorteil im Symptomcluster Zurückgezogenheit für 2) |
Verschlechterung je 1 pro Gruppe |
10 drop-out (3 TCP) |
TCP ja wenn ausreichend lange, erfolglos mit AP allein behandelt |
|
Mena 1964 [26] |
RCT 1) TCP+Plz 2) TCP+TFP |
27 |
TCP: 40 TFP: 4 |
Ambulante, therapieresistente Schizophrenie, ohne Akutsymptomatik |
4 Wochen |
Symptomatische Besserung: 1) 40,7%, 2) 40,0% |
Keine Verschlechterung in 1) und 2) |
1) Mundtrockenheit, orthostatische Dysregulation, 2) Benommenheit |
Besserung auch ohne AP möglich |
|
Bucci 1969 [8] |
Offen 1) CPZ+TCP |
20 |
CPZ: 300–450 TCP: 20 |
Paranoide Schizophrenie, mehrere Monate erfolglos mit AP behandelt, Tagesklinik |
4 Monate |
16 stark gebessert, 4 sehr wenig gebessert |
Keine |
Keine |
Kombination relativ sicher und klinisch nützlich, TCP verstärkt antipsychotischen Effekt von CPZ |
|
Hedberg 1971 [19] |
RCT, 1) TFP+Plz 2) TFP+TCP 3) TCP+Plz |
96 |
TFP: 8–32 TCP: 20–30 |
Akut, chronische Schizophrenie u. a. (nicht speziell Negativsymptomatik) |
2 Monate pro Therapiearm |
Beste Response bei chronischer Schizophrenie: 1) 26%, 2) 40%, 3) 34%, signifikante Besserung Anhedonie und Depression bei Übergang von 1) auf 2) |
2) n. u. |
Kombination: gegenseitige Abschwächung der UAW, verringertes Risiko Tyramineffekt |
Keine |
|
Bucci 1987 [9] |
RCT 1) CPZ+Plz 2) CPZ+TCP |
30 |
CPZ: 300 TCP: 20 |
Persistierende Negativsymptomatik, ca. 30% mit leichter Positivsymptomatik, ambulant |
4 Monate |
1) 0% R, 2) 73% R, in einer 2. Behandlungsphase von 4 Monaten auch in 1) 87% R nach Beginn TCP |
n. u. |
TCP reduziert EPS, verringertes Risiko Tyramineffekt |
CPZ+TCP sicher, Bezeichnung MAO-Hemmer allein als AD nicht korrekt |
AD: Antidepressivum, AP: Antipsychotika, CPZ: Chlorpromazin, EPS: extrapyramidal-motorische Nebenwirkungen, NR: Nonresponder, n. u.: nicht untersucht, PhT: Phenothiazine, Plz: Plazebo, R: Responder, RCT: randomisierte und kontrollierte Studie, TCP: Tranylcypromin, TFP: Trifluoperazin, UAW: unerwünschte Arzneimittelwirkungen
Unerwünschte Arzneimittelwirkungen (UAW) und Positivsymptomatik
Entsprechend den vorgefundenen Beschränkungen einer retrospektiven Auswertung von Patientenakten kann das Profil nicht schwerwiegender UAW nicht eingeschätzt werden. Offensichtlich wurde auf die Dokumentation nicht schwerwiegender UAW in den Patientenakten weitestgehend verzichtet (Dokumentations-Bias). Die wenigen dokumentierten UAW entsprechen aber dem bekannten Spektrum der Therapie depressiver Patienten. Nicht auszuschließen, und in einer prospektiven Studie zu klären, wäre, ob durch die Komedikation mit Antipsychotika der zweiten Generation tatsächlich weniger UAW auftreten und ob die Spezifik der Erkrankung zu einer anderen Ausprägung oder Wahrnehmung häufiger UAW von TCP wie etwa Unruhe und Schlafstörungen führt. Bezüglich schwerwiegender UAW trifft ein möglicher Dokumentations-Bias vermutlich weniger zu. Es kann deshalb davon ausgegangen werden, dass schwerwiegende UAW tatsächlich nicht aufgetreten sind. Darauf deutet auch hin, dass nur ein Patient die Therapie mit TCP abgebrochen hat. Für ein besonderes Risiko der Exazerbation von Positivsymptomatik wurden in dieser Studie keine Hinweise gefunden. Auch in früheren Studien mit Antipsychotika der ersten Generation und TCP wurde dieses Risiko als gering und beherrschbar, das heißt reversibel nach Absetzen von TCP, eingeschätzt. Erfahrene Verordner plädierten dafür, eine vorübergehende Verschlechterung der Positivsymptomatik hinzunehmen, da später oft sogar eine Besserung unter das Ausgangsniveau gefunden wurde [9]. In einer Studie mit TCP-Dosen bis 60 mg/Tag verschlechterte sich die Positivsymptomatik bei 20 von 70 Patienten [4]. Bei Dosen bis 40 mg/Tag scheint das Risiko geringer zu sein (Tab. 3). Sogar in einer Übersicht zur Monotherapie mit MAO-Hemmern (chronisch Schizophrene ohne akute Dekompensation, n=281) betrug die Rate der Exazerbation von Positivsymptomatik nur 3% und war nicht signifikant verschieden von Plazebo [26]. Darin eingeschlossen war eine kontrollierte Studie zur Monotherapie mit TCP (n=14) [7], worunter keine Verschlechterung der Positivsymptomatik auftrat.
Tyraminarme Diät
Oft bestehen bei wenig Vertrautheit mit der Anwendung von MAO-Hemmern bei Schizophrenie besondere Bedenken wegen der Tyraminproblematik. Dies beruht auf der Vorstellung, dass schizophrene Patienten im besonderen Maß nicht in der Lage sind, die geforderte tyraminarme Diät zu befolgen. Die vorgefundenen geringen Daten zur Diät-Compliance lassen leider keine Aussagen über mögliche geringfügige Abweichungen zu. Immerhin scheinen aber schwerwiegende Verletzungen der tyraminarmen Diät tatsächlich nicht vorgekommen zu sein. Das ist in Übereinstimmung mit Daten von prospektiven Studien. Nicht in einem Fall wird über Diätverletzungen berichtet, weder für TCP gemeinsam mit Antipsychotika (Tab. 3) noch für Monotherapie mit MAO-Hemmern [7]. In einem neueren Fallbericht wird betont, dass ein schizophrener Patient und seine Familie keine Schwierigkeiten mit der Umsetzung der Diät hatten [25]. Schizophrene Patienten und ihre Umgebung scheinen demzufolge bei entsprechender Anleitung und Kontrolle für die Befolgung der Tyramindiät ausreichend organisiert zu sein.
Dosis von TCP
Die verwendete Dosis von durchschnittlich 36 mg/Tag (20 bis 50) liegt unterhalb der bei therapieresistenter Depression heute gebräuchlichen Dosen von durchschnittlich 51,9 mg/Tag (20 bis 100) [1] und 60,5 mg/Tag (30 bis 100) [5]. Hintergrund dieser Dosiswahl ist das Risiko von Exazerbationen der schizophrenen Positivsymptomatik bei TCP-Dosen von 60 bis 80 mg/Tag [4, 38]. Pharmakologische Ursache dafür könnte die direkte Wirkung von TCP auf die Dopaminfreisetzung bei hohen Dosen sein. In der Mehrheit von vergleichbaren Studien betrug die TCP-Dosis 20 bis 30 mg/Tag (Tab. 3).
Klinische Besserung
Eine symptomatische Besserung bei 47% der Patienten, wenn auch zum Teil nur gering ausgeprägt, stellt aus unserer Sicht einen bedeutsamen klinischen Gewinn dar. Der Schwerpunkt der Besserung im Symptom „reduzierter Antrieb“ bestätigt die frühere Bezeichnung von MAO-Hemmern als „energizer“. Angesichts der schwer kranken Patienten und der sonst ungünstigen Prognose wurden schon geringere Responderraten von 22,5% [22] und 35,7% [4] als klinisch signifikant eingeschätzt. In einer Studie betrug die Responderrate 73% für die Kombination von Chlorpromazin mit TCP gegenüber 0% mit Plazebo [9]. Insgesamt folgt aus unseren Daten ein günstiges Nutzen-Risiko-Verhältnis für adjuvantes TCP und Antipsychotika der zweiten Generation bei schizophrenen Patienten mit überwiegender Negativsymptomatik. Auffallend ist, dass etwa 20% der Patienten (n=11) erst verhältnismäßig kurze Zeit erkrankt waren und fünf Patienten TCP ohne vorangegangene Therapieversuche mit anderen Antidepressiva erhielten. TCP muss also nicht in jedem Fall als Psychopharmakon der 2. Wahl gesehen werden, wie heute für Depression üblich. In Frage steht angesichts der Hypothese einer dopaminergen und noradrenergen Hypofrontalität, ob TCP bevorzugt erst nach Therapieversuchen mit anderen Antidepressiva, die meist serotonerg wirken, verwendet werden sollte. Die Ergebnisse zur Kombination von Antipsychotika mit SSRI waren nicht eindeutig. Eine Metaanalyse ergab keinen Vorteil der Kombination mit SSRI gegenüber Antipsychotika allein, wenn alle Patienten einbezogen wurden, sondern nur für eine Untergruppe der am schwersten und längsten erkrankten Patienten [37].
Schlussfolgerungen
1) In Übereinstimmung mit älteren Studien, darunter kontrollierte Studien, die aber nicht dem heutigen Stand der klinischen Forschung entsprechen, ergeben sich folgende bevorzugte Eckpunkte der TCP-adjuvanten Antipsychotika-Behandlung von schizophrenen Patienten mit überwiegender Negativsymptomatik: keine oder geringe Positivsymptomatik (maximal zwei Symptome), Antipsychotika-Therapie bei mittleren Dosen (heute bevorzugt Antipsychotika der zweiten Generation), TCP-Dosis 20 bis 40 mg/Tag, keine Benzodiazepine, Therapiedauer mindestens zwei bis drei Monate, stationäre Einstellung mit möglicher ambulanter Weiterbehandlung.
2) Die klinische Wertigkeit einer auch nur geringen Besserung der Negativsymptomatik kann nicht hoch genug eingeschätzt werden. Verstärkter Antrieb, bessere Affektmodulation und Motivation sowie eine verbesserte kognitive Leistungsfähigkeit sind wichtige Bausteine in einem Gesamtbehandlungsplan schizophrener Patienten. Die Chance, dass Patienten sich sozial und beruflich wieder integrieren können, wird erhöht.
3) Aufgrund der Grenzen des Studiendesigns einer retrospektiven Datenauswertung der Therapieroutine (keine Kontrollgruppe, Selektivität der Patienten, fehlende Daten, keine Verwendung standardisierter psychiatrischer Ratingskalen) haben die Schlussfolgerungen Erfahrungswert. Entsprechend einer streng wissenschaftlichen Herangehensweise ist die Bestätigung in kontrollierten Studien notwendig.
Danksagung
Die Autoren danken Frau Anette Küster, wissenschaftlicher Außendienst der esparma GmbH, für die gezeigte Initiative.
Literatur
1. Adli M, Pilhatsch M, Bauer M, Köberle U, et al. Safety of high-intensity treatment with the irreversible monoamine oxidase inhibitor tranylcypromine in patients with treatment-resistant depression. Pharmacopsychiatry 2008;41:252–7
2. Amiri A, Noorbala AA, Nejatisafa AA, Ghoreishi A, et al. Efficacy of selegiline add-on therapy to risperidone in the treatment of the negative symptoms of schizophrenia: a double-blind randomized placebo-controlled study. Hum Psychopharmacol 2008;23:79–86.
3. Baker GB, Coutts RT, McKenna KF, Sherry-McKenna RL. Insights into the mechanism of action of the MAO inhibitors phenelzine and tranylcypromine: a review. J Psychiat Neurosci 1993;17:206–14.
4. Barsa JA, Saunders JC. Tranylcypromine in the treatment of chronic schizophrenics. Am J Psychiatry 1962;118:933–4.
5. Birkenhäger TK, van den Broek WW, Mulder PG, Bruijn JA, et al. Efficacy and tolerability of tranylcypromine versus phenelzine: a double-blind study in antidepressant-refractory depressed inpatients. J Clin Psychiatry 2004;65:1505–10.
6. Bodkin JA, Siris SG, Bermanzohn PC, Hennen J, et al. Double-blind, placebo-controlled, multicenter trial of selegiline augmentation of antipsychotic medication to treat negative symptoms in outpatients with schizophrenia. Am J Psychiatry 2005;162:388–90.
7. Brenner R, Shopsin B. The use of monoamine oxidase inhibitors in schizophrenia. Biol Psychiatry 1980;15:633–47
8. Bucci L. The monoamine oxidase inhibitors: their usefulness and their safety. Dis Nerv Syst 1969;30:843–7.
9. Bucci L. Negative symptoms of schizophrenia and monoamine oxidase inhibitors. Psychopharmacol 1987;91:104–8.
10. Buffaloe WJ, Sandifer MG. A study of combined therapy with stelazine and parnate (SKF 385) in chronic anergic schizophrenics. Am J Psychiatry 1961;117:1030–1.
11. Burke WJ, Li SW, Chung HD, Ruggiero DA, et al. Neurotoxicity of MAO metabolites of catecholamine neurotransmitters: role in neurodegenerative diseases. Neurotoxicol 2004;25:101–15.
12. Coutts RT, Rao TS, Baker GB, Micetich G, et al. Neurochemical and neuropharmacological properties of 4-fluorotranylcypromine. Cell Mol Neurobiol 1987;7:271–90.
13. Da Prada M, Kettler R, Burkard WP, Lorez HP, et al. Some basic aspects of reversible inhibitors of monoamine oxidase-A. Acta Psychiatr Scand 1990;360(S):7–12.
14. Da Silva AF, Figee M, Vamelsvoort T, Veltman D, et al. The revised dopamine hypothesis of schizophrenia: Evidence from pharmacological MRI studies with atypical antipsychotic medication. Psychopharmacol Bull 2008;41:121–32.
15. Frieling H, Bleich S. Tranylcypromine: new perspectives on an “old” drug. Eur Arch Psychiatry Clin Neurosci 2006;256:268–73.
16. Geller W. Zur Entwicklung der Behandlung mit Monoaminoxidasehemmern. Nervenarzt 1962;33:124–9.
17. Greenshaw AJ, Rao TS, Nazarali AJ, Baker GB, et al. Chronic effects of tranylcypromine and 4-fluorotranylcypromine on regional brain monoamine metabolism in rats: a comparison with clorgyline. Biol Psychiatry 1989;25:1014–20.
18. Hampson DR, Baker GB, Coutts RT. A comparison of the neurochemical properties of the stereoisomers of tranylcypromine in the central nervous system. Cell Mol Biol 1986;32:593–9.
19. Hedberg DL, Houck JH, Glueck BC. Tranylcypromine-trifluoperazine combination in the treatment of schizophrenia. Am J Psychiatry 1971;127:1141–6.
20. Hordern A, Somerville DM, Krupinski J. Does chronic schizophrenia respond to a combination of a neuroleptic and an antidepressant? J Nerv Ment Disord 1962;134:361–76.
21. Janssen PA, Leysen JE, Megens AA, Awouters FH. Does phenylethylamine act as an endogenous amphetamine in some patients? Int J Neuropsychopharmacol 1999;2:229–40.
22. Kruse W. Trifluoperazine and tranylcypromine in chronic refractory schizophrenics. Am J Psychiatry 1960;117:548–9.
23. Leucht S, Corves C, Arbter D, Engel RR, et al. Second-generation versus first-generation antipsychotic drugs for schizophrenia: a meta-analysis. Lancet 2009;373:31–41.
24. Levi-Minzi S, Bermanzohn PC, Siris SG. Bromocriptine for “negative” schizophrenia. Compr Psychiatry 1991;32:210–6.
25. Melamed Y, Karniel E, Szor H. Phenelzine as a possible treatment for depression in schizophrenic patients. Isr J Psychiat Relat Sci 1996;33:211–2.
26. Mena A, Heistadt G, Schiele BC, Janecek J. A comparison of tranylcypromine alone with tranylcypromine plus trifluoperazine in the treatment of chronic outpatients: a double blind controlled study. J Neuropsychiatry 1964;5:542–50.
27. Merikangas KR, Merikangas JR. Combination monoamine oxidase inhibitor and beta-blocker treatment of migraine, with anxiety and depression. Biol Psychiatry 1995;38:603–10.
28. Möller HJ. Management of the negative symptoms of schizophrenia: new treatment options. CNS Drugs 2003;17:793–823.
29. Möller HJ. Wirksamkeit neuer Antipsychotika bei schizophrener Negativsymptomatik. Psychopharmakotherapie 2003;10:95–101.
30. Murphy BP, Chung YC, Park TW, McGorry PD. Pharmacological treatment of primary negative symptoms in schizophrenia: a systematic review. Schizophr Res 2006;88:5–25.
31. Ohmori T, Koyama T, Inoue T, Matsubara S, et al. B-HT 920, a dopamine D2 agonist, in the treatment of negative symptoms of chronic schizophrenia. Biol Psychiatry 1993;33:687–93.
32. Powell JH, al-Adawi S, Morgan J, Greenwood RJ. Motivational deficits after brain injury: effects of bromocriptine in 11 patients. J Neurol Neurosurg Psychiatry 1996;60:416–21.
33. Roesch-Ely D, Göhring K, Gruschka P, Kaiser S, et al. Pergolide as adjuvant therapy to amisulpride in the treatment of negative and depressive symptoms in schizophrenia. Pharmacopsychiatry 2006;39:115–6.
34. Rummel C, Kissling W, Leucht S. Antidepressants as add-on treatment to antipsychotics for people with schizophrenia and pronounced negative symptoms: a systematic review of randomized trials. Schizophr Res 2005;80:85–97.
35. Schiele BC, Vestre ND, MacNaughton DV. Treatment of hospitalised schizophrenics with trifluoperazine plus tranylcypromine: A double-blind controlled study. Compr Psychiatry 1963;4:68–79.
36. Schmidt LG, Grohmann R, Rüther E. Unerwünschte Wirkungen von Antidepressiva in der Routinebehandlung. Psychopharmakotherapie 1994;1:6–15.
37. Sepehry AA, Potvin S, Elie R, Stip E. Selective serotonin reuptake inhibitor (SSRI) add-on therapy for the negative symptoms of schizophrenia: a meta-analysis. J Clin Psychiatry 2007;68:604–10.
38. Singh H, Free RM. A preliminary report on the use of stelazine and parnate in chronic regressed and withdrawn patients. Am J Psychiatry 1960;117:364–5.
39. Spahn-Langguth H, Hahn G, Mutschler E, Möhrke W, et al. Enantiospecific HPLC assay with fluorescence detection for monoamine oxidase inhibitor tranylcypromine and its applicability in pharmacokinetic studies. J Chromatogr B 1992;584:229–37.
40. Stoll AL, Haura G. Tranylcypromine plus risperidone for treatment-refractory major depression. J Clin Psychopharmacol 2000;20:495–6.
41. Vogt AH. The use of stelazine and parnate in chronic withdrawn patients. Am J Psychiatry 1961;118:256–7.
Dr. med. Daniela Roesch-Ely, Prof. Dr. med. Matthias Weisbrod, Klinik für allgemeine Psychiatrie, Zentrum für Psychosoziale Medizin, Voss-Straße 4, 69115 Heidelberg, E-Mail: daniela_roesch@med.uni-heidelberg.de
Laura Speck, Klinik für Psychiatrie und Psychotherapie, SRH Klinikum Karlsbad-Langensteinbach
Priv.-Doz. Dr. rer.nat. Sven Ulrich, Ltr. MedWiss/Pharmakovigilanz, esparma GmbH, Magdeburg (seit 10/2010: Abt. MedWiss Pharmakovigilanz, Aristo Pharma GmbH, Wallenroder Str. 8–10, 13435 Berlin)
Adjuvant tranylcypromine with second generation antipsychotic drugs in the treatment of schizophrenia with negative symptoms: Retrospective analysis of treatment routine of 53 patients and short review of the literature
Since introduction into clinical practice, the irreversible MAO-inhibitor tranylcypromine (TCP), an antidepressant drug, has also been used as an adjuvant to first generation antipsychotic drugs in the treatment of schizophrenic patients having predominantly negative symptoms. The approach is derived today from the concept of an improved balance of neurotransmitter function in dopaminergic and norepinephrinergic hypofrontality, which has been found in association schizophrenia with predominantly negative symptoms. In a chart review from 2001 to 2006, treatment routine has been analysed for 53 patients who were treated with a combination of a second generation antipsychotic drug and TCP (20 to 50 mg/day). Other antidepressants which were used unsuccessfully for treatment of schizophrenia with predominantly negative symptoms before TCP were discontinued.
No drug interactions or severe adverse effects were encountered. There was no exacerbation of positive symptoms. No data was found for a lower compliance with tyramine restrictive diet in schizophrenics compared with depressive patients. Improvement of negative symptoms occurred in 43% of patients (n=23) after a mean duration of treatment of 9 weeks. Mostly, this included an improvement in reduced activity (n=20). For 47% of patients (n=25) an improvement in at least one symptom of negative schizophrenia or depression was found. Despite the limits of the study design, the result is evaluated as clinical significant and shows a positive risk-benefit-ratio taking into account the severity of the disease. In a modern clinical environment, treatment with a combination of second generation antipsychotics and TCP is a reasonable approach for schizophrenia with predominantly negative symptoms, at least after unsuccessful trials with other antidepressants. A confirmation in controlled trials is needed.
Key words: Tranylcypromine, MAO-inhibitor, negative symptoms, schizophrenia, second generation antipsychotics
Psychopharmakotherapie 2011; 18(02)
