John Peter Doerr und Dieter Riemann, Freiburg
Ein- und/oder Durchschlafstörungen sind in Hausarztpraxen eine der häufigsten Beschwerden überhaupt [4]. Verschiedene epidemiologische Studien kommen zu dem Ergebnis, dass etwa 10 bis 20% der Bevölkerung an behandlungsbedürftigen chronischen Insomnien leiden [30]. Psychische Erkrankungen stellen die häufigste Ursache für Ein- und/oder Durchschlafstörungen dar. Die sogenannte primäre oder – nach ICD-10 – nichtorganische Insomnie wird diagnostiziert, wenn insomnische Beschwerden mindestens dreimal pro Woche auftreten, zu klinisch signifikanten Leiden und einer kognitiven Beschäftigung mit der Schlaflosigkeit führen sowie Beeinträchtigungen in sozialen, beruflichen oder anderen wichtigen Funktionsbereichen verursachen. Außerdem muss eine körperliche oder psychiatrische Ursache ausgeschlossen sein. Letztlich erhöht die chronische Insomnie deutlich das Risiko, an einer psychischen Störung zu erkranken [32]. Die Prävalenz chronischer Schlafstörungen ist in der Altersgruppe der über 65-Jährigen am höchsten. Frauen sind häufiger betroffen als Männer. Die Bedeutung der Insomnie wird bei der Betrachtung der jährlichen indirekten und direkten Kosten deutlich. In den USA wurden die direkten Kosten auf 13,9 Milliarden US-Dollar pro Jahr eingestuft, während die indirekten Kosten sogar auf 77 bis 92 Milliarden US-Dollar geschätzt wurden [41]. Eine Vielzahl an Studien belegt die Wirksamkeit verschiedener pharmakologischer Stoffklassen in der Behandlung der primären Insomnie. Bislang existieren jedoch kaum Langzeitstudien. Eszopiclon stellt diesbezüglich eine Ausnahme dar.
Eszopiclon wird in den USA von Sepracor Inc. hergestellt und dient allein der Behandlung der primären Insomnie. Im Dezember 2004 ließ die FDA Eszopiclon auf dem amerikanischen Markt unter dem Handelsnamen Lunesta zu. Es ist sowohl für Patienten mit Ein- als auch für Durchschlafstörungen vorgesehen und wird in den USA neben der Kurzzeit- auch in der Langzeitbehandlung eingesetzt. Da der Ausschuss für Humanarzneimittel (CHMP) der Europäischen Zulassungsbehörde (EMEA) Ende 2008 die Zulassung befürwortet hatte, schien lange der Einsatz für die Kurzzeitbehandlung auch auf dem europäischen Markt möglich [9, 23]. Allerdings hatte der Hersteller zusätzlich beantragt, Eszopiclon als neuen Wirkstoff zu klassifizieren, was jedoch vom CHMP abgelehnt wurde. Daraufhin beschlossen die Hersteller im Mai dieses Jahres, den Antrag zurückzuziehen. Somit wird Eszopiclon wahrscheinlich nicht auf den deutschen Markt kommen. Trotzdem ist die aktuelle Studienlage aus verschiedenen Gründen interessant. Eszopiclon wird weiterhin über Auslandsapotheken erhältlich sein. Auch die Verschreibungsraten von Z-Substanzen (Zolpidem, Zopiclon, Zaleplon) vor allem über Privat-Rezepte scheinen zuzunehmen [15]. Außerdem ist in den USA nur Eszopiclon (und nicht Zopiclon) auf dem Markt erhältlich, weshalb viele amerikanische Studien nur über dieses Präparat berichten werden. Aufgrund der Ähnlichkeit zu Zopiclon sind Vergleiche über Wirkung und Nebenwirkungen sehr wahrscheinlich möglich. Auch die pharmakologischen Eigenschaften überschneiden sich in vielerlei Hinsicht.
Pharmakologische Eigenschaften
Eszopiclon ist das S-Enantiomer von Zopiclon und ist ein Benzodiazepin-ähnliches Hypnotikum aus der Gruppe der Cyclopyrrolone mit sedierenden, hypnotischen und anxiolytischen Eigenschaften. Darüber hinaus wirkt Zopiclon muskelrelaxierend und antikonvulsiv. Als spezifischer GABA-Agonist entfaltet Zopiclon seine Wirkung über den GABA-Ω-(BZ1 und BZ2)-Rezeptor-Komplex und Modulation des Chloridionenkanals. Eszopiclon hat nun eine höhere Affinität an den GABA-A-Benzodiazepin-Rezeptorkomplex als das R-Enantiomer und die sedierenden Eigenschaften von Zopiclon scheinen vor allem an das S-Enantiomer gebunden [5, 6]. In vivo ließ sich keine Stereokonversion des S-Enantiomers zum R-Enantiomer beobachten [12]. Weitere Details zu den genauen Wirkungsmechanismen von Eszopiclon als Hypnotikum sind nicht bekannt.
Eszopiclon wird nach oraler Gabe schnell absorbiert und erreicht seine maximale Plasmakonzentration innerhalb von einer Stunde. Die Plasmaeiweißbindung von Eszopiclon beträgt nur 52 bis 59% [12, 23]. Die Absorption und Verteilung wird somit kaum durch andere Medikamente beeinträchtigt. Bei 3 mg Eszopiclon beträgt die Halbwertszeit nach einmaliger Gabe 5 bis 8 beziehungsweise 7 Stunden im Steady-State [24]. In klinischen Studien zeigte sich, dass allenfalls durch sehr fetthaltige Mahlzeiten geringfügige Effekte auf die Absorption auftreten können. Hierdurch kann ein Erreichen der maximalen Wirkung um eine Stunde verzögert werden. Folglich sollten Patienten darüber aufgeklärt werden, Eszopiclon nicht direkt mit oder kurz nach einer fettreichen Mahlzeit einzunehmen. Die Halbwertszeit scheint sich jedoch hierdurch nicht zu verändern. Die pharmakokinetischen Eigenschaften entsprachen nach einmaliger Einnahme denen einer Steady-State-Gabe. Die Metabolisierung erfolgt über das Cytochrom-P450-(CYP-)Isoenzym 3A4 und 2E1. Die Komedikation mit CYP3A4-Induktoren oder -Inhibitoren kann die pharmakokinetischen Auswirkungen von Eszopiclon beeinflussen [2, 23]. Potente CYP3A4-Inhibitoren sind beispielsweise Ketoconazol, Clarithromycin (bzw. 14-Hydroxy-Clarithromycin) oder Verapamil; CYP3A4-Induktoren sind beispielsweise Carbamazepin (bzw. Carbamazepin-Epoxid) oder Johanniskraut.
Die Elimination erfolgt über die Niere. Weniger als 10% von Eszopiclon wird unverändert ausgeschieden. Bei Patienten mit einer Niereninsuffizienz erscheint keine Dosisanpassung notwendig. Im Vergleich zu Gesunden ist die Kumulation des Wirkstoffs bei älteren Patienten und bei Patienten mit eingeschränkter Leberfunktion erhöht. Für diese Patienten ist die empfohlene Dosierung mit 1 bis 2 mg pro Nacht geringer als die übliche Dosierung von 2 bis 3 mg [23].
Therapeutische Wirksamkeit
Pharmakotherapeutische Maßnahmen in der Insomniebehandlung orientieren sich zunächst an der Ursache der insomnischen Beschwerden. Für die Behandlung der nichtorganischen Insomnie stehen pharmazeutische und psychotherapeutische Behandlungsmöglichkeiten, insbesondere kognitiv-verhaltenstherapeutische Strategien zur Verfügung. Zu den medikamentösen Strategien in Deutschland gehören neben den sogenannten Benzodiazepin-Rezeptoragonisten (z. B. Zopiclon, Zolpidem, Flunitrazepam oder Zaleplon) vor allem die sedierenden Antidepressiva (z. B. Trazodon, Doxepin, Trimipramin oder Mirtazapin), allerdings auch häufig Antihistaminika, Neuroleptika oder „alternative“ Behandlungsmöglichkeiten, wie Baldrian oder Melatonin, welches zuletzt ebenfalls zur Behandlung der Insomnie bei Patienten älter als 55 Jahre zugelassen wurde.
Eszopiclon wurde in verschiedenen Plazebo-kontrollierten, doppelblinden klinischen Studien an Patienten mit chronischen primären und sekundären insomnischen Beschwerden getestet. Eine Verbesserung in den entsprechenden Parametern der subjektiven und objektiven Ein- und Durchschlafparameter konnten mit 2 und 3 mg bei jüngeren Patienten [20, 43] und mit 2 mg bei Patienten über 65 Jahre erreicht werden. Bei jüngeren Patienten stellten Rosenberg und Kollegen 2005 nach einmaliger Gabe eine signifikante Verkürzung der polysomnographisch gemessenen Einschlaflatenz um 5 Minuten und eine Verlängerung der Gesamtschlafzeit um 10 Minuten fest [34]. Bei den älteren Patienten verkürzte sich nach zwei Wochen die objektive Einschlafzeit im Vergleich zu Plazebo um etwa 15 Minuten, während sich die Gesamtschlafzeit um etwa 30 Minuten verlängerte [25, 37]. Letztlich wird bei älteren Patienten und einer Einschlafstörung eine Tagesdosis von 1 mg und bei zusätzlichen Durchschlafstörungen 2 mg empfohlen. Bei allen Patienten sollte die Medikamenteneinnahme direkt vor dem Zubettgehen erfolgen.
Derzeit ist Eszopiclon das einzige zugelassene Arzneimittel in der Behandlung der chronischen nicht organischen Insomnie, dessen Wirksamkeit in einer doppelblinden Plazebo-kontrollierten Studie über 12 Monate festgestellt wurde. In der Studie mit insgesamt 800 Patienten (21–69 Jahre) mit primärer Insomnie (mittleres Alter: 44,3±11,4 Jahre) konnten in den ersten sechs Monaten eine signifikante Verkürzung der mittleren subjektiven Einschlaflatenz um 43 Minuten und eine signifikante Zunahme der mittleren Gesamtschlafzeit um 76 Minuten gegenüber der Baseline-Untersuchung festgestellt werden (Abb. 1) [20, 35].
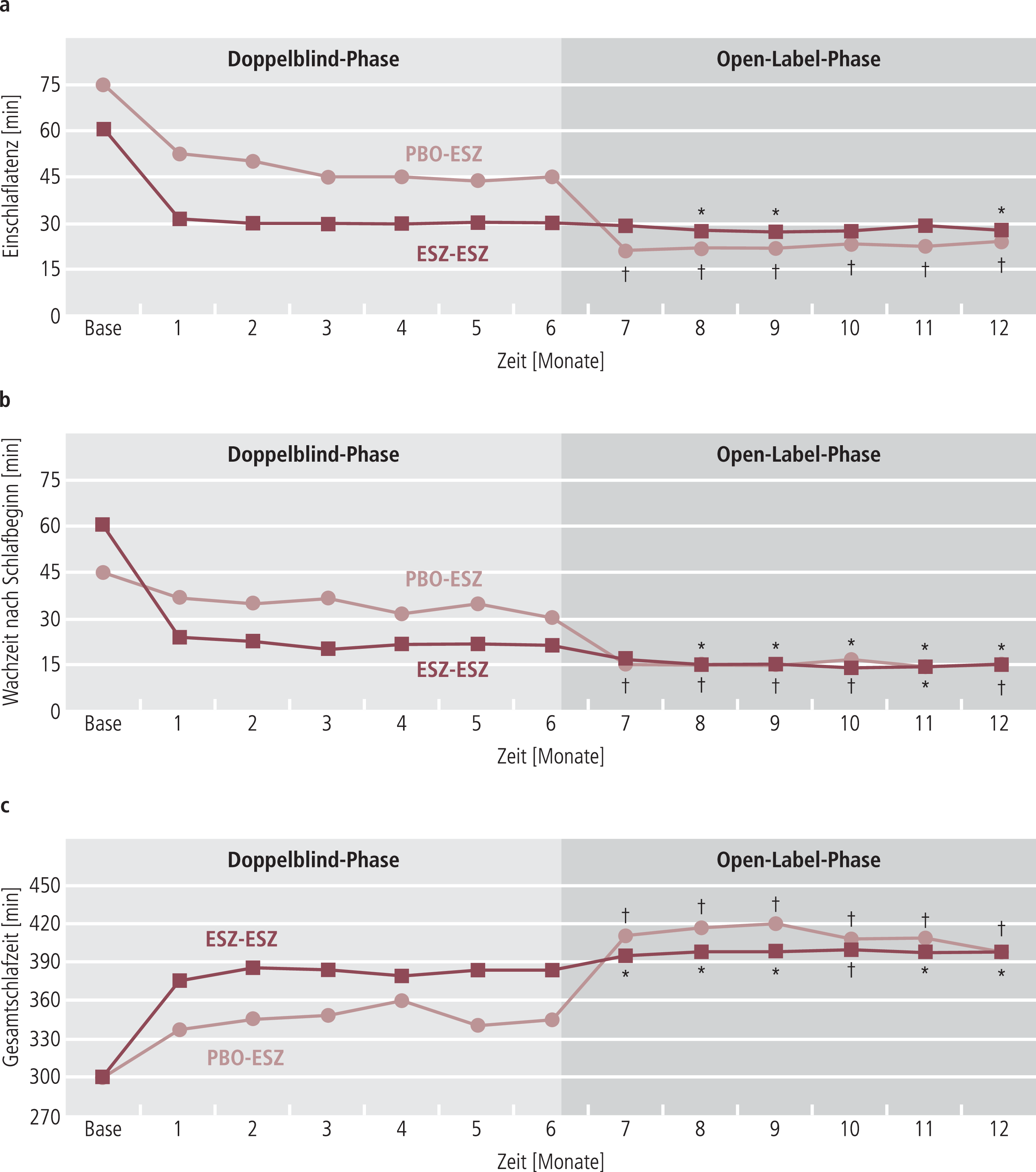
Abb. 1. Langzeitwirksamkeit von Eszopiclon (ESZ) vs. Plazebo (PBO). Dargestellt sind die Mediane der Einschlaflatenz (a), der Wachzeit nach Schlafbeginn (b) und der Gesamtschlafzeit (c) im Verlauf einer 6-monatigen Doppelblindstudie und einer anschließenden 6-monatigen Open-Label-Phase. Statistischer Vergleich der beiden Gruppen in der Doppelblind-Phase: a) p<0,0001; b) p=0,0032; c) p<0,0001. Statistischer Vergleich mit dem Ausgangswert (Monat 6) in der Open-Label-Phase: *p<0,05, †p<0,0001 [20, 35].
Über die Behandlungszeit waren diese Befunde stabil und es ergaben sich nach dem Absetzen keine Hinweise auf Entzugssymptome oder Rebound-Insomnien. Darunter versteht man das Absinken der Schlafqualität unter das Ausgangsniveau nach Absetzen einer hypnotischen Substanz, was insbesondere bei Benzodiazepinen mit kurzer Halbwertszeit vorkommt. Anzumerken ist hier jedoch, dass auch in der Plazebo-Gruppe eine deutliche Reduktion der mittleren subjektiven Einschlaflatenz nach sechs Monaten um 33 Minuten auftrat, so dass die Differenz gegenüber Plazebo im Verlauf tendenziell nachließ (Median: 15 Minuten, Abb. 1). Anschließend wurde eine Open-Label-Extension-Studienphase mit insgesamt 330 Patienten (21–64 Jahre) über sechs Monate durchgeführt (Abb. 1). Die 110 Patienten, die zuvor Plazebo erhalten hatten, berichteten sofort nach Einstellung auf Eszopiclon eine über sechs Monate anhaltende Besserung der Einschlaflatenz, der Gesamtschlafzeit und der Wachzeit nach Schlafbeginn. Ebenso verbesserten sich signifikant die Tagesbeeinträchtigungen [35].
Zuletzt ergaben Studien mit Patienten (<65 Jahre), die an einer sekundären Insomnie litten, dass durch die zusätzliche Gabe von Eszopiclon – unter laufender Therapie der Grunderkrankung – eine Verbesserung der insomnischen Beschwerden zu erreichen war. Die Insomnie-auslösenden Erkrankungen waren eine depressive Störung [10], eine generalisierte Angststörung [31], insomnische Beschwerden im Rahmen der Menopause [40] oder im Rahmen einer rheumatoiden Arthritis [36]. Auch die subjektive Schlafqualität und die Leistungsfähigkeit am Tag verbesserten sich im Vergleich zu Plazebo. Bei den Patienten, die unter stabiler Standardtherapie der jeweiligen Erkrankung waren, konnte durch die Gabe von Eszopiclon außerdem eine Verbesserung in den komorbiden Beschwerden aufgezeigt werden. Gemessen wurden diese jeweils mit der Hamilton Depression Rating Scale (HAM-D), der Hamilton Anxiety Rating Scale (HAM-A), den Arthritis Pain and Ability to Function-Scores und der Green Climacteric Scale (GCS) [10, 31, 36, 40].
Insgesamt muss jedoch kritisch angemerkt werden, dass bislang noch keine unabhängigen Studien zur Substanz Eszopiclon vorliegen.
Nebenwirkungen
In den bislang durchgeführten klinischen Plazebo-kontrollierten Studien wurden nur leichte Nebenwirkungen berichtet. Die häufigsten waren ein unangenehmer Geschmack nach der Einnahme – wie bei Zopiclon – oder Kopfschmerzen.
Weitere Nebenwirkungen, die dosisabhängig auftraten, waren: virale Infektionen (z. B. Pharyngitis), Myalgien, Muskelschwäche, Schwindel, Benommenheit, Schläfrigkeit, Koordinationsstörungen, Übelkeit, Mundtrockenheit, Hautausschläge, verschiedene körperliche Schmerzen (z.B. Herz-, Rückenschmerzen), eine Reduktion der sexuellen Appetenz und eine Zunahme von Menstruationsbeschwerden. Anterograde Amnesien und eine erhöhte Unfall- und Sturzgefahr wurden vor allem bei älteren Patienten beobachtet. Die Abbruchrate aufgrund von Nebenwirkungen war in der größten Studie in der Eszopiclon-Gruppe 12,8% und in der Plazebo-Gruppe 7,1% [25]. Außerdem sind psychiatrische Nebenwirkungen bekannt. Hierzu gehören das Demaskieren/Verschlechtern von Depressionen, was mit einer Erhöhung von Suizidgedanken einherging, sowie das Auftreten von Halluzinationen/Psychosen. Zusätzlich können sogenannte paradoxe Reaktionen (Unruhe, Reizbarkeit, Aggressivität, Wut, Halluzinationen, Antriebssteigerung) auftreten. Schlafmedizinisch wurden sowohl Alpträume als auch Schlafwandeln beobachtet [11]. Generelle Vorsicht besteht bei alten und gebrechlichen Patienten und bei Patienten mit relevanten körperlichen Erkrankungen, da die Metaanalyse von Glass et al. 2005 den Nutzen sedierender Hypnotika nur als geringfügig bewertete und dieser durch die dabei auftretenden Nebenwirkungen und Risiken egalisiert werde [13].
In Anbetracht der im Vergleich mit dem R-Enantiomer 50-fach höheren Bindungsaffinität des S-Enantiomers von Zopiclon an die wirkspezifischen Benzodiazepin-Rezeptoren erscheint – wie bei den Benzodiazepinen – eine Entzugssymtomatik beim Absetzen nach längerer Anwendung trotz der Ergebnisse der oben genannten Langzeitstudie [25] wahrscheinlich. Hierbei wären Symptome wie Schwitzen, innere Unruhe, Muskelkrämpfe, Übelkeit und Erbrechen sowie epileptische Anfälle möglich. Eine Überdosierung kann mit komatösen Zuständen und kardialen Reizleitungsveränderungen einhergehen. Schließlich ist eine exaktere Klärung der Nebenwirkungen erst durch zusätzliche unabhängige klinische Studien möglich. Diese Vermutung stützt sich auf eine Veröffentlichung im Journal of Clinical Sleep Medicine, die darauf hinwies, dass die Wahrscheinlichkeit für eine positive Darstellung des Nebenwirkungsrisikos einer gegebenen Substanz 3,6-mal höher war, wenn die Studie finanzielle Unterstützung durch ein Unternehmen der pharmazeutischen Industrie erhalten hatte [18].
Kontraindikationen
Bislang sind speziell für Eszopiclon noch keine spezifischen Kontraindikationen bekannt, allerdings sollte bei der Verordnung von Z-Substanzen stets berücksichtigt werden, dass Schlafstörungen eines der führenden Symptome vieler psychischer Erkrankungen sind. Somit sollte grundsätzlich vor einer Behandlung die Ursache der Beschwerden genau evaluiert werden, um die wirksameren Alternativen, beispielsweise die sedierenden Antidepressiva bei einer Depression, einzusetzen. Nach einer Studie von Kripke und Kollegen steigt unter GABA-ergen Substanzen die Morbidität und Mortalität [19]. Folglich können psychische Erkrankungen durchaus eine Kontraindikation darstellen. Kontraindiziert ist auch der Einsatz bei Schwangeren, da hierzu bislang noch keinerlei Daten vorliegen. Dies gilt auch während der Stillzeit, da Zopiclon in die Muttermilch übertritt.
Aufgrund der leicht muskelrelaxierenden Wirkung stellen Muskelerkrankungen wie beispielsweise die Myasthenia gravis, eine schwere Ateminsuffizienz oder auch ein schweres Schlaf-Apnoe-Syndrom weitere Kontraindikationen dar.
Ein vermehrter Drogen- und/oder Alkoholabusus beziehungsweise eine aktuelle oder frühere Abhängigkeitserkrankung sind ebenso Kontraindikationen, da auch Eszopiclon – wie die anderen Z-Substanzen und die Benzodiazepine – zu den sogenannten „schedule 4“-Substanzen gerechnet wird. In den USA werden Arzneimittel aufgrund ihres Missbrauchs und des psychischen und physischen Abhängigkeitspotenzials in eine von fünf Kategorien eingestuft, wobei die Schedule-5-Substanzen (z.B. Codein-Tropfen) die risikoärmsten darstellen. Pharmakologisch wirksame Alternativen in der Insomniebehandlung wie sedierende Antidepressiva, Melatonin oder Neuroleptika – im Einsatz bei älteren Patienten – stellen bei diesen Erkrankungen keine Kontraindikation dar.
Wirksame Alternativen
Zunächst ist vor einem längerfristigen Therapiebeginn neben der Abklärung organischer Ursachen eine differenzialdiagnostische Einordnung im Rahmen einer psychologisch/psychiatrischen Untersuchung, inklusive essenzieller Hilfsmittel wie Schlaftagebücher oder dem Beck-Depressions-Inventar (BDI), erforderlich. Ziel ist es, eine dominierende psychische Erkrankung auszuschließen.
Bei der nach der revidierten internationalen Classification of Sleep Disorders (ICSD-2) sogenannten Anpassungs-Insomnie [1], bei der insomnische Beschwerden nach einem akut traumatischen/belastenden Ereignis auftreten und meist nicht länger als vier Wochen anhalten, sind die Z-Substanzen unbestritten Therapie der 1. Wahl. In einer Vielzahl Plazebo-kontrollierter Studien konnte die Wirksamkeit dieser Substanzen, unter anderem Zopiclon in der Kurzzeittherapie, bestätigt werden. Für Zolpidem (12,5 mg) existiert sogar eine kontrollierte Studie über 24 Wochen, die den Einsatz einer intermittierenden selbstständigen Einnahme (3–7 Tabletten/Woche) untersuchte und positive Effekte auf die Schlafkontinuität und die Einschlafzeit berichtete, ohne das Rebound-Phänomene auftraten [21]. Trotzdem wird die Langzeittherapie nicht empfohlen. Der Vergleich Eszopiclon (2 mg) versus Zolpidem (10 mg) ergab keine Unterschiede in den objektiven Schlafparametern [8]. Vergleichsstudien zwischen Zopiclon und Eszopiclon fehlen bislang.
Bei chronischen Insomnien steht eine Vielzahl anderer Optionen zur Verfügung. Insbesondere haben sich sedierende Antidepressiva (v. a. Trimipramin, Doxepin, Trazodon oder Mirtazapin) durchgesetzt, obwohl die Studienlage bezüglich der Behandlung der nichtorganischen Insomnie im Vergleich zu den Z-Substanzen eingeschränkter erscheint, jedoch durchaus auch überzeugend ist. Die Wirksamkeit von Trimipramin auf Durchschlafstörungen konnte durch unsere Arbeitsgruppe bereits 1994 in einer Pilotstudie [16] und erneut 2002 [33] in einer Studie gegenüber der Referenzsubstanz Lormetazepam und Plazebo belegt werden. In einer Studie von Hajak und Kollegen kam es mit Doxepin bei einer Dosierung von 25 bis 50 mg zu einer signifikanten Zunahme der Schlafzeit von fast einer Stunde, die über vier Wochen stabil war [14]. Zuletzt wurden sogar unter 1 mg, 3 mg und 6 mg Doxepin positive Effekte auf die subjektive und objektive Durchschlafqualität bei älteren Patienten gegenüber Plazebo berichtet [38]. Trazodon wurde ebenso Plazebo-kontrolliert mit Zolpidem verglichen und hatte einen positiven Effekt auf die Schlafkontinuität [42]. Trotzdem ist insgesamt die Datenlage für sedierende Antidepressiva in der Therapie der primären Insomnie leider noch geringer als die der Z-Substanzen. Im klinischen Alltag haben sich diese Substanzen jedoch bewährt, so dass beispielsweise Trazodon zu den am häufigsten als Hypnotikum eingesetzten Substanzen in den USA gehört [7]. Letztlich muss bei allen medikamentösen Behandlungsoptionen das jeweilige Nebenwirkungsprofil stets beachtet werden.
Zur Wirksamkeit und Effektivität kognitiv-verhaltenstherapeutischer Therapien (KVT) in der Behandlung der chronischen nichtorganischen beziehungsweise der sogenannten psychophysiologischen Insomnie besteht eine breite evidenzbasierte Studienlage. Aufgrund des komplexen Hintergrunds der Entstehung auf emotionalen, kognitiven und physiologischen/motorischen Ebenen bestätigte sich die Überlegenheit kognitiv-verhaltenstherapeutischer Strategien gegenüber Plazebo-Interventionen unter anderem in Studien von Morin und Mitarbeitern [26] sowie von Mur- tagh und Greenwood [29] auch mit langfristigen Effekten über sechs Monate. Essenzielle Bestandteile zur Lösung der verschiedenen Problemebenen sind das Erklären schlafhygienischer Regeln mit Psychoedukation, spezifische verhaltenstherapeutische Interventionen wie Entspannungsmethoden, Stimuluskontrolle sowie das Verfahren der Schlafrestriktion. Auch die wirksamen kognitiven Techniken wie die paradoxen Intervention und die Technik des Gedankenstopps werden ausführlich bei Riemann und Kollegen [3] dargestellt. In den letzten Jahren wurden einige vergleichende Studien publiziert, in denen prospektiv beide Therapiestrategien direkt miteinander verglichen wurden. In einer Studie zu Trazodon erschien kürzlich, dass dieses in Kombination mit der etablierten kognitiv verhaltenstherapeutischen Behandlung neben der signifikanten Verbesserung des Durchschlafens positive Auswirkungen auf den Anteil an Tiefschlaf hatte [44].
Morin und Kollegen [27] verglichen hingegen die Monotherapie mit Temazepam versus KVT allein (Abb. 2) und der Kombination beider Therapien, während Jacobs und Kollegen [17] die kognitive Verhaltenstherapie (KVT) mit Zolpidem, der Kombinationsbehandlung (KVT und Zolpidem) und Plazebo verglichen. In keiner dieser Studien zeigte sich im Langzeit-Follow-up eine Überlegenheit der pharmakologischen Therapie gegenüber der Verhaltenstherapie. Vielmehr ergab die aktuellste Studie von Morin (2009), dass das beste Langzeittherapieergebnis (nach 6 Monaten) in der Patientengruppe festzustellen war, die initial eine Kombinationsbehandlung (KVT und Zolpidem) und nach 4 Wochen eine KVT-Monotherapie erhalten hatte [28].
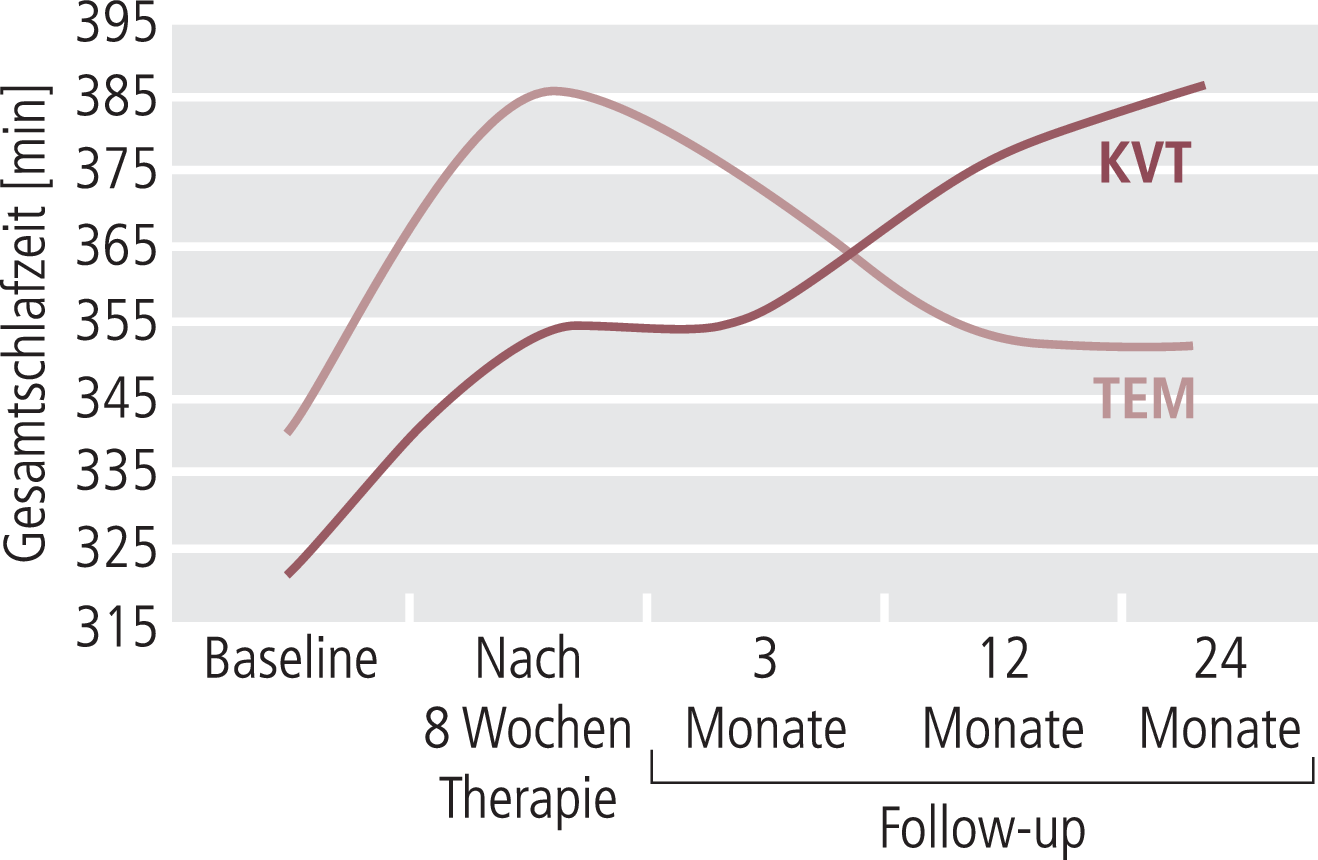
Abb. 2. Temazepam (TEM) vs. kognitive Verhaltenstherapie (KVT) in der Behandlung der primären Insomnie. Gesamtschlafzeit bei Patienten mit chronischer Insomnie; nach 24 Monaten besteht eine Überlegenheit der KVT gegenüber der Monotherapie mit Temazepam [27].
Sivertsen und Kollegen untersuchten die Behandlung mit KVT versus Zopiclon bei älteren Patienten [39]. Die KVT war der medikamentösen Therapie hier sogar überlegen. Da bislang keine vergleichende Studie zwischen Eszopiclon und der KVT existiert, ist interessant, dass zwischen den Z-Substanzen Zolpidem und Eszopiclon zuletzt kein signifikanter Unterschied zu finden war [8]. Letztlich sind vergleichende Studien zwischen Eszopiclon und konservativen therapeutischen Maßnahmen wünschenswert.
Zusammenfassung
Die Wirksamkeit von Eszopiclon, dem S-Enantiomer von Zopiclon, wurde in der Kurzzeittherapie (3 bis 4 Wochen) der primären Insomnie von der EMEA bestätigt und wird in den USA seit 2004 in der Kurz- und Langzeittherapie eingesetzt. Mit der Markteinführung in Deutschland ist allerdings nicht zu rechnen, da letztlich die Hersteller den Zulassungsantrag im Mai 2009 zurückgezogen haben. Begründet wurde dies damit, dass Eszopiclon nicht als neuer Wirkstoff klassifiziert worden war. Somit bleibt in Deutschland weiterhin Zopiclon – als vergleichbare Substanz – eine Therapieoption in der Behandlung akuter insomnischer Beschwerden. Allerdings sollten trotz positiver Ergebnisse andere Behandlungsoptionen nicht als unterlegen betrachtet werden. Insbesondere für die kognitive Verhaltenstherapie existieren evidenzbasierte Daten in der Kurz- und auch in der Langzeittherapie. Zur Stützung der Behauptung einer besseren Wirksamkeit von Z-Substanzen bzw. Eszopiclon sind weitere vergleichende Studien notwendig.
Literatur
1. American Academy of Sleep Medicine. The International Classification of Sleep Disorders. 2nd edition. Westchester, IL: One Westbrook Corporate Center, 2005.
2. Anderson AJ, Maier G, Skolly SM. Pharmacokinetic interaction between eszopiclone and ketoconazole in healthy volunteers at steady state (abstract No 137). Pharmacotherapy 2005;25:474.
3. Backhaus J, Riemann D. Schlafstörungen. Fortschritte der Psychotherapie. Band VII. Göttingen: Hogrefe, 1999.
4. Backhaus J, Müller-Popkes K, Hajak G, Voderholzer U, et al. Prevalence, diagnosis and treatment of insomnia in general practice. J Sleep Res 1998;7:13.
5. Blaschke G, Hempel G, Müller WE. Preparative and analytical separation of the zopiclone enantiomers and determination of their affinity to the benzodiazepine receptor binding site. Chirality 1993;5:419–21.
6. Carlson JN, Haskew R, Wacker J, Maisonneuve IM, et al. Sedative and anxiolytic effects of zopiclone’s enantiomers and metabolite. Eur J Pharmacol 2001;415:181–9.
7. Compton-Mc Bride S, Schweitzer PK, Walsh JK. Most commonly drugs to treat insomnia in 2002. Sleep 2004;27(Suppl):A255.
8. Erman MK, Zammit G, Rubens R, Schaefer K, et al. A polysomnographic placebo-controlled evaluation of the efficacy and safety of eszopiclone relative to placebo and zolpidem in the treatment of primary insomnia. J Clin Sleep Med 2008;4:229–34.
9. European Medicines Agency Pre-Authorisation Evaluation of Medicines for Human use: Committee for Medicinal products for human use. Summary of positive opinion for Lunivia, London 23 Oct 2008; Doc.REF.EMEA/CHMP/546022/2008.
10. Fava M, McCall WV, Krystal A, et al. Eszopiclone co-administered with fluoxetine in patients with insomnia coexisting with major depressive disorder. Biol Psychiatry 2006;59:1052–106.
11. Ferentinos P, Paparrigopoulos T. Zopiclone and sleepwalking. Int J Neuropsychopharmacol 2009;12:141–2. Epub 2008 Oct 17.
12. Fernandez C, Alet P, Davrinche C, Adrien J, et al. Stereoselective distribution and stereoconversion of zopiclone enantiomers in plasma and brain tissues in rats. J Pharm Pharmacol 2002;54:335–40.
13. Glass J, Lanctot KL, Herrmann N, et al. Sedative hypnotics in older people with insomnia: meta-analysis of risks and benefits. BMJ 2005;331:1169–75.
14. Hajak G, Rodenbeck A, Voderholzer U, et al. Doxepin in the treatment of primary insomnia. J Clin Psychiatry 2001;62:453–63.
15. Hoffmann F, Scharffetter W, Glaeske G. Use of zolpidem and zopiclone on private prescriptions between 1993 and 2007. Nervenarzt 2009;80:578–83.
16. Hohagen F, Montero RF, Weiss E, Lis S, et al. Treatment of primary insomnia with trimipramine: an alternative to benzodiazepine hypnotics? Eur Arch Psychiatry Clin Neurosci 1994;244:65–72.
17. Jacobs GD, Pace-Schott EF, Stickgold R, Otto MW. Cognitive behaviour therapy and pharmacotherapy for insomnia: Arch Intern Med 2004;164:1888–96.
18. Kripke DF. “Who should sponsor sleep disorders pharmaceutical trials?”. J Clin Sleep Med 2007;3:671–3.
19. Kripke DF. Risks of chronic hypnotic use. In: Lader M, Cardinali DP, Pandi-Perumal SR (eds.). Sleep and sleep disorders – a neuropsychopharmacological approach. New York: Springer, 2006:141–5.
20. Krystal AD, Walsh JK, Laska E, Caron J, et al. Sustained efficacy of eszopiclone over 6 months of nightly treatment: results of a randomized, double-blind, placebo-controlled study in adults with chronic insomnia. Sleep 2003;26:793–9.
21. Krystal AD, Erman M, Zammit GK, Soubrane C, et al.; ZOLONG study group. Long-term efficacy and safety of zolpidem extended-release 12.5 mg, administered 3 to 7 nights per week for 24 weeks, in patients with chronic primary insomnia: a 6-month, randomized, double-blind, placebo-controlled, parallel-group, multicenter study. Sleep 2008;31:79–90.
22. Krystal A, Fava M, Rubens R, Wessel T, et al. Evaluation of eszopiclone discontinuation after co-therapy with fluoxetine for insomnia with coexisting depression. J Clin Sleep Med 2007;3:48–55.
23. Lunesta® (eszopiclone) tablets 1 mg, 2 mg, 3 mg: US prescribing information. Marlborough (MA): Sepracor Inc, 2008:2.
24. Maier G, Koch P, Caron J, et al. Dose proportionally and time to steady state of eszopiclone in healthy adult volunteers following single and multiple dosing. AAPS PharmSci 2003;5:abstract No. M1325.
25. McCall WV, Erman M, Krystal AD, Rosenberg R, et al. A polysomnography study of eszopiclone in elderly patients with insomnia. Curr Med Res Opin 2006;22:1633–42.
26. Morin CM, Culbert JP, Schwartz SM. Non-pharmacological interventions for insomnia: A meta-analysis of treatment efficacy. Am J Psychiatry 1994;151:1172–80.
27. Morin CM, Colecchi C, Stone J, et al. Behavioural and pharmacological therapies for late-life insomnia. JAMA 1999;281:991–9.
28. Morin CM, Vallières A, Guay B, Ivers H, et al. Cognitive behavioral therapy, singly and combined with medication, for persistent insomnia: a randomized controlled trial. JAMA 2009;301:2005-15.
29. Murtagh DR, Greenwood KM. Identifying effective psychological treatments for insomnia: a meta-analysis. J Consult Clin Psychol 1995;63:79–89.
30. Ohayon M. Epidemiology of insomnia: what we know and what we still need to learn. Sleep Med Rev 2002;6:97–111.
31. Pollack M, Kinrys G, Krystal A, McCall WV, et al. Eszopiclone coadministered with escitalopram in patients with insomnia and comorbid generalized anxiety disorder. Arch Gen Psychiatry 2008;65:551–62.
32. Riemann D, Voderholzer U. Primary insomnia: a risk factor to develop depression? J Affect Disord 2003;76:255–9.
33. Riemann D, Voderholzer U, Cohrs S, et al. Trimipramine in primary insomnia: results of a polysomnographic double-blind controlled study. Pharmacopsychiatry 2002;35:165–74.
34. Rosenberg R, Caron J, Roth T, Amato D. An assessment of the efficacy and safety of eszopiclone in the treatment of transient insomnia in healthy adults. Sleep Med 2005;6:15–22.
35. Roth T, Walsh JK, Krystal A, Wessel T, et al. An evaluation of the efficacy and safety of eszopiclone over 12 months in patients with chronic primary insomnia. Sleep Med 2005;6:487–95.
36. Rubens R, Wilson P, Schaefer K, McCall W, et al. Changes in sleep outcomes with placebo treatment in patients with primary insomnia and insomnia co-morbid with peri-menopausal transition or rheumatoid arthritis. Sleep 2007;30(Suppl):A247.
37. Scharf M, Erman M, Rosenberg R, Seiden D, et al. A 2-week efficacy and safety study of eszopiclone in elderly patients with primary insomnia. Sleep 2005;28:720–7.
38. Scharf M, Rogowski R, Hull S, Cohn M, et al. Efficacy and safety of doxepin 1 mg, 3 mg, and 6 mg in elderly patients with primary insomnia: A randomized, double-blind, placebo-controlled crossover study. J Clin Psychiatry 2008;69:1557–64.
39. Sivertsen B, Omvik S, Pallesen S, Bjorvatn B, et al. Cognitive behavioural therapy vs. zopiclone for treatment of chronic primary insomnia in older adults: a randomized controlled trial. JAMA 2006;295:2851–8.
40. Soares CN, Joffe H, Rubens R, Caron J, et al. Eszopiclone in patients with insomnia during perimenopause and early postmenopause: a randomized controlled trial. Obstet Gynecol 2006;108:1402–10.
41. Walsh JK, Engelhardt CL. The direct economic costs of insomnia in the United States for 1995. Sleep 1999;22(Suppl 2):S386–93.
42. Walsh JK, Erman M, Erwin M, et al. Subjective hypnotic efficacy of trazodone and zolpidem in DMS-III-R primary insomnia. Hum Psychopharmacol 1998;13:191–8.
43. Zammit GK, McNabb LJ, Caron J, Amato DA, et al. Efficacy and safety of eszopiclone across 6-weeks of treatment for primary insomnia. Curr Med Res Opin 2004;20:1979–91.
44. Zavesicka L, Brunovsky M, Horacek J, Matousek M, et al. Trazodone improves the results of cognitive behaviour therapy of primary insomnia in non-depressed patients. Neuro Endocrinol Lett 2008;29:895–901.
Dr. med. John Peter Doerr, Prof. Dr. Dieter Riemann, Abteilung für Psychiatrie und Psychotherapie der Universitätsklinik Freiburg, Hauptstr. 5, 79104 Freiburg, E-Mail: john-peter.doerr@uniklinik-freiburg.de
Treating insomnia with eszopiclone
The European Medicines Agency (EMEA) recently confirmed the efficacy of eszopiclone, the S-enantiomer of zopiclone, for short-term treatment of patients with primary insomnia. Since 2004 eszopiclone is commonly used in the USA for short- and long-term treatment. However, in Germany the commercial launch seems to be unlikely because the developing company withdrew their marketing application. The reason for this was that the Committee did not consider eszopiclone as a new active substance. Thus, the comparable substance zopiclone will remain as a treatment option for acute insomnia. Other treatment options however should not be considered as inferior. Especially for the cognitive-behavioral therapy evidence based data exist for short-term as well as long-term treatment. Further comparative studies are necessary to prove the claim that Z-substances like eszopiclone would be superior.
Keywords: Insomnia, sleep, eszopiclone
Psychopharmakotherapie 2009; 16(05)
