Thomas Messer, Kathrin Meyer zur Capellen, Augsburg, Wolfgang Trapp, Bamberg, Gerd Laux, Wasserburg, Wilfried Günther, Bamberg, Max Schmauss, Augsburg, Reinhard Steinberg, Klingenmünster, Norbert Müller, München, Heinrich Schulze Mönking, Telgte, Hans-Jürgen Möller, München, Karl-Ludwig Täschner, Stuttgart, und Ulrich Frommberger, Offenburg
Die vorliegende Arbeit repräsentiert den letzten Teil einer Ärztebefragung, die an bundesdeutschen psychiatrischen Versorgungskliniken durchgeführt wurde. Die Ergebnisse zu Antipsychotika, Tranquilizern/Hypnotika, Antidementiva und Antidepressiva wurden 2008 und 2009 in der vorliegenden Zeitschrift publiziert [36, 46, 74, 82]. Ziel dieser Befragung war es, naturalistisch die gegenwärtige Verordnungspraxis in der Behandlung von bipolaren Störungen zu identifizieren und mit den derzeit gültigen nationalen und internationalen Behandlungsempfehlungen und Therapieleitlinien zu vergleichen.
Einleitung
Trotz sehr unterschiedlicher Angaben zur Lebenszeitprävalenz gehört die bipolare Störung zu den psychischen Erkrankungen, die häufig mit einem sehr frühen Krankheitsbeginn, einem hohen Rezidivrisiko und langen Krankheitsepisoden einhergeht [39, 51, 56]. Die manischen Episoden bleiben oft jahrelang unerkannt und deswegen untherapiert, können aber bei klinischer Manifestation rapide das individuelle soziale Gefüge erschüttern [25, 40]. Die im Vergleich zur manischen Episode anhaltenden depressiven Phasen dominieren den Verlauf und sind hinsichtlich des allgemein geforderten Kriteriums der Vollremission häufig therapieresistent. Sie können intensive Reintegrationsbemühungen zum Scheitern bringen und die Lebensqualität dadurch erheblich beeinträchtigen [26, 42, 49, 59]. Im Vergleich zur Allgemeinbevölkerung, aber auch zu monopolar depressiv Erkrankten ist das Suizidrisiko mit bis zu 20% deutlich erhöht [17, 28].
Langzeituntersuchungen ergaben, dass nach einer manischen Episode weniger als die Hälfte der Betroffenen ausreichend gut auf die Behandlung anspricht [59].
Das Verordnungsverhalten in der Behandlung bipolarer Störungen hat sich in den vergangenen Jahren grundlegend verändert. Während früher zur Behandlung der akuten Manie entweder konventionelle Antipsychotika („first generation antipsychotics“ [FGA]) oder Lithiumsalze eingesetzt wurden, haben seit ihrer Zulassung Antipsychotika der zweiten Generation („second generation antipsychotics“ [SGA]) ihren Stellenwert ebenso erhöht wie die Antikonvulsiva [3, 57, 85]. Ebenso werden in der Phasenprophylaxe bipolarer Störungen und insbesondere zur Behandlung der bipolaren Depression atypische Antipsychotika wie Quetiapin und stimmungsstabilisierende Antikonvulsiva wie Lamotrigin zunehmend eingesetzt.
Methodik
Die nachfolgend dargestellten Ergebnisse entstammen aus einer Befragung von Ärzten in deutschen psychiatrischen Kliniken (n=283), die auf Veranlassung der Arbeitsgemeinschaft Biologische Psychiatrie der deutschen Bundesdirektorenkonferenz durchgeführt wurde. Einzelheiten sind den genannten Vorpublikationen zu entnehmen [36, 46, 74, 82].
Die im Folgenden dargestellten Ergebnisse beziehen sich auf den Fragebogenteil zu den „Antimanika/ Stimmungsstabilisierer (Mood Stabilizer)“.
Hier wurde zunächst nach den präferierten Substanzen in der Akutbehandlung manischer und depressiver Episoden bei bipolaren Störungen gefragt. Die Einschätzung sollte anschließend noch einmal nach Alter, Geschlecht sowie Erst- vs. Mehrfachmanifestation der behandelten Patienten differenziert werden.
Anschließend an die Frage, welche Informationen (Angaben des Herstellers, klinische Effekte, Nebenwirkungen und Blutspiegel) bei der Dosisentscheidung relevant sind, wurde um eine Angabe gebeten, auf welche Substanzen bei mangelnder klinischer Wirksamkeit am ehesten umgestellt wird. Bezüglich des Monitorings der medikamentösen Therapie interessierten die Zeitdauer, in der auf das Eintreffen der klinischen Effekte gewartet wird, die Berücksichtigung unerwünschter Effekte sowie die zeitlichen Abstände für Routineuntersuchungen (EKG, EEG und Labor).
Den Abschluss bildeten Fragen zur Kombinationsbehandlung manischer und depressiver Symptome bei der Akut- und Dauerbehandlung bipolarer Störungen.
Im Ergebnisteil sind zur besseren Vergleichbarkeit ausschließlich Prozentangaben dargestellt. Diese Prozentangaben beziehen sich jeweils auf die 235 Befragten, die auch die Fragen zu den Stimmungsstabilisierern, die den Abschluss des Fragebogens bildeten, bearbeiteten.
Neben der rein numerischen Darstellung der Ergebnisse wurden zu einzelnen Fragen statistische Tests durchgeführt, um entweder zu prüfen, ob die zu Beginn des Fragebogens erfragten persönlichen Merkmale der befragten Ärztinnen und Ärzte (Berufserfahrung, hierarchische Stellung, Größe des Hauses etc.) einen Einfluss auf die Verordnungsgewohnheiten haben, oder um die Präferenzen bei verschiedenen Anwendungsbereichen (z.B. Akut- vs. Langzeitbehandlung oder manische vs. depressive Episode) miteinander zu vergleichen. Im ersten Fall (unabhängige Stichproben) wurden hierzu Chi2-Tests durchgeführt, im zweiten Fall (abhängige Stichproben) wurden McNemar-Chi2-Tests beziehungsweise Wilcoxon-Rangsummentests berechnet. Das erreichte Signifikanzniveau ist im Text jeweils angegeben.
Tabelle 1 gibt die zur Auswahl stehenden Antimanika und die Stimmungsstabilisierer wieder.
Tab. 1. Auswahlliste für die Angabe bevorzugter Stimmungstabilisierer und Antipsychotika
|
Kürzel |
Bezeichnung |
|
Stimmungsstabilisierer |
|
|
LIT |
Lithiumsalze |
|
LAM |
Lamotrigin |
|
CBZ |
Carbamazepin |
|
VAL |
Valproinsäure |
|
GAB |
Gabapentin |
|
Antipsychotika |
|
|
OLA |
Olanzapin |
|
RIS |
Risperidon |
|
CLZ |
Clozapin |
|
QUE |
Quetiapin |
Ergebnisse
Für die Akutbehandlung einer manischen Episode bei vordiagnostizierter bipolarer Störung benannten die Befragten an erster Stelle Lithiumsalze mit 41,3%, Valproinsäure mit 25,5% und Olanzapin mit 20,4%. Als zweite Wahl wurde mit 26,2% Valproinsäure, mit 20,5% Olanzapin und mit 17,9% Carbamazepin genannt. Die dritte Wahl fiel mit 25,5% auf Carbamazepin, mit 22,7% auf Valproinsäure und mit 18,1% auf Olanzapin. Am wenigsten häufig wurden Lamotrigin, Gabapentin, Risperidon, Clozapin und Quetiapin genannt (Abb. 1).
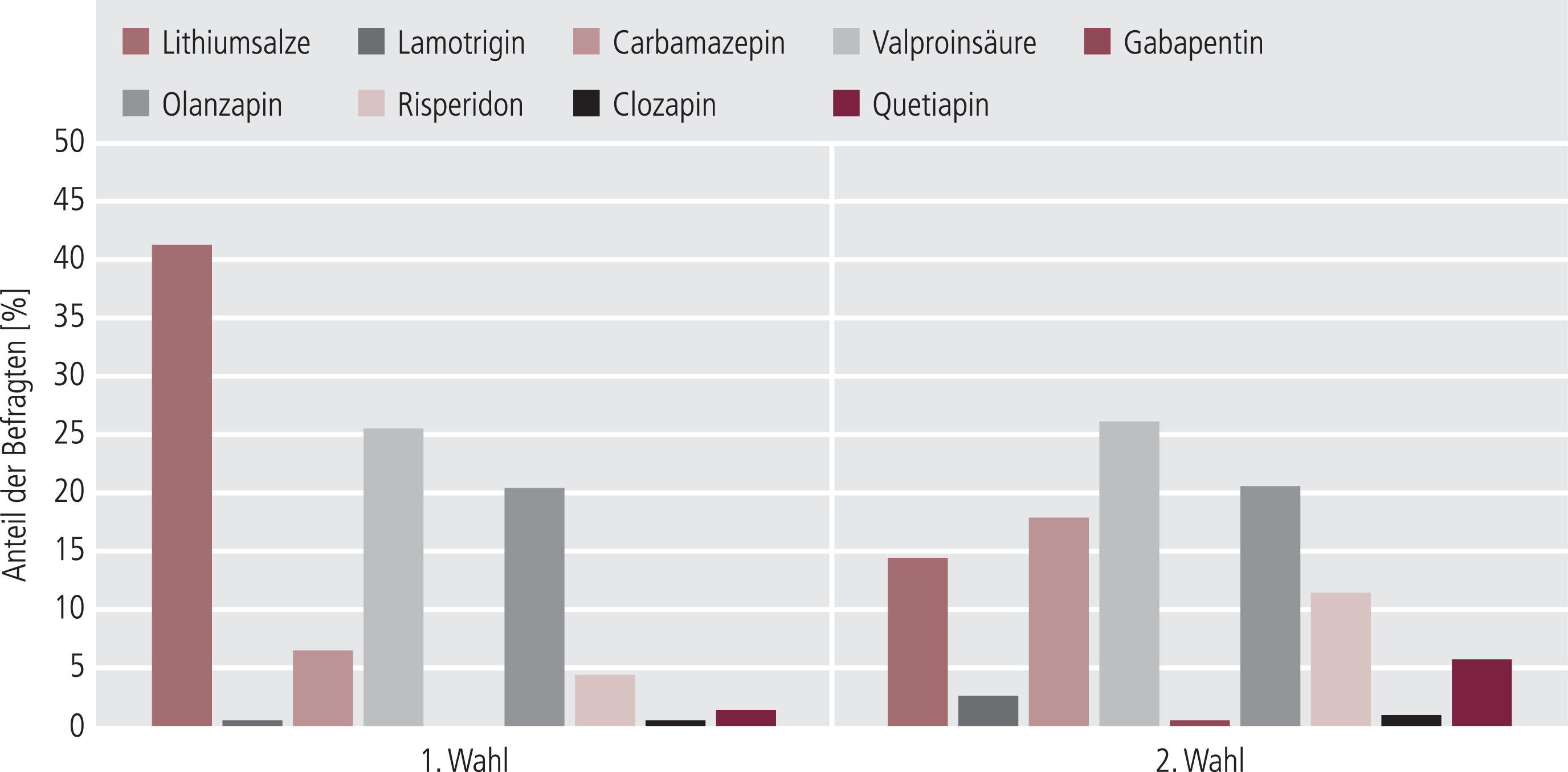
Abb. 1. Akutbehandlung der manischen Episode bei bipolarer Störung (n=235)
Für die Akutbehandlung der depressiven Episode bei vordiagnostizierter bipolarer Störung fiel die erste Wahl mit 53,4% auf Lithiumsalze, mit 20,6% auf Lamotrigin und mit je 8,5% auf Carbamazepin und Olanzapin. An zweiter Stelle wurden von den Ärzten mit 23,9% Lamotrigin, mit je 21,6% Carbamazepin und Valproinsäure sowie mit 17,4% Lithiumsalze ausgewählt. Die dritte Wahl fiel bei 26,5% auf Valproinsäure, bei 24,7% auf Carbamazepin, bei 14,7% auf Olanzapin und bei 11,8% auf Lithiumsalze. Am wenigsten häufig wurden Risperidon und Quetiapin genannt, Clozapin wurde sehr selten und Gabapentin gar nicht genannt (Abb. 2).
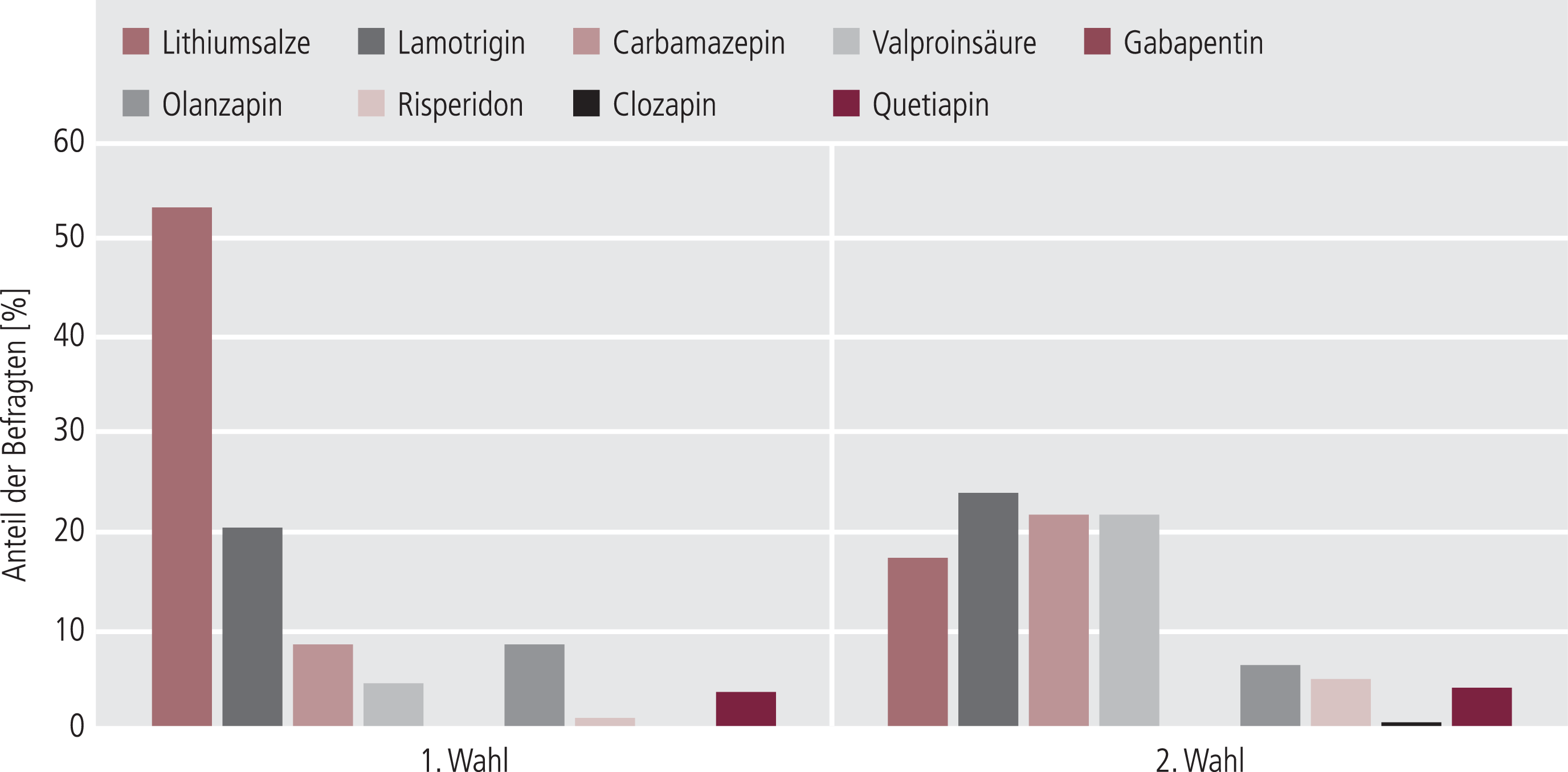
Abb. 2. Akutbehandlung der depressiven Episode bei bipolarer Störung (n=235)
Für die Akutbehandlung der bipolaren Störung bei älteren Patienten nannten die befragten Ärzte an erster Stelle Valproinsäure mit 43,6%, Lithiumsalze und Carbamazepin mit je 11,4% und Olanzapin mit 10%. Als zweite Wahl entfielen 22,8% ebenfalls zunächst auf Valproinsäure, 20,6% auf Carbamazepin und 15,6% auf Lithiumsalze. Als dritte Wahl entschieden sich 23% für Lithiumsalze, 17,8% für Carbamazepin und 16,3% für Valproinsäure. Am wenigsten häufig wurden Lamotrigin, Gabapentin und Clozapin genannt, die Atypika Risperidon und Quetiapin erst häufiger ab der dritten Wahl.
Bei jüngeren Patienten wurden Lithiumsalze mit 43,2% an erster Stelle genannt, 26,8% der Ärzte entschieden sich für Valproinsäure und 13,1% für Olanzapin. Die zweite Wahl fiel mit 23,6% auf Carbamazepin, mit 21,3% auf Olanzapin, mit 17,4% auf Lithiumsalze und mit 16,9% auf Valproinsäure. An dritter Stelle wurde zunächst Valproinsäure mit 28,3%, Carbamazepin mit 19,1% und Olanzapin mit 18,4% genannt. Am wenigsten häufig genannt wurden Lamotrigin, Gabapentin, Risperidon, Clozapin und Quetiapin.
Beim Vergleich der Behandlung von älteren und jüngeren Patienten entschieden sich hochsignifikant (p<0,001) mehr Ärzte für eine Behandlung mit Lithiumsalzen bei jüngeren Patienten als bei älteren Patienten (39% vs. 10% von 235 Befragten).
Für die Behandlung von Frauen versus Männern ergaben sich keine signifikanten Unterschiede.
Zur Behandlung der akuten Erstmanifestation einer bipolaren Erkrankung würden die befragten Ärzte erstrangig Valproinsäure (30,2%), Lithiumsalze (29,7%) oder Olanzapin (22,9%) verordnen (Abb. 3).
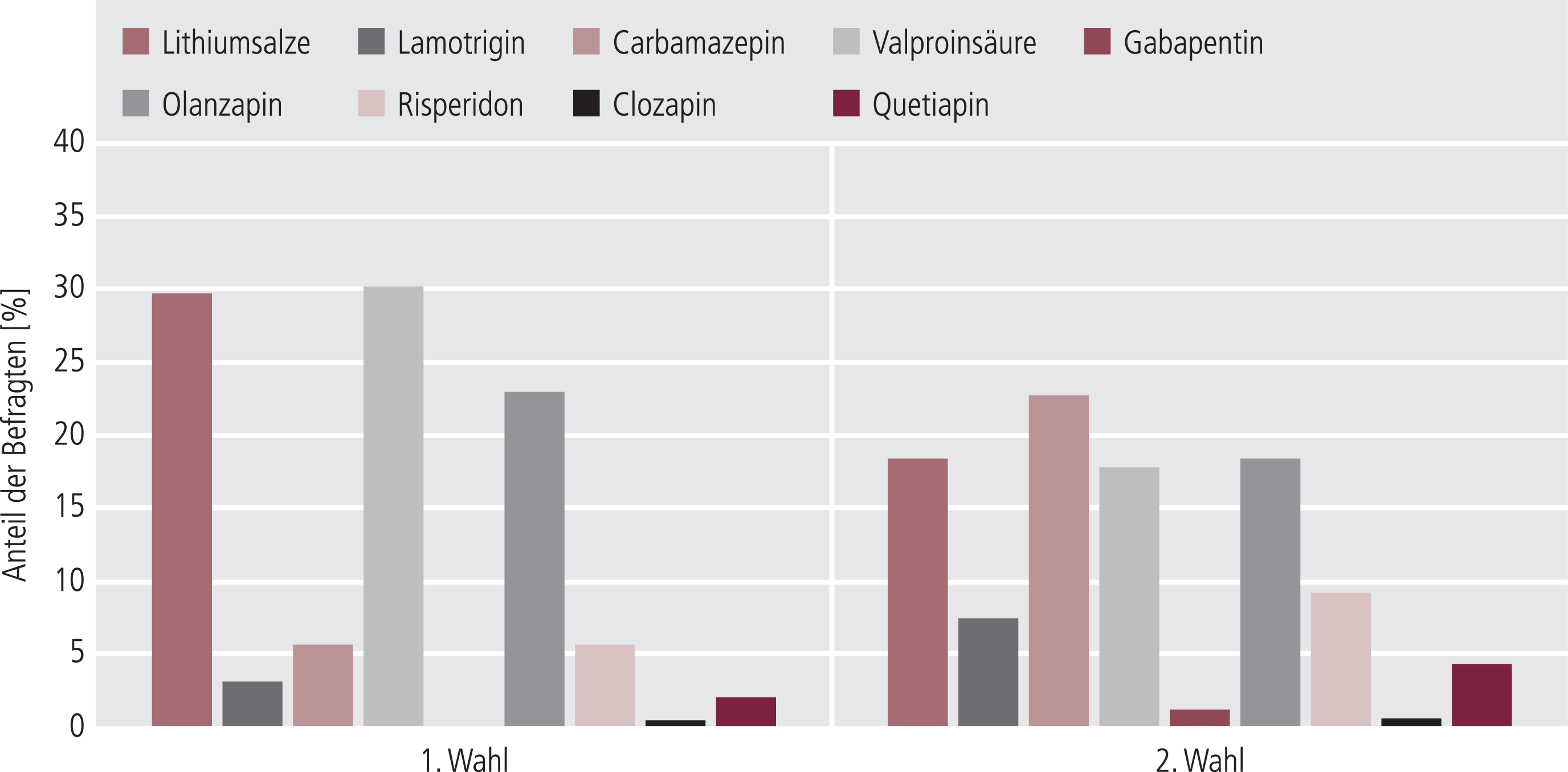
Abb. 3. Akutbehandlung der bipolare Störung bei Erstmanifestation (n=235)
Zur Akutbehandlung von Mehrfachmanifestationen einer bipolaren Störung wurden erstrangig Lithiumsalze von 51,1% der Befragten favorisiert, gefolgt von Valproinsäure mit 26,6% und Olanzapin mit 8% (Abb. 4).
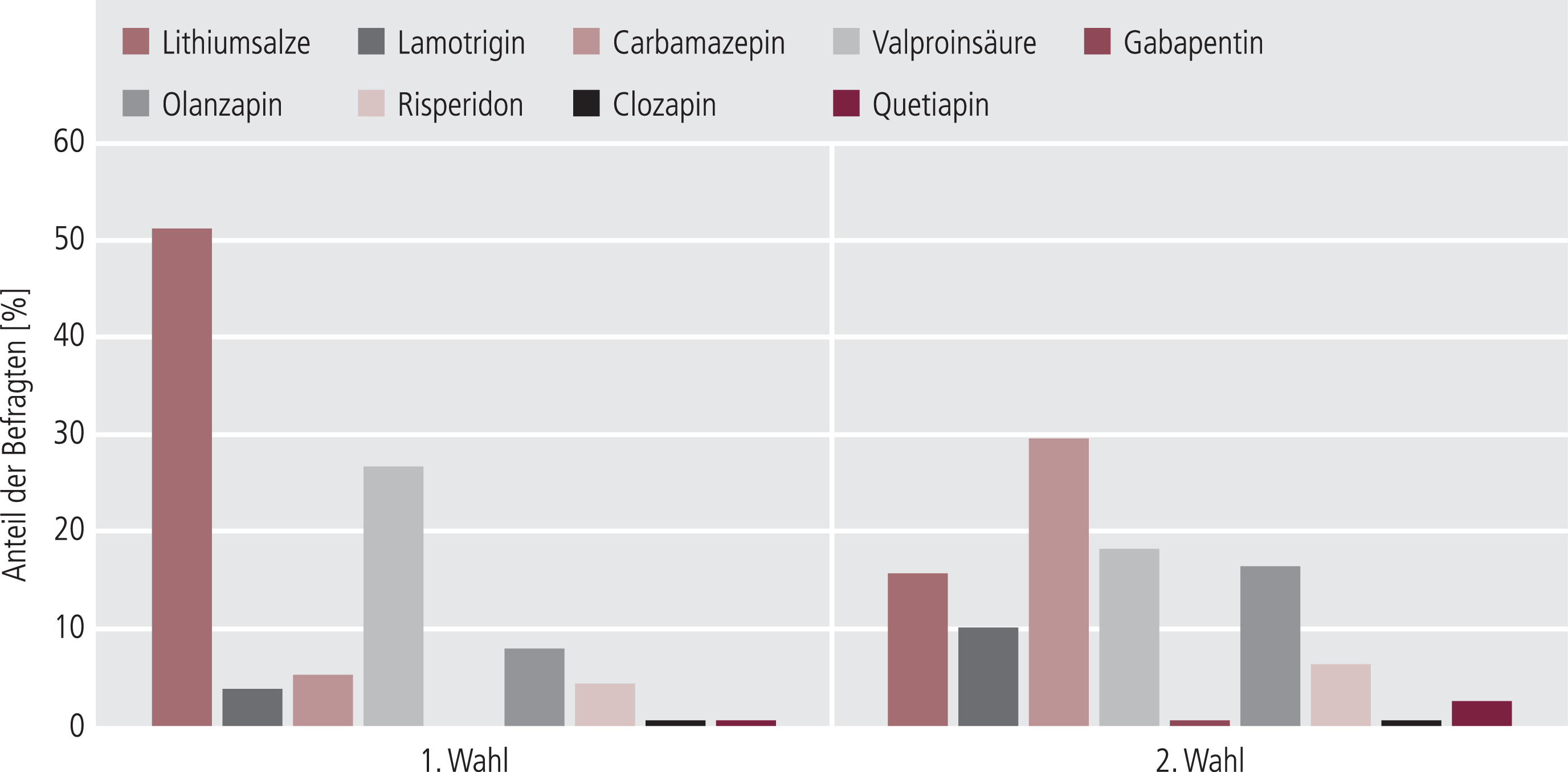
Abb. 4. Akutbehandlung der bipolaren Störung bei Mehrfachmanifestation (n=235)
Bei der Frage nach der Relevanz der Herstellerangaben, der klinischen Effekte, der Nebenwirkungen sowie des Blutspiegels für die Dosisentscheidung hielten 66,4% der Ärzte die Angaben des Herstellers für relevant, die klinischen Effekte wurden zu 96,6% als relevant bezeichnet. Ähnliche Angaben ließen sich bei den Nebenwirkungen finden (96,1%). Serumspiegelbestimmungen wurden immerhin von 83,1% der Ärzte als dosisfindungsrelevant angesehen.
Ein weiterer Aspekt war die Frage nach der medikamentösen Umstellung in der Akut- und Langzeittherapie bei mangelnder klinischer Wirksamkeit, falls eine Monotherapie noch möglich ist. Von Lithiumsalzen würden beispielsweise in der Akutbehandlung 49% auf Valproinsäure, 24,7% auf Carbamazepin und 13,9% auf Olanzapin umstellen, in der Langzeittherapie 50,8% auf Valproinsäure, 28,4% auf Carbamazepin und 15,3% auf Lamotrigin (Tab. 2).
Tab. 2. Umstellungen bei mangelnder klinischer Wirksamkeit (Angaben in %)
|
Von … auf … |
Akutbehandlung |
Langzeitbehandlung |
||
|
Lithiumsalz |
Valproinsäure Carbamazepin Olanzapin Lamotrigin |
49,0 24,7 13,9 8,8 |
Valproinsäure Carbamazepin Lamotrigin |
50,8 28,4 15,3 |
|
Carbamazepin |
Valproinsäure Lithiumsalz Olanzapin |
46,6 38,6 8,0 |
Lithiumsalz Lamotrigin Valproinsäure |
42,9 6,5 48,8 |
|
Valproinsäure |
Lithiumsalz Carbamazepin Lamotrigin Olanzapin |
50,0 18,5 13,7 11,9 |
Lithiumsalz Carbamazepin Lamotrigin Olanzapin |
58,6 19,1 13,6 4,3 |
|
Olanzapin |
Risperidon Lithiumsalz Valproinsäure Quetiapin Carbamazepin |
34,5 19,6 17,6 16,9 7,4 |
Risperidon Lithiumsalz Valproinsäure Quetiapin Carbamazepin |
26,8 23,9 22,5 11,6 8,7 |
Bei den Fragen der Umstellung von Lamotrigin, Gabapentin, Risperidon, Clozapin und Quetiapin auf eine alternative Monotherapie war auffällig, dass sowohl hinsichtlich der Akut- als auch der Langzeitbehandlung keine Angaben gemacht wurden.
Ein signifikanter Unterschied fand sich bei der Umstellungsfavorisierung von Lithiumsalzen in der Langzeittherapie bezüglich der Altersgruppen der Ärzte (p<0,05). Von den Ärzten unter 30 Jahren wählten 70% der Befragten für die Umstellung Valproinsäure, in den beiden Altersgruppen „30 bis 39 Jahre“ und „40 bis 49 Jahre“ wählten jeweils etwa die Hälfte Valproinsäure und etwa ein Viertel Carbamazepin. Bei den Ärzten ab 50 Jahren wählten jeweils rund 40% Valproinsäure und Carbamazepin.
Weiterhin ließen sich signifikante Unterschiede bei der Umstellungsfavorisierung von Olanzapin auf einen anderen Stimmungsstabilisierer in der Langzeittherapie bezüglich des Ausbildungsstandes finden (p<0,05). Assistenzärzte bevorzugten mit 32% Valproinsäure und mit 23% Risperidon, Fachärzte verordneten als Umstellungsoption nach Olanzapin mit 30% Risperidon und mit 29% Lithiumsalze.
Die Wartezeit bis zur Umstellung bei erfolgloser antimanischer oder antidepressiver Akutbehandlung ist in Abbildung 5 wiedergegeben.
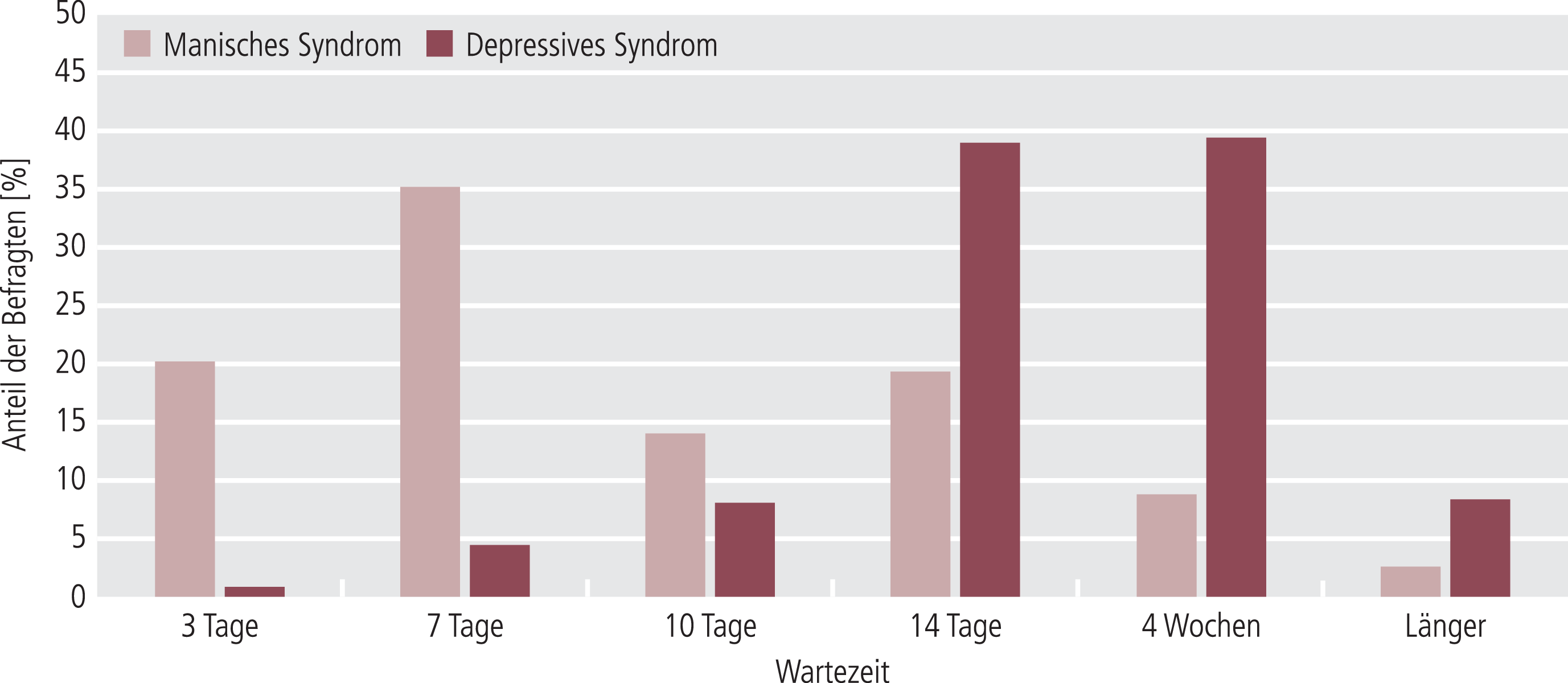
Abb. 5. Wartezeit auf klinische Effekte (Akuttherapie) bis zur Umstellung (n=235)
Die Wichtigkeit unerwünschter Nebenwirkungen (UAW) ist in Tabelle 3 wiedergegeben.
Tab. 3. Wichtigkeit von (unerwünschten) Effekten unter Therapie mit Stimmungsstabilisierern (Angaben in %)
|
UAW |
Gar nicht oder weniger wichtig |
Wichtig oder sehr wichtig |
||
|
Akutbehandlung |
Langzeitbehandlung |
Akutbehandlung |
Langzeitbehandlung |
|
|
Zentralnervös |
20,6 |
4,4 |
79,4 |
95,6 |
|
Gastrointestinal |
28,6 |
14,7 |
71,4 |
85,3 |
|
Dermatologisch |
26,0 |
14,2 |
74,0 |
85,8 |
|
Hämatologisch |
3,5 |
2,6 |
96,5 |
97,4 |
|
Endokrinologisch |
19,7 |
9,0 |
80,3 |
91,0 |
|
Kardiovaskulär |
2,6 |
4,9 |
97,4 |
95,1 |
|
Gewichtszunahme |
50,2 |
13,4 |
49,8 |
86,6 |
Insgesamt fanden sich bei den Beurteilungen der unerwünschten Nebenwirkungen hochsignifikante Unterschiede (p<0,01) beim Vergleich zwischen Akut- und Langzeitbehandlung bei den zentralnervösen, gastrointestinalen, dermatologischen und endokrinologischen Nebenwirkungen sowie der Gewichtszunahme. Signifikante Unterschiede ergaben sich in den verschiedenen Altersgruppen der Ärzte bei der Einschätzung von zentralnervösen UAW in der Langzeittherapie (p<0,05) sowie bei den gastrointestinalen UAW in der Akutbehandlung (p<0,05). 82% der unter 30-jährigen Ärzte und jeweils rund 97% der befragten Ärzte in den Gruppen „30 bis 39“, „40 bis 49“ und „älter als 50“ Jahre entschieden sich für die Beurteilung „wichtig oder sehr wichtig“ bei den zentralnervösen UAW in der Langzeitbehandlung. Gastrointestinale UAW in der Akutbehandlung hielten 59% der unter 30-Jährigen, 68% der 30- bis 39-Jährigen, 65% der 40- bis 49-Jährigen und 88% der über 50-Jährigen für „wichtig oder sehr wichtig.“ Ebenfalls fanden sich bei den dermatologischen UAW signifikante Unterschiede in der Langzeitbehandlung im Hinblick auf die Altersgruppen (p<0,05). Die unter 30-Jährigen hielten zu 59% diese UAW für „wichtig oder sehr wichtig“, 85% der 30- bis 39-Jährigen, 88% der 40- bis 49-Jährigen und 93% der ab 50 Jahre alten Ärzte teilten diese Einschätzung.
Signifikante Unterschiede in der Beurteilung der dermatologischen UAW in der Akut- und Langzeitbehandlung konnten bei der Tätigkeitsdauer sowie dem Ausbildungsstand ermittelt werden.
In der Langzeitbehandlung hielten nur 25% der bis sechs Jahre tätigen Ärzte und 10% der über sieben Jahre tätigen Ärzte die dermatologischen UAW für „gar nicht oder weniger wichtig“. In der Akutbehandlung beurteilten rund 50% der Assistenzärzte, aber nur rund 20% der Ärzte mit „Facharztausbildung oder höher“ die dermatologischen UAW als „gar nicht oder weniger wichtig“, in der Langzeitbehandlung entschieden sich rund 25% der Assistenzärzte und nur 7% der Ärzte mit „Facharztausbildung oder höher“ für diese Beurteilung.
Die zeitlichen Abstände, in welchen verschiedene Routineuntersuchungen bei der Behandlung von bipolaren Störungen durchgeführt werden, wurden ebenfalls erfragt. In der Akutbehandlung gaben beim EKG die meisten Befragten an, dies wöchentlich durchführen zu wollen (44%), 28,9% hielten eine 14-tägige und 21,8% eine monatliche Durchführung für sinnvoll. Das EEG würden 42% monatlich durchführen, 29,2% vierteljährlich und 18,9% 14-tägig. Laboruntersuchungen wurden von 74,2% in wöchentlichen Abständen gefordert und von 14,7% in 14-tägigen Abständen. In der Langzeitbehandlung sprachen sich 41,8% der Ärzte für eine vierteljährliche EKG-Kontrolle aus, 25,5% für eine halbjährliche, 13,2% für eine monatliche und 10,5% für eine 2-monatliche Untersuchung. Bei der EEG-Untersuchung verteilten sich die Prozente mit 41,6% auf eine jährliche, 31,1% auf eine halbjährliche und 19,1% auf eine vierteljährliche Kontrolle, beim Labor mit 41,4% auf eine vierteljährliche, mit 31,4% auf eine monatliche und mit 17,7% auf eine 2-monatliche Kontrolle.
Als häufigste Kombinationstherapie der ersten Wahl in der Akutbehandlung eines manischen Syndroms einer bipolaren Störung wurde mit einer Häufigkeit von 25,9% Valproinsäure und Olanzapin von den befragten Psychiatern bevorzugt, 20,5% entschieden sich für Lithiumsalze und Olanzapin, 8,6% für ein Antipsychotikum der ersten Generation (FGA) in Kombination mit Lithiumsalzen und 8,2% für Lithiumsalze und Valproinsäure. Als zweite Wahl wurde mit 14,5% Lithiumsalze und Olanzapin genannt, mit 11,4% Valproinsäure und Risperidon, mit 10,9% Valproinsäure und Olanzapin und mit 7,7% Lithiumsalze und Valproinsäure. An dritter Stelle wurde mit 9,5% Lithiumsalze und Olanzapin vorgeschlagen, mit 8,6% Valproinsäure und Risperidon und mit 7,7% FGA und Valproinsäure.
In der Akutbehandlung des depressiven Syndroms (Kombinationstherapie) wurden als erste Wahl die in Abbildung 6 wiedergegebenen Substanzen angegeben.
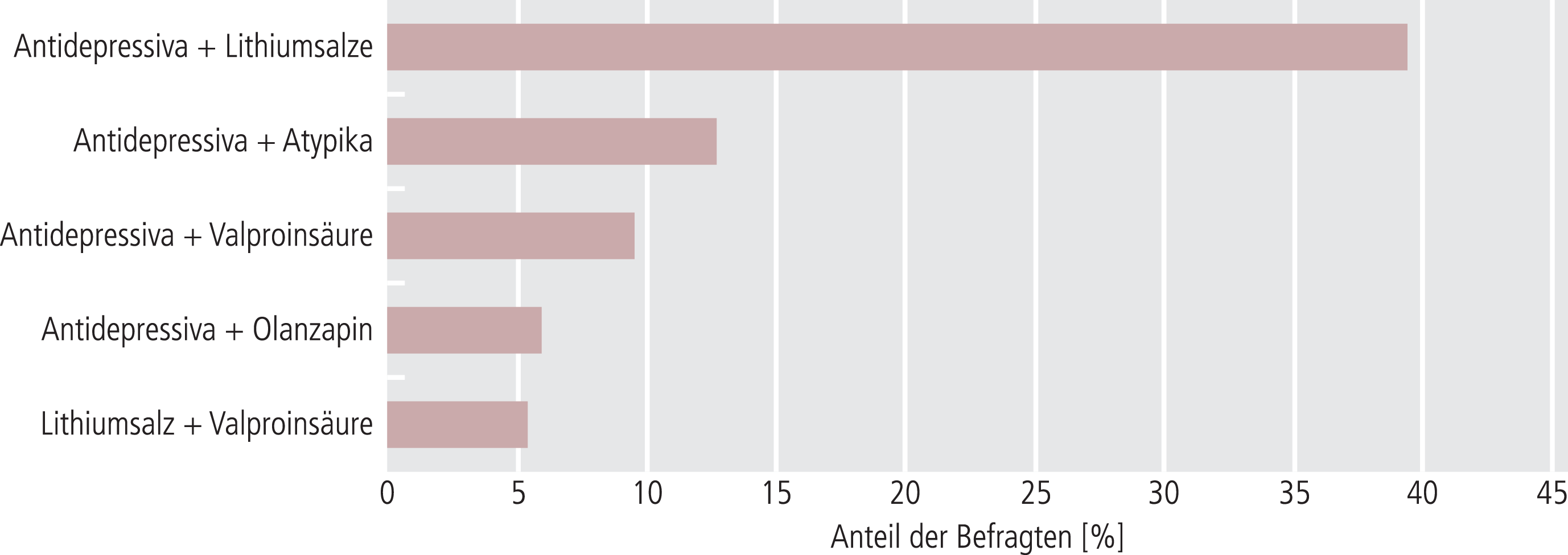
Abb. 6. Kombinationstherapien in der Akutbehandlung bei depressivem Syndrom, erste Wahl (n=235)
In der Langzeitbehandlung des manischen Dekompensationstyps einer bipolaren Störung nannten 27,6% der Befragten Lithiumsalze und Olanzapin als erste Wahl bei einer Kombinationstherapie, 20,6% Valproinsäure und Olanzapin, 14,5% Lithiumsalze und Valproinsäure und 7,9% Lithiumsalze und Risperidon. Die zweite Wahl fiel in 15% der Fälle auf Lithiumsalze und Olanzapin, mit je 14% auf Lithiumsalze und Risperidon sowie Valproinsäure und Olanzapin, in 7,9% der Fälle auf Valproinsäure und Risperidon.
In der Langzeitbehandlung des depressiven Dekompensationstyps einer bipolaren Störung fiel bei 45,8% der Befragten die erste Wahl auf die Kombination eines Antidepressivums (AD) mit Lithiumsalzen, bei 9% auf Lithiumsalze und Olanzapin, bei 8% auf Lithiumsalze und Valproinsäure sowie bei 7,1% auf ein AD und Valproinsäure. Bei der zweiten Wahl wurde mit 19,8% ein AD und Valproinsäure, mit 13,7% AD und Carbamazepin sowie mit 7,5% AD und Lithiumsalzen genannt.
Bei den Kombinationstherapien in der Akutbehandlung des depressiven Syndroms sowie in der Langzeitbehandlung des manischen und depressiven Dekompensationstyps ließen sich keine signifikanten Unterschiede hinsichtlich Tätigkeitsdauer, Geschlecht, Altersgruppe, Ausbildungsstand, Region oder Größe des Hauses finden.
Signifikante Unterschiede fanden sich beim Vergleich von Akut- und Langzeittherapie des manischen Syndroms bzw. Dekompensationstyps bei verschiedenen Kombinationen (p<0,05) (Berechnungen nur für erste Wahl). Von den Befragten, die die Kombination Valproinsäure und Lithiumsalz überhaupt als erste Wahl genannt hatten, favorisierten 66% diese in der Akutbehandlung und 38% in der Langzeitbehandlung. Für die Kombination Valproinsäure und Olanzapin waren 59% in der Akut- und 77% in der Langzeittherapie. Die Kombination FGA und Lithiumsalz wurde mit 21% in der Akut- und 44% in der Langzeittherapie bevorzugt.
Ein signifikanter Unterschied fand sich beim Vergleich der Akut- und Langzeitbehandlung des depressiven Syndroms oder Dekompensationstyps bei der Kombination AD und SGA (p=0,01): Von den Befragten, die diese Kombination als erste Wahl angegeben hatten, entschieden sich 21% dafür in der Akut- und 60% in der Langzeitbehandlung.
Diskussion
Behandlung der akuten manischen Episode
Für die Behandlung der akuten manischen Episode stehen aktuell Stimmungsstabilisatoren und Antipsychotika zur Verfügung. Der bestehende Trend zur evidenzbasierten Medizin trägt zu einer Vielfalt an Praxisleitlinien bei, in denen von verschiedenen nationalen und internationalen Expertenkomitees unterschiedliche Behandlungsstrategien empfohlen werden [27, 35].
Für mehr als ein Drittel der befragten Ärzte sind in der Behandlung der akuten Manie Lithiumsalze erste Wahl, was angesichts der Ansprechrate von mindestens 50% durchaus plausibel ist [35, 71]. Dabei bleibt allerdings die Tatsache, dass der antimanische Effekt von Lithiumsalzen erst mit einer Latenz von Tagen bis Wochen einsetzt, offenbar weitgehend unberücksichtigt. Bei den meisten prospektiven Studien, in denen Lithiumsalze mit einem älteren Antipsychotikum verglichen wurden, erwies sich Lithium gegenüber Chlorpromazin überlegen und gleichwertig zu Haloperidol. Eine methodisch herausragende Studie, in der Lithiumsalze mit Valproinsäure und Plazebo verglichen wurden, ergab bei einer niedrigen Responderquote eine Gleichwertigkeit der beiden Phasenprophylaktika und eine Überlegenheit gegenüber Plazebo [12]. Die Studien, in denen Lithiumsalze mit Carbamazepin verglichen wurden, ergaben ebenfalls Vorteile für Lithium [47, 48, 68].
An zweiter Stelle wurde Valproinsäure genannt, das in seiner Wirksamkeit zur Behandlung der akuten Manie im Vergleich zu Lithiumsalzen als gleichwertig angesehen werden kann [13]. In einer Metaanalyse erwies sich Valproinsäure gegenüber Plazebo signifikant überlegen, gegenüber Lithiumsalzen und Carbamazepin gleichwertig und im Vergleich zu Olanzapin etwas weniger wirksam [50]. Lamotrigin und Gabapentin wurden für die Akutbehandlung der Manie nicht genannt, wofür es auch aus kontrollierten oder offenen Studien keine hinreichende Begründung gibt [8, 22, 54, 58].
Antipsychotika der zweiten Generation (SGA) werden seit Jahren zunehmend zur Behandlung manischer Episoden erfolgreich eingesetzt. In randomisierten kontrollierten Studien (RCT) konnten Olanzapin, Risperidon, Quetiapin, Ziprasidon und Aripiprazol ihre Wirksamkeit in der Behandlung der bipolaren Manie beweisen, allerdings mit unterschiedlichen Effektstärken [18], wobei diese Substanzen alle gleich oder stärker wirksam sind als Lithiumsalze oder Valproinsäure [52]. Neben einem raschen Wirkungseintritt weisen diese Substanzen ein günstigeres Nebenwirkungsprofil auf als konventionelle Antipsychotika und entfalten zudem auch stimmungsstabilisierende Qualitäten [43, 75]. Für fast drei Viertel der Befragten ist Olanzapin erste Wahl, wenn eine Behandlung mit einem Antipsychotikum erwogen wird. Diese Vorgehensweise wird durch zwei Plazebo-kontrollierte, randomisierte, doppelblinde Studien gestützt, die die Überlegenheit einer Monotherapie mit Olanzapin gegenüber Plazebo belegen [79, 81]. Im Vergleich zu Lithiumsalzen und Valproinsäure ist Olanzapin als gleichwertig anzusehen [9, 86]. An zweiter Stelle rangierte Risperidon, für das in kontrollierten Studien ebenfalls eine antimanische Wirkung nachgewiesen wurde [38, 44, 63, 65, 70]. Für Quetiapin, das in der Befragung den dritten Platz einnimmt, existieren zwei kontrollierte Monotherapiestudien, die eine Überlegenheit des Verums gegenüber Plazebo nachgewiesen haben [15, 53].
Sofern eine Behandlung mit einem konventionellen Antipsychotikum erfolgen muss, wird von mehr als 60% der Befragten Haloperidol als gut steuerbare und parenteral applizierbare Substanz der Vorzug vor anderen Antipsychotika der ersten Generation gegeben. Allerdings muss kritisch bedacht werden, dass trotz der in älteren Studien gesicherten antimanischen Wirksamkeit der FGA diese Patienten wegen ihrer besonderen Vulnerabilität ein hohes Risiko für extrapyramidale Störungen mit einer geschätzten Prävalenz von 19 bis 41% für Tardivdyskinesien haben [61, 66, 67, 87].
Carbamazepin wurde nur als zweite oder dritte Wahl genannt, obgleich eine Ansprechrate von 27 bis 70% versus 22 bis 29% unter Plazebo festgestellt wurde [37, 84]. Bei Betrachtung der meisten Maniestudien kann davon ausgegangen werden, dass Carbamazepin einen vergleichbaren antimanischen Effekt hat wie Lithiumsalze, allerdings einen etwas geringeren als konventionelle Antipsychotika, wie beispielsweise Chlorpromazin [52]. Allerdings existiert auch eine Untersuchung, die eine Unterlegenheit gegenüber Lithiumsalzen beziehungsweise Valproinsäure bestätigt [83]. In Deutschland ist Carbamazepin für die Behandlung der akuten Manie nicht zugelassen.
Bipolare Depression
Die bipolare Depression stellt für die Betroffenen im Hinblick auf die soziale Integration, die individuelle Lebensqualität und das Suizidrisiko eine ungleich größere Belastung dar [1, 2]. Während manische Episoden mit dem verfügbaren medikamentösen Repertoire in der Regel rasch remittieren, verlaufen die depressiven Phasen oftmals langwierig und remittieren nur unvollständig.
Die älteren trizyklischen Antidepressiva, die dualen Antidepressiva und die Monoaminoxidase-(MAO-)Hemmer sind zwar in der Behandlung der depressiven Episode wirksam, beinhalten allerdings ein Risiko von bis zu 35%, in die Manie umzuschlagen („Switch“) [2, 7, 11, 45, 55]. Auf die transatlantisch teilweise kontrovers diskutierte Frage, ob und inwieweit Antidepressiva in der Behandlung der bipolaren Depression eingesetzt werden sollen, kann hier nicht eingegangen werden, da einzelne Antidepressiva bei diesem Interview nicht angegeben werden konnten.
Befragt zum Einsatz von Stimmungsstabilisierern, wurden von fast 60% der Teilnehmer Lithiumsalze und Lamotrigin erstrangig genannt. Diese Bewertung stimmt mit den Empfehlungen verschiedener Leitlinien überein, die angesichts vorliegender Studien trotz der substanzspezifischen Einschränkungen Lithiumsalze als Therapie der ersten Wahl in Behandlung der bipolaren Depression betrachten [10, 32, 88]. Auch Lamotrigin wird trotz der eher moderaten Evidenz in den Leitlinien der amerikanischen Fachgesellschaft APA als First-Line-Drug genannt, weil zumindest eine randomisierte kontrollierte Studie für die Akutbehandlung ambulanter Patienten als auch die Langzeitstudien positive Ergebnisse erbrachten. Valproinsäure und Carbamazepin nahmen in der Befragung nur eine untergeordnete Stellung ein, was angesichts der begrenzten Evidenz für diese beiden Substanzen in dieser Indikation eine folgerichtige Beurteilung darstellt.
Neben den Stimmungsstabilisierern werden in den USA in den letzten Jahren zunehmend moderne Antipsychotika wie Olanzapin und Quetiapin als alleinige Pharmakotherapie präferiert, obwohl hierzu nur wenige Studien existieren. Diese Therapieoption ist allerdings für die hier befragten Psychiater offenbar von nachrangiger Bedeutung.
Langzeittherapie des manischen oder depressiven Dekompensationstyps
In dieser Indikation favorisieren fast die Hälfte der Befragten eine Kombination von Lithiumsalz oder Valproinsäure mit Olanzapin, gefolgt von der Kombination Lithiumsalz plus Valproinsäure. Hier ist festzustellen, dass die Evidenz für eine rezidivprophylaktische Wirkung von Lithiumsalzen gut ist [24]. Allerdings gibt es auch Berichte darüber, dass die Rückfallrate unter einer Lithiumbehandlung innerhalb von zwei Jahren auf 54% steigt [6]. In einer Plazebo-kontrollierten Studie über ein Jahr waren Lithiumsalze nicht wirksamer als Plazebo in der Rückfallprophylaxe [13].
Für Carbamazepin konnte gezeigt werden, dass es bei sogenannten „atypischen“ Fällen mit stimmungskongruentem Wahn oder gemischten Episoden in der Rezidivprophylaxe vorteilhaft ist [33]. Eine Metaanalyse, in der Carbamazepin mit Lithiumsalzen in der Rezidivprophylaxe verglichen wurde, ergab allerdings kein überzeugendes Resultat für Carbamazepin [19]. Für Valproinsäure belegen lediglich offene Studien eine Verringerung des Rezidivrisikos. Für Lamotrigin bestätigen zwei doppelblinde Plazebo-kontrollierte Studien mit Lithiumsalzen eine vergleichbare rezidivprophylaktische Wirksamkeit [14, 16]. Eine differenzielle Betrachtung zeigt eine gering bessere Wirksamkeit für Lamotrigin in der Prophylaxe depressiver Episoden, für Lithiumsalze in der Verhütung der Manie [31].
Für die SGA hat Olanzapin den Nachweis geliefert, insbesondere manische Remanifestationen zu verhindern. Aber auch hinsichtlich der Verhütung depressiver Episoden zeigt es statistisch signifikante Wirksamkeit, wobei jedoch die Effektstärke weniger ausgeprägt ist [76, 78, 80].
Kombinationstherapien
Obwohl verschiedene Leitlinien in der Langzeittherapie bipolarer Störungen prinzipiell zunächst eine Monotherapie empfehlen, werden wegen des häufig unzureichenden Ansprechens bzw. fehlender Remission zunehmend Kombinationsbehandlungen durchgeführt [23, 60, 62, 72]. In der EMBLEM-Studie (European mania in bipolar longitudinal evaluation of medication; n=3461) hatten fast 40% der Patienten in der akuten Manie eine Kombinationsbehandlung erhalten [29]. Im Rahmen der Erhebungen aus dem bayerischen Pharmakovigilanzsystem AMÜP-AGATE wurde festgestellt, dass bipolare Patienten in stationärer Behandlung durchschnittlich drei Psychopharmaka erhalten. Einige Metaanalysen stützen diese klinische Einschätzung, wonach eine Augmentations- bzw. Kombinationsstrategie mit einem Antipsychotikum plus einem Mood-Stabilizer wirksamer ist als eine Behandlung mit einem Mood-Stabilizer allein [57, 69].
Fast die Hälfte der Befragten bevorzugen als Kombinationsstrategie in der Akutbehandlung des manischen Syndroms Olanzapin plus Valproinsäure oder einem Lithiumsalz. Dieser Auffassung kann zugestimmt werden, da in zwei RCT eine bessere Wirksamkeit der Kombinationstherapie im Vergleich zur Monotherapie nachgewiesen wurde [5, 77]. Auch gibt es positive Befunde zur Kombination von Lithiumsalzen mit Valproinsäure [73] oder Lithiumsalzen mit Carbamazepin. Die Kombination von Risperidon, Quetiapin oder einem anderen SGA mit einem Stimmungsstabilisierer wurde kaum in Betracht gezogen, obwohl auch hier positive Studienergebnisse zu Behandlung der bipolaren Manie vorliegen.
Als Kombinationsstrategie für die Akutbehandlung des depressiven Syndroms wurden von 40% bis 50% der Befragten Lithiumsalze in Kombination mit einem Antidepressivum (AD) favorisiert. Ein deutlich geringerer Teil bevorzugt ein SGA plus ein AD oder Valproinsäure plus ein AD. Einige internationale Leitlinien empfehlen hingegen, die Behandlung mit einem Antidepressivum generell mit einem Stimmungsstabilisierer zu kombinieren, um einem Umschlagen in die Manie vorzubeugen [30, 34]. Eine Kombination mit Lithiumsalz und Carbamazepin wird nicht als vielversprechend angesehen, obwohl diese Kombination in einer Post-hoc-Analyse im Vergleich zu einer Lithium- bzw. Carbamazepin-Monotherapie zu einer signifikanten Verringerung der Rehospitalisierungsquote führte, allerdings mit einer 2,5-fach erhöhten Nebenwirkungsrate einherging [4]. In einem randomisierten Vergleich einer Lithium- oder Carbamazepin-Monotherapie mit den Kombinationen Lithiumsalz/Carbamazepin und Lithiumsalz/Valproinsäure/Carbamazepin über die Dauer eines Jahres zeigte sich eine niedrige Ansprechrate von 35% für die Monotherapien. Unter der Kombination von Lithiumsalz und Carbamazepin stieg die Ansprechquote auf 55%. Von denjenigen, die immer noch keine hinreichende Besserung aufwiesen, konnten einige noch von einer Augmentation mit Valproinsäure profitieren [20].
Geschlechts- und Alterseinflüsse
Bei bipolaren Erkrankungen sind klinisch relevante Geschlechtsunterschiede bekannt. So haben weibliche Patienten ein höheres Risiko für depressive Episoden, affektive Mischzustände, dysphorische Hypomanien oder einen Rapid-Cycling-Verlauf. Weibliche Patienten im Alter zwischen 40 und 59 Jahre weisen in den ersten beiden Jahren einer Lithium-Therapie eine Prävalenz von 10,4% für Lithium-induzierte Hypothyreosen auf [41]. Bei der vorliegenden Befragung ergaben sich keine geschlechtsspezifischen Therapieunterschiede.
Für die Akutbehandlung älterer Patienten wird Valproinsäure dem Lithium vermutlich wegen des besseren Verträglichkeitsprofils eindeutig vorgezogen, was auch der Beobachtung in anderen Kliniken entspricht [64].
Unerwünschte Nebenwirkungen
Hämatologische und kardiologische Effekte der Medikamente werden von nahezu allen Befragten sowohl in der Akut- als auch in der Langzeitbehandlung als sehr wichtig oder wichtig angesehen. Das in der Behandlung mit Stimmungsstabilisierern und einigen SGA aktuell vielfach diskutierte Problem der Gewichtszunahme wird für die Akutbehandlung als untergeordnet und hinsichtlich der Langzeitbehandlung nur von 40 bis 50% der Teilnehmer als wichtig bis sehr wichtig erachtet. Hier kann festgestellt werden, dass in Studien das Risiko für eine signifikante Gewichtszunahme bei Kombination mit einem SGA (Olanzapin oder Quetiapin) höher war als unter einer Monotherapie [77]. Gastrointestinale, dermatologische, zentralnervöse und endokrine Nebenwirkungen werden für die Langzeitbehandlung als relevanter angesehen als für die Akutbehandlung. In der Akutbehandlung halten mehr als 40% ein wöchentliches EKG sowie ein monatliches EEG für erforderlich, wöchentliche Laborkontrollen sogar drei Viertel der Befragten.
Tabelle 4 gibt eine synoptische Gegenüberstellung der Leitlinien des Canadian Network for Mood and Anxiety Treatments (CANMAT) mit der Befragung der Bundesdirektorenkonferenz wieder.
Tab. 4. CANMAT-Guidelines Update 2007 [85a] und die Ergebnisse der BDK-Umfrage im Vergleich
|
Substanz |
Manie |
Depression |
Prophylaxe |
|||
|
CANMAT |
BDK |
CANMAT |
BDK |
CANMAT |
BDK |
|
|
Lithium |
# |
X |
# |
X |
# |
X |
|
Valproinsäure |
# |
X |
VAL+SSRI |
(X+AD) |
# |
X |
|
Lamotrigin |
– |
x |
# |
X |
# |
(x) |
|
Olanzapin |
# |
X |
OLA+SSRI |
(X) |
# |
(x) |
|
Quetiapin |
# |
(X) |
# |
(X) |
– |
(X) |
|
Carbamazepin |
– |
xx |
– |
xx |
– |
xx |
#=CANMAT-Empfehlung; –=keine Option bei CANMAT; X=bestätigt durch BDK-Befragte; (X)=selten oder nicht in allen Punkten bestätigt durch BDK-Befragte; xx=Vorschlag der BDK-Befragten
Literatur
(Das Literaturverzeichnis einschließlich der Titel der zitierten Artikel finden Sie im Internet unter www.ppt-online.de → Inhalt → Heft 4/2009.)
1. Altshuler LL, Gitlin MJ, Mintz J, Leight KL, et al. J Clin Psychiatry 2002;63:807–11.
2. Altshuler LL, Post RM, Leverich GS, Mikalauskas K, et al. Am J Psychiatry 1995;152:1130–8.
3. Attarbaschi T, Kasper S. Nervenarzt 2006;77:1310–22.
4. Baethge C, Baldessarini RJ, Mathiske-Schmidt K, Hennen J, et al. J Clin Psychiatry 2005;66:174–82.
5. Baker RW, Brown E, Akiskal HS, Calabrese JR, et al. Br J Psychiatry 2004;185:472–8.
6. Baldessarini RJ, Tohen M, Tondo L. Arch Gen Psychiatry 2000;57:490–2.
7. Belmaker RH. Engl J Med 2004;351:476–86.
8. Bennett J, Goldman WT, Suppes T. J Clin Psychopharmacol 1997;17:141–2.
9. Berk M, Ichim L, Brook S. Int Clin Psychopharmacol 1999;14:339–43.
10. Blanco C, Laje G, Olfson M, Marcus SC, et al. Am J Psychiatry 2002;159:1005–10.
11. Bottlender R, Rudolf D, Strauss A, Möller HJ. J Affect Disord 2001;63:79–83.
12. Bowden CL, Brugger AM, Swann AC, Calabrese JR, et al. JAMA 1994;271:918–24.
13. Bowden CL, Calabrese JR, McElroy SL, Gyulai L, et al. Arch Gen Psychiatry 2000;57: 481–9.
14. Bowden CL, Calabrese JR, Sachs G, Yatham LN, et al. Arch Gen Psychiatry 2003;60: 392–400.
15. Bowden CL, Grunze H, Mullen J, Brecher M, et al. J Clin Psychiatry 2005;66:111–21.
16. Calabrese JR, Bowden CL, Sachs G, Yatham LN, et al. J Clin Psychiatry 2003;64:1013–24.
17. Calabrese JR, Hirschfeld RM, Reed M, Davies MA, et al. J Clin Psychiatry 2003;64:425–32.
18. Chengappa KN, Suppes T, Berk M. Expert Rev Neurother 2004;4(Suppl 2):S17–25.
19. Dardennes R, Even C, Bange F, Heim A. Br J Psychiatry 1995;166:378–81.
20. Denicoff KD, Smith-Jackson EE, Bryan AL, Ali SO, et al. Am J Psychiatry 1997;154: 1456–8.
21. Dilsaver SC, Chen YW, Swann AC, Shoaib AM, et al. Am J Psychiatry 1994;151:1312–5.
22. Frye MA, Ketter TA, Kimbrell TA, Dunn RT, et al. J Clin Psychopharmacol 2000;20:607–14.
23. Frye MA, Ketter TA, Leverich GS, Huggins T, et al. J Clin Psychiatry 2000;61:9–15.
24. Geddes JR, Burgess S, Hawton K, Jamison K, et al. Am J Psychiatry 2004;161:217–22.
25. Goldberg JF, Garno JL, Harrow M. Curr Psychiatry Rep 2005;7:456–61.
26. Goldberg JF, Harrow M. J Affect Disord 2005;89:79–89.
27. Goodwin FK. J Clin Psychiatry 2002;63 (Suppl 10):5–12.
28. Goodwin FK, Jamison KR. Manic-Depressive Illness. New York: Oxford University Press, 1990.
29. Goodwin G, Vieta E. Eur Psychiatry 2005;20: 365–71.
30. Goodwin GM. J Psychopharmacol 2003;17: 149–73.
31. Goodwin GM, Bowden CL, Calabrese JR, Grunze H, et al. J Clin Psychiatry 2004;65:432–41.
32. Goodwin GM, Young AH. J Psychopharmacol 2003;17(Suppl 4):3–6.
33. Greil W, Kleindienst N, Erazo N, Müller-Oerlinghausen B. J Clin Psychopharmacol 1998;18:455–60.
34. Grunze H, Kasper S, Goodwin G, Bowden C, et al. World J Biol Psychiatry 2002;3:115–24.
35. Grunze H, Kasper S, Goodwin G, Bowden C, et al. World J Biol Psychiatry 2003;4:5–13.
36. Günther W, Noegel T, Trapp W, Frommberger U, et al. Psychopharmakotherapie 2008;15: 202–8.
37. Hirschfeld RM, Kasper S. Int J Neuropsychopharmacol 2004;7:507–22.
38. Hirschfeld RM, Keck PE Jr., Kramer M, Karcher K, et al. Am J Psychiatry 2004;161: 1057–65.
39. Hirschfeld RM, Keller MB, Panico S, Arons BS, et al. JAMA 1997;277:333–40.
40. Hirschfeld RM, Lewis L, Vornik LA. J Clin Psychiatry 2003;64:161–74.
41. Johnston AM, Eagles JM. Br J Psychiatry 1999;175:336–9.
42. Judd LL, Akiskal HS. Curr Psychiatry Rep 2003;5:417–8.
43. Kasper S, Stamenkovic M, Letmaier M, Schreinzer D. Int Clin Psychopharmacol 2002;17(Suppl 3):S1–10.
44. Khanna S, Vieta E, Lyons B, Grossman F, et al. Br J Psychiatry 2005;187:229–34.
45. Kusumakar V. J Clin Psychiatry 2002;63 (Suppl 10):23–8.
46. Laux G, Artmann S, Günther W, Trapp W, et al. Psychopharmakotherapie 2008;15: 265–71.
47. Lerer B, Moore N, Meyendorff E, Cho SR, et al. J Clin Psychiatry 1987;48:89–93.
48. Lusznat RM, Murphy DP, Nunn CM. Br J Psychiatry 1988;153:198–204.
49. MacQueen GM, Young LT, Joffe RT. Acta Psychiatr Scand 2001;103:163–70.
50. Macritchie K, Geddes JR, Scott J, Haslam D, et al. Cochrane Database Syst Rev 2003;(1):CD004052.
51. Marangell LB, Bauer MS, Dennehy EB, Wisniewski SR, et al. Bipolar Disord 2006;8: 566–75.
52. McElroy SL, Keck PE Jr. Biol Psychiatry 2000;48:539–57.
53. McIntyre RS, Brecher M, Paulsson B, Huizar K, et al. Eur Neuropsychopharmacol 2005;15:573–85.
54. Pande AC, Crockatt JG, Janney CA, Werth JL, et al. Bipolar Disord 2000;2:249–55.
55. Peet M. Br J Psychiatry 1994;164:549–50.
56. Perala J, Suvisaari J, Saarni SI, Kuoppasalmi K, et al. Arch Gen Psychiatry 2007;64: 19–28.
57. Perlis RH, Welge JA, Vornik LA, Hirschfeld RM, et al. J Clin Psychiatry 2006;67:509–16.
58. Perugi G, Toni C, Ruffolo G, Sartini S, et al. Pharmacopsychiatry 1999;32:136–41.
59. Post RM, Denicoff KD, Leverich GS, Altshuler LL, et al. J Clin Psychiatry 2003;64:680–90.
60. Post RM, Ketter TA, Pazzaglia PJ, Denicoff K, et al. Epilepsy Res Suppl 1996;11:153–80.
61. Prien RF, Caffey EM Jr., Klett CJ. Arch Gen Psychiatry 1972;26:146–53.
62. Rittmannsberger H, Meise U, Schauflinger K, Horvath E, et al. Eur Psychiatry 1999;14:33–40.
63. Sachs GS, Grossman F, Ghaemi SN, Okamoto A, et al. Am J Psychiatry 2002;159:1146–54.
64. Sanderson DR. Psychiatr Serv 1998;49:1145–7.
65. Segal J, Berk M, Brook S. Clin Neuropharmacol 1998;21:176–80.
66. Sernyak MJ, Woods SW. Psychopharmacol Bull 1993;29:375–81.
67. Shopsin B, Gershon S, Thompson H, Collins P. Arch Gen Psychiatry 1975;32:34–42.
68. Small JG, Klapper MH, Milstein V, Kellams JJ, et al. Arch Gen Psychiatry 1991;48:915–21.
69. Smith LA, Cornelius V, Warnock A, Tacchi MJ, et al. Acta Psychiatr Scand 2007;115:12–20.
70. Smulevich AB, Khanna S, Eerdekens M, Karcher K, et al. Eur Neuropsychopharmacol 2005;15:75–84.
71. Solomon DA, Keitner GI, Miller IW, Shea MT, et al. J Clin Psychiatry 1995;56:5–13.
72. Solomon DA, Keitner GI, Ryan CE, Miller IW. Psychopharmacol Bull 1996;32:579–87.
73. Solomon DA, Keitner GI, Ryan CE, Miller IW. J Clin Psychopharmacol 1998;18:38–49.
74. Steinberg R, Günther W, Laux G, Müller N, et al. Psychopharmakotherapie 2008;15:209–16.
75. Strakowski SM, Del Bello MP, Adler CM, Keck PE Jr. Expert Opin Pharmacother 2003;4:751–60.
76. Tohen M, Chengappa KN, Suppes T, Baker RW, et al. Br J Psychiatry 2004;184:337–45.
77. Tohen M, Chengappa KN, Suppes T, Zarate CA Jr., et al. Arch Gen Psychiatry 2002;59: 62–9.
78. Tohen M, Greil W, Calabrese JR, Sachs GS, et al. Am J Psychiatry 2005;162:1281–90.
79. Tohen M, Jacobs TG, Grundy SL, McElroy SL, et al. Arch Gen Psychiatry 2000;57:841–9.
80. Tohen M, Ketter TA, Zarate CA, Suppes T, et al. Am J Psychiatry 2003;160:1263–71.
81. Tohen M, Sanger TM, McElroy SL, Tollefson GD, et al. Am J Psychiatry 1999;156:702–9.
82. Trapp W, Günther W, Ziegelmayer C, Frommberger U, et al. Psychopharmakotherapie 2009;16:19–25.
83. Vasudev K, Goswami U, Kohli K. Psychopharmacology (Berl) 2000;150:15–23.
84. Weisler RH, Keck PE Jr., Swann AC, Cutler AJ, et al. J Clin Psychiatry 2005;66:323–30.
85. Wolfsperger M, Greil W, Rössler W, Grohmann R. J Affect Disord 2006;99:9–17.
85a.Yatham LN, Kennedy SH, O’Donovan C, Parikh SV, et al., for CANMAT guidelines group. Bipolar Disord 2006;8:721–39.
86. Zajecka JM, Weisler R, Sachs G, Swann AC, et al. J Clin Psychiatry 2002;63:1148–55.
87. Zarate CA Jr. Antipsychotic drug side effect issues in bipolar manic patients. J Clin Psychiatry 2000;61(Suppl 8):52–61.
88. Zornberg GL, Pope HG Jr. Treatment of depression in bipolar disorder: new directions for research. J Clin Psychopharmacol 1993;13:397–408.
Priv.-Doz. Dr. med. Thomas Messer, Bezirkskrankenhaus Augsburg, Dr.-Mack-Straße 1, 86156 Augsburg, E-Mail: thomas.messer@bkh-augsburg.de Dr. med. Kathrin Meyer zur Capellen, Prof. Dr. Max Schmauß, Bezirkskrankenhaus Augsburg, Dr.-Mack-Straße 1, 86156 Augsburg Dr. Wolfgang Trapp, Prof. Dr. Dr. Wilfried Günther, Klinik für Psychiatrie, Psychotherapie und Psychosomatik, St.-Getreu-Straße 14–18, 96049 Bamberg Prof. Dr. Gerd Laux, Inn-Salzach-Klinikum des Bezirks Oberbayern gGmbH, 83512 Wasserburg Prof. Dr. med. Reinhard Steinberg, Pfalzklinikum, Weinstraße 100, 76889 Klingenmünster Prof. Dr. Norbert Müller, Prof. Dr. Hans-Jürgen Möller, Psychiatrische Klink der Ludwig-Maximilians-Universität München, Nussbaumstraße 7, 80336 München Prof. Dr. Heinrich Schulze Mönking, St. Rochus Hospital, Am Rochus-Hospital 1, 48291 Telgte Prof. Dr. Karl-Ludwig Täschner, Psychiatrische Klinik Bürgerhospital, Tunzhofer Straße 14–16, 70191 Stuttgart Priv.-Doz. Dr. Ulrich Frommberger, MediClin Klinik an der Lindenhöhe, Klinik für Psychiatrie, Psychotherapie und Psychosomatik, Bertha-von-Suttner-Straße 1, 77654 Offenburg
Prescribing habits with regard to psychotropic drugs in German psychiatric hospitals – Part V: Mood stabilizers
Concerning prescription habits of psychopharmacologic drugs in German psychiatric hospitals no data exist so far. This article presents results of a survey that describes the medication concepts of n=235 physicians regarding mood stabilizers. A large acceptance of traditional substances like lithium or valproate could be confirmed as well as of atypical antipsychotics. With respect to relapse prevention combination strategies are frequently favoured. Significant differences resulted in the evaluation of unwanted side effects depending on acute treatment or long term treatment. Compared to present international guidelines, e.g. CANMAT, the survey indicates an amazingly large agreement of the interviewed doctors.
Keywords: Mood stabilizers, pharmacoepidemiology, prescription habits, guidelines
Psychopharmakotherapie 2009; 16(04)
