Siegfried Kasper, Wien, Markus Gastpar, Berlin, Walter E. Müller, Frankfurt, Hans-Peter Volz, Werneck, Angelika Dienel, Karlsruhe, und Hans-Jürgen Möller, München
Im Zusammenhang mit der Einnahme von Antidepressiva wird in klinischen Studien wie auch im Praxisalltag immer wieder über Gewichtsveränderungen berichtet [1, 5, 7, 10, 17, 19, 20]. Dabei werden Antidepressiva – insbesondere Trizyklika, und unter diesen wiederum besonders Amitriptylin und Imipramin – mit einer Zunahme des Körpergewichts in Verbindung gebracht. Eine Gewichtszunahme wurde auch unter Behandlung mit selektiven Serotonin-Wiederaufnahmehemmern (SSRI) – vor allem mit Paroxetin – beobachtet [1, 4, 5, 7, 10, 16].
Die Untersuchung des Zusammenhangs zwischen Patientengewicht und Antidepressiva-Einnahme wird dadurch erschwert, dass Gewichtsveränderungen auch als Begleiterscheinung der Erkrankung selbst zu sehen sind und auch dann bei der Mehrzahl der Patienten zu beobachten waren, wenn keine medikamentöse Behandlung erfolgte [17]. Dabei zeigten bis zu 75% der depressiven Patienten während einer akuten Episode eine Gewichtsabnahme [14], wohingegen bei bis zu 30% eine Gewichtszunahme beschrieben wurde [20]. Als ausschlaggebend für die Richtung der Gewichtsveränderung während der akuten Depression werden psychopathologische Faktoren angesehen [19]. Häufig können Gewichtszu- oder -abnahme unter Therapie auch als Veränderungen in Richtung auf den vor Beginn der depressiven Episode bestehenden Zustand verstanden werden.
Aus den publizierten Daten ergeben sich jedoch Hinweise auf einen klaren Zusammenhang zwischen Gewichtsveränderung und einer spezifischen antidepressiven Medikation. So konnte bei mit Imipramin und Amitriptylin behandelten Patienten eine vom Erfolg der Behandlung unabhängige Gewichtszunahme nachgewiesen werden [4, 10, 16], und unter Einnahme von Amitriptylin kam es im Gegensatz zu einer Plazebo-Kontrollgruppe während der Langzeit-Prophylaxe auch dann noch zu Gewichtszunahmen, als sich die Patienten bereits für längere Zeit in Remission befanden [5, 16].
Hypericumextrakt-Präparate gehören zu den im deutschen Sprachraum am häufigsten eingesetzten Medikamenten zur Akuttherapie und Langzeitbehandlung von Depressionen [15]. Ihre Beliebtheit basiert unter anderem auf ihrer guten Verträglichkeit [9]. Der Einfluss der Einnahme von Hypericumextrakt zur Behandlung von Depressionen auf das Körpergewicht wurde jedoch bisher noch nicht systematisch untersucht.
Methoden
Basierend auf den Originaldaten aus drei randomisierten Doppelblindstudien zum Vergleich der antidepressiven Wirksamkeit und Verträglichkeit des Johanniskrautextrakts WS® 5570 (Neuroplant®) mit denen von Plazebo und dem SSRI Paroxetin wurde die Veränderung des Körpergewichts der behandelten Patienten unter der Studienmedikation analysiert. Tabelle 1 zeigt die zentralen Charakteristika der Primärstudien.
Tab. 1. Charakteristika der analysierten Primärstudien
|
Studie |
I |
II |
III |
|
Publikation |
Lecrubier et al., 2002 [11] |
Szegedi et al., 2005 [18] |
Kasper et al., 2006 [8] |
|
Behandlung |
3-mal 300 mg/d WS® 5570 oder Plazebo, 6 Wochen |
Akutphase: 3-mal 300 mg/d WS® 5570 oder 1-mal 20 mg/d Paroxetin, 2 Wochen, gefolgt von 3-mal 300 bzw. 3-mal 600 mg/d WS® 5570 oder 1-mal 20 bzw. 1-mal 40 mg/d Paroxetin, 4 Wochen Erhaltungsphase: 3-mal 300 bzw. 3-mal 600 mg/d WS® 5570 oder 1-mal 20 bzw. 1-mal 40 mg/d Paroxetin, 26 Wochen |
Akutphase: 1-mal 600 oder 2-mal 600 mg/d WS® 5570 oder Plazebo, 6 Wochen Erhaltungsphase: 1-mal 600 oder 2-mal 600 mg/d WS® 5570 oder Plazebo, 26 Wochen |
|
Patientenzahl (Intention to treat) |
WS® 5570: 186 |
Akutphase: WS® 5570 900 mg/d: 53 WS® 5570 1800 mg/d: 69 Paroxetin: 122 WS® 5570 900 mg/d: 33 WS® 5570 1800 mg/d: 38 Paroxetin: 62 |
Akutphase: WS® 5570 600 mg/d: 124 WS® 5570 1200 mg/d: 119 Plazebo: 81 Erhaltungshase: WS® 5570 600 mg/d: 68 WS® 5570 1200 mg/d: 69 Plazebo: 24 |
|
Spezifische Auswahlkriterien |
Leichte oder mittelschwere „Major Depression“ (DSM-IV); |
Mittelschwere oder schwere „Major Depression“ (DSM-IV); |
Leichte oder mittelschwere „Major Depression“ (DSM-IV); |
Alle Primärstudien waren doppelblind und randomisiert. Die Schwere der Depression wurde primär mit der Hamilton-Depressionsskala (HAMD) [6] beurteilt. Patienten der Studien II und III, deren HAMD-Gesamtscore sich während der Akutphase um mindestens 50% des Ausgangswerts reduziert hatte, konnten danach bei gleicher Medikation optional in eine Erhaltungsphase übernommen werden. Die vorgesehene Behandlungsdauer betrug für Patienten, die nur an der Akutphase teilnahmen, sechs Wochen und für die Teilnehmer an der Erhaltungsphase insgesamt 32 Wochen. Bei den mittelschwer und schwer depressiven Patienten von Studie II war zwei Wochen nach Behandlungsbeginn bei nicht ausreichender Therapieantwort (HAMD-Verbesserung <20%) eine Dosisverdoppelung vorgesehen; in allen anderen Studien war die Hypericumextrakt-Dosis während der gesamten Beobachtungsperiode konstant.
Für die Reanalyse wurden die Daten aller Patienten der Intention-to-treat-Kollektive der Primärstudien mit gültigen Angaben zum Körpergewicht gepoolt und nach der applizierten WS® 5570-Tagesdosis getrennt ausgewertet (für Studie II wurde dabei die ab der dritten Woche der Akutphase verabreichte Dosis zugrunde gelegt). Ausgewertet wurde die intraindividuelle Veränderung des Körpergewichts zwischen Beginn und Ende der Akutphase (Behandlungswoche 1–6), zwischen Beginn und Ende der Erhaltungsphase (Behandlungswoche 7–32) sowie über beide Phasen hinweg. Für die mittleren Gewichtsveränderungen wurden paarweise deskriptive Behandlungsgruppenvergleiche mittels zweiseitigen t-Tests vorgenommen.
Ergebnisse
Tabelle 2 zeigt die Veränderungen im Körpergewicht nach Behandlung und Studienphase. Während der sechswöchigen Akutbehandlung waren in keiner der Medikationsgruppen systematische Gewichtsveränderungen in eine bestimmte Richtung zu beobachten; das 95%-Konfidenzintervall des arithmetischen Mittels schloss in allen Fällen den Wert „0“ ein. In Einzelfällen ergaben sich zwar Gewichtsveränderungen zwischen einer Abnahme um 22 kg und einer Zunahme um 10,5 kg. Die mittleren 50% der Patienten aller Behandlungsgruppen befanden sich jedoch am Ende der Akutphase in keinem Fall außerhalb eines Veränderungsbereichs von ±1 kg gegenüber dem Baseline-Wert, und im arithmetischen Mittel zeigte keine der Gruppen eine Abnahme um mehr als 0,2 kg oder eine Zunahme um mehr als 0,3 kg. Dementsprechend waren auch alle Unterschiede in der Gewichtsveränderung zwischen den verschiedenen Tagesdosen von WS® 5570 einerseits und Paroxetin und Plazebo andererseits nicht statistisch signifikant (Tab. 3).
Tab. 2. Gewichtsveränderung [kg] unter Behandlung mit WS® 5570, Paroxetin und Plazebo (Fallzahl, arithmetisches Mittel ± Standardabweichung [Wertebereich])
|
Akutphase |
Erhaltungsphase |
Gesamtzeitraum |
|
|
WS® 5570 600 mg |
n=112 0,1±1,8 (–5; +9) |
n=43 |
n=43 0,1±1,9 (–5; +5) |
|
WS® 5570 900 mg |
n=226 –0,1±2,2 (–22; +6) |
n=21 –0,5±2,1 (–5; +5) |
n=21 –1,5±5,3 (–22; +4) |
|
WS® 5570 1200 mg |
n=115 0,3±1,8 (–4; +7) |
n=43 |
n=43 –0,5±2,4 (–8; +5) |
|
WS® 5570 1800 mg |
n=67 –0,2±1,5 (–22; +9) |
n=22 0,2±1,5 (–4; +3) |
n=22 0,5±1,8 (–4; +3) |
|
WS® 5570 gesamt |
n=520 0,0±2,0 (–22; +9) |
n=129 –0,2±2,2 (–11; +9) |
n=129 –0,3±2,9 (–22; +5) |
|
Paroxetin |
n=114 –0,1±1,7 (–6; +8) |
n=41 1,5±2,9 (–4; +10) |
n=41 1,7±3,0 (–3; +8) |
|
Plazebo |
n=253 0,1±1,7 (–6; +10,5) |
n=19 –0,9±2,3 (–7; +2) |
n=19 –0,89±2,9 (–7; +4) |
Positive Werte bedeuten Gewichtszunahme
Auch während der Erhaltungsphase waren die mittleren Veränderungen des Körpergewichts bei den mit WS® 5570 behandelten Patienten klinisch unbedeutend. Dabei ergab sich im arithmetischen Mittel für die 900- und die 1200-mg-Tagesdosis eine geringe Gewichtsabnahme und für 600 sowie 1800 mg/d eine ebenso geringe Zunahme. Jeweils mindestens 75% der Patienten aller mit WS® 5570 behandelten Gruppen nahmen während der 26-monatigen Erhaltungsphase nicht mehr als 2 kg ab und nicht mehr als 1 kg zu. Die Paroxetin-Gruppe zeigte auch eine einzige statistisch bedeutsame Gewichtszunahme gegenüber dem Ende der Akutbehandlung (95%-Konfidenzintervall des arithmetischen Mittels: 0,6–2,4 kg). 9 der 38 mit Paroxetin behandelten Patienten (22%) nahmen während der Erhaltungsphase mindestens 2 kg zu, während es unter allen untersuchten Dosierungen von WS® 5570 und in der Plazebo-Gruppe jeweils weniger als 10% waren. Tabelle 3 zeigt, dass der Unterschied zwischen der Gewichtszunahme während der Erhaltungsphase unter Paroxetin und jeder der vier Dosierungen von WS® 5570 trotz der während dieser Studienphase vergleichsweise kleinen Fallzahlen auch statistisch signifikant war (jeweils p≤0,05). Dagegen fanden sich in keinem Fall signifikante Unterschiede in der Gewichtsveränderung zwischen WS® 5570 und Plazebo.
Abbildung 1 veranschaulicht die Verteilungs-Charakteristika zur Gewichtsveränderung zwischen dem Beginn der Akutbehandlung und dem Ende der Erhaltungsphase. Für den Gesamtzeitraum (ausgewertet wurden hier nur diejenigen Patienten, die über das Ende der Akutphase hinaus behandelt wurden) zeigten sich in keinem Fall relevante Unterschiede zwischen der Gewichtsveränderung unter einer der Dosierungen von WS® 5570 und Plazebo (Tab. 3). Für WS® 5570 1800 mg lag der Durchschnittsbereich der mittleren 50% der Stichprobenverteilung leicht über demjenigen der übrigen Hypericum-Dosierungen, jedoch befand sich der Wertebereich der mit 1800 mg/d behandelten Patientinnen und Patienten vollständig innerhalb der Wertebereiche aller übrigen Dosierungen sowie für Plazebo (Abb. 1). Dagegen war die Gewichtszunahme in der Paroxetin-Gruppe mit einem arithmetischen Mittel von 1,7 kg signifikant größer als für die WS® 5570-Tagesdosen von 600, 900 und 1200 mg.
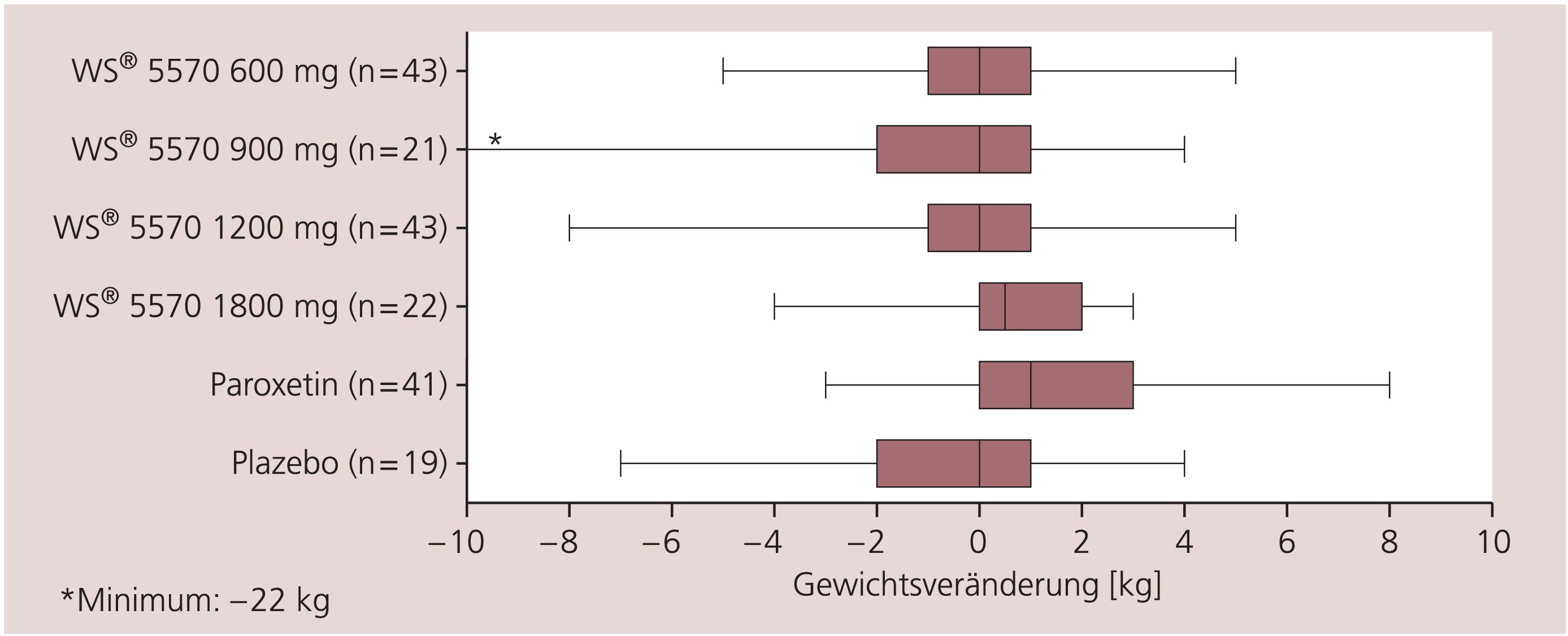
Abb. 1. Gewichtsveränderung zwischen Behandlungsbeginn und Ende der Erhaltungsphase (Median, Quartile, Minimum, Maximum)
Der Anteil der Patienten pro Behandlungsgruppe, deren Gewicht sich im Gesamtzeitraum um mehr als 2 kg veränderte, ist in Abbildung 2 dargestellt. In allen mit WS® 5570 behandelten Gruppen nahmen jeweils weniger als 10% der Patienten während des Beobachtungszeitraums um mehr als 2 kg zu; in der Paroxetin-Gruppe waren es dagegen 29,3% (12/41 Patienten). Gewichtsabnahmen um mehr als 2 kg wurden dagegen insbesondere unter WS® 5570 900 mg/d (5/21 Patienten, 23,8%), unter WS® 5570 1200 mg/d (6/43 Patienten, 14,0%) und in der Plazebo-Gruppe (4/19 Patienten, 21,1%) beobachtet.
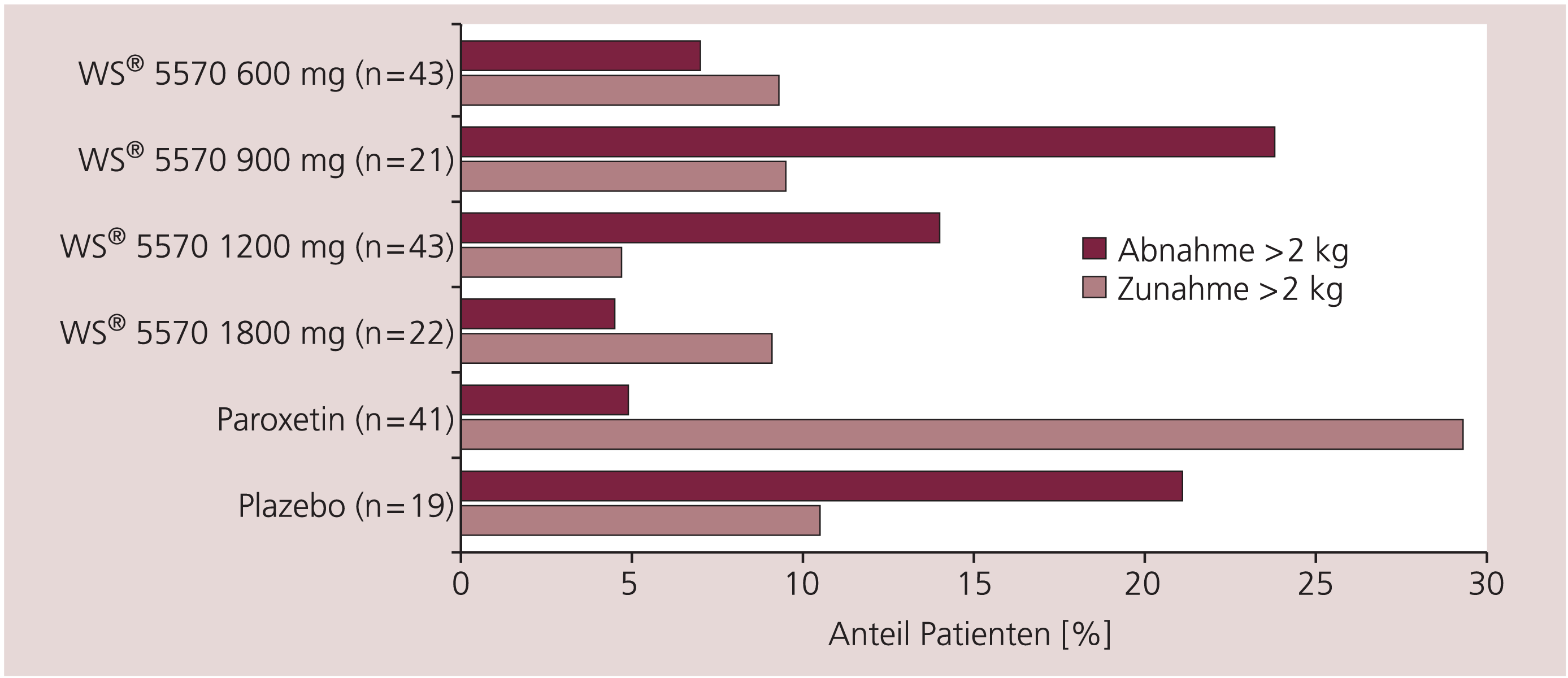
Abb. 2. Anteil von Patienten mit Gewichtsveränderung von mehr als 2 kg zwischen Behandlungsbeginn und dem Ende der Erhaltungsphase
Bei den mit WS® 5570 behandelten Personen zeigte sich keine monotone Beziehung zwischen Tagesdosis und Gewichtsveränderung. In den Gruppen mit Tagesdosen von 600 und 1800 mg lagen alle beobachteten Veränderungen innerhalb eines Bereichs von ±7% des Gewichts vor Beginn der Behandlung, unter 900 mg/d WS® 5570 wurden bei 3/21 Patienten (14,3%) und unter 1200 mg/d bei 3/43 Patienten (7,0% – bei beiden Dosierungen jeweils 2-mal Abnahme und 1-mal Zunahme) Veränderungen um mindestens 7% des Anfangsgewichts beobachtet. Für die Kontrollgruppen lagen die entsprechenden Anteile bei 14,6% (Paroxetin; 6/41 Patienten mit Gewichtszunahme > 7%) bzw. bei 15,8% (Plazebo; 3/19 Patienten – 2-mal Abnahme, 1-mal Zunahme).
Gewichtsverluste infolge von Appetitlosigkeit werden bei depressiven Patienten häufiger beobachtet. Die Daten der Metaanalyse zeigen hier jedoch keinen systematischen Zusammenhang zwischen (unzureichendem) Therapieeffekt und Gewichtsabnahme: Die Pearson-Korrelationen zwischen der HAMD-Gesamtwert-Veränderung unter Behandlung und der Gewichtsveränderung waren in allen Behandlungsgruppen statistisch unbedeutend und lagen mit einer Ausnahme sowohl für die Akutphase als auch für den gesamten Beobachtungszeitraum im Bereich zwischen rmin = –0,16 und rmax = 0,14; lediglich in der Paroxetin-Gruppe wurde während der Akutphase eine Korrelation von r = –0,26 (p<0,01) beobachtet, das heißt, die Patienten nahmen tendenziell um so mehr zu, je deutlicher der Rückgang der depressiven Symptomatik war.
Die im Verlauf der Behandlung beobachteten Gewichtsveränderungen waren auch nicht durch Regressionseffekte zur Mitte hin zu erklären: Für untergewichtige Patientinnen und Patienten mit initialem Body-Mass-Index <20 kg/m2 wurden während der Akutphase bei mittleren Differenzen von 0,2±0,8 kg für WS® 5570 600 mg/d (n=6), 0,4±0,8 kg für WS® 5570 900 mg/d (n=23), 0,4±1,2 kg für WS® 5570 1200 mg/d (n=8), –0,5±0,7 kg für WS® 5570 1800 mg/d (n=2), 0,2±1,3 kg für Paroxetin (n=5) und 0,3±1,5 kg für Plazebo (n=32) nur marginal größere Gewichtszunahmen beobachtet als in der Gesamtstichprobe aller Patienten der gleichen Behandlungsgruppen (vgl. Tab. 2). Im Verlauf der Erhaltungsphase veränderte sich das Gewicht von keiner der unter Beobachtung verbliebenen Personen mit initialem Body-Mass-Index <20 kg/m2 um mehr als 2 kg (Gruppen-Kennwerte wurden wegen der geringen Fallzahlen von n=5 für alle Dosierungen von WS® 5570, sowie jeweils n=1 für Paroxetin und Plazebo nicht berechnet).
Diskussion
Gewichtszunahme ist eine häufige Ursache für mangelnde Einnahme-Compliance [12]. Das ist besonders auch dann relevant, wenn Antidepressiva im Zustand der Remission zur Verhinderung des Wiederauflebens einer abgeklungenen Episode oder zur Prophylaxe über einen längeren Zeitraum eingenommen werden müssen. Die Ergebnisse unserer Analysen zeigen, dass eine medikamenteninduzierte Gewichtszunahme bei Einnahme von Hypericumextrakt WS® 5570 weder während der Akutbehandlung noch im Rahmen einer anschließenden prophylaktischen Erhaltungstherapie aufgetreten ist. Die untersuchten Tagesdosen zwischen 600 und 1800 mg decken dabei den gesamten therapeutischen Bereich ab. Dass WS® 5570 das Gewicht der Patienten nicht systematisch beeinflusst, zeigt sich auch darin, dass es mit steigender WS® 5570-Tagesdosis weder zu vermehrten Zu- noch zu häufigeren Abnahmen im Patientengewicht kam: Während sich über den gesamten Beobachtungszeitraum hinweg bei den beiden „mittleren“ Dosierungen (900 und 1200 mg/d) im Durchschnitt eine geringe Gewichtsabnahme zeigte, wurde für die niedrigste und die höchste Tagesdosis (600 und 1800 mg) eine ebenso geringe Zunahme beobachtet. Insgesamt lagen die beobachteten Gewichtsveränderungen aber – trotz einer beachtlichen interindividuellen Schwankungsbreite von einer Abnahme um 22 kg bis hin zu einer Zunahme um 5 kg –, ebenso wie diejenigen unter Plazebo beim Gros der Patienten im gesamten Untersuchungszeitraum in einem Bereich, der auch bei unbehandelten, nicht depressiven Personen als klinisch unauffällig gilt und für die Tagesdosen von 600 und 1800 mg WS® 5570 wurden überhaupt keine Veränderungen in einer klinisch relevanten Größenordnung von mehr als 7% des Ausgangsgewichts beobachtet [2]. Selbst bei der höchsten Dosis von WS® 5570 (1800 mg/d) kam es über den gesamten Beobachtungszeitraum hinweg zu einer maximalen Gewichtszunahme von 3 kg (während andere Patienten unter dieser Dosierung im selben Zeitraum bis zu 4 kg abnahmen); dagegen wurden unter Paroxetin Zunahmen um bis zu 8 kg beobachtet. Dass sich diese beiden Gruppen dennoch nicht statistisch signifikant voneinander unterschieden (p=0,13 zugunsten von WS® 5570; vgl. Tab. 3), ist primär durch die wegen der geringen Fallzahlen nicht ausreichende Teststärke erklärbar (ein teststatistischer Vergleich bezüglich Gewichtsveränderung war in den in die Analyse aufgenommenen Primärstudien ja auch nicht geplant).
Tab. 3. Gewichtsveränderung – Behandlungsgruppenvergleiche, WS® 5570 versus Paroxetin und Plazebo, nach Behandlungsphase (zweiseitige t-Tests; Fallzahlen s. Tab. 2)
|
WS®-5570-Gruppe |
Vergleichsgruppe |
p-Wert |
|
Akutphase (Woche 1–6) |
||
|
WS® 5570 600 mg |
Paroxetin |
0,48 |
|
Plazebo |
0,86 |
|
|
WS® 5570 900 mg |
Paroxetin |
0,86 |
|
Plazebo |
0,30 |
|
|
WS® 5570 1200 mg |
Paroxetin |
0,12 |
|
Plazebo |
0,25 |
|
|
WS® 5570 1800 mg |
Paroxetin |
0,79 |
|
Plazebo |
0,40 |
|
|
Erhaltungsphase (Woche 7–32) |
||
|
WS® 5570 600 mg |
Paroxetin |
0,02 |
|
Plazebo |
0,08 |
|
|
WS® 5570 900 mg |
Paroxetin |
<0,01 |
|
Plazebo |
0,58 |
|
|
WS® 5570 1200 mg |
Paroxetin |
<0,01 |
|
Plazebo |
0,13 |
|
|
WS® 5570 1800 mg |
Paroxetin |
0,05 |
|
Plazebo |
0,13 |
|
|
Gesamtzeitraum (Woche 1–32) |
||
|
WS® 5570 600 mg |
Paroxetin |
0,02 |
|
Plazebo |
0,21 |
|
|
WS® 5570 900 mg |
Paroxetin |
<0,01 |
|
Plazebo |
0,49 |
|
|
WS® 5570 1200 mg |
Paroxetin |
<0,01 |
|
Plazebo |
0,65 |
|
|
WS® 5570 1800 mg |
Paroxetin |
0,13 |
|
Plazebo |
0,13 |
|
Die unter Paroxetin beobachtete Gewichtszunahme während der Erhaltungsphase deckt sich mit den Befunden anderer Arbeitsgruppen, die bei 25,5% [3] bzw. bei 14,3% [13] der Patienten nach einem halben Jahr eine Gewichtserhöhung von mindestens 7% gefunden hatten (in unserer Analyse nahmen 29,3% der Patienten unter Paroxetin mehr als 2 kg zu; 14,6% zeigten eine Gewichtszunahme um mindestens 7% des Ausgangsgewichts). Das Ergebnis belegt gleichzeitig die Sensitivität unserer Untersuchung, therapieinduzierte Gewichtsveränderungen von spontanen zu unterscheiden, und ist damit ein weiteres Indiz für das Hauptergebnis, dass sich aus den analysierten Daten keine Anhaltspunkte für eine systematische Gewichtszunahme unter Behandlung mit WS® 5570 ergeben.
Die Reanalyse von Daten aus drei kontrollierten Doppelblindstudien zeigt somit, dass der Johanniskrautextrakt WS® 5570 während der Akutbehandlung depressiver Episoden und der sich daran anschließenden, prophylaktischen Erhaltungstherapie nicht zu systematischen Gewichtsveränderungen führt. Er bietet damit günstige Voraussetzungen für eine gute Einnahme-Compliance auch bei längerfristiger Anwendung.
Literatur
1. Benazzi F. Weight gain in depression remitted with antidepressants: pharmacological or recovery effect? Psychother Psychosom 1998;67:271–4.
2. Deshmukh R, Franco K. Managing weight gain as a side effect of antidepressant therapy. Cleve Clin J Med 2003;70:614–23.
3. Fava M, Judge R, Hoog SL, Nilsson ME, et al. Fluoxetine versus sertraline and paroxetine in major depressive disorder: changes in weight with long-term treatment. J Clin Psychiatry 2000;61:863–7.
4. Fernstrom MH, Krowinski RL, Kupfer DJ. Chronic imipramine treatment and weight gain. Psychiatry Res 1986;17:269–73.
5. Gottfries CG. Influence of depression and antidepressants on weight. Acta Psychiatr Scand Suppl 1981;290:353–6.
6. Hamilton M. Development of a rating scale for primary depressive illness. Br J Soc Clin Psychol 1967;6:278–96.
7. Harris B, Young J, Hughes B. Changes occurring in appetite and weight during short-term antidepressant treatment. Br J Psychiatry 1984;145:645–8.
8. Kasper S, Anghelescu I, Szegedi A, Dienel A, et al. Superior efficacy of St John’s wort extract WS® 5570 compared to placebo in patients with major depression: a randomized, double-blind, placebo-controlled, multi-center trial. BMC Med 2006;4:14 doi10.1186/1741-7015-4-14.
9. Knüppel L, Linde K. Adverse effects of St. John’s wort: a systematic review. J Clin Psychiatry 2004;65:1470–9.
10. Kupfer DJ, Coble PA, Rubinstein D. Changes in weight during treatment for depression. Psychosom Med 1979;41:535–44.
11. Lecrubier Y, Clerc G, Didi R, Kieser M. Efficacy of St. John’s wort extract WS 5570 in major depression: a double-blind, placebo-controlled trial. Am J Psychiatry 2002;159:1361–6.
12. Levitt AJ, Joffe RT, Esche I, Sherret D. The effect of desipramine on body weight in depression. J Clin Psychiatry 1987;48:27–8.
13. Maina G, Albert U, Salvi V, Bogetto F. Weight gain during long-term treatment of obsessive-compulsive disorder: a prospective comparison between serotonin reuptake inhibitors. J Clin Psychiatry 2004;65:1365–71.
14. Mezzich JE, Raab ES. Depressive symptomatology across the Americas. Arch Gen Psychiatry 1980;37:818–23.
15. Müller WE, Kasper S. Editorial Hypericum extract (LI 160) as a herbal antidepressant. Pharmacopsychiatry 1997;30:71.
16. Paykel ES. The classification of depression. Br J Clin Pharmacol 1983;15(Suppl 2):155S–9S.
17. Stunkard AJ, Fernstrom MH, Price A, Frank E, et al. Direction of weight change in recurrent depression. Consistency across episodes. Arch Gen Psychiatry 1990;47:857–60.
18. Szegedi A, Kohnen R, Dienel A, Kieser M. Acute treatment of moderate to severe depression with hypericum extract WS 5570 (St John’s wort): randomised controlled double blind non-inferiority trial versus paroxetine. Br Med J 2005;330:503–6.
19. Weissenburger J, Rush AJ, Giles DE, Stunkard AJ. Weight change in depression. Psychiatr Res 1986;17:275–83.
20. Wurtman JJ. Depression and weight gain: the serotonin connection. J Affect Disord 1993;29:183–92.
O. Univ. Prof. Dr. Dr. h. c. Siegfried Kasper, Universitätsklinik für Psychiatrie und Psychotherapie, Medizinische Universität Wien/AKH, Währinger Gürtel 18–20, 1090 Wien, Österreich, E-Mail: sci-genpsy@meduniwien.ac.at
Prof. Dr. Markus Gastpar, Fliedner-Klinik, Charlottenstr. 65, 10117 Berlin
Prof. Dr. Walter E. Müller, Pharmakologisches Institut für Naturwissenschaftler, Johann Wolfgang Goethe-Universität Frankfurt, Biozentrum, Max-von-Laue-Str. 9, 60438 Frankfurt a. M.
Prof. Dr. Hans-Peter Volz, Krankenhaus für Psychiatrie, Psychotherapie und psychosomatische Medizin Schloss Werneck, Balthasar-Neumann-Platz 1, 97440
Werneck Angelika Dienel, Dr. Willmar Schwabe GmbH & Co. KG, Willmar-Schwabe-Str. 4, 76227 Karlsruhe
Prof. Dr. Hans-Jürgen Möller, Klinik für Psychiatrie und Psychotherapie, Ludwig-Maximilians-Universität München, Nussbaumstraße 7, 80336 München
Treatment of depression with St. John’s wort extract WS® 5570. No influence on patients’ weight
Drug treatment of depression is frequently associated with weight increase. Such effects have been demonstrated for tricyclics, selective serotonin reuptake inhibitors and other antidepressants. Weight increase has been identified as a major cause of malcompliance which may jeopardize treatment success.
In three randomized double-blind trials 900 patients with mild, moderate or severe major depression were treated with 600, 900, 1,200, or 1,800 mg/day St. John’s wort extract WS® 5570, 20 or 40 mg/day paroxetine, or placebo for six weeks. Responders to acute treatment were offered participation in a 26-week continuation phase with the same treatments. In a reanalysis of the pooled original data we investigated weight changes during antidepressant treatment.
Neither patients treated with WS® 5570 nor those randomized to placebo showed systematic weight changes during the 32-week period of observation. Marked weight gain or loss were observed only in individual cases. For both drugs average weight change during acute and continuation treatment did not exceed a range of ±1 kg compared to baseline. During the 26-week continuation treatment patients randomized to paroxetine showed an average weight increase of 1.5 kg that was significantly different compared to all dosages of WS® 5570 investigated (p≤0.05).
During acute and subsequent continuation treatment of depressive episodes St. John’s wort extract WS® 5570 does not cause weight changes. The herbal drug thus provides a favorable basis for good treatment compliance.
Keywords: St. John’s wort, WS® 5570, Hypericum, depression, weight gain
Psychopharmakotherapie 2008; 15(01)
