Karin Zeller, Darmstadt, und Markus Gastpar, Berlin
Depressionen zählen mit einer Lebenszeitprävalenz von 4,4 bis 18% neben den Angststörungen zu den häufigsten psychischen Erkrankungen in der Allgemeinarztpraxis [13]. Leider bleiben bis zu der Hälfte dieser Patienten unbehandelt, weil das Krankheitsbild wegen besonderer Diagnose-Schwierigkeiten im Einzelfall oft unerkannt bleibt. Zudem sind Allgemeinärzte mit der Verschreibung antidepressiv wirkender Medikamente zurückhaltend, und auch auf Seiten der Patienten bestehen nicht selten Vorbehalte, beispielsweise gegenüber einer ausreichend dosierten Pharmakotherapie, die eine suffiziente Behandlung aufgrund nicht tolerierter Nebenwirkungen erschweren [7, 10]. Eine Alternative zu den klassischen, chemisch definierten Antidepressiva stellt der pflanzliche Extrakt aus Johanniskraut (Hypericum perforatum) dar. Die Wirkung von Hypericumextrakt wurde in den letzten 15 Jahren in zahlreichen Studien untersucht. Die Ergebnisse sind in einem Cochrane-Review zusammengefasst worden [11]. Diese Metaanalyse kommt zu der Schlussfolgerung, dass zwar der Hypericumextrakt in seiner Wirkung mit chemisch definierten Antidepressiva vergleichbar ist, jedoch teilweise nur eine geringe Überlegenheit zu Plazebo zeigte. Alle ausgewerteten Studien wurden mit Hypericumextrakten durchgeführt, die mehrfach täglich eingenommen werden mussten. Plazebo-kontrollierte Studien zur Einmalgabe von Hypericumextrakt fehlen bisher, obwohl gerade bei der langfristigen Therapie depressiver Patienten die Einmalgabe die Compliance, und damit die Genesung fördert [3, 4]. Die überwiegende Mehrheit der Johanniskraut-Studien wurde bei leichten bis mittelschweren Depressionen, also der weniger schwerwiegenden Erkrankung, durchgeführt und in nur etwa 10% wurden ausschließlich mittelschwer depressive Patienten eingeschlossen. Die vorliegende dreiarmige Studie sollte diese Datenlücke schließen. Sie hatte zum Ziel, die Überlegenheit der täglichen Einmalgabe von Hypericumextrakt über Plazebo eindeutig darzustellen und gleichzeitig zu zeigen, dass dieser Extrakt mit einem chemisch definierten Standardantidepressivum in seiner Wirkung vergleichbar ist. Durch den mitgeführten Plazebo-Arm kann außerdem die Validität der Studiendurchführung gezeigt werden. Als Prüfpräparat wurde der Hypericumextrakt STW3-VI (Laif® 900) und als Vergleichspräparat die Leitsubstanz Citalopram, ein besonders wirksamer und nebenwirkungsarmer selektiver Serotonin-Wiederaufnahmehemmer (SSRI) [12], gewählt.
Patienten und Methoden
Diese doppelblinde, randomisierte, multizentrische Plazebo- und Verum-kontrollierte Phase-III–Studie wurde nach den Grundsätzen für Standards der guten klinischen Praxis (GCP) bei der Durchführung von Studien mit Arzneimitteln am Menschen in der EU, den ICH-Guidelines und den Prinzipien der Deklaration von Helsinki durchgeführt. Die erforderlichen Unterlagen wurden zuvor einer unabhängigen Ethik-Kommission vorgelegt und von dieser positiv bewertet. Zwischen Oktober 2002 und Mai 2003 wurden die Patienten in Praxen von Allgemeinmedizinern und hausärztlich tätigen Internisten rekrutiert. Die Ärzte waren in der Anwendung der Diagnosekriterien und Fremdbeurteilungsskalen erfahren und nahmen zusätzlich vor Studienbeginn an einem Ratertraining teil.
Weibliche und männliche ambulante Patienten mit mittelschwerer Depression (ICD-10 F32.1, F33.1) wurden in die Studie aufgenommen. Die Patienten wurden randomisiert den drei Behandlungsgruppen zugeteilt. Sie erhielten jeweils einmal täglich entweder 900 mg Johanniskrautextrakt STW3-VI oder 20 mg Citalopram oder Plazebo.
Die individuelle Studiendauer betrug sechs Wochen. In dieser Zeit wurde der Verlauf der Depression an Hand der Hamilton-Depressionsskala (HAMD), der Befindlichkeitsskala nach von Zerssen (Bf-S) und der Clinical-Global-Impression(CGI)-Skala dokumentiert. Die Daten der Wirksamkeit und Verträglichkeit wurden an Tag 0, 7, 14, 21 und 42 erhoben.
Zielkriterien der Wirksamkeit und Sicherheit
Als Hauptzielkriterium sollte erstens gezeigt werden, dass Hypericumextrakt STW3-VI nach sechs Wochen Behandlung dem chemischen Antidepressivum Citalopram therapeutisch gleichwertig ist und zweitens gegenüber der Plazebo-Behandlung überlegen ist. Als sekundäre Zielkriterien wurden die Wirksamkeitsskalen BfS und CGI ausgewertet, des Weiteren die Verträglichkeit anhand der CGI-Skala, einer Beurteilung der Prüfärzte und des Auftretens von unerwünschten Ereignissen und abnormen Laborwerten.
Weiterhin wurde der Therapieerfolg auf Basis der Responderbetrachtung evaluiert. Dabei galt eine Besserung des HAMD-Scores von mindestens 50% gegenüber dem Ausgangswert beziehungsweise ein Score von unter 10 Punkten als Erfolg.
Statistische Methoden
Aufgrund der zwei primären Zielkriterien wurde die Irrtumswahrscheinlichkeit α auf α/2 adjustiert (Bonferroni).
Unter Beachtung der Zielsetzung der klinischen Prüfung wurde die Hypothese der therapeutischen „non-inferiority“ von Hypericum gegenüber Citalopram einseitig konfirmatorisch geprüft. Dieses Testproblem wurde auf der Grundlage des PP(Per-Protokoll)-Kollektivs mit einem α/2-Niveau von 0,0125 betrachtet.
Zweitens wurde die Überlegenheit von STW3-VI gegenüber Plazebo auf der Basis der ITT(Intention-to-treat)-Population untersucht. Hier wurde ein zweiseitiger Test mit einem α von 0,025 angewendet.
Um die Validität der Studienergebnisse zu überprüfen, wurde zusätzlich die Überlegenheit der Referenzsubstanz Citalopram gegenüber Plazebo in der ITT-Population getestet. Dieser Test wurde zweiseitig mit einem α/2-Niveau von 0,025 durchgeführt.
Für die sekundären Wirksamkeitsparameter wurde die Hypothese der Überlegenheit eines der beiden Prüfparameter betrachtet. Die Analysen wurden in einem zweiseitigen Test auf der Basis der ITT-Population durchgeführt (α=5%). Generell wurde im Falle fehlender Daten der LOCF-Zugang (Last observation carried forward) gewählt.
Ergebnisse
388 Patienten im Alter von 18 bis 74 Jahren mit einer ambulant behandlungsbedürftigen mittelschweren Depression wurden in die Studie und in das ITT-Kollektiv aufgenommen. Unter Berücksichtigung verschiedener Prüfplanverstöße konnten 312 Patienten in das PP-Kollektiv aufgenommen werden. Von den 388 (312) Patienten im ITT(PP)-Kollektiv erhielten 131 (103) Patienten Hypericumextrakt STW3-VI, 127 (104) Patienten Citalopram und 130 (105) Patienten Plazebo. Wenn nicht anders vermerkt, beziehen sich alle Daten und Abbildungen auf das ITT-Kollektiv.
Patientencharakteristika
Die demographischen Daten der einzelnen Behandlungsgruppen waren vergleichbar. Das Durchschnittsalter lag bei 50 Jahren und etwa zwei Drittel der in die Studie aufgenommenen Patienten waren Frauen. Die Erstdiagnose der Depression wurde im Mittel drei Jahre vor Studienbeginn gestellt und 29,4% der Patienten waren mit Depressionen familiär vorbelastet (Tab. 1).
Tab. 1. Demographische und klinische Daten zu Studienbeginn (ITT-Population). Die Behandlungsgruppen unterschieden sich nicht signifikant.
|
Basisdaten |
STW3-VI |
Citalopram |
Plazebo |
|
Geschlecht [n] |
|||
|
–Männlich |
45 (34,4%) |
45 (35,4%) |
35 (26,9%) |
|
–Weiblich |
86 (65,6%) |
82 (64,6%) |
95 (73,1%) |
|
Alter [Jahre] |
50,8±12,1 |
49,3±10,7 |
49,4±12,7 |
|
Familiäre Vorbelastung |
33,6% |
27,6% |
26,9% |
|
HAMD-Skala [Punkte] |
21,9±1,2 |
21,8±1,2 |
22,0±1,2 |
|
BfS-Skala [Punkte] |
35,9±9,7 |
34,8±11,6 |
33,8±11,8 |
|
CGI-Schweregrad mäßig, deutlich oder schwer krank |
87,7% |
92,9% |
92,3% |
Wirksamkeit – Hamilton-Depressionsskala (HAMD)
Die Verbesserung des HAMD-Scores war in beiden Behandlungsgruppen nahezu identisch. In der Hypericum-Gruppe zeigte sich eine Abnahme um 11,6 Punkte von 21,9±1,2 Punkten zu Therapiebeginn auf 10,3±6,4 Punkte am Studienende. In der Citalopram-Gruppe reduzierten sich die Werte um 11,5 Punkte von 21,8±1,2 Punkten auf 10,3±6,4 Punkte nach sechs Wochen Behandlung. Die Werte der Plazebo-Gruppe verringerten sich während der Behandlungszeit um 9 Punkte von 22,0±1,2 auf 13,0±6,9 Punkte (Abb. 1). Hypericumextrakt STW3-VI war in seiner Wirksamkeit mindestens gleichwertig zu Citalopram (p<0,0001, PP).
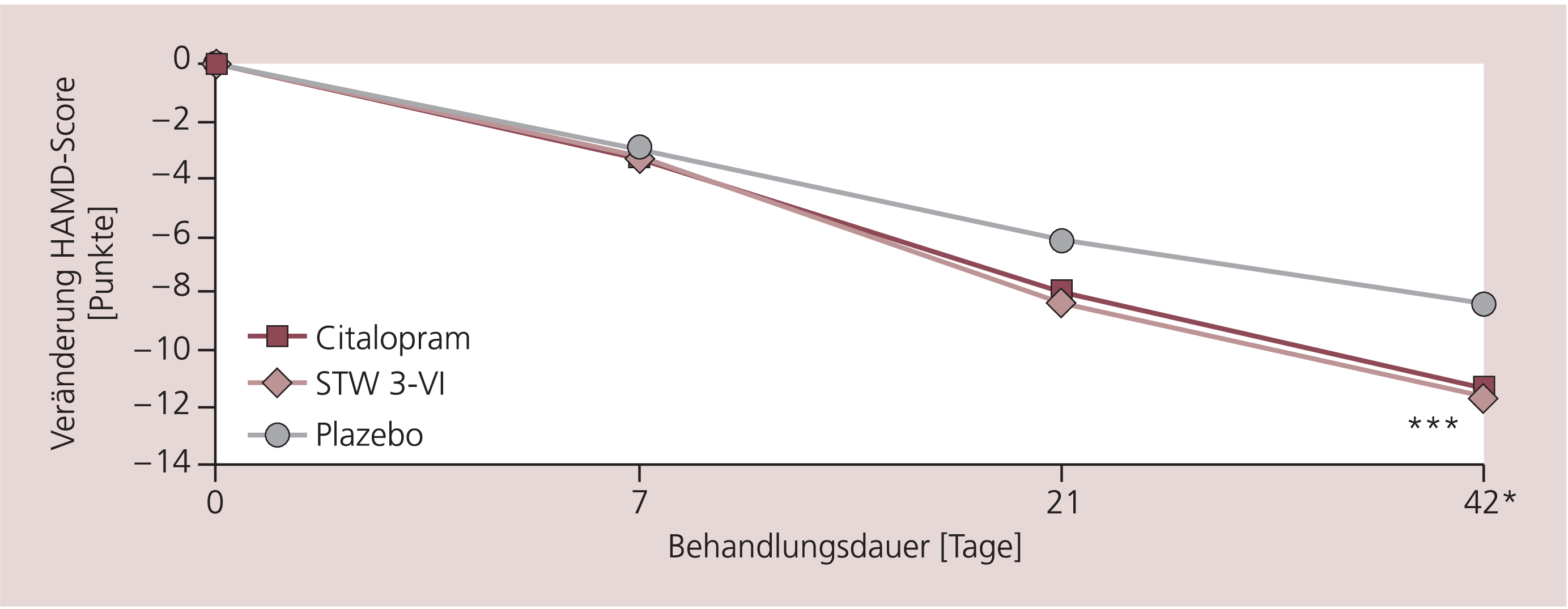
Abb. 1. Abnahme des Hamilton-Depression-Scores während des Studienverlaufs (*** p<0,0001)
Anschließend wurde die Überlegenheit von Hypericumextrakt gegenüber Plazebo getestet (ITT). Hypericum war Plazebo hochsignifikant überlegen (p<0,0001).
Die Citalopram-Gruppe war der Plazebo-Gruppe ebenfalls hochsignifikant überlegen (p<0,0001, ITT), das bedeutet, dass die dargestellten Studienergebnisse valide sind.
Sekundäre Wirksamkeitsparameter
Der Behandlungserfolg (Therapieresponse) war als eine Besserung der HAMD-Skala um 50% beziehungsweise Erreichen eines Punktwerts unter 10 definiert.
Nach Ende der sechswöchigen Therapie waren in der Hypericum-Gruppe 54,2% und in der Citalopram-Gruppe 55,9% Responder. In der Plazebo-Gruppe sprachen nur 39,2% der Patienten auf die Therapie an.
Die paarweisen Vergleiche zeigten für den Hypericumextrakt STW3-VI und Citalopram eine hochsignifikante Überlegenheit gegenüber Plazebo, die beiden Verum-Gruppen unterschieden sich jedoch nicht signifikant. Im Behandlungsverlauf zeigte sich in beiden Verum-Gruppen eine Verbesserung der Responderraten (Abb. 2).
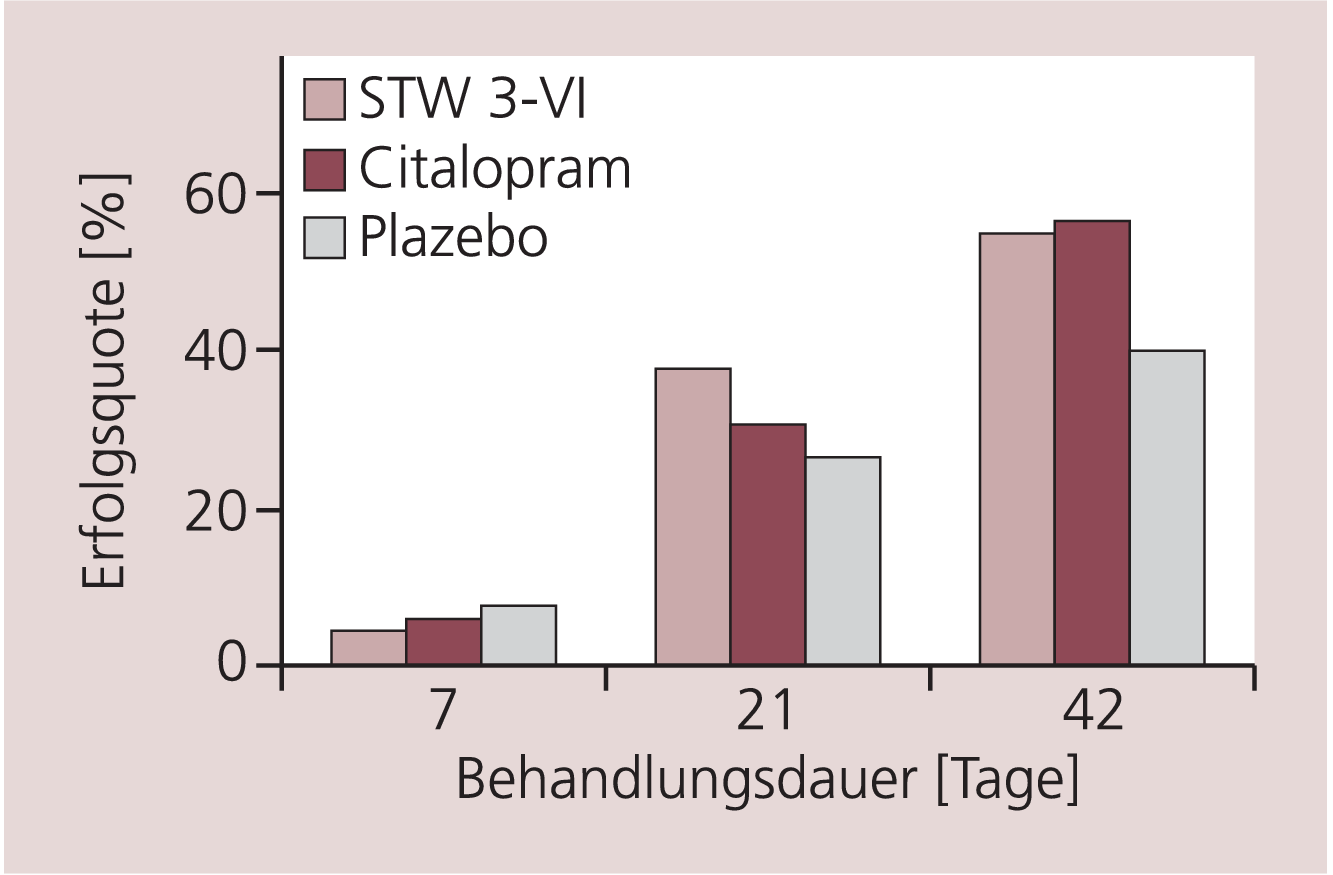
Abb. 2. Responderraten nach 6 Wochen Behandlung (mindestens 50% Reduktion des HAMD-Scores bzw. HAMD-Score unter 10 Punkten) (p<0,01 für beide Verum-Gruppen vs. Plazebo an Tag 42)
Die Ergebnisse der von den Patienten selbstständig ausgefüllten Befindlichkeitsskalen sowie der von den Ärzten beurteilten CGI-Skalen und die Wirksamkeitseinschätzung stimmen mit den dargestellten Daten überein.
Sicherheit und Verträglichkeit
Bei 39 Patienten der Hypericumextrakt-Gruppe wurden insgesamt 58 unerwünschte Ereignisse (UE), bei 53 Patienten der Citalopram-Gruppe 94 UE und bei 46 Patienten der Plazebo-Gruppe 70 UE dokumentiert.
Bei bestimmungsgemäßem Gebrauch von Johanniskrautpräparaten sind Nebenwirkungen selten (<0,1%). Photosensibilisierung insbesondere bei hellhäutigen Patienten sowie allergische Hautausschläge, Magen-Darm-Beschwerden, Müdigkeit oder Unruhe können auftreten. Bei Citalopram sind vor allem verstärkte Schweißneigung, Kopfschmerzen, Tremor, Somnolenz, Schlaflosigkeit, trockener Mund, Übelkeit, Verstopfung und Asthenie als sehr häufige (>10%) Nebenwirkungen bekannt. Häufig (>1%) können unter anderem folgende Nebenwirkungen auftreten: Hautausschlag, Juckreiz, Myalgie, Schwindel, Parästhesie, extrapyramidal-motorische Störungen (EPS), Geschmacksstörungen, Sehstörungen, Nervosität, Angst, Agitiertheit, verändertes Träumen, Libidoabnahme oder Apathie.
In einem möglichen, wahrscheinlichen oder sicheren Zusammenhang mit der Studienmedikation standen in der Hypericum-Gruppe eine deutlich geringere Anzahl der UE (17,2%) als in der Citalopram-Gruppe (53,2%) oder der Plazebo-Gruppe (30,0%) (Abb. 3).
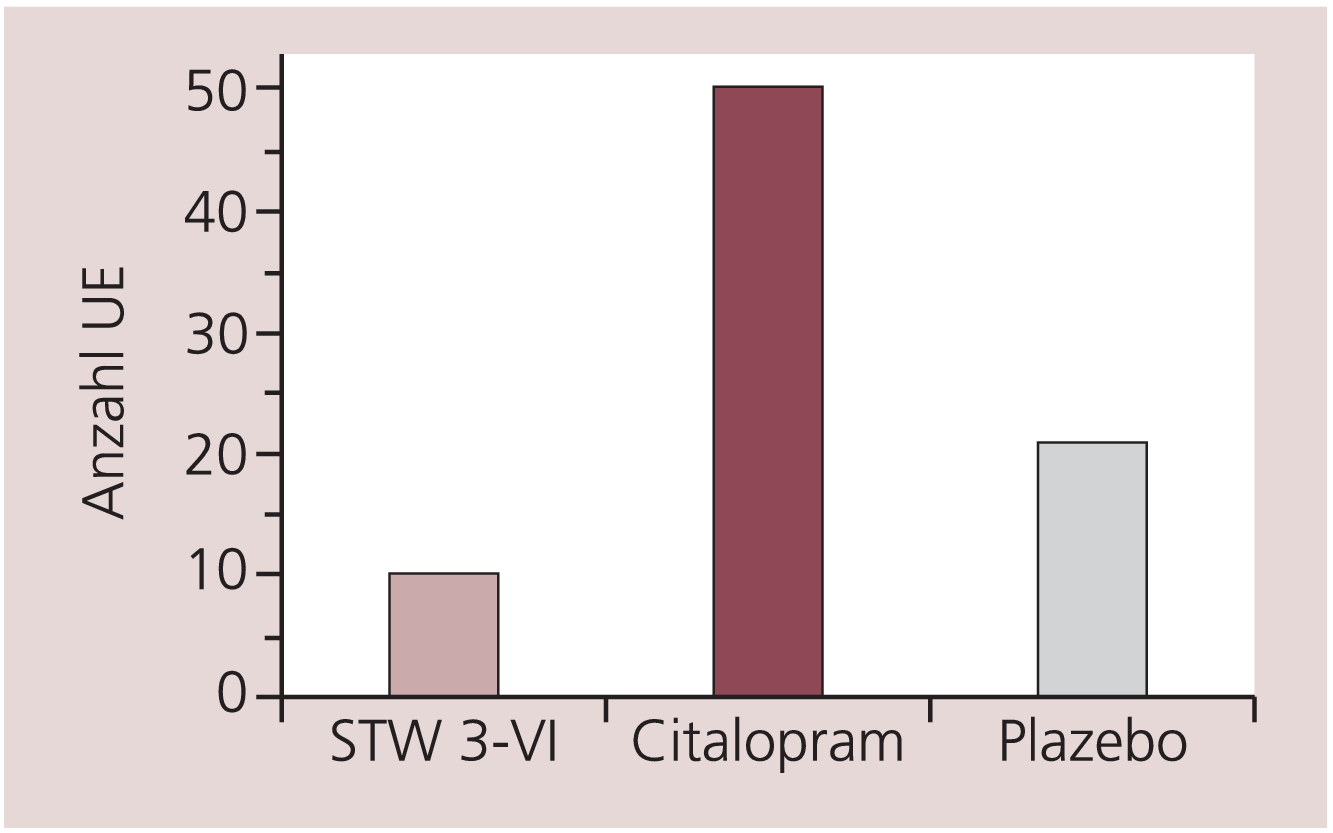
Abb. 3. Anzahl der unerwünschten Ereignisse mit Kausalzusammenhang zur Prüfmedikation
Insgesamt brachen 21 Patienten die Studie wegen unerwünschter Ereignisse ab. Davon waren vier Patienten (6,9%) in der Hypericumextrakt-Gruppe, elf Patienten (11,7%) in der Citalopram-Gruppe und sechs (8,6%) Patienten in der Plazebo-Gruppe.
Während der Studie wurden sechs schwerwiegende UE beobachtet (Citalopram: 2; Plazebo: 4). Bei keinem Patienten stand das schwerwiegende UE in kausalem Zusammenhang mit der Prüfmedikation. Interaktionen zwischen den Prüfpräparaten und Begleitmedikation der Patienten sind nicht aufgetreten.
In den überwiegenden Fällen wurde die Verträglichkeit beider Studienmedikamente von den Prüfärzten als „sehr gut“ oder „gut“ bewertet.
Nach Behandlungsende wurde eine mäßige oder schlechte Verträglichkeit in der Citalopram-Gruppe bei 11% der Patienten und bei 2,3% der Patienten der Plazebo-Gruppe dokumentiert. In der Hypericum-Gruppe vertrugen alle Patienten die Medikation „sehr gut“ bis „gut“ und damit signifikant besser als in den anderen Behandlungsgruppen. Die Vital- und Laborwerte zeigten während der gesamten Studienzeit in allen drei Gruppen keine klinisch relevanten Änderungen.
Diskussion
Hypericum-Präparate sind Phytopharmaka deren Wirksamkeit und Unbedenklichkeit bisher in zahlreichen Studien untersucht wurde [11]. Allerdings wurden in den letzten Jahren auch einige Negativstudien publiziert, welche die antidepressive Wirksamkeit des Johanniskrauts wieder in die Diskussion brachten.
Um eindeutige und aussagekräftige Ergebnisse einer Depressionsstudie zu erhalten, empfiehlt die aktuelle Depressions-Leitlinie für Kurzzeitstudien ein dreiarmiges Studiendesign mit einem Plazebo-Arm und zusätzlich einem Standardpräparat [2]. Trotz dieses Designs ist es nicht immer leicht, die Wirksamkeit von Johanniskraut zu beweisen, wie die viel beachtete US-amerikanische doppelblinde, Verum- und Plazebo-kontrollierte Studie der Hypericum DTSG [8] zeigte. Allerdings weist diese Studie einige methodische Besonderheiten auf. So gibt es Hinweise auf schwere Krankheitsausprägungen in der Studienpopulation, da die depressive Phase der Patienten im Schnitt schon zwei Jahre andauerte und über 40% der Patienten die zusätzliche Charakterisierung des Subtyps Melancholie hatten, der ebenfalls auf eine schwere Depression hinweist. Für Patienten mit schweren Depressionen ist die Behandlung mit Hypericum-Präparaten ohnehin nicht indiziert [5]. In einer anderen dreiarmigen Plazebo-kontrollierten Studie konnte ebenfalls weder die Überlegenheit von Johanniskraut noch die von Fluoxetin über Plazebo gezeigt werden [1]. In den letzten Jahren wurden insgesamt zehn Vergleichsstudien mit Hypericum und selektiven Serotonin-Wiederaufnahmehemmern durchgeführt. Dabei stellte sich heraus, dass die Wirksamkeit der Johanniskraut-Gabe bei leichter bis mittelschwerer Depression der Verabreichung von SSRI vergleichbar, oftmals sogar leicht überlegen war [11]. Die vorliegende Studie ist die erste, die Plazebo-kontrolliert die gleichwertige Wirksamkeit zwischen Hypericum und SSRI bei mittelschweren Depressionen eindeutig bestätigt. Hier zeigt sich, dass die Mittelwertsdifferenzen gegenüber Plazebo nach sechswöchiger Behandlung für Hypericumextrakt STW3-VI und Citalopram gleich sind (2,7 Punkte). Darüber hinaus sind auch die Responderraten praktisch gleich und liegen deutlich über Plazebo (Hypericum 55,0%, Citalopram 56,7%, Plazebo 39,2%). Solche Ergebnisse sind im Hinblick auf die vorliegende Literatur als klinisch relevant anzusehen [9].
Die Überlegenheit des Standards über Plazebo zeigt die valide Studiendurchführung und sichert damit die Aussagekraft der Ergebnisse.
In der Metaanalyse von Röder et al. [13] über 30 Studien ergibt sich bezüglich der beobachteten Nebenwirkungen ein signifikanter Unterschied zum Vorteil der Johanniskraut-Therapie. Während unerwünschte Nebenwirkungen unter Johanniskraut bei 24,5% aller Studienpatienten angeben wurden, sind dies in der SSRI-Gruppe 32,8%. In dieser Studie ist der Unterschied zwischen den beiden Verum-Gruppen (17,2% vs. 53,2%) noch deutlicher.
Hypericumextrakte werden in Bezug auf Interaktionen häufig diskutiert. Sie aktivieren sowohl ein in der Dünndarmmukosa lokalisiertes Transportprotein (P-Glykoprotein) als auch die für den Stoffwechsel vieler Arzneimittel verantwortlichen Cytochrom-P450-Isoenzyme der Leber. Daraus resultiert, dass die Wirkspiegel vieler Komedikationen abnehmen können. Klinisch und experimentell belegt sind allerdings nur Interaktionen mit Arzneimitteln, die eine geringe therapeutischer Breite haben, wie Antikoagulanzien (z.B. Phenprocoumon [Marcumar®]) und Immunsupressiva [15]. In der vorliegenden Studie wurden keine Interaktionen zwischen dem Hypericumextrakt STW3-VI und Begleitmedikation dokumentiert.
Gerade bei psychisch kranken Patienten ist eine regelmäßige Einnahme der Medikamente für den Therapieerfolg unerlässlich. Das geringer ausgeprägte Nebenwirkungsprofil von Johanniskraut wirkt sich positiv auf die Akzeptanz und Compliance der Patienten aus. Die Vielzahl und Intensität der Nebenwirkungen chemischer Standardpräparate beeinflusst die Bereitschaft zu einer konsistenten Einnahme und führt häufig zum Therapieabbruch. Weiterhin kann die Compliance der Patienten durch die tägliche Einmalgabe des verordneten Medikaments unterstützt werden. Patienten mit depressiven Erkrankungen benötigen meist eine längere Behandlungsdauer, so dass die Gabe einer täglichen Einzeldosis für diese Patienten besser geeignet ist [3]. Wie die meisten SSRI ermöglicht auch der untersuchte Hypericumextrakt STW3-VI dieses Einnahmeschema. Die als wirksamkeitsrelevant eingestuften Inhaltsstoffe Hypericin, Pseudohypericin und Hyperforin haben eine Halbwertszeit von über 17 Stunden [14]. In einer vergleichenden Langzeitstudie wurde die Wirksamkeit von Hypericumextrakt STW3 in der täglichen Einmalgabe in der Erhaltungstherapie gezeigt [6].
Schlussfolgerung
Die Studie zeigt, dass Johanniskrautextrakt STW3-VI in der Behandlung mittelschwer depressiver Patienten ein sehr gut verträgliches Medikament ist. Bei gleicher Wirksamkeit wie das chemische Standardmedikament stellt der Johanniskrautextrakt eine ernst zu nehmende Therapieoption für die ambulante Depressionsbehandlung dar.
Literatur
1. Bjerkenstedt L, Edman GV, Alken RG, Mannel M. Hypericum extract LI 160 and fluoxetine in mild to moderate depression. A randomized, placebo-controlled multi-center study in outpatients. Eur Arch Psychiatry Clin Neurosci 2005; 255:40–7.
2. CPMP/EWP/518/97 Note for Guidance on clinical investigation of medicinal products in the treatment of depression, October 2002.
3. Demyttenaere K. Risk factors and predictors of compliance in depression. Eur Neuropsychopharmacol 2003;13:69–75.
4. Eisen SA, Miller DK, Woodward RS, Spitznagel E, et al. The effect of prescribed daily dose frequency on patient medication compliance. Arch Intern Med 1990;150:1881–4.
5. ESCOP (European Scientific Cooperative on Phytotherapy)-Monographs: Hyperici herba. Stuttgart, New York: Thieme, 2003:257–81.
6. Gastpar M, Singer A, Zeller K. Efficacy and tolerability of Hypericum extract STW3 in long-term treatment with a once daily dosage in comparison with sertraline. Pharmacopsychiatry 2005;38:78–86.
7. Härter M, Bermejo I, Dausend S, Schneider F, et al. Vernetzte Versorgung depressiver Patienten – Entwicklung und Evaluation von Diagnose- und Therapieempfehlungen. Psychoneuro 2003;29:217–26.
8. Hypericum Depression Trial Study Group. Effect of Hypericum perforatum (St John’s Wort) in major depressive disorder: a randomized controlled trial. JAMA 2002;287:1807–14.
9. Kirsch I, Moore TJ, Scoboria A, Nicholls SS. The emperor’s new drugs: An analysis of antidepressant medication data submitted to the U.S. Food and Drug Administration. Prev Treatment 2002;5:1–15.
10. Lepine JP, Gastpar M, Mendlewicz J, Tylee A. Depression in the community: the first pan-European study DEPRES (Depression research in European society). Int Clin Psychopharmacol 1997;12:19–29.
11. Linde K, Ramirez G, Mulrow CD, Berner M, et al. St John’s Wort for depression. The Cochrane Database of systematic reviews 2005. Issue 3. Art. No.: CD000448.pub2. DOI:10.1002/14651858.CD000448.pub2
12. Müller WE. Neue Erkenntnisse zur Pharmakologie von Antidepressiva. Sind die Substanzunterschiede therapeutisch relevant? Psychopharmakotherapie 2005;(Suppl 13):59–67.
13. Röder C, Schaefer M, Leucht S. Metaanalyse zu Wirksamkeit und Verträglichkeit der Behandlung der leichten und mittelschweren Depression mit Johanniskraut. Fortschr Neurol Psychiat 2004;72:330–43.
14. Schulz H-U, Schürer M, Bässler D, Weiser D. Investigation of pharmacokinetic data of hypericin, pseudohypericin, hyperforin and the flavonoids quercetin and isorhamnetin revealed from single and multiple oral dose studies with a hypericum extract containing tablet in healthy male volunteers. Arzneimittelforschung Drug Res 2005;55:561–8.
15. Schulz V. Therapierisiken durch Johanniskraut? Dtsch Apoth Ztg 2006;41:42–55.
Dr. Karin Zeller, Steigerwald Arzneimittelwerk GmbH, Havelstr. 5, 64295 Darmstadt Prof. Dr. Markus Gastpar, Fliedner-Klinik, Charlottenstr. 65, 10117 Berlin
Hypericum extract STW3-VI in comparison to citalopram und placebo in patients with moderate depression
The primary objective of this 3-arm design study was to demonstrate the non-inferiority of Hypericum extract STW3-VI (900 mg) to the SSRI citalopram (20 mg) and the superiority of Hypericum over placebo. For the 6-week treatment, outpatients (n=388) suffering from moderate depression were randomized with either 900 mg hypericum extract, 20 mg citalopram or placebo once a day.
The course of depression was documented by use of HAMD total score (items 1–17). From almost identical baseline values of 21.9±1.2 points (Hypericum extract), 21.8±1.2 points (citalopram) and 22.0±1.2 points (placebo), the HAMD score was reduced to 10.3±6.4 (Hypericum extract), 10.3±6.4 (citalopram) and 13.0±6.9 (placebo), respectively. Based on these data, the statistically significant therapeutic equivalence of Hypericum extract STW3-VI to citalopram (p<0.0001) and the superiority of this Hypericum extract over placebo (p<0,0001) was demonstrated. The secondary efficacy parameters, change in BfS, CGI and amount of therapy responders showed that the Hypericum group was not statistically different from the citalopram group, and significantly superior to the placebo group.
At the end of treatment 54.2% (Hypericum extract), 55.9% (citalopram) and 39.2% (placebo) of the patients were assessed as therapy responders.
Significantly more adverse events with relation to study medication were documented in the citalopram group (Hypericum: 17.2%, citalopram: 53.2%, placebo: 30%).
These results revealed that Hypericum extract STW3-VI in a daily single dose is a good alternative to chemically defined antidepressants in the treatment of outpatients with moderate depression.
Keywords: St. John’s Wort, SSRI, moderate depression, Hypericum extract, citalopram
Psychopharmakotherapie 2007; 14(02)
