Dr. Christiane Potz-Biedermann, Tübingen
Als Initialtherapie der Parkinson-Krankheit wird häufig Levodopa mit einem Decarboxylase-Hemmer (z.B. Nacom®, Madopar®) verabreicht. Doch mit abnehmender Wirkungsdauer der einzelnen Levodopa-Gaben bei fortgeschrittenen Stadien der Erkrankung kommt es zu Wirkungsschwankungen, die klinisch unter anderem zu motorischen Fluktuationen und Hyperkinesien bei den Patienten führen.
Mit Levodopa-Retardpräparaten lassen sich Plasmaspiegel ohne Levodopa-Spitzen gewährleisten. Sie werden vor allem zur abendlichen Einnahme verordnet, um nächtliche Akinesien und frühmorgendliche Dystonie zu reduzieren. Auch schlafbezogene Symptome, wie Ein- und Durchschlafstörungen, nächtliche Atempausen, Krämpfe und Nykturie, lassen sich damit therapeutisch beeinflussen.
In einer Anwendungsbeobachtung mit 294 Patienten wurde retardiertes Levodopa/Carbidopa zur Tagestherapie eingesetzt. Die Patienten litten an einem idiopathischen Parkinson-Syndrom und hatten zuvor Levodopa in Kombination mit einem Decarboxylase-Hemmer erhalten. Wegen motorischer Fluktuationen (leichte Peak-Dose-Dyskinesien, End-of-Dose-Akinesien) wurden sie auf ein Levodopa-Retardpräparat umgestellt und acht Wochen lang beobachtet. Andere Parkinson-Medikamente wurden nach individueller Entscheidung des behandelnden Arztes beibehalten, in der Dosierung angepasst oder reduziert.
Zur Beurteilung der Kardinalsymptome sowie Fluktuationen und Lebensqualität wurden die Patienten mit einem standardisierten Erfassungsbogen von ihren behandelnden Ärzten befragt. Die Schlafqualität wurde mit der Parkinson’s Disease Sleep Scale (PDSS) von den Patienten selbst erfasst. Anhand von 15 Fragen (Items) beurteilten sie ihre Schlafstörungen auf einer visuellen Analogskala mit Werten zwischen 0 (schwere Symptomatik) und 10 (keine Schlafstörung).
Am Ende der Beobachtungsperiode erhielten 94% der teilnehmenden Patienten retardiertes Levodopa gegenüber 27% vor Umstellung der Medikation. Die mittlere effektive Gesamtdosis (Levodopa Retard + Standard) bezogen auf das Gesamtkollektiv lag bei 360,8 mg/d nach Umstellung im Vergleich zu 348,5 mg/d vor Änderung der Medikation. Fast zwei Drittel der Patienten bekamen zusätzlich eine morgendliche Dosis eines unretardierten Levodopa-Präparats („Kick-Start“), um den verzögerten Wirkungseintritts des morgens verabreichten retardierten Levodopas auszugleichen.
Nach der Umstellung der Medikation auf eine retardierte Levodopa-Formulierung zeigte eine Mehrzahl der Patienten eine deutliche Reduktion der Symptome Akinesie, Rigor und Tremor. Ebenso verminderten sich motorische Fluktuationen und schmerzhafte Dyskinesien zugunsten Phasen guter Beweglichkeit (Abb.1).
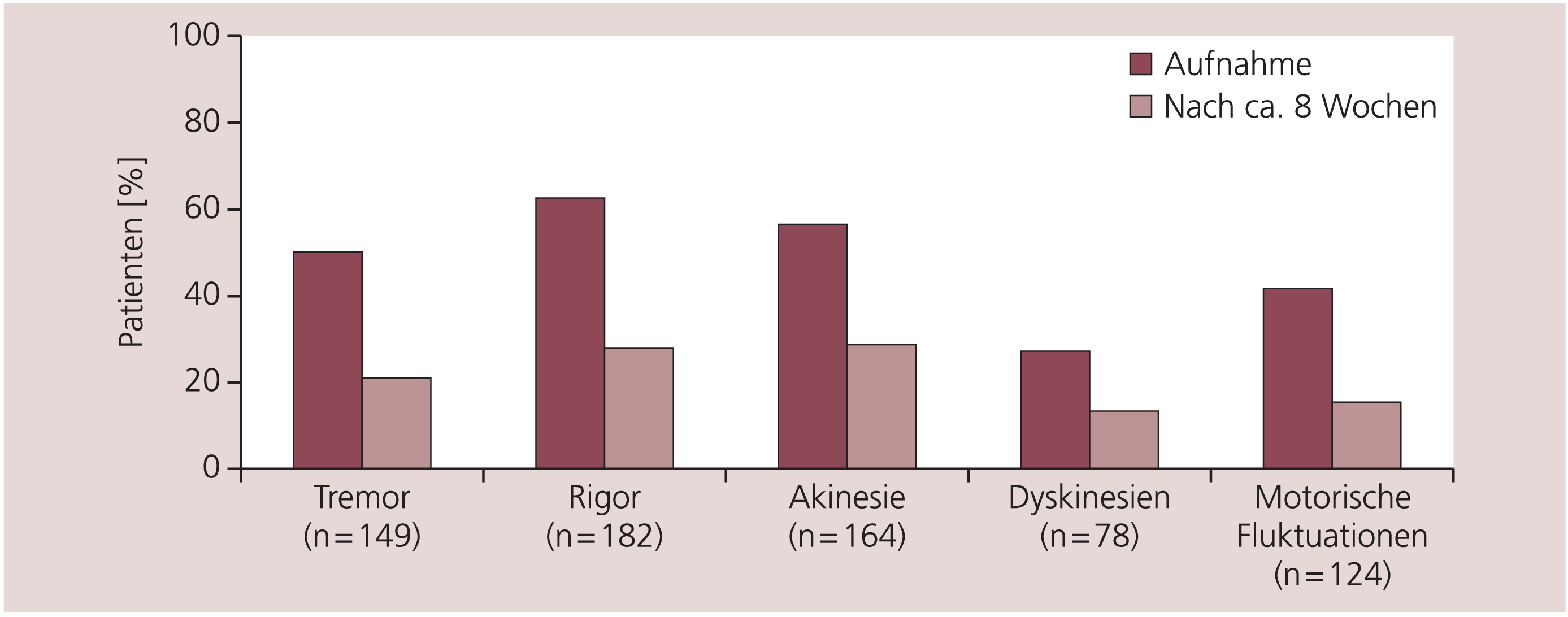
Abb. 1. Leitsymptome des Parkinson-Syndroms nach Umstellung auf morgendliche Einnahme von retardiertem Levodopa. Dargestellt ist jeweils der Anteil der Patienten mit mäßigen bis sehr starken Symptomen.
In der Selbstbeurteilung der Patienten ergab sich eine signifikante Verbesserung des Nachtschlafs verbunden mit einem deutlichen Anstieg der Lebensqualität und Alltagskompetenz, da die Schlaf-assoziierten Parameter (z.B. plötzliches Einschlafen, Schmerzen in den Beinen/Armen nach dem Aufwachen, Inkontinenz), die tagsüber von Bedeutung sind, sich verringerten. Die untersuchenden Ärzte schätzten die Lebensqualität bei fast 80% der Patienten höher ein als zu Beginn der Untersuchung. Die Verträglichkeit der retardierten Levodopa-Formulierung wurde bei ebenfalls fast 80% der Patienten als sehr gut oder gut beurteilt.
Quelle
Trenkwalder C, et al. Retardiertes L-Dopa in der Tagestherapie des idiopathischen Parkinson-Syndroms [Poster]. 4. Deutscher Parkinson-Kongress, Frankfurt/M., 3. bis 5. März 2005.
Psychopharmakotherapie 2006; 13(02)
