Markus Gastpar, Essen, und Karin Zeller, Darmstadt
In der Allgemeinarztpraxis zählen Depressionen zu den wichtigsten psychischen Erkrankungen. Etwa 20% der Patienten sind betroffen. Leider bleiben bis zu der Hälfte dieser Patienten unbehandelt, weil das Krankheitsbild oft unerkannt bleibt. Zudem sind Allgemeinärzte mit der Verschreibung antidepressiv wirkender Medikamente zurückhaltend, denn bei bis zu 30% der Patienten kommt es zu unerwünschten Arzneimittelwirkungen, die größtenteils zum Absetzen des Medikaments führen [12].
So ist eine wirksame medikamentöse Behandlung der Depression mit einer geringeren Nebenwirkungsrate bei moderaten Kosten eine sinnvolle Ergänzung der Depressionstherapie.
Eine Alternative zu den klassischen chemisch definierten Antidepressiva, wie beispielsweise den trizyklischen Antidepressiva, Serotonin-Wiederaufnahmehemmern (SSRI) oder MAO-Hemmern, ist ein Extrakt aus Johanniskraut (Hypericum perforatum). Die antidepressive Wirkung von Hypericum-Extrakt konnte im Vergleich zu Plazebo [8, 9, 14] sowie im Vergleich zu Imipramin und Fluoxetin [16, 19, 23] in mehreren Kurzzeitstudien gezeigt werden. Die Nebenwirkungsraten waren nicht unterschiedlich zu Plazebo und weitaus geringer als bei klassischen Antidepressiva.
Allerdings wurden die Testpräparate mehrheitlich 2- bis 3-mal täglich gegeben und die Studien nur über meist sechs bis acht Wochen durchgeführt [17]. Patienten mit depressiven Erkrankungen benötigen in der Regel eine längere Behandlung von mehreren Monaten. Zudem ist bekannt, dass ein nur einmal täglich verordnetes Medikament die Compliance dieser Patienten bessert [3, 4].
Kontrollierte Daten zu einer Behandlung mit Johanniskraut-Extrakt einmal täglich und länger als 12 Wochen gegeben liegen bisher nicht vor. Die Wirkung eines Johanniskraut-Extrakts bei leichteren Depressionen in der Langzeittherapie wurde in einer offenen Einjahresstudie untersucht, in der signifikante Verbesserungen auf der Hamilton-Depressionsskala (HAMD) gezeigt werden konnten, doch das Präparat musste dreimal täglich eingenommen werden [6]. In einer Plazebo-kontrollierten Studie konnte mit einem einmal täglich gegebenen Johanniskraut-Extrakt eine signifikante Verbesserung auf der Montgomery-Asperg-Depressionsskala (MADRS) und der HAMD gezeigt werden, doch dauerte diese Studie nur sechs Wochen [1].
In der vorliegenden doppelblinden Studie sollte die Wirksamkeit eines Johanniskraut-Extrakts in einer Einmaldosierung in der Erhaltungstherapie über mindestens drei bis zu sechs Monaten gezeigt werden. Ziel war es weiterhin, die therapeutische Äquivalenz („non-inferiority“) des Hypericum-Extrakts im Vergleich zu einem chemisch definierten Standardmedikament bei mittelschwer depressiven Patienten zu zeigen.
Als Prüfmedikament diente Hypericum-Extrakt STW3 (Laif® 600), als Vergleichsmedikament der selektive Serotonin-Wiederaufnahmehemmer Sertralin (Zoloft®). Mit einer Halbwertszeit von etwa 25 Stunden erlaubt Sertralin die einmal tägliche Gabe. Auch für den Johanniskraut-Extrakt STW3 liegen Kinetikdaten vor, die die tägliche Einmalgabe stützen. Die antidepressiv wirksamen Inhaltsstoffe Hypericin, Pseudohypericin und Hyperforin haben mit über 19 Stunden [22] ausreichend lange Halbwertszeiten, um für eine Einmaldosierung geeignet zu sein. Sertralin ist gegenüber der klassischen Referenzsubstanz der Antidepressiva, dem von der WHO als Standardpräparat („essential drug“) eingestuften Imipramin, deutlich überlegen [11]. Nach den Ergebnissen einer Plazebo-kontrollierten Doppelblindstudie an 369 ambulanten depressiven Patienten (nach DSM-IIIR) wird 50 mg Sertralin pro Tag als ausreichende Dosierung in der ambulanten Therapie betrachtet [11].
Patienten und Methoden
Die doppelblinde, randomisierte, multizentrische, Phase-III-Studie wurde nach den Grundsätzen für Standards der Guten Klinischen Praxis (GCP) bei der Durchführung von Studien mit Arzneimitteln am Menschen in der EU, den ICH-Guidelines und den Prinzipien der Deklaration von Helsinki durchgeführt. Die erforderlichen Unterlagen wurden zuvor einer unabhängigen Ethik-Kommission vorgelegt und von dieser positiv bewertet.
Weibliche und männliche ambulante depressive Patienten wurden in diese Studie aufgenommen, wenn sie die in Tabelle 1 aufgeführten Einschlusskriterien erfüllten.
Tab. 1. Ein- und Ausschlusskriterien
|
Einschlusskriterien |
|
• Alter zwischen 18 und 70 Jahren • Patientinnen nicht gebärfähig oder mit einer anerkannten Kontrazeptions-Methode • Einverständniserklärung gemäß §§ 40 und 41 Arzneimittelgesetz (AMG) nach Aufklärung über Wesen, Bedeutung und Tragweite der Prüfung durch den behandelnden Arzt • Depression mit einem Score von 20 bis 24 Punkten auf der Hamilton-Depressionsskala (Items 1–17) • Mittelschwere Depression (auch Erstmanifestation) definiert nach ICD-10: F32.1, F33.1 (entsprechend DSM-IV 296.2x und 296.3x) |
|
Allgemeine Ausschlusskriterien |
|
• Teilnahme an einer klinischen Studie innerhalb der letzten 30 Tage • Gleichzeitige Teilnahme an einer anderen klinischen Prüfung • Teilnahme an dieser Studie zu einem früheren Zeitpunkt • Unmündige Patienten • Patienten mit klinisch relevanten Laborwertabweichungen • Schwangerschaft oder Stillzeit • Gebärfähige Frauen, die orale Kontrazeptiva mit einem geringen Hormonanteilanteil (Mikropille, • Gleichzeitige Behandlung mit Antikoagulantien vom Cumarintyp • Krebs- und AIDS-Patienten • Alkoholiker, Medikamenten- oder Drogenabhängige • Psychiatrische Erkrankungen, die das Ergebnis der Studie beeinflussen können • Epilepsie |
|
Anamnestische Ausschlusskriterien |
|
• Therapieresistente Depression • Bekannte Schizophrenie, Psychose oder Demenz • Depressive Stimmungslage durch eine schwerwiegende Grunderkrankung • Bekannte Unverträglichkeit gegenüber den Studienmedikamenten • Bekannte Photosensibilität • Spezifische Psychotherapie in den letzten 2 Monaten • Behandlung mit Antidepressiva in den letzten 6 Wochen vor Eintritt in die Studie • Festgestellte Suizidalität aufgrund eines HAMD-Scores von > 2 in Item 3 der Skala • Bekannter Suizidversuch |
Auf einen zusätzlichen Plazebo-Arm wurde aus ethischen Gründen aufgrund der langen Beobachtungszeit und der Daten aus zahlreichen Plazebo-kontrollierten Johanniskraut-Extrakt-Studien verzichtet.
Die Studie wurde in 21 Praxen von Allgemeinmedizinern und hausärztlich tätigen Internisten von Juli 2000 bis April 2001 durchgeführt. Die Ärzte waren in der Anwendung der Diagnosekriterien und Fremdbeurteilungsskalen erfahren. Um eine einheitliche Bewertung zu gewährleisten, nahmen die Ärzte vor Studienbeginn an einem Ratertraining teil. Der Studienverlauf unterteilte sich in zwei Phasen. In den ersten 12 Wochen (erste Behandlungsphase) erhielten alle Patienten die Studienmedikation. In den zweiten 12 Wochen wurde nach Beurteilung des behandelnden Arztes die Behandlung entweder weitergeführt (zweite Behandlungsphase) oder die Medikation wurde nach der 12. Woche beendet (Nachbeobachtung ohne Medikation). Die Patienten erschienen in beiden Fällen zu den vorgesehenen Visiten. Der Studienverlauf ist in Tabelle 2 aufgezeigt.
Tab. 2. Studienverlauf
|
Visite 1 |
Visite 2 |
Visite 3 |
Visite 4 |
Visite 5 |
Visite 6 |
Visite 7 |
Visite 8 |
Visite 9 |
|||||
|
Ein- und Ausschlusskriterien |
X |
||||||||||||
|
Aufklärung/Einverständnis |
X |
||||||||||||
|
Körperliche Untersuchung/Vitalparameter |
X |
X |
X |
X |
X |
X |
X |
X |
X |
||||
|
HAMD, Bf-S, CGI |
X |
X** |
X |
X |
X |
X |
X |
X |
X |
||||
|
Labor |
X |
X |
X* |
||||||||||
|
Begleiterkrankungen/Begleitmedikamente |
X |
X |
X |
X |
X |
X |
X |
X |
X |
||||
|
Medikamentenausgabe |
X |
X |
X |
X* |
X* |
X* |
|||||||
|
Complianceüberprüfung |
X |
X |
X |
X* |
X* |
X* |
|||||||
|
Erfassung unerwünschter Ereignisse |
X |
X |
X |
X |
X |
X |
X |
X |
|||||
|
Beurteilung der Wirksamkeit und Verträglichkeit |
X |
X |
X |
X |
X |
X* |
X* |
X* |
|||||
X* Wurde durchgeführt, falls die Gabe der Prüfmedikamente fortgeführt wird
X** An Tag 7 war nur der CGI auszufüllen
Innerhalb der 24-wöchigen Studiendauer wurde der Verlauf der Depression an Hand der Hamilton-Depressionsskala (HAMD), der Befindlichkeits-Skala nach von Zerssen (Bf-S) und der Clinical-Global-Impression(CGI)-Skala dokumentiert.
Die Patienten wurden randomisiert den einzelnen Behandlungsgruppen zugeteilt. Da die Darreichungsformen von Hypericum-Extrakt STW3 und Sertralin optisch unterschiedlich sind, wurde zur Verblindung die „double-dummy“-Technik gewählt.
Die Patienten-Compliance wurde bei jeder Medikamentenrücknahme durch das Zählen der zurückgegebenen Tabletten überprüft und dokumentiert. Eine Einnahme von weniger als 75% und mehr als 125% der Tabletten galt als non-compliant.
Zielkriterien der Effizienz und Sicherheit
Primäres Zielkriterium war der Nachweis der „non-inferiority“ (Nicht-Unterlegenheit) der Behandlung mit Hypericum-Extrakt STW3 im Vergleich zur Behandlung mit Sertralin anhand der Hamilton-Depressionsskala nach 12 Wochen Behandlung. Weiterhin wurde der Therapieerfolg auf Basis der Responderbetrachtung für die gesamte Studienzeit evaluiert. Dabei galt eine Besserung des HAMD-Scores von mindestens 50% gegenüber dem Ausgangswert oder ein Score von unter 10 Punkten als Erfolg. Die Patienten-Selbstbeurteilung wurde mit der BfS-Skala, die Verträglichkeit mit der CGI-Skala sowie dem Auftreten von unerwünschten Ereignissen und der Laborparameter ausgewertet.
Statistische Methoden
Für die im Rahmen dieser Studie erhobenen Daten wurden zunächst entsprechend der Verteilung der Parameter deskriptive univariate Kenngrößen berechnet.
Die statistische Auswertung erfolgte entsprechend der Verteilung der Zielgrößen mit Kovarianzanalysemodellen (kontinuierliche Parameter) mit den Faktoren Behandlung und Zentrum sowie der Kovariablen Ausgangswert oder dem nach Zentren stratifizierten Cochran-Mantel-Haenszel-Test (kategorielle Parameter).
Unter Beachtung der Zielsetzung der klinischen Prüfung wurde die Hypothese der therapeutischen Nicht-Unterlegenheit („non-inferiority“) von Hypericum-Extrakt gegenüber Sertralin mit der Nicht-Unterlegenheitsgrenze δ=3 (Punkte auf der HAMD) einseitig auf der Grundlage des folgenden Testproblems konfirmatorisch geprüft: der Nullhypothese (H0) μ(H) < μ(S)–δ (Überlegenheit der aktiven Referenz Sertralin) und der Alternativhypothese (H1) μ(H) ≥ μ(S)–δ (Nicht-Unterlegenheit von Hypericum-Extrakt oder Hypericum-Extrakt ist der Referenz Sertralin wenigstens gleichwertig). Hierin bezeichnen μ(H) und μ(S) die unbekannten, aber wahren, Baseline-adjustierten Populationsmittelwerte des Hamilton-Scores unter Hypericum-Extrakt oder Sertralin. Dieses Testproblem wurde mit einem Risiko für den Fehler erster Art (Irrtumswahrscheinlichkeit α) von 0,025 betrachtet. Generell wurde für dieses und andere Testprobleme im Falle fehlender Daten der LOCF-Zugang („Last observation carried forward“), gewählt. Für die Ergebnisse wird zusätzlich ein einseitiges Konfidenzintervall (97,5 %) angegeben.
Für die anderen, nicht primären Wirksamkeitsparameter wurde die Hypothese der Überlegenheit einer der beiden Prüfparameter betrachtet, das heißt die Nullhypothese (H0) μ(H)=μ(S) getestet.
Entsprechend der primären Fragestellung wurden die Analysen auf Basis der Per-Protokoll-(PP-)Population durchgeführt. Weitere Analysen auf Basis der Intention-to-treat-(ITT-)Population sind als Sensitivitätsanalyse zu betrachten.
Ergebnisse
241 Patienten im Alter von 18 bis 70 Jahren mit einer ambulant behandlungsbedürftigen mittelgradigen Depression wurden in die Studie und in das ITT-Kollektiv aufgenommen. Davon erhielten 123 Patienten Hypericum-Extrakt STW3 und 118 Patienten Sertralin. Unter Berücksichtigung verschiedener Prüfplanverstöße (Ausschluss vor Visite 12, falls nicht durch ein unerwünschtes Ereignis oder Wirksamkeit/Unwirksamkeit der Prüfmedikation bedingt, mangelnde Termincompliance, unerlaubte Begleittherapie) konnten 200 Patienten in das PP-Kollektiv aufgenommen werden. Davon erhielten 102 Patienten Hypericum-Extrakt und 98 Patienten Sertralin.
Von den 200 Patienten des PP-Kollektivs wurden 81 Patienten der Hypericum-Extrakt-Gruppe und 80 Patienten der Sertralin-Gruppe nach Woche 12 mit der Studienmedikation weiterbehandelt. Die übrigen 39 Patienten im PP-Kollektiv wurden zwischen Woche 12 und 24 nicht medikamentös behandelt.
Patientencharakteristika
Die in die Studie aufgenommenen Patienten waren zu etwa drei Viertel Frauen. Die demographischen Daten der einzelnen Behandlungsgruppen waren vergleichbar.
Bei etwa 75% der Patienten lag die Erstdiagnose der Depression länger als sechs Monate zurück, im Median dauerte die Depression 16 Monate. Innerhalb der beiden Behandlungsgruppen gab es keine signifikanten Unterschiede in der Dauer der Erkrankung und der familiären Vorbelastung (Depressionen in der Familie wurden bei 28,5% der Patienten dokumentiert).
Ergebnisse zur Wirksamkeit (HAMD)
Die Verbesserung des HAMD-Scores war in beiden Behandlungsgruppen nahezu identisch. In der Hypericum-Extrakt-Gruppe zeigte sich eine Abnahme von 22,0±1,1 Punkten zu Therapiebeginn auf 8,3±5,5 Punkte, in der Sertralin-Gruppe von 22,1±1,1 Punkten auf 8,1±5,6 Punkte nach Woche 12. Die Abnahme des HAMD-Scores bei den einzelnen Visiten zeigte in beiden Behandlungsgruppen ebenfalls vergleichbare Werte (Abb. 1).
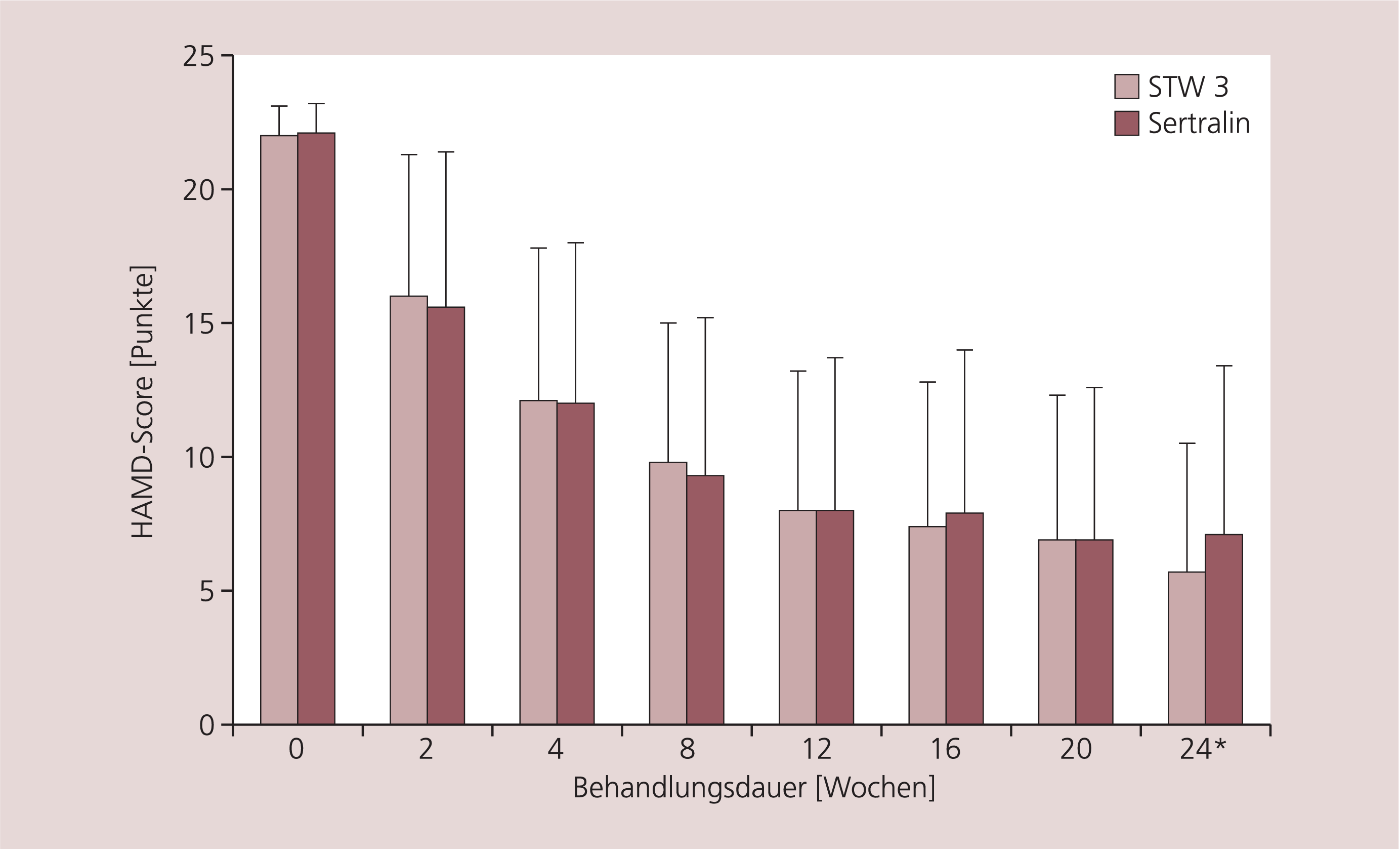
Abb. 1. Abnahme des HAMD-Scores während der 24-wöchigen Arzneimitteltherapie
(Mittelwerte ± SD, PP-Population, n=200)
* Die Daten an Woche 24 wurden nach LOCF ermittelt (n=157)
Die Kovarianzanalyse ergab für den Test auf Nicht-Unterlegenheit von Hypericum-Extrakt ein eindeutig signifikantes Ergebnis. Die Hypothese der Unterlegenheit von Hypericum-Extrakt konnte mit einem p-Wert von weniger als 0,0001 (einseitiges Konfidenzintervall für den Behandlungsunterschied [–∞, 1,3772]) verworfen werden, das heißt, die Wirksamkeit von Hypericum-Extrakt STW3 ist Sertralin mindestens gleichwertig.
Dieses Ergebnis konnte in der ITT-Population mit einem hoch signifikanten Ergebnis von p<0,0003 (einseitiges Konfidenzintervall [–∞, 1,6730]) ebenfalls verifiziert werden.
In der anschließenden zweiten Studienphase kam es zu einer weiteren Verbesserung des HAMD-Scores im PP-Kollektiv mit medikamentöser Weiterbehandlung. In der Hypericum-Extrakt-Gruppe verringerte sich der HAMD-Wert in der 24. Woche auf 5,7±4,8 und in der Sertralin-Gruppe auf 7,1±6,3 Punkte.
Nach 12 Wochen Behandlung sprachen 68,6% der Patienten der Hypericum-Extrakt-Gruppe und 70,4% der Patienten der Sertralin-Gruppe auf die Therapie an, wobei der Gruppenunterschied nicht signifikant ist. Nach 24 Wochen Behandlung sprachen 84,0% der Patienten mit Hypericum- und 81,3% der Patienten mit Sertralin-Behandlung auf die Therapie an (Abb. 2). Auch hier bestätigte die Analyse der ITT-Population die Ergebnisse der PP-Population.
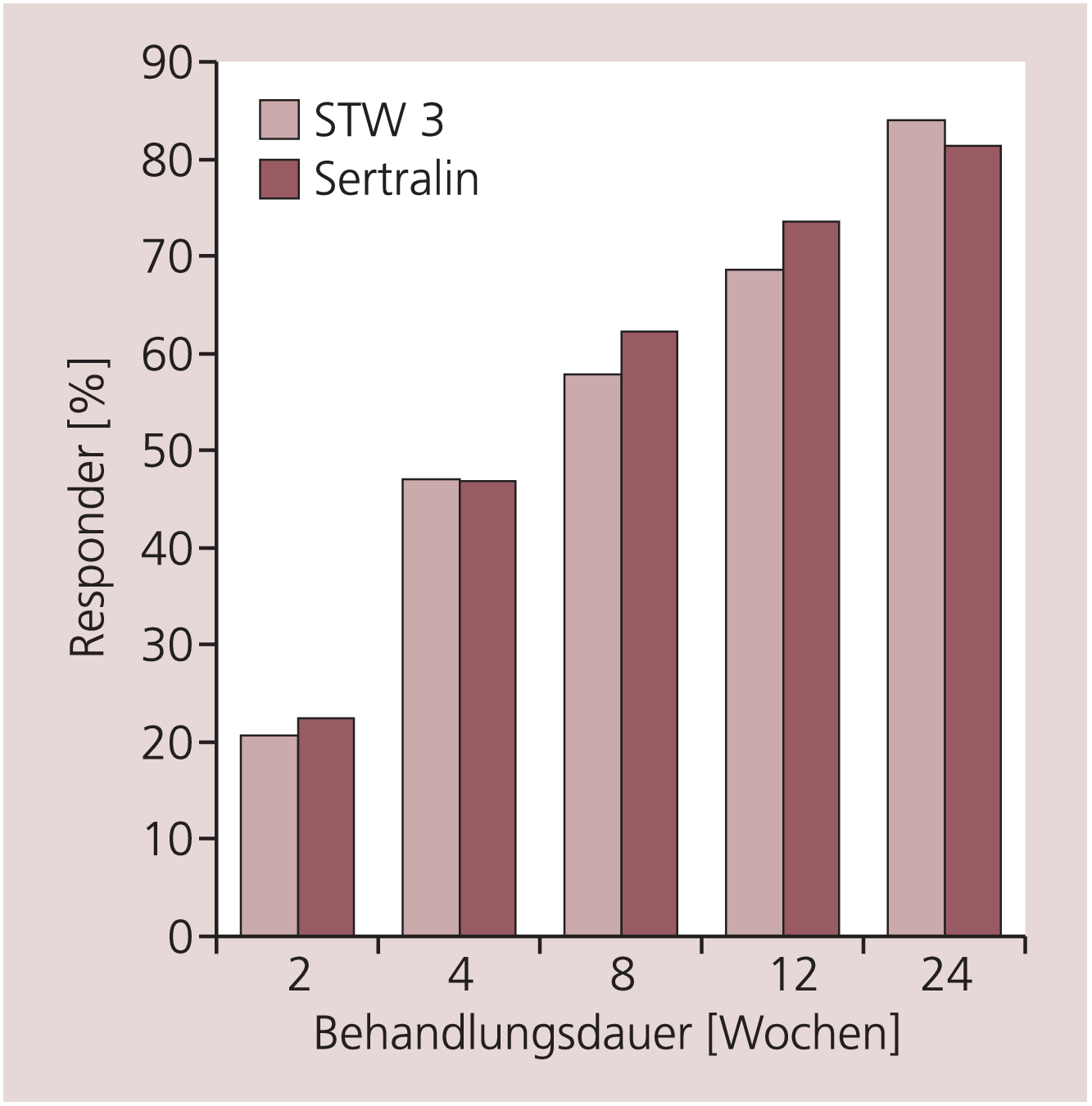
Abb. 2. Therapieresponder während der 24-wöchigen Arzneimitteltherapie (PP-Population, n=200). An Woche 24 nur Patienten mit Weiterbehandlung (n=157).
Einer weiteren Analyse wurden Patienten, die einen Rückfall erlitten, unterzogen. Als Rückfall galt nach einer positiven Therapieantwort innerhalb der ersten 12-wöchigen Therapiephase eine deutliche Steigerung des HAMD-Scores auf mindestens 16 Punkte in der zweiten Studienphase. Insgesamt kam es im PP-Kollektiv bei fünf Patienten zu einem Rückfall. Vier Rückfall-Patienten (5,0%) waren mit Sertralin, ein Patient (1,2%) mit Hypericum-Extrakt behandelt worden. Von diesen Patienten wurden alle bis auf einen (Sertralin-Gruppe) in der zweiten Studienphase medikamentös weiterbehandelt.
Befindlichkeits-Skala (Bf-S)
In den von den Patienten selbständig ausgefüllten Befindlichkeits-Skalen ergab sich in der Hypericum-Extrakt-Gruppe eine Verbesserung von 40,5±12,2 Punkten auf 19,8±13,7 nach 12 Wochen und auf 16,3±14,6 Punkte am Studienende. In der Sertralin-Gruppe nahm der Score von 42,4±12,0 Punkten auf 21,4±16,3 Punkte in Woche 12 und auf 18,6±15,8 Punkte nach 24 Wochen ab. Der Unterschied in den beiden Behandlungsgruppen war nicht signifikant (p=0,8915) für die PP- und die ITT-Population.
Clinical-Global-Impression(CGI)-Scores
Zum Zeitpunkt der Aufnahme in die Studie wurden 96,1% der Patienten der Hypericum-Extrakt-Gruppe und 96,9% der Patienten der Sertralin-Gruppe von den Prüfärzten als mäßig, deutlich oder (extrem) schwer krank unter dem Punkt „Schweregrad der Krankheit“ bewertet. Am Ende der Beobachtungszeit der ersten 12 Wochen fielen diese Werte auf 26,4% in der Hypericum-Extrakt-Gruppe und 34,7% in der Sertralin-Gruppe ab. Zwischen den beiden Behandlungsgruppen waren die Unterschiede nicht signifikant (p=0,2647). Nach 24 Wochen Behandlung waren 39 Patienten (48,1%) der Hypericum-Extrakt-Gruppe und 29 Patienten (36,3%) der Sertralin-Gruppe überhaupt nicht krank oder ein Grenzfall psychiatrischer Erkrankung. Bei Patienten ohne Weiterbehandlung in der Follow-up-Phase waren nach 24 Wochen 42,8% (Hypericum-Extrakt-Gruppe, n=9) und 44,5% (Sertralin-Gruppe, n=8) der Patienten überhaupt nicht krank oder ein Grenzfall psychiatrischer Erkrankung.
Die Auswertung der Scores zu den einzelnen Visiten ergab ebenfalls keine signifikanten Unterschiede zwischen den beiden Behandlungsgruppen.
Unter dem Gesichtspunkt „Beurteilung der Zustandsänderung“ wurde von den Prüfärzten nach 24 Wochen im Vergleich zum Studienbeginn 75,3% der Patienten in der Hypericum-Extrakt-Gruppe und 68,8% in der Sertralin-Gruppe als viel besser oder sehr viel besser eingestuft. Auch hier lagen keine nennenswerten Unterschiede zwischen den beiden Behandlungsgruppen vor.
Der auf die Arzneimittelwirkung bezogene therapeutische Effekt wurde unter dem Gesichtspunkt „Therapeutische Wirksamkeit“ von den Prüfärzten nach 12 Wochen als „sehr gut“ bei 54,9% der Hypericum-Extrakt-Gruppe und bei 50,0% der Sertralin-Gruppe beurteilt. Die Unterschiede zwischen den beiden Behandlungsgruppen waren nicht signifikant (p=0,3258). Die therapeutische Wirksamkeit der Studienmedikation wurde nach 24 Wochen Behandlung bei 69,1% der Hypericum-Extrakt-Gruppe und bei 63,8% der Sertralin-Gruppe mit „sehr gut“ dokumentiert.
Ergebnisse zur Sicherheit und Verträglichkeit
Bei 74 Patienten (60,2%) der Hypericum-Extrakt-Gruppe wurden 189 unerwünschte Ereignisse und bei 60 Patienten (50,8%) der Sertralin-Gruppe 112 unerwünschte Ereignisse dokumentiert. In einem möglichen oder wahrscheinlichen Zusammenhang mit der Studienmedikation standen unerwünschte Ereignisse bei 12 Patienten (9,8%) der Hypericum-Extrakt-Gruppe und bei 16 Patienten (13,6%) der Sertralin-Gruppe. Bei 5 Patienten der Hypericum-Extrakt-Gruppe und bei 10 Patienten der Sertralin-Gruppe (insgesamt 15 Patienten, 6,2%) führte das Ereignis zum Absetzen der Studienmedikation. Aus der Hypericum-Extrakt-Gruppe brach 1 Patient und aus der Sertralin-Gruppe brachen 2 Patienten die Studie wegen unerwünschter Ereignisse vorzeitig ab. Weitere Gründe, durch die ein vorzeitiger Studienabbruch ausgelöst wurde, sind in Tabelle 3 aufgeführt.
Tab. 3. Gründe für einen vorzeitigen Studienabbruch (Mehrfachnennungen möglich)
|
STW 3 |
Sertralin |
||||
|
n |
[%] |
n |
[%] |
||
|
Widerruf der Patienteneinwilligung |
Vor Woche 12 |
1 |
5,0 |
2 |
8,7 |
|
Nach Woche 12 |
2 |
6,9 |
0 |
0,0 |
|
|
Verschlechterung des Gesundheitszustandes |
Vor Woche 12 |
1 |
5,0 |
1 |
4,3 |
|
Nach Woche 12 |
1 |
3,4 |
0 |
0,0 |
|
|
Mangelnde Compliance des Patienten |
Vor Woche 12 |
7 |
35,0 |
6 |
26,1 |
|
Nach Woche 12 |
2 |
6,9 |
3 |
18,8 |
|
|
Auftreten nicht tolerabler UE |
Vor Woche 12 |
1 |
5,0 |
2 |
8,7 |
|
Nach Woche 12 |
0 |
0,0 |
0 |
0,0 |
|
|
Mangelnde Wirksamkeit der Studienmedikamente |
Vor Woche 12 |
1 |
5,0 |
0 |
0,0 |
|
Nach Woche 12 |
5 |
17,2 |
2 |
12,5 |
|
|
Verletzung der Ein- oder Ausschlusskriterien |
Vor Woche 12 |
2 |
10,0 |
2 |
8,7 |
|
Nach Woche 12 |
2 |
6,9 |
2 |
12,5 |
|
|
Tod eines Patienten |
Vor Woche 12 |
0 |
0,0 |
0 |
0,0 |
|
Nach Woche 12 |
1 |
3,4 |
0 |
0,0 |
|
|
Tod eines Prüfarztes |
Vor Woche 12 |
5 |
25,0 |
6 |
26,1 |
|
Nach Woche 12 |
5 |
17,2 |
3 |
18,8 |
|
|
Andere Gründe |
Vor Woche 12 |
2 |
10,0 |
4 |
17,4 |
|
Nach Woche 12 |
11 |
37,9 |
6 |
37,5 |
|
In beiden Behandlungsgruppen wurden während des Studienverlaufs jeweils drei schwerwiegende unerwünschte Ereignisse beobachtet: In der Hypericum-Extrakt-Gruppe kam es bei einem Patienten zur Prellung des Schulterblatts nach einem Sturz, ein Bezug zur Studienmedikation erschien unwahrscheinlich und die Behandlung wurde nicht unterbrochen; bei einem Patienten wurde bei Krankenhausaufnahme unter der Diagnose einer Somatisierungsstörung die Therapie abgebrochen; ein Patient mit Hypertonie verstarb an einer Hirnblutung, auch hier wurde kein Zusammenhang mit der Studienmedikation festgestellt. In der Sertralin-Gruppe wurde die Studienmedikation bei einem Patienten nach Aufnahme in eine psychosomatische Fachklinik beendet; bei einem Patienten kam es wegen einer Unterarmfraktur zu einer 3-tägigen stationären Behandlung, es wurde kein Zusammenhang zur Studienmedikation gesehen, wie auch bei einem Patienten mit anaphylaktischer Hautreaktion unbekannten Ursprungs, bei dem die Studie allerdings beendet wurde.
In den überwiegenden Fällen wurde die Verträglichkeit beider Studienmedikamente als „sehr gut“ oder „gut“ bewertet. Zum Therapieabbruch wegen schlechter Verträglichkeit kam es lediglich bei zwei Patienten aus der Sertralin-Gruppe und bei einem Patient aus der Hypericum-Extrakt-Gruppe. Eine mäßige oder schlechte Verträglichkeit lag während der ersten Behandlungsphase in der Hypericum-Extrakt-Gruppe maximal bei einem Patient (0,8%) und in der Sertralin-Gruppe bei sechs Patienten (5,1%) pro Visite vor (Abb. 3). Die in der CGI dokumentierten unerwünschten Wirkungen lagen pro Visite in der Hypericum-Extrakt-Gruppe bei einem Patient (0,8%) und in der Sertralin-Gruppe bei drei Patienten (2,5%).
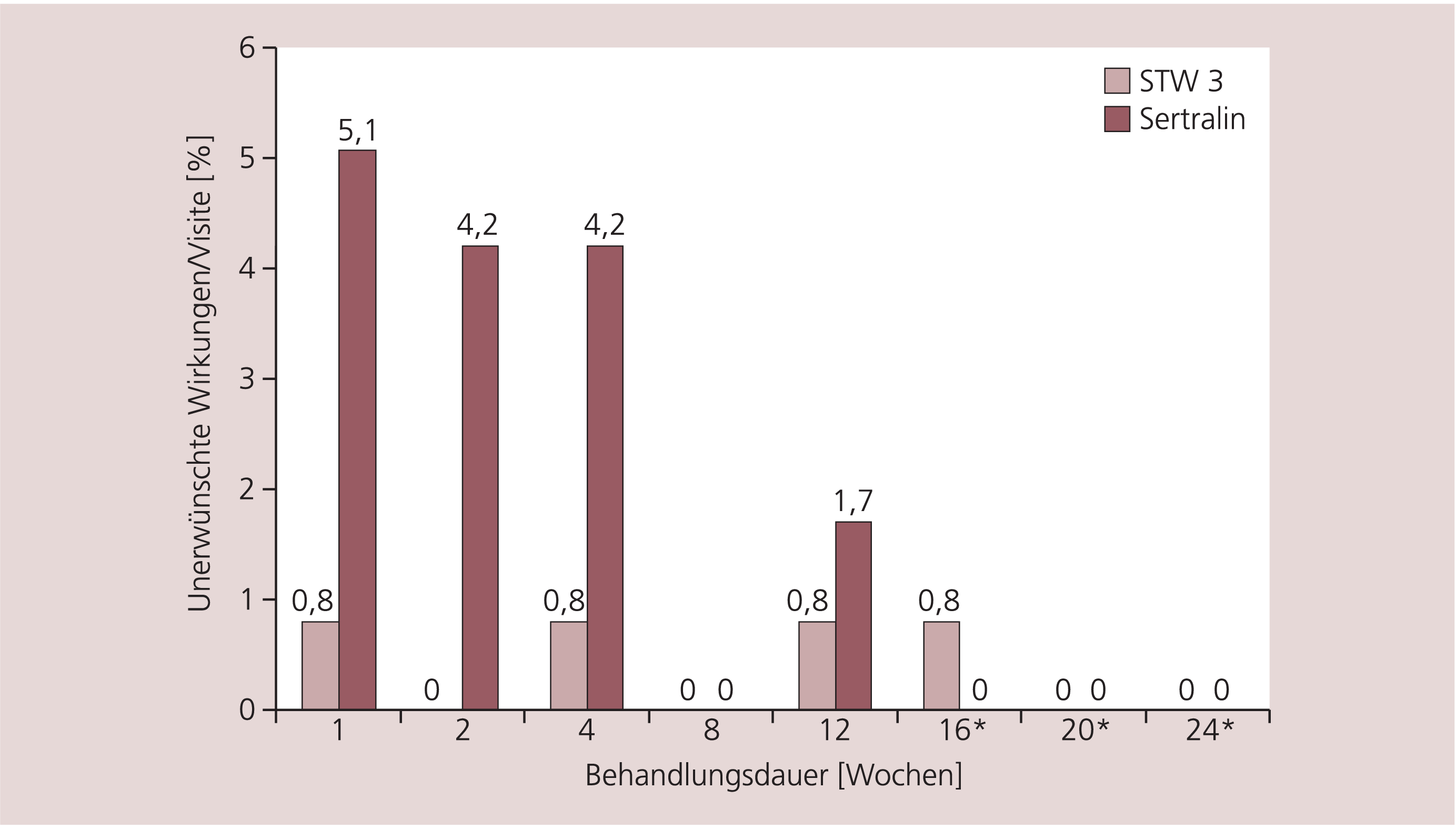
Abb. 3. Prozentuale Angabe der unerwünschten Wirkungen (CGI 3.2), die den Patienten wesentlich beeinträchtigten oder die therapeutische Wirkung überwiegen (ITT). Die Daten an Woche 12 und 24 wurden nach locf ermittelt.
* Patienten mit medikamentöser Weiterbehandlung
Wechselwirkungen mit Begleitmedikation wurde nicht dokumentiert.
Die Vital- und Laborwerte zeigten während der gesamten Studienzeit in beiden Behandlungsgruppen keine klinisch relevanten Änderungen.
Diskussion
In mehreren klinischen Plazebo- sowie Verum-kontrollierten Studien an über 3000 Patienten konnte in den letzten zehn Jahren die antidepressive Wirkung von Hypericum-Extrakt belegt werden [9, 14, 17, 21].
Frühere kontrollierte Studien wurden meist mit einer Mehrfachgabe der Hypericum-Extrakte und nicht länger als 12 Wochen durchgeführt. In der vorliegenden klinischen Prüfung konnte nun gezeigt werden, dass der Johanniskraut-Extrakt STW3 in einer täglichen Einmaldosierung über einen Behandlungszeitraum von bis zu sechs Monaten eine therapeutische Alternative zu den klassischen chemisch definierten Antidepressiva darstellt.
Als Vergleichsmedikament diente der selektive Serotonin-Wiederaufnahmehemmer Sertralin, der als Standard-Antidepressivum in der zu prüfenden Indikation gilt.
Das Ergebnis stimmt mit den Ergebnissen aus einer 6- und einer 12-wöchigen Vergleichsstudie zwischen Hypericum-Extrakt und Fluoxetin [19] oder Sertralin überein [5].
In einer früheren Untersuchung wurde die Wirksamkeit der Einmalgabe von Johanniskraut-Extrakt gezeigt. Rychlik et al. [18] erzielten bei leicht bis mittelschwer depressiven Patienten mit einer täglichen Einmal- (600 mg) oder Zweimalgabe (2 x 600 mg) von Johanniskraut-Extrakt eine übereinstimmende, signifikante Abnahme im HAMD-Score. Diese Ergebnisse wurden von Lemmer et al. [13] mit 3 x 300 mg Johanniskraut-Extrakt bestätigt. Für die wesentlichen wirksamkeitsmitbestimmenden Inhaltsstoffe von Johanniskraut-Extrakt, die Hypericine und das Hyperforin wurde eine lange Halbwertszeit von über 19 Stunden gezeigt [10, 22]. Diese Ergebnisse unterstützen das Dosisschema der täglichen Einmalgabe von Johanniskraut-Extrakt. Darüber hinaus fanden Yýldýz und Sachs [24] in ihrer Metaanalyse zur Wirksamkeit antidepressiver Medikamente keinerlei Vorteile der Mehrfachgabe gegenüber der Einmalgabe, selbst bei Wirkstoffen mit kurzen Halbwertszeiten (< 12 Stunden).
In einer Pilotstudie wurde gezeigt, dass die Wirkung von Johanniskraut-Extrakt der von Sertralin statistisch nicht unterlegen ist [2]. Bei leicht bis mittelschwer depressiven Patienten verminderte sich der HAMD-Score nach einer Behandlungsdauer von sieben Wochen in der mit Hypericum-Extrakt behandelten Patientengruppe von 21,3 auf 12,7 Punkte und auch in der Sertralin-Gruppe von 21,7 auf 12,5 Punkte signifikant. Diese Ergebnisse stimmen mit der vorliegenden Studie überein.
In einer anderen Plazebo-kontrollierten Vergleichsstudie wurde ebenfalls ein signifikanter Rückgang der HAMD-Werte in den Verum-Gruppen, Johanniskraut und Sertralin, beobachtet. Allerdings nahm auch der HAMD-Wert in der Plazebo-Gruppe deutlich ab, so dass nach acht Wochen weder Hypericum-Extrakt noch Sertralin Plazebo überlegen waren [7]. Dabei ist zu beachten, dass die Patienten aus psychiatrischen Ambulanzen stammten und mit einem Baseline-HAMD-Score zwischen 18 und 33 Punkten eingeschlossen wurden. Bei mehr als einem Drittel der Patienten dauerte die aktuelle Episode länger als zwei Jahre. Es scheint, dass sich die Patienten der amerikanischen Studie grundlegend von dem Kollektiv der mittelschwer depressiven Patienten im niedergelassenen Bereich unterscheiden, das in dieser Studie eingeschlossen wurde und für das die Behandlung mit Johanniskraut-Extrakt indiziert ist.
Außerdem ist nicht zu vergessen, dass nahezu 50% der Plazebo-kontrollierten Studien mit Antidepressiva ihr Ziel nicht erreichen und auch die Plazeboresponder-Raten abhängig von unterschiedlichen Einflüssen sehr variabel sein können.
Da es ethisch nicht vertretbar ist, Patienten während einer akuten Phase länger als sechs Wochen mit Plazebo zu behandeln, wurde in der vorliegenden Studie von einem zusätzlichen Plazebo-Arm abgesehen. Ein Vergleich mehrerer Plazebo-kontrollierter Hypericum-Studien zeigte, dass der kalkulatorische Arzneimitteleffekt in der Regel weniger als ein Drittel des therapeutischen Gesamteffekts beträgt [20]. Die persönliche Zuwendung des Arztes bei Gesprächen mit dem Patienten trägt einen maßgeblichen Anteil am Therapieerfolg, und so darf auch in dieser Studie ein möglicher Plazebo-Effekt nicht unberücksichtigt bleiben. Diesbezüglich kann aber bei der deutlichen Verbesserung des HAMD-Scores um etwa 14 Punkte nach 12 Wochen und sogar 17 Punkte nach 24 Wochen ein alleiniger Plazebo-Effekt ausgeschlossen werden.
In den überwiegenden Fällen wurde die Verträglichkeit der Studienmedikamente mit „gut“ oder „sehr gut“ bewertet, eine „mäßige“ oder „schlechte“ Verträglichkeit wurde nur in Ausnahmefällen beobachtet (maximal 5% der Patienten pro Visite). Unerwünschte Ereignisse mit mindestens möglichem Zusammenhang zur Prüfmedikation traten in der Sertralin-Gruppe etwas häufiger auf (13,6% vs. 9,8% in der Hypericum-Extrakt-Gruppe). Außerdem wurde in der Sertralin-Gruppe bei zwei Patienten ein Therapieabbruch wegen schlechter Verträglichkeit dokumentiert. Trotzdem erscheint die Nebenwirkungsrate von Sertralin niedriger als erwartet. Das kann an der relativ niedrigen Dosis für ambulante Patienten liegen, denn in zwei anderen Studien wurden höhere Tagesdosierungen (75–200 mg) verabreicht [7, 15]. Die Studie von Brenner et al. [2] hingegen zeigte gleich gute Verträglichkeit von Sertralin in der Dosierung 50 bis 75 mg und Johanniskraut-Extrakt.
Schlussfolgerung
In dieser ersten kontrollierten, doppelblinden, randomisierten, 24-wöchigen Multicenterstudie mit einem Johanniskrautpräparat in der täglichen Einmaldosierung konnte der Nachweis einer mit Sertralin vergleichbaren Wirksamkeit und Verträglichkeit erbracht werden. Die gleichwertige Wirksamkeit in der Akut- und Erhaltungstherapie und die gute Verträglichkeit machen den Hypericum-Extrakt STW3 bei Patienten mit mittelschweren Depressionen zu einem geeigneten Mittel in der ambulanten Therapie.
Literatur
1. Bracher A. Johanniskraut 1x täglich: Wirkung klinisch belegt/HYP611-Studie bestätigt Wirksamkeit. Verlagsbeilage Ärztliche Praxis 2001;5:1–4.
2. Brenner R, Azbel V. Comparison of an extract of hypericum (LI 160) and sertraline in the treatment of depression: a double-blind, randomised pilot study. Clin Ther 2000;22:411–9.
3. Demyttenaere K. Risk factors and predictors of compliance in depression. Eur Neuropsychopharmacol 2003;13:S69–S75.
4. Eisen SA, Miller DK, Woodward RS, Spitznagel E, et al. The effect of prescribed daily dose frequency on patient medication compliance. Arch Intern Med 1990;150:1881–4.
5. van Gurp G, Meterissian GB, Haiek LN, McCusker J, et al. St. John’s wart or sertraline? Randomized controlled trial in primary care. Can Fam Physician 2002;48:905–12.
6. Hübner WD, Arnoldt KH. Johanniskraut – Einjahresstudie. Z Phytother 2000;21:306–10.
7. Hypericum depression trial study group. Effect of hypericum perforatum (St. John´s wart) in major depressive disorders – a randomized controlled trial. JAMA 2002;287:1807–14.
8. Kalb R, Trautmann-Sponsel RD, Kieser M. Efficacy and tolerability of hypericum extract WS 5572 versus placebo in mildly to moderately depressed patients. A randomized double-blind multicenter clinical trial. Pharmacopsychiatry 2001;34:96–103.
9. Kasper S. Hypericum perforatum – a review of clinical studies. Pharmacopsychiatry 2001;34(Suppl 1):51–5.
10. Kerb R, Brockmoller J, Staffeldt B, Ploch M, et al. Single-dose and steady-state pharmacokinetics of hypericin and pseudohypericin. Antimicrob Agents Chemother 1996;40:2087–93.
11. Kötter HU, Möller HJ, Hampel H. Sertralin: Ein moderner selektiver Serotonin-Wiederaufnahmehemmer in der antidepressiven Therapie. Arzneimitteltherapie 1999;17:395–401.
12. Laux G, Dietmaier O, König W. Pharmakopsychiatrie. München, Jena: Urban & Fischer Verlag, 2000.
13. Lemmer W, Von den Driesch V. Klieser E. Johanniskraut-Spezialextrakt WS 5572 bei leichter bis mittelschwerer Depression. Wirksamkeit und Verträglichkeit von Neuroplant 300 Filmtabletten. Fortschr Med Orig 1999;117:143–54.
14. Linde K, Ramirez G, Mulrow CD, Pauls A, et al. St. John’s wart for depression (Cochrane Review). In: The Cochrane Library, Issue 3, 2003. Oxford: update software – an overview and meta-analysis of randomised clinical trials. BMJ 1996;313:253–8.
15. Moscovitch A, Blashko CA, Eagles JM, Darcourt G, et al. A placebo-controlled study of sertraline in the treatment of outpatients with seasonal affective disorder. Psychopharmacology 2003:[Epub ahead of print].
16. Philipp M, Kohen R, Hiller KO. Hypericum extract versus imipramine or placebo in patients with moderate depression: randomised multicenter study of treatment for eight weeks. BMJ 1999;319:1534–9.
17. Röder C, Schaefer M, Leucht S. Meta-Analyse zu Wirksamkeit und Verträglichkeit der Behandlung der leichten und mittelschweren Depression mit Johanniskraut. Fortschr Neurol Psychiatr 2004;72:330–43.
18. Rychlik R, Siedentop H, von den Driesch V, Kasper S. St. John’s wart extract WS 5572 in minor to moderately severe depression. Effectiveness and tolerance of 600 and 1 200 mg active ingredient daily. Fortschr Med Orig 2001;119:119–28.
19. Schrader E. Equivalence of St. John’s wart extract (Ze 117) and fluoxetine: a randomized, controlled study in mild-moderate depression. Int Clin Psychopharmacol 2000;15:61–8.
20. Schulz V. The psychodynamic and pharmacodynamic effects of drugs: A differenciated evaluation of the efficacy of phytotherapy. Phytomed 2000;7:73–81.
21. Schulz V. Klinische Studien mit Hypericum-Extrakten bei Patienten mit Depressionen. Z Phytother 2002;23:11–5.
22. Schulz H-U, Schürer M, Bässler D, Weiser D. Investigation of the bioavailability of hypericin, pseudohypericin, hyperforin and the flavonoids quercetin and isorhamnetin following single and multiple oral dosing of a hypericum extract containing tablet. Drug Res 2005;1:15–22.
23. Vorbach EU, Hübner WD, Arnoldt KH. Wirksamkeit und Verträglichkeit des Hypericum-Extraktes LI 160 im Vergleich mit Imipramin. Nervenheilkunde 1993;12:290–6.
24. Yyldyz A, Sachs GS. Administration of antidepressants. Single versus split dosing: a meta-analysis. J Affect Disord 2001;66:199–206.
Prof. Dr. Markus Gastpar, Rheinische Kliniken, Klinik für Psychiatrie und Psychotherapie, Universität Duisburg-Essen, Postfach 10 30 43, 45030 Essen
Dr. Karin Zeller, Leiterin Medizinische Information und Klinische Forschung, Steigerwald Arzneimittelwerk GmbH, Havelstraße 5, 64297 Darmstadt, E-Mail: zeller@steigerwald.de
Comparison of hypericum extract STW3 and sertraline in the treatment of moderate depression: a double-blind randomized 24-week-study
The objective of this double-blind, randomised, multicenter clinical study was to demonstrate the efficacy and tolerability of the hypericum extract STW3 in acute and maintenance therapy over the recommended period of up to six months in outpatients with moderate depression. Sertraline was used as the comparative drug.
241 outpatients with moderate depression were included in this study. According to the study protocol, 200 patients were treated at least for 12 weeks with a once daily dosage of 612 mg hypericum extract or 50 mg sertraline. Beyond, 161 patients were treated after week 12 for additional 12 weeks. The course of depression was documented by use of the Hamilton Depression Scale (HAMD), the Adjective Mood Scale (BfS), and the Clinical Global Impression (CGI) Scale.
From almost identical initial values (22.0 and 22.1 points) the HAMD score was reduced to 8.3 points in patients treated with hypericum and to 8.1 points in patients treated with sertraline after the first 12 week treatment period (primary endpoint). This significant decrease demonstrated non-inferiority of hypericum extract STW3 versus sertraline (p < 0.0001). After 24 weeks treatment the HAMD score was reduced to 5.7 points and to 7.1 points, respectively.
After 12 weeks treatment, 68.6% of the patients in the hypericum group and 70.4% in the sertraline group were assessed as therapy responders, after 24 weeks 84.0% or 81.3%, respectively. The analysis of the other secondary endpoints confirmed these findings.
In most cases, the investigators assessed the tolerability of hypericum extract and sertraline as “good” or “very good”. The results of the study indicate that hypericum extract STW3 is therapeutically non-inferior to sertraline and that it is a well-tolerated drug for the treatment of moderate depression.
Keywords: St John’s wort, selective serotonin reuptake inhibitor, depression, clinical trial, long-term therapy
Psychopharmakotherapie 2005; 12(04)
