Heinz Reichmann, Dresden
Die Diagnose eines idiopathischen Parkinson-Syndroms ist nach wie vor insbesondere vom klinischen Untersuchungsbefund abhängig. Die typischen Kardinalsymptome sind neben der Akinese, die nach den Kriterien der British Brain Bank immer vorhanden sein muss, der Tremor sowie der Rigor und die posturale Instabilität [4]. Bradykinese äußert sich zu Beginn der Erkrankung meist darin, dass die Patienten beim Gehen einen ihrer Arme nicht richtig mitschwingen, dass das Schriftbild klein und krakelig wird. Der Tremor äußert sich insbesondere bei Aufregung, psychischer und physischer Anspannung. Beim Froment-Manöver soll der Patient einseitig ein rasches repetitives Tippen des Zeigefingers gegen den Daumen durchführen. Dies fördert in der zu untersuchenden kontralateralen Hand den Rigor besser zutage. Die posturale Instabilität oder Stabilität wird durch den so genannten Zugtest geprüft, wo sich der Untersucher hinter den Patienten stellt und diesen nach Vorwarnung nach hinten oder nach vorn und zur Seite stößt. Zusätzlich zu diesen Symptomen fallen sehr häufig eine Hypomimie, eine Seborrhö, eine Sialorrhö, eine Volumenminderung der Sprache sowie ein kleinschrittiges Gangbild mit Trippelschritten auf [3]. Neben den klassischen vier Symptomen gibt es häufig für den Patienten genauso beschwerliche Begleitsymptome aus dem psychiatrischen Fachgebiet, nämlich unbestimmte Angst, Depression und Demenz. Viele Patienten weisen Störungen des autonomen Nervensystems, eine Schlafstörung und insbesondere, wie die eigene Arbeitsgruppe nachweisen konnte, eine Riechstörung auf [5, 6, 8].
Frühe Symptome der Parkinson-Erkrankung bestehen in der Obstipation, einer Schriftbildveränderung (klein, unleserlich, krakelig, schräg gestellt), Störung des Farbkontrastsehens (z. B. Verschwimmen von zwei eng aneinander gemalten roten Balken), Riechstörung, Auftreten von Ruhetremor unter Provokation (psychischer oder physischer Stress), aber auch Symptome wie Spannungskopfschmerz, Schulter-Arm-Schmerzen, „Herz“-Schmerzen sowie Lumbago.
Wir selbst favorisieren die Riechstörung als das erste nachweisbare Parkinson-Symptom, nach dem wir in der eigenen Praxis bei über 90 % der Parkinson-Patienten eine Hyposmie bis Anosmie feststellen konnten [5, 6]. Diese Untersuchungen werden mit Riechstiften (so genannten „sniffing sticks“) durchgeführt. Hierbei wird die Riechschwelle getestet, wobei einer von drei Stiften einen Geruchsstoff enthält. Es wird die Diskrimination geprüft, indem zwei Stifte eines Tripletts gleich riechen, sowie die Identifikation von vorgegebenen Gerüchen dahingehend getestet, dass man unter schriftlich vorgegebenen Duftstoffen den gerochenen auswählen muss. Insgesamt kann man beim Riechtest 48 Punkte erreichen, wobei alle Punktwerte unter 30 einer Hyposmie und alle unter 15 einer funktionellen Anosmie entsprechen. Müller et al. [5] konnten bei über 50 Patienten mit Parkinson-Syndrom und atypischen Parkinson-Syndromen nachweisen, dass typischerweise Patienten mit idiopathischem Parkinson-Syndrom am schlechtesten riechen können und dass Patienten mit Multisystematrophie initial und solche mit progressiver supranukleärer Lähmung, kortikobasaler Degeneration und essenziellem Tremor dagegen normal riechen können. Somit kommt dieser Riechuntersuchung zum Teil eine differenzialdiagnostisch hohe Wertigkeit zu. Die Basisdiagnostik sollte, wie bereits erwähnt, in einer sorgfältigen klinischen Untersuchung bestehen, wobei es sich anbietet, operationalisierte und standardisierte Tests wie beispielsweise die Unified Parkinson’s Disease Rating Scale (UPDRS), die Webster-Skala, Schwab- und England-Skala und andere zu verwenden, um zum Beispiel Verlaufskontrollen zu gewährleisten.
Sehr wertvoll ist der Levodopa-Test, bei dem meist 200 mg Levodopa aufgelöst dem Patienten zum Trinken angeboten werden und wo etwa 30 bis 60 Minuten später eine 30%ige Verbesserung der Motorik verlangt wird, um die Verdachtsdiagnose eines idiopathischen Parkinson-Syndroms unterstützen zu können.
Der Apomorphin-Test besteht in subkutaner Applikation des rasch wirkenden Dopamin-Agonisten Apomorphin, wobei wegen seiner starken emetischen Wirkung eine Vorbehandlung mit Domperidon unabdingbar ist. Der Apomorphin-Test wird sehr unterschiedlich durchgeführt [z. B. 2]. Meist beginnt man mit 2 mg und steigert bis allenfalls 8 mg unter kontinuierlicher Evaluation mittels einer der oben genannten motorischen Skalen.
Die Laboruntersuchungen beim Parkinson-Syndrom können auf die Analysen von Elektrolyten, Kupfer, Coeruloplasmin, Schilddrüsenhormonen und Leberenzymen reduziert und beschränkt werden. Diese Untersuchungen sind somit kein hoher Kostenfaktor. Wichtig aus unserer Sicht ist, dass jeder Parkinson-Patient eine Bildgebung erhalten sollte, bevorzugt ein kranielles MRT, alternativ dazu ein kranielles Computertomogramm. Diese Untersuchung ist nicht zur Bestätigung des idiopathischen Parkinson-Syndroms notwendig, sondern vielmehr zum Ausschluss atypischer Parkinson-Syndrome. Typischerweise weisen beispielsweise Patienten mit Multisystematrophie Typ C eine Kleinhirnatrophie und Hirnstammverschmächtigung und Patienten mit progressiver supranukleärer Lähmung das so genannte Mickey-Mouse-Zeichen des Hirnstamms auf (Nähreres dazu in einem Beitrag von Geser und Wenning im nächsten Heft). Wichtig ist auch der Ausschluss eines Normaldruckhydrozephalus und einer subkortikalen arteriosklerotischen Enzephalopathie.
Eine Methode, die zunächst nicht auf Anerkennung stieß, ist die sonographische Parenchymdarstellung des Hirnstamms sowie der Basalganglien (Abb. 1). Becker war der erste, der nachweisen konnte, dass in der Substantia nigra bei Parkinson-Patienten aufgrund des Eisens eine vermehrte Hyperechogenität besteht [2]. Viele Nachuntersuchungen, auch in der eigenen Klinik, bestätigten die Beobachtungen von Becker und dienen uns heute zur Frühdiagnostik des Parkinson-Syndroms, wo wir sehr häufig kontralateral zur betroffenen Seite eine vermehrte Hyperechogenität der Substantia nigra feststellen können.
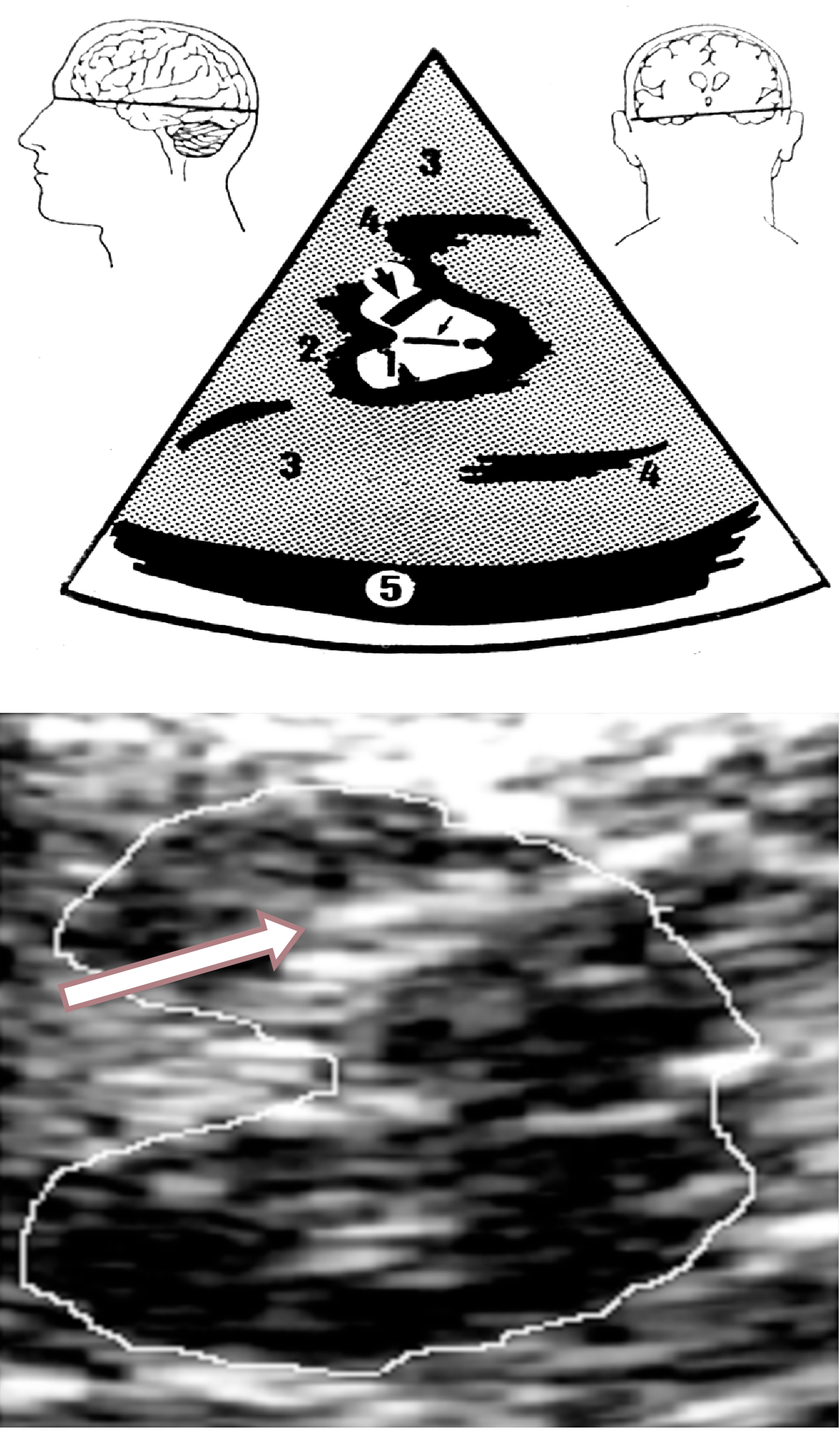
Abb. 1. Parenchym-Sonographie der Substantia nigra mit einseitig ausgeprägter Hyperechogenität. Im oberen Teil der Abbildung ist ein Schema des Hirnstammes mit schwarz markierter Substantia nigra. Im unteren Teil der Abbildung findet sich ein typischer Befund eines idiopathischen Parkinson-Syndroms.
Speziell beim idiopathischen Parkinson-Syndrom vom Tremor-Dominanz-Typ kommt es immer wieder zu schwierigen differenzialdiagnostischen Überlegungen bezüglich eines essenziellen Tremors. Hier und zur Diagnosebestätigung eines idiopathischen Parkinson-Syndroms hat sich der Dopamin-Transporter-Scan, ein SPECT-Verfahren, hervorragend bewährt [7]. In unserer Klinik werden die Patienten vor dieser Untersuchung mit einer Schilddrüsenblockade versehen und dann wird Iod-markiertes β-CIT ([123I]2β-Carboxymethoxy-3β[4-iodophenyl]tropan) intravenös appliziert und drei bis sechs Stunden nach dieser Injektion der Dopamin-Transporter bestimmt. Davor sind alle Parkinson-Medikamente, die Einfluss auf diesen Dopamin-Transporter nehmen, wie beispielsweise Modafinil oder Serotonin-Wiederaufnahmehemmer, abzusetzen. Erfreulicherweise müssen Levodopa und Dopamin-Agonisten nicht abgesetzt werden. Die Dopamin-Rezeptoren können ebenfalls mit einer SPECT-Methode, nämlich dem IBZM-SPECT, untersucht werden. Hier müssen interferierende Dopamin-Agonisten und Neuroleptika abgesetzt werden, wohingegen Levodopa keinen Einfluss auf die Untersuchungsmethode aufweist.
Kostspieliger sind Untersuchungen mittels PET-Verfahren, die aber noch eine bessere Trennschärfe aufweisen. Die Strahlenbelastung entspricht etwa dem, was normalerweise pro Jahr aus der Atmosphäre an Strahlenbelastung auf uns einströmt. Die Gesamtuntersuchungskosten bewegen sich um etwa 1000 bis 1200 Euro pro Untersuchung.
Etwas weniger ergiebig sind quantitative Tremoranalysen mittels Oberflächenelektroden oder einem Akzelerometer, die mit einem gängigen Elektromyographiegerät durchgeführt werden können. Bei diesen Analysen wird insbesondere die häufig auftretende Tremorfrequenz gemessen; bei einer Frequenz von 4 bis 6 Hz kann ein idiopathisches Parkinson-Syndrom festgestellt werden. Höhere Frequenzen zwischen 10 und 12 Hz entsprechen eher einem essenziellen Tremor, so dass im Idealfall durch die quantitative Tremoranalyse eine Differenzialdiagnose gelingt.
Im Verlaufe der Parkinson-Krankheit können Analysen des autonomen Nervensystems wertvolle diagnostische und therapeutische Ansätze liefern. Bei Parkinson-Patienten treten Störungen des kardiovaskulären, sekretosudomotorischen, gastrointestinalen, urogenitalen, neuroendokrinologischen Systems sowie des Schlafs auf. Je nach Studie wird berichtet, dass 14 bis 80 % der Parkinson-Patienten eine autonome Funktionsstörung haben und dass dies bei 50 % der Patienten mit subjektiven Beeinträchtigungen im Alltag verbunden ist. Problematisch bezüglich der Störungen des autonomen Nervensystems ist, dass sie nicht nur im Rahmen eines idiopathischen Parkinson-Syndroms auftreten können, sondern eine davon unabhängige Dysfunktion des autonomen Nervensystems darstellen können, dass sie im Rahmen einer anderen Grunderkrankung, wie beispielsweise dem Diabetes mellitus, auftreten können, dass sie Ausdruck eines atypischen Parkinson-Syndroms sind und dass sie letzten Endes auch als Nebenwirkungen von Antiparkinson- oder anderer Therapie auftreten können. Bei uns im Labor spielen Untersuchungen der Kreislaufregulation deswegen eine besonders große Rolle, weil die Patienten sehr häufig über Schwindel beim raschen Aufstehen, Fallneigung und Stürze klagen. Für den Orthostase-Test benutzen wir den Kipptisch, mit dem Patienten relativ rasch um 60° nach oben gekippt werden. Hier sollte eine nicht zu starke Senkung des systolischen und diastolischen Blutdrucks bei guter Gegenregulation durch Tachykardie festgestellt werden können. Patienten mit Störungen des autonomen Nervensystems weisen sehr starke Blutdruckabfälle sowie eine nur geringe Steigerung der Herzfrequenz auf. Das urogenitale System ist bei vielen Parkinson-Patienten im Sinne eines imperativen Harndrangs gestört, wobei auch eine Pollakisurie aufgrund ungehemmter Detrusorkontraktion mit zum Teil unwillkürlichem Harnabgang bei schon kleinen Füllungsmengen festgestellt werden kann. Hier helfen Parasympathikolytika weiter, die den Blasendom etwas ruhig stellen, konkret Imipramin (z. B. Tofranil®) 50 bis 100 mg, Oxybutynin (Dridase®) 10 bis 15 mg pro Tag oder Tolterodin (Detrusitol®) 2 x 1 Tablette. Potenzstörungen werden mit den modernen Medikamenten wie beispielsweise Sildenafil (Viagra®) oder Tadalafil (Cialis®) behoben.
Literatur
1. Becker G, Seufert J, Bogdahn U, Reichmann H, et al. Degeneration of substantia nigra in chronic Parkinson’s disease visualized by transcranial color-coded real-time sonography. Neurology 1995;45:182–4.
2. Gasser T, Schwarz J, Arnold G, Trenkwalder C, et al. Apomorphine test for dopaminergic responsiveness in patients with previously untreated Parkinson’s disease. Arch Neurol 1992;49:1131–4.
3. Gerlach M, Reichmann H, Riederer P (editors). Die Parkinson Krankheit. Wien New York: Springer-Verlag, 2003.
4. Hughes AJ, Daniel SE, Kilford L, Lees AJ. Accuracy of clinical diagnosis of idiopathic Parkinson’s disease: a clinico-pathological study of 100 cases. J Neurol Neurosurg Psychiatry 1992;55:181–4.
5. Mueller A, Reichmann H, Livermore A, Hummel T. Olfactory function in idiopathic Parkinson’s disease (IPD): results from cross-sectional studies in IPD patients and long-term follow-up of de-novo IPD patients. J Neural Transm 2002;109:805–11.
6. Mueller A, Abolmaali N, Hummel T, Reichmann H. Riechstörungen – ein frühes Kardinalsymptom des idiopathischen Parkinson-Syndroms. Akt Neurol 2003;30:239–43.
7. Schwarz J, Storch A, Koch W, Pogarell O, et al. Loss of dopamine transporter binding in Parkinson’s disease follows a single exponential rather than linear decline. J Nucl Med 2004;45:1694–7.
8. Sommer U, Hummel T, Cormann K, Mueller A, et al. Detection of presymptomatic Parkinson’s disease: Combining smell tests, transcranial sonography, and SPECT. Mov Disord 2004;19:1196–1202.
Prof. Dr. med. Heinz Reichmann, Klinik und Poliklinik für Neurologie, Universitätsklinikum Carl Gustav Carus, Technische Universität Dresden, Fetscherstr. 74, 01307 Dresden
Diagnosis of idiopathic Parkison’s syndrome
Even today the most useful diagnostic procedure to detect idiopathic Parkinson’s syndrome is clinical examination and search for olfactory malfunction, bradykinesia, rigidity, resting tremor and postural instability. Clinical test like the levo-dopa and apomorphine tests are performed to study improvement of UPDRS. Useful apparative tests are cranial MRI to differentiate idiopathic Parkinson’s disease from atypical forms and some laboratory investigations. In some cases parenchymal sonography of substantia nigra, radioactive tests for dopamine metabolism, dopamine transporter and dopamine receptors and quantitative analyses of gait and tremor may be performed to establish diagnosis.
Keywords: Idiopathic Parkinson’s syndrome, diagnosis, smell impairment, parenchymal sonography, tremor analysis
Psychopharmakotherapie 2005; 12(01)
