Simon Faissner und Ralf Gold, Bochum
Die multiple Sklerose (MS) ist eine chronisch entzündliche Erkrankung des Zentralnervensystems (ZNS), die durch Demyelinisierung und damit einhergehend axonalen Schaden mit Neurodegeneration gekennzeichnet ist [12]. Die Erkrankung manifestiert sich bei 85 % der Patienten als schubförmig-remittierende Form (RRMS), die durch fast 20 Medikamente unterschiedlicher Wirkstärke, mit unterschiedlichen Wirkungsmechanismen sowie differierenden Applikationsintervallen und -wegen mittlerweile gut behandelt werden kann. Ohne die Einleitung einer Immuntherapie kommt es bei der Hälfte der Patienten nach 15 bis 20 Jahren zu einem sekundär-chronisch progredienten Verlauf der Erkrankung [30], bei dem die Schubaktivität in den Hintergrund gerät und die Zunahme schleichender Behinderung vordringlich wird. Ein geringer Anteil von 10 bis 15 % der Patienten hat von Beginn an einen primär-progredienten Verlauf (PPMS), bei dem keine Schubaktivität abgegrenzt werden kann. Durch Änderung der MS-Diagnosekriterien und bessere diagnostische Möglichkeiten werden Patienten zunehmend früher diagnostiziert [24], sodass die Einleitung einer Immuntherapie eher gelingen kann. Ein erstes demyelinisierendes klinisches Ereignis (klinisch isoliertes Syndrom [KIS]), bei dem die MS-Diagnose noch nicht gestellt werden kann, kann bereits mittels Immuntherapie behandelt werden.
Die Veränderung der Diagnosekriterien und die besseren therapeutischen Möglichkeiten haben dazu geführt, dass Patienten nach ihrer Diagnose heutzutage deutlich später bestimmte Behinderungsmeilensteine erreichen. So wurde ein EDSS (Expanded disability status score) von 3,0, einer moderaten Behinderung entsprechend, bei einem 20-Jährigen, der 1995 diagnostiziert wurde, in etwa 54 % der Fälle schon im Alter von 26 Jahren erreicht; nach 20 Jahren lag die Wahrscheinlichkeit bei 79 %. Bei der Diagnose im Jahr 2017 haben rechnerisch nach 20 Jahren erst 33 % der Patienten einen EDSS von 3,0 erreicht [24]. Durch die Verfügbarkeit von abgestuft effektiven Substanzen gab es in den letzten Jahren zunehmend eine Diskussion über deren definierte Anwendung. So ist insbesondere die Einteilung von Immuntherapien und die Entscheidung über Therapieabfolgen in den letzten Jahren in Deutschland kontrovers diskutiert worden [31].
Durch Daten aus großen Registerstudien hat sich in den letzten Jahren die Erkenntnis durchgesetzt, dass die frühe Einleitung einer Immuntherapie langfristig das Risiko reduzieren kann, Krankheitsprogression zu erfahren [15]. Außerdem gibt es immer bessere Untersuchungen, die einen Vorteil einer frühen hoch-effektiven Immuntherapie gegenüber der primären Einleitung mit einer Basistherapie zeigen [25].
Im Folgenden werden die Empfehlungen für unterschiedliche Szenarien und Fragen beleuchtet:
- Klinisch isoliertes Syndrom (KIS)
- Schubförmig-remittierende MS
- Entscheidungsalgorithmus für die Einleitung einer Immuntherapie
- Sekundär-chronisch progrediente (SP) und primär progrediente (PP) MS
- Sequenzierung von Immuntherapien
- Deeskalation und Therapie in der Schwangerschaft
Klinisch isoliertes Syndrom (KIS)
Mittlerweile gilt es als gut etabliert, dass eine Immuntherapie früh im Erkrankungsverlauf initiiert werden sollte, um das Risiko zu verringern, dass sich nach einem erstmaligen demyelinisierenden Ereignis eine definitive MS entwickelt. In Barcelona wurde eine Kohorte von 401 Patienten über mindestens 10 Jahre nachverfolgt (Durchschnitt 14,4 Jahre). Patienten, die innerhalb von vier Monaten nach einem ersten demyelinisierenden Ereignis behandelt wurden, hatten ein signifikant reduziertes Risiko, einen EDSS von 3,0 zu entwickeln, gegenüber Patienten, die erst nach einem zweiten Schubereignis im Median 36 Monate nach dem ersten Ereignis behandelt wurden (adjustiertes Hazard-Ratio [aHR] 0,4; 95%-Konfidenzintervall [KI] 0,2–0,7) [27]. Eine höhere T2-Läsionslast war mit einem höheren Risiko der Transition zu einer MS sowie früherem Risiko einer irreversiblen Behinderung assoziiert. Der Cut-off lag bei 20 Läsionen und zwei Kontrast-aufnehmenden Herden. Patienten mit einem KIS sollten daher eine Immuntherapie erhalten. Zugelassen sind hierfür Interferone und Glatirameracetat. Trotzdem kann es abhängig von dem Risiko einer Behinderungsprogression bzw. der Transition zu einer MS notwendig sein, schon bei einem KIS höher aktive Immuntherapien einzusetzen [31]. Auch Dimethylfumarat und Teriflunomid werden entsprechend der Leitlinie bereits beim KIS eingesetzt [17]. Die Entscheidung sollte unter anderem davon abhängig gemacht werden, ob es sich um ein mono- oder multifokales Ereignis handelt, wie hoch die Läsionslast ist und ob ein höheres Risiko für Behinderungszunahme besteht (z. B. bei infratentoriellen Läsionen).
Schubförmig-remittierende MS
Um die Stufentherapie der RRMS ist in den letzten Jahren eine lebhafte Diskussion im deutschsprachigen Raum entstanden. Dies bezieht sich auf die letzte Aktualisierung der Leitlinie zur MS-Therapie, die – anders als die europäischen Leitlinien – mehrere Eskalationsstufen bei Immuntherapien vorsieht. So werden folgende Kategorien unterschieden [17]:
- Bei einem klinisch isolierten Syndrom Wirkstoffe der Kategorie 1: Dimethylfumarat, Glatirameracetat, Interferon beta, Teriflunomid
- Bei einer RRMS Kategorie 2: Cladribin, Fingolimod, Ozanimod
- Bei hochaktiver RRMS Kategorie 3: Alemtuzumab, Natalizumab, Ocrelizumab, ggf. Rituximab
Die europäischen Leitlinien von ECTRIMS/EAN nehmen keine derart klare Kategorisierung vor, da sie ja auch strukturell schlechtere Länder mitberücksichtigen [22]. Hier wird vielmehr empfohlen, aus dem breiten therapeutischen Spektrum von Medikamenten zu wählen und die Entscheidung anhand von Patientencharakteristika und Komorbiditäten, der Erkrankungsschwere und -aktivität, dem Sicherheitsprofil des Medikaments sowie dem Zugang zur Therapie zu treffen [22] (Consensus Statement). Diese Herangehensweise wird auch von dem „White Paper“ aus dem deutschsprachigen Raum getragen, bei dem eine Unterscheidung in die Kategorien mild/moderat sowie hocheffektive Erst- und Zweitlinientherapien getroffen wird [31] und die auch von den Autoren dieses Manuskripts unterstützt wird (Tab. 1).
- Substanzen der Kategorie mild/moderat umfassen Dimethylfumarat, Diroximelfumarat, Glatirameracetat, Interferone, Teriflunomid und formal Azathioprin (Letzteres wird heutzutage nur noch selten aufgrund der guten Therapiealternativen für die MS-Behandlung eingesetzt, v. a., wenn eine Neuromyelitis-optica-Spektrumserkrankung als Differenzialdiagnose in Frage kommt)
- Hochaktive Substanzen für die Erst- und Zweitlinie:
- Kontinuierliche Therapien: Natalizumab, Ofatumumab, Fingolimod, Ozanimod, Ponesimod
- Gepulste Therapien: Alemtuzumab, Cladribin, Ocrelizumab
Tab. 1. Einsatz von Immuntherapien bei unterschiedlichen MS-Verlaufsformen (adaptiert nach [31])
|
Schubförmige MS (RMS) |
Progrediente MS (PMS) |
||||
|
Klinisch isoliertes Syndrom |
RRMS |
SPMS |
PPMS |
||
|
(Hoch-)aktive Verlaufsformen |
Gepulste Therapien:
Kontinuierliche Therapien:
|
Mit Schüben
|
Ohne Schübe, mit MRT-Aktivität
|
Mit klinischer/MRT-Aktivität
|
|
|
Milde/moderate Verlaufsformen |
|
|||
S1P: Sphingosin-1-phosphat
Zunächst einmal ist es unstrittig, dass die Einleitung einer Immuntherapie Patienten mit einer RRMS angeboten werden sollte. Alle verfügbaren Immuntherapien waren in den Zulassungsstudien wirksam, entweder gegenüber Placebo oder gegenüber einem aktiven Komparator, gemessen hinsichtlich einer Reduktion von Schubaktivität sowie kernspintomographischer entzündlicher Aktivität [31]. Außerdem konnte in einem Teil der Studien eine Wirkung hinsichtlich der Reduktion von Behinderungsprogression nachgewiesen werden. Neben der klinischen Wirksamkeit von Immuntherapien der ersten, zweiten sowie ab 2010 dritten Generation von Immuntherapien konnte über viele Jahre auch eine gute Evidenz hinsichtlich des Sicherheitsprofils generiert werden (für ausführliche Übersichtsarbeiten siehe [7, 8]). Durch die Einleitung einer Immuntherapie soll inflammatorische Aktivität reduziert und dadurch die neuronale Reserve erhalten bleiben [31]. Auch das Risiko einer Konversion zu einer SPMS wird durch die frühe Einleitung einer Immuntherapie reduziert [1]. Entscheidend bei der Einleitung einer Immuntherapie ist, dass Patienten an einem erfahrenen Zentrum behandelt werden, bei dem eine adäquate Infrastruktur vorgehalten wird, die Erkrankung gut beurteilt werden kann, ein kontinuierliches Monitoring von Erkrankung und Therapie sowie das Erkennen und Behandeln von Nebenwirkungen gewährleistet werden kann [31]. Welches Präparat zunächst eingesetzt wird, hängt vom Wirkungsmechanismus sowie individuellen Charakteristika des entsprechenden Patienten ab. Im Sinne eines „Shared Decision-Making“, das State of the Art in der therapeutischen Entscheidungsfindung ist, werden auch Patientenpräferenzen erfasst und berücksichtigt. Dies kann zum Beispiel die Applikationsform (Spritzentherapie vs. orale Therapie vs. Infusionstherapie) oder das Therapieintervall betreffen (kontinuierlich vs. gepulst). Auch das Nebenwirkungsprofil ist bei der therapeutischen Entscheidung wichtig.
Entscheidungsalgorithmus für die Einleitung einer Immuntherapie
Eine Immuntherapie wird anhand von verschiedenen Parametern wie Prognose, Krankheitsaktivität und Krankheitsschwere sowie dem Alter und Geschlecht, Begleiterkrankungen und Liquorparametern wie positiven oligoklonalen Banden (OKBs) als auch dem Nebenwirkungsprofil ausgewählt [31].
Prinzipiell unterscheidet man das Konzept einer Eskalationsstrategie, bei der zunächst mit einer Substanz für milde/moderate Verläufe therapiert wird und das Prinzip einer frühen Therapie mit einer Substanz, die für hochaktive Verläufe eingesetzt werden kann („hit hard and early“).
Eine hoch aktive MS ist definiert durch: ≥ 1 Schub innerhalb der letzten 12 Monate, ≥ 2 Schübe innerhalb der letzten 24 Monate oder ≥ 3 neue T2-Läsionen oder ≥ 1 neue Gadolinium aufnehmende (Gd+) Läsion in einem Folge-MRT. Eine hocheffektive Immuntherapie sollte bereits als Erstlinienbehandlung eingesetzt werden, wenn
- Eine hohe Schubaktivität vorliegt (≥ 1 Schub innerhalb der letzten 12 Monate, ≥ 2 Schübe innerhalb der letzten 24 Monaten oder ≥ 3 neue T2-Läsionen oder ≥ 1 neue Gd+-Läsion in einem Folge-MRT
- Schübe mit deutlicher Behinderungszunahme assoziiert sind bzw. eine schnelle Behinderungsprogression besteht
- Bei hoher Herdlast bzw. Herden mit Risiko von schneller Behinderungszunahme (infratentoriell, spinal)
Die Einleitung einer hocheffektiven Immuntherapie hat verschiedene Vorteile. So zeigen mehrere retrospektive Kohortenstudien, dass durch eine frühe hochaktive Immuntherapie das Risiko reduziert wird, dass es relativ rasch zu einer sekundär-chronisch progredienten MS kommt [1]. Auch die Behinderungsprogression wird bei einer früheren hochaktiven Therapie gegenüber einer späteren Eskalation positiv beeinflusst [15]. In dieser retrospektiven Arbeit aus dem MSBase-Register sowie dem schwedischen MS-Register erfolgte ein Vergleich der Langzeitbehinderung zwischen Patienten, bei denen die Behandlung innerhalb von zwei Jahren nach Erkrankungsbeginn begonnen wurde, mit Patienten, bei denen nach vier bis sechs Jahren eine hochwirksame Therapie initiiert wurde. Es zeigte sich eine geringere kumulative Wahrscheinlichkeit einer Behinderungszunahme nach Beginn einer hochaktiven Behandlung (HR 0,34; KI 0,23–0,51; p < 0,0001) [15]. Der EDSS lag nach sechs Jahren in der frühen Behandlungsgruppe bei 2,2 (SD 1,6) vs. 2,9 (SD 1,8) in der späten Behandlungsgruppe (p < 0,0001) [15]. Prospektive Studien, die eine frühe hocheffektive Therapiestrategie untersuchen, laufen gegenwärtig und werden in den nächsten Jahren die bisher bestehende Evidenz basierend auf retrospektiven Registererhebungen verbessern.
Sollte man daher mittlerweile bei jedem Patienten hochaktiv behandeln? Dies wäre der falsche Schluss. So muss eine gute Risikoabwägung zwischen Effektivität und Sicherheitsprofil getroffen werden, die gerade bei einem milden Verlauf oder einer milden Erstmanifestation zugunsten einer mild/moderaten Therapie ausfallen kann; hierunter fallen zum Beispiel Patienten mit einem monosymptomatischen leichten Schub wie einer sensiblen Störung mit guter Rückbildung, Patienten mit einer niedrigen Läsionslast und Patienten mit wenig Krankheitsaktivität. Patienten, die sich hingegen mit einem schweren, polysymptomatischen Schub vorstellen, sollten eher schon früh mit einer hocheffektiven Immuntherapie behandelt werden.
Sekundär-chronisch progrediente (SP) und primär progrediente (PP) MS
Aktuell verfügbare Therapieoptionen sind leider nach wie vor nur eingeschränkt bei SPMS wirksam, wenngleich es eine Vielzahl von Substanzen gibt, die in der Entwicklung sind [6, 9, 10]. Gründe hierfür sind Veränderungen von zugrunde liegenden Mechanismen, die bei schubförmiger und progredienter MS teils unterschiedlich geartet sind. Mechanismen bei Progression umfassen unter anderem Aktivierung von residenten Immunzellen des Zentralnervensystems wie Mikroglia mit Freisetzung von oxidativen Metaboliten sowie Mechanismen von Neurodegeneration durch z. B. mitochondrialen Schaden und Veränderung der Ionenkanalzusammensetzung (für eine ausführliche Übersichtsarbeit zu zugrundeliegenden Mechanismen und Substanzen in der Entwicklung siehe [12]).
Klassische Immuntherapien sind bei SPMS dann wirksam, wenn noch inflammatorische Aktivität mit aktiven Schüben besteht, wie mittels Daten aus der MSBase-Datenbank anhand von 1621 Patienten gezeigt werden konnte [21]. Für die Behandlung der SPMS sind Interferon beta-1b, Mitoxantron und Siponimod zugelassen. Siponimod ist für die Behandlung der aktiven SPMS, gemessen mittels kernspintomographischer Aktivität oder Schubaktivität, zugelassen. Weiterhin können Ponesimod und Ozanimod bei aktiver schubförmiger MS (RMS) eingesetzt werden; hierunter fallen auch Patienten mit einer SPMS mit Schubaktivität. Für die Behandlung der aktiven PPMS ist Ocrelizumab verfügbar.
Die therapeutischen Optionen bei Progression sind somit deutlich weniger ausgeprägt. Durch die Entwicklung von Substanzen, die vermutete Mechanismen von Progression gezielter adressieren, ist zu erwarten, dass in den nächsten Jahren verbesserte Möglichkeiten zur Verfügung stehen werden. So befinden sich Substanzen von mehreren Herstellern in unterschiedlichen Phasen der klinischen Prüfung, die die Aktivität der Bruton-Tyrosinkinase hemmen, die in Mikroglia sowie B-Zellen aktiv ist. Diese Substanzklasse kann neue therapeutische Möglichkeiten für Patienten mit Progression ermöglichen [6].
Sequenzierung von Immuntherapien
Neben den oben diskutierten Fragen der Vorteile einer eskalativen gegenüber einer initial hochaktiven Therapie gibt es auch zunehmend Daten zu Therapiefolgen, die sinnvoll sind. So ist es zum Beispiel wenig ratsam, nach zwei Jahren Natalizumab bei einem Anstieg des Anti-JCV-Titers eine Deeskalation auf eine Plattformtherapie wie beispielsweise Glatirameracetat durchzuführen, da bei der hochaktiven MS eine deutliche Zunahme der Schubaktivität erwartet werden muss. In diesem Setting wäre es möglich, innerhalb von etwa vier bis sechs Wochen nach Natalizumab auf eine B-Zell-Depletion mit entweder Ocrelizumab oder Ofatumumab umzusetzen. In einer kleinen Beobachtungs-Kohortenstudie (n = 42) mit einem medianen Follow-up von 21 Monaten zeigte sich bei 83 % der Patienten keine Krankheitsaktivität bei den Patienten, die direkt umgestellt wurden [28]. Bei den sogenannten indirekten Umstellungen lag dieser Anteil bei nur 50 %. Bei den direkten Umstellungen wurden jedoch zwei Patienten mit einer übertragenen („Carry-over“) progressiven multifokalen Leukenzephalopathie (PML) diagnostiziert, das heißt, die PML-Symptomatik bestand subklinisch bereits vor der Umstellung und wurde erst danach erkannt. Somit sollte gerade bei Patienten mit einer Anti-JCV-Titer-Dynamik liquorchemisch und mittels aktueller MRT eine PML vor Umstellung ausgeschlossen werden.
Auch nach einer Behandlung mit einem S1P-Rezeptor-Modulator stellt sich die Frage nach einer sinnvollen Therapiefolge. Daten aus dem MSBase-Register zeigen, dass nach Absetzen einer mindestens 6-monatigen Behandlung mit Fingolimod und dem Beginn einer Folgetherapie mit Natalizumab und Ocrelizumab Schubaktivität besser kontrolliert werden kann als mit Cladribin. So lag die jährliche Schubrate mit Ocrelizumab bei 0,07; mit Natalizumab bei 0,11. Unter Cladribin zeigte sich eine jährliche Schubrate von 0,25 [32]. Behinderungsprogression differierte jedoch nicht zwischen den Folgetherapien. Insbesondere bei den S1P-Rezeptor-Modulatoren spielt auch das Timing der Umstellung eine große Rolle. So liegt die Halbwertzeit bei Fingolimod (6 Wochen) und Ozanimod (2–3 Monate) deutlich über derjenigen von Ponesimod (7 Tage) und Siponimod (10 Tage), sodass bei den erstgenannten Substanzen eine Therapiepause von etwa drei bis vier Wochen eingehalten werden muss, bevor eine neue Behandlung initiiert wird. Bei Ponesimod und Siponimod sollte man nach etwa ein bis zwei Wochen eine Anschlusstherapie beginnen. Diese Dynamik spielt auch hinsichtlich der Auswahl von geeigneten Patienten eine Rolle, da Patienten mit schlechter Compliance eher keine Substanz mit kurzer Halbwertzeit erhalten sollten, um ein erneutes Auftitrieren zu vermeiden und das Risiko des Aufflammens von schwerer Krankheitsaktivität („Rebound“) bis hin zur Entwicklung von tumefaktiven MS-Läsionen zu verhindern [11] (s. Kasuistik).
Kasuistik
Eine Anfang 60-jährige Patientin mit über 16-jähriger Erkrankungsdauer wurde unter dem Verdacht auf tumefaktive MS-Läsionen, differenzialdiagnostisch eine opportunistische Infektion mit Zystizerkose, zugewiesen. Klinisch war die Pat. mit einem Psychosyndrom und Desorientiertheit aufgefallen. Kernspintomographisch zeigten sich multiple, supratentorielle, ringförmig Kontrastmittel aufnehmende Läsionen. In der Lumbalpunktion konnte eine leichtgradige Pleozytose von 16 Zellen/µl nachgewiesen werden. Anamnestisch ließ sich eruieren, dass die Patientin über einen längeren Zeitraum die Immuntherapie mit Fingolimod unregelmäßig eingenommen hatte. Nach dem Ausschluss einer opportunistischen Infektion kam es unter einer Cortisonpulstherapie zu einer deutlichen klinischen Besserung und Regredienz der Kontrastmittelaufnahme (Abb. 1). Der Fall unterstreicht die Notwendigkeit einer guten Compliance bei der Behandlung mit einer kontinuierlich zu applizierenden Substanz, insbesondere bei S1P-Rezeptor-Modulatoren.
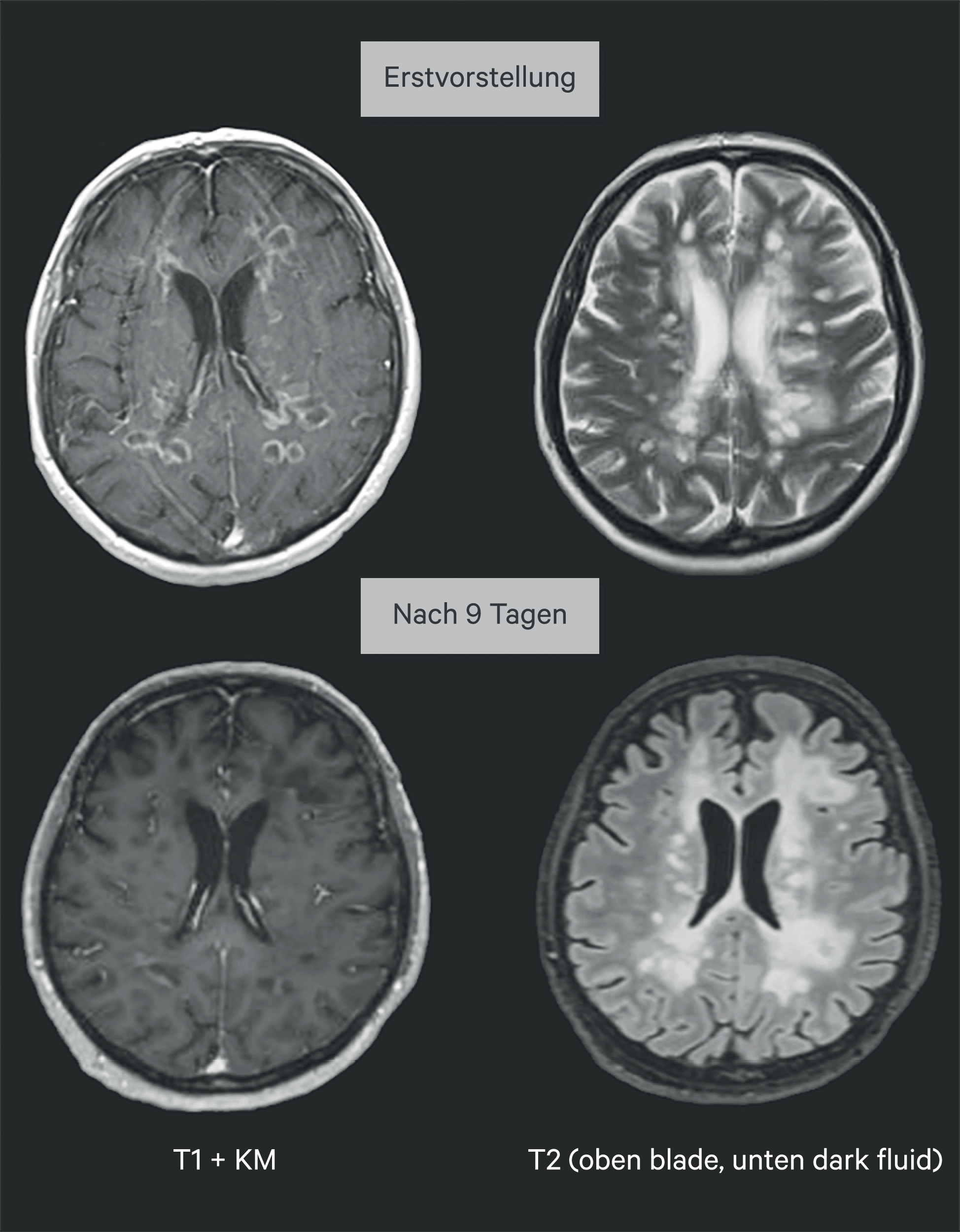
Abb. 1. Kernspintomographie des Neurocraniums, obere Reihe bei Erstvorstellung, links T1 mit Kontrastmittel, rechts T2. Unten 9 Tage nach Erstvorstellung nach Durchführung einer hochdosierten intravenösen Behandlung mit Methylprednisolon über mehrere Tage.
Prinzipiell sollte somit bei einer Behandlung mit einer Substanz aus der Gruppe der hocheffektiven Therapeutika ebenso mit einer solchen Substanz weiter behandelt werden, wenn die Erkrankung weiter hochaktiv ist. Eine Deeskalation auf eine moderat wirksame Therapieoption empfiehlt sich aufgrund des Risikos von klinischer und/oder kernspintomographischer Krankheitsaktivität nur dann, wenn die Erkrankung lange stabil ist oder die Lebensumstände eine Deeskalation verlangen.
Deeskalation und Therapie in der Schwangerschaft
Deeskalation und Absetzen
Neben der Frage nach der richtigen Therapiefolge hat in den letzten Jahren zunehmend die Diskussion um eine Therapiedeeskalation bzw. das Absetzen einer Immuntherapie Raum in der Diskussion der MS-Behandlung gewonnen. Dies liegt unter anderem darin begründet, dass MS-Patienten immer älter werden, in höherem Alter zunehmend Begleiterkrankungen relevant werden und das Risiko von Infektionen bei Immunoseneszenz steigen kann. Kardiovaskuläre Risikofaktoren tragen zudem zu einem höheren Risiko von Schubaktivität, Behinderungsprogression sowie der Notwendigkeit einer Therapieeskalation bei [23]. Durch Immunoseneszenz gerät klassisch inflammatorische Aktivität durch das adaptive Immunsystem, gemessen anhand der Schubaktivität sowie der kernspintomographischen Aktivität, zunehmend in den Hintergrund [29], verschwindet jedoch nicht, sodass auch noch in dem Alter jenseits der 60 eine Immuntherapie diskutiert werden kann und sollte. Insbesondere spielt die heutzutage hohe Lebenserwartung eine Rolle.
Ob und ab wann über die Beendigung einer Immuntherapie nachgedacht werden kann, ist weiterhin umstritten. So zeigt eine Arbeit aus dem MSBase-Register, dass die Zeit bis zum ersten Schub nach Absetzen bei einem medianen Alter von 45 Jahren (Einschlusskriterien: keine Schübe seit ≥ 5 Jahren nach Absetzen, Follow-up ≥ 3 Jahre, keine neues krankheitsmodifizierende Therapie [DMT] ≥ 3 Jahre nach Stopp) sich zwar nicht unterscheidet, die Zeit bis zu einer Behinderungsprogression jedoch wesentlich kürzer bei den Patienten ist, die eine Immuntherapie absetzen (aHR = 1,47; 95%- KI 1,18–1,84; p = 0,001) [19]. Ab wann eine Altersgrenze erreicht sein könnte, ab der man eine Immuntherapie guten Gewissens beenden kann, ist nach wie vor umstritten, zumal auch bei über 55-jährigen Patienten noch etwa ein Drittel der Patienten inflammatorische Aktivität aufweist [5].
Therapie in der Schwangerschaft
Eine Besonderheit stellt die Behandlung in der Schwangerschaft dar. Durch die Schwangerschaft kommt es zu einer Abnahme der Schubrate mit postpartal erneuter Zunahme der Krankheitsaktivität [2]. Bei älteren DMTs gibt es mittlerweile eine gute Datenbasis zum Risiko für das Ungeborene bei einer Exposition in der Schwangerschaft. Die Behandlung mit Glatirameracetat [18], Interferon beta [26] sowie Natalizumab [4] während des ersten Trimenons, dokumentiert über das deutschsprachige Multiple Sklerose und Kinderwunsch Register (DMSKW), erhöht nicht das Risiko für ein schlechtes Outcome der Schwangerschaft. Eine weitere Arbeit konnte bei 369 Patientinnen, die in der Schwangerschaft mit Natalizumab behandelt worden waren, ebenfalls zeigen, dass es kein erhöhtes Risiko für Aborte sowie kein spezifisches Muster von Fehlbildungen gibt [13]. Bei einer Behandlung mit Natalizumab im dritten Trimenon können milde bis moderate hämatologische Veränderungen auftreten, wie in einer kleinen Fallserie bei 10 von 13 Kindern gezeigt wurde [14]. In einer Kohorte von 255 Frauen mit 274 Schwangerschaften, bei denen Natalizumab vor der Schwangerschaft (n = 85) oder während des ersten Trimenons (n = 189) abgesetzt wurde, kam es bei 67 % der Schwangerschaften zu Schüben während der Schwangerschaft bzw. postpartum [16]. In 16 % der Schwangerschaften wurden schwere und in 1 % lebensbedrohliche Schübe dokumentiert. Außerdem kam es in 11 % der Fälle zu einem signifikanten Anstieg des EDSS um mindestens zwei Punkte ein Jahr postpartal. Somit sollte man bei hochaktiver MS erwägen, die Behandlung mit Natalizumab bis etwa in die 30. Schwangerschaftswoche fortzuführen und bei hochaktiver MS nicht frühzeitig abzusetzen. Die Behandlung sollte nach Möglichkeit vier Wochen nach der Entbindung wieder aufgenommen werden, um das deutlich erhöhte Risiko von postpartalen Schüben zu reduzieren.
Die Behandlung mit einer B-Zell-depletierenden Therapie wie Rituximab oder Ocrelizumab könnte die Schwangerschaft potenziell überbrücken, wenn die Behandlung vor der Schwangerschaft stattfindet. In einer Analyse des DMSKW und der Neuromyelitis-optica-Studiengruppe (NEMOS) von 88 Schwangerschaften zeigte sich ein erhöhtes Risiko für Frühgeburten (9,8 % gegenüber 45 %) bei einer Exposition während der Schwangerschaft [20]. Ob es ein spezifisches Risiko für Nebenwirkungen beim Kind gibt, ist bisher wenig untersucht. Eine weitere Möglichkeit besteht in der Behandlung mit Cladribin, da nach dem Zyklus für etwa ein Jahr keine Therapie notwendig ist. Bei einer Kohorte von 39 Schwangerschaften mit 27 Geburten zeigte sich eine schwere Fehlbildung [3]. Die Kontrolle der Krankheitsaktivität war aber sehr gut, es kam nur zu einem Schub während der Schwangerschaft bzw. postpartal. Da die Evidenz bisher auf geringen Fallzahlen beruht, sollte eine Schwangerschaft bis zu sechs Monate nach dem letzten Cladribin-Zyklus vermieden werden.
Zusammenfassung
Die Entwicklung der Therapielandschaft der multiplen Sklerose ist zweifellos eine der großen Erfolgsgeschichten der Neurologie der letzten Jahrzehnte. Hierdurch ist es jedoch auch herausfordernder geworden, die richtige Substanz bei unterschiedlichen Patienten einzusetzen. Die Stratifizierung anhand von Risikofaktoren wie Schubaktivität, Dynamik der Behinderungsprogression, Prädilektion von Läsionen, Alter, Geschlecht und Komorbiditäten erlauben es, individuell zugeschnittene Therapiestrategien zu entwickeln. Die Vorstellung einer initial hochwirksamen gegenüber einer eskalativen Strategie ist dabei nicht als sich diametral gegenüberstehendes „Schwarz-Weiß-Konzept“ zu sehen, sondern zeigt vielmehr das breite Spektrum der therapeutischen Möglichkeiten auf, das individuell passende Lösungen ermöglicht. Unstrittig ist, dass Patienten früh behandelt werden sollten, um das Risiko von früher Behinderungsakkumulation zu reduzieren und dass ab einer gewissen Erkrankungsschwere schon initial höher effektiv behandelt werden sollte.
Abkürzungen
|
Gd+ |
Gadolinium aufnehmend |
|
KIS |
Klinisch isoliertes Syndrom |
|
MS |
Multiple Sklerose |
|
OKBs |
oligoklonale Banden |
|
PPMS |
Primär progrediente MS |
|
RRMS |
Schubförmig-remittierende MS |
|
SPMS |
Sekundär-chronisch progrediente MS |
Interessenkonflikterklärung
SF erhielt Reisekostenerstattung und/oder Vortrags- und Beratungshonorare von Biogen, BMS, Celgene, Genesis Pharma, Janssen, Novartis und Roche und Drittmittel von der Ruhr-Universität Bochum, DMSG, Stiftung für therapeutische Forschung, Lead Discovery Center GmbH und Novartis. Dies steht nicht in Zusammenhang mit diesem Manuskript.
RG erhielt Vortrags- und Beratungshonorare von Baxter, Bayer Schering, Biogen Idec, CSL Behring, Genzyme, Merck Serono, Novartis, Stendhal, Talecris und TEVA. Seine Klinik erhielt Drittmittelunterstützung von Bayer Schering, BiogenIdec, Genzyme, Merck Serono, Novartis und TEVA. Dies steht nicht in Zusammenhang mit diesem Manuskript.
Literatur
1. Brown JWL, Coles A, Horakova D, Havrdova E, et al. Association of initial disease-modifying therapy with later conversion to secondary progressive multiple sclerosis. JAMA 2019;321:175–87.
2. Confavreux C, Hutchinson M, Hours MM, Cortinovis-Tourniaire P, Moreau T. Rate of pregnancy-related relapse in multiple sclerosis. Pregnancy in Multiple Sclerosis Group. N Engl J Med 1998;339:285–91.
3. Dost-Kovalsky K, Thiel S, Ciplea AI, Gold R, Hellwig K. Cladribine and pregnancy in women with multiple sclerosis: The first cohort study. Mult Scler 2022:13524585221131486.
4. Ebrahimi N, Herbstritt S, Gold R, Amezcua L, et al. Pregnancy and fetal outcomes following natalizumab exposure in pregnancy. A prospective, controlled observational study. Mult Scler 2015;21:198–205.
5. EME C. ECTRIMS Online Library 2022;P302.
6. Faissner S, Bongert M, Gold R. Progression bei multipler Sklerose – Stillstand durch fortschrittliche Behandlungen. Arzneimitteltherapie 2021;39:186–95.
7. Faissner S, Gold R. Efficacy and safety of multiple sclerosis drugs approved since 2018 and future developments. CNS Drugs 2022;36:803–17.
8. Faissner S, Gold R. Efficacy and safety of the newer multiple sclerosis drugs approved since 2010. CNS Drugs 2018;32:269–87.
9. Faissner S, Gold R. [New therapeutic approaches in progressive multiple sclerosis]. Fortschr Neurol Psychiatr 2019;87:653–71.
10. Faissner S, Gold R. Progressive multiple sclerosis: latest therapeutic developments and future directions. Ther Adv Neurol Disord 2019;12:1756286419878323.
11. Faissner S, Hoepner R, Lukas C, Chan A, et al. Tumefactive multiple sclerosis lesions in two patients after cessation of fingolimod treatment. Ther Adv Neurol Disord 2015;8:233–8.
12. Faissner S, Plemel JR, Gold R, Yong VW. Progressive multiple sclerosis: from pathophysiology to therapeutic strategies. Nat Rev Drug Discov 2019.
13. Friend S, Richman S, Bloomgren G, Cristiano LM, Wenten M. Evaluation of pregnancy outcomes from the Tysabri® (natalizumab) pregnancy exposure registry: a global, observational, follow-up study. BMC Neurol 2016;16:150.
14. Haghikia A, Langer-Gould A, Rellensmann G, Schneider H, et al. Natalizumab use during the third trimester of pregnancy. JAMA Neurol 2014;71:891–5.
15. He A, Merkel B, Brown JWL, Zhovits Ryerson L, et al. Timing of high-efficacy therapy for multiple sclerosis: a retrospective observational cohort study. Lancet Neurol 2020;19:307–16.
16. Hellwig K, Tokic M, Thiel S, Esters N, et al. Multiple sclerosis disease activity and disability following discontinuation of natalizumab for pregnancy. JAMA Netw Open 2022;5:e2144750.
17. Hemmer B. Diagnose und Therapie der Multiplen Sklerose, Neuromyelitis-optica-Spektrum-Erkrankungen und MOG-IgG-assoziierten Erkrankungen, S2k-Leitlinie. Deutsche Gesellschaft für Neurologie (Hrsg), Leitlinien für Diagnostik und Therapie in der Neurologie 2021.
18. Herbstritt S, Langer-Gould A, Rockhoff M, Haghikia A, et al. Glatiramer acetate during early pregnancy: A prospective cohort study. Mult Scler 2016;22:810–6.
19. Kister I, Spelman T, Alroughani R, Lechner-Scott J, et al. Discontinuing disease-modifying therapy in MS after a prolonged relapse-free period: a propensity score-matched study. J Neurol Neurosurg Psychiatry 2016;87:1133–7.
20. Kümpfel T, Thiel S, Meinl I, Ciplea AI, et al. Anti-CD20 therapies and pregnancy in neuroimmunologic disorders: A cohort study from Germany. Neurol Neuroimmunol Neuroinflamm 2021;8.
21. Lizak N, Malpas CB, Sharmin S, Havrdova EK, et al. Association of sustained immunotherapy with disability outcomes in patients with active secondary progressive multiple sclerosis. JAMA Neurol 2020;77:1398–407.
22. Montalban X, Gold R, Thompson AJ, Otero-Romero S, et al. ECTRIMS/EAN Guideline on the pharmacological treatment of people with multiple sclerosis. Mult Scler 2018;24:96–120.
23. Petruzzo M, Reia A, Maniscalco GT, Luiso F, et al. The Framingham cardiovascular risk score and 5-year progression of multiple sclerosis. Eur J Neurol 2021;28:893–900.
24. Sorensen PS, Sellebjerg F, Hartung HP, Montalban X, et al. The apparently milder course of multiple sclerosis: changes in the diagnostic criteria, therapy and natural history. Brain 2020;143:2637–52.
25. Spelman T, Magyari M, Piehl F, Svenningsson A, et al. Treatment escalation vs immediate initiation of highly effective treatment for patients with relapsing-remitting multiple sclerosis: Data from two different national strategies. JAMA Neurol 2021;78:1197–204.
26. Thiel S, Langer-Gould A, Rockhoff M, Haghikia A, et al. Interferon-beta exposure during first trimester is safe in women with multiple sclerosis – A prospective cohort study from the German Multiple Sclerosis and Pregnancy Registry. Mult Scler 2016;22:801–9.
27. Tintore M, Arrambide G, Otero-Romero S, Carbonell-Mirabent P, et al. The long-term outcomes of CIS patients in the Barcelona inception cohort: Looking back to recognize aggressive MS. Mult Scler 2020;26:1658–69.
28. van Lierop Z, Toorop AA, Coerver E, Willemse E, et al. Ocrelizumab after natalizumab in JC-virus positive relapsing remitting multiple sclerosis patients. Mult Scler J Exp Transl Clin 2021;7:20552173211013831.
29. Vaughn CB, Jakimovski D, Kavak KS, Ramanathan M, et al. Epidemiology and treatment of multiple sclerosis in elderly populations. Nat Rev Neurol 2019;15:329–42.
30. Weinshenker BG, Bass B, Rice GP, Noseworthy J, et al. The natural history of multiple sclerosis: a geographically based study. I. Clinical course and disability. Brain 1989;112:133–46.
31. Wiendl H, Gold R, Berger T, Derfuss T, et al. Multiple Sclerosis Therapy Consensus Group (MSTCG): position statement on disease-modifying therapies for multiple sclerosis (white paper). Ther Adv Neurol Disord 2021;14:17562864211039648.
32. Zhu C, Zhou Z, Roos I, Merlo D, et al. Comparing switch to ocrelizumab, cladribine or natalizumab after fingolimod treatment cessation in multiple sclerosis. J Neurol Neurosurg Psychiatry 2022;93:1330–7.
Univ.-Prof. Dr. med. Simon Faissner, Univ.-Prof. Dr. med. Ralf Gold, Klinik für Neurologie, Universitätsklinikum der Ruhr-Universität Bochum, St. Josef-Hospital, Gudrunstr. 56, 44791 Bochum, E-Mail: simon.faissner@rub.de
Therapeutic algorithms of multiple sclerosis
Multiple sclerosis (MS) is a chronic inflammatory disease of the central nervous system leading to demyelination, axonal damage and neurodegeneration. In recent decades, several new classes of compounds and modes of action have been introduced, which now lead to the comfortable situation of being able to choose from almost 20 MS therapies for different disease courses and severities. This situation leads to an increasingly complex therapeutic landscape with the difficult question in which sequence immunotherapies should be administered. In particular, the concepts of escalation therapy and treatment according to the notion of „hit hard and early“ interact with each other. De-escalation or discontinuation of immunotherapies are also subject of current discussions. In this review we will discuss the current state of knowledge on stepwise therapy of MS and provide a guide for its implementation in daily practice.
Key words: Multiple sclerosis, escalation therapy, hit hard and early, neuroprotection; progression
Psychopharmakotherapie 2023; 30(02):47-53
