Jacqueline Schwartz, Yann-Nicolas Batzler und Martin Neukirchen, Düsseldorf
In der Palliativmedizin gehört der Einsatz von Psychopharmaka zum klinischen Alltag. Palliativmedizin ist durch eine ganzheitliche Symptomerfassung sowie Symptomkontrolle gekennzeichnet. Dabei werden Symptome auf der physischen und psychischen Ebene erfasst und therapiert. Aber auch die soziale (Versorgung, Angehörige) sowie die spirituelle Dimension (Existenzkrisen, Konfrontation mit der eigenen Endlichkeit) spielen für eine suffiziente Symptomkontrolle eine wichtige Rolle und dürfen nicht vernachlässigt werden. Das Ziel ist die Verbesserung der Lebensqualität. Auf der psychischen Ebene stehen Beschwerden wie Angst und Unruhe, Depressionen sowie therapierefraktäre Delirformen im Vordergrund. Die vorliegende Übersichtsarbeit soll einen Überblick über die medikamentöse Therapie dieser Beschwerden aus palliativmedizinischer Sicht bieten. Dabei erfolgt die medikamentöse Therapie immer eingebettet in eine intensive multiprofessionelle therapeutische Begleitung durch speziell weitergebildete Ärzte, Pflegende und Psychologen und weitere Therapeuten.
Angst
Angst gehört zu den häufigsten psychischen Beschwerden von Palliativpatienten, die unter Umständen einer medikamentösen Therapie bedürfen. Dabei handelt es sich in der Regel nicht um Angst im Sinne einer Angststörung nach ICD-10, die differenzialdiagnostisch ausgeschlossen werden soll, sondern um eine situativ adäquate, regelhaft auch existenzielle Angst, die mit einer Prävalenz von bis zu 48 % angegeben wird [13]. Diese Ängste beziehen sich auf bestehende oder befürchtete Symptome wie Schmerzen, Luftnot, Verlust der Mobilität, aber auch unspezifischer auf die Angst vor Leiden und Tod. Das Vorliegen wie auch die Intensität von Angst sollen nach Empfehlung der S3-Leitlinie Palliativmedizin für Patienten mit einer nicht-heilbaren Krebserkrankung regelmäßig anhand von Screening-Instrumenten, zum Beispiel MIDOS (Minimales Dokumentationssystem für Palliativpatienten) oder GAD-2 (Generalized Anxiety Disorder-2), und zum Beispiel der numerischen Rating-Skala (NRS) zur Abschätzung der Symptomintensität evaluiert werden [14]. Zur Therapie der Angst werden medikamentöse, aber auch nicht nichtmedikamentöse Maßnahmen eingesetzt.
Nichtmedikamentöse Maßnahmen zur Therapie von Angst
In der Palliativmedizin spielen neben der rein medikamentösen Therapie andere, supportive Maßnahmen zur Symptomkontrolle eine große Rolle, die immer begleitend, häufig auch zuerst eingesetzt werden. Hierzu gehören psychologische bzw. psychotherapeutische Gespräche, Verfahren wie Kunst-, Musik- oder tiergestützte Therapie, Atemtherapie, Aromatherapie entspannende Massagen, physiotherapeutische Interventionen, aber auch sozialarbeiterische sowie spirituelle Begleitung. Supportive Gespräche durch Pflegekräfte und Ärzten ergänzen neben Symptomerfassung und -evaluation die Arbeit im multiprofessionellen Team (Abb. 1).
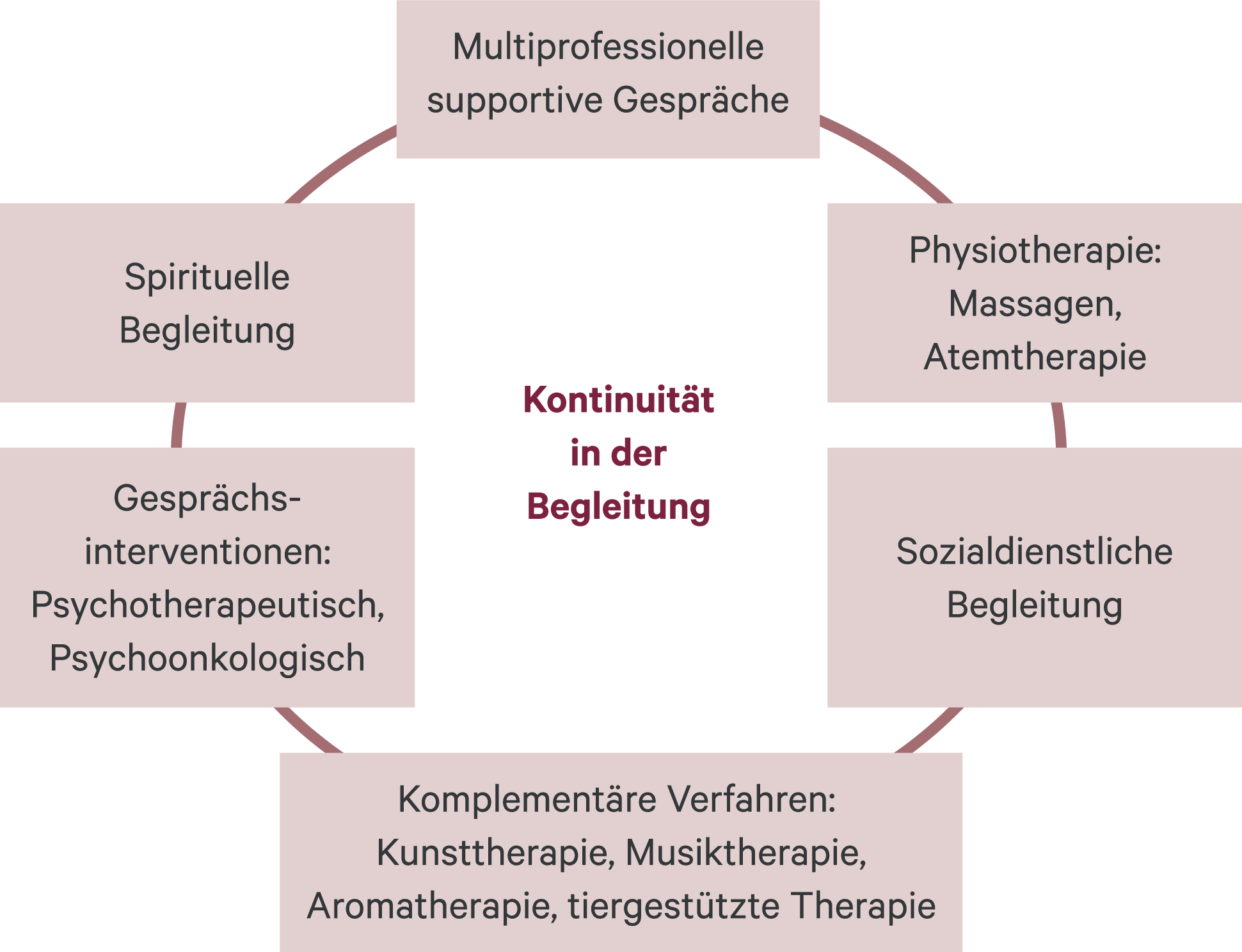
Abb. 1. Allgemeine Maßnahmen bei Angst und Unruhe, Depression und Delir
Medikamentöse Therapie der Angst
Reichen nichtmedikamentöse Therapiemaßnahmen nicht aus, sind sie nicht anwendbar oder machen akute sowie chronische Belastungssituationen eine rasche Symptomlinderung notwendig, erfolgt eine medikamentöse Therapie. Beispielhaft sei hier die akute Dyspnoe-Symptomatik erwähnt. Atemnot verursacht Angst, Angst wiederum führt zu Tachypnoe, was die Atemnot im Sinne eines Circulus vitiosus unterhält. Dies erfordert gegebenenfalls neben einer Atemnot lindernden Opiattherapie eine anxiolytische Therapie. Hier werden dann kurzwirksame Benzodiazepine mit schnellem Wirkungseintritt erfolgreich verwendet. Zum Einsatz kommen hier zum Beispiel Lorazepam 0,5 mg s. l. oder auch Midazolam 2,5 mg s. c. als Off-Label-Use, wenn eine orale Zufuhr nicht möglich ist. Dosis und Therapiedauer richten sich dabei nach der subjektiven Symptomlast der Patienten und müssen engmaschig evaluiert und regelmäßig reflektiert werden [14].
Außerhalb der akuten Belastungssituation oder einer Panikattacke können Benzodiazepine bei z. B. rezidivierender Angst auch regelmäßig verordnet werden. Patienten berichten häufig über Ängste und Gedankenkreisen in der Nacht, was zu einem konsekutiv gestörten Nachtschlaf und entsprechender Tagesmüdigkeit führt. Die in der Regel zusätzlich bestehende Fatigue wird dadurch noch intensiviert. Hier kann eine regelmäßige Benzodiazepin Gabe Symptomlast reduzieren, wobei gleichzeitig die dadurch bedingte Müdigkeit zu bedenken ist. Dabei spielt die Prognose der Patienten eine wichtige Rolle. Ist die Prognose begrenzt (< 2–4 Wochen), können Benzodiazepine je nach Halbwertszeit ein bis drei Mal täglich verordnet werden, zum Beispiel Lorazepam 0,5 bis 1 mg zwei bis drei Mal täglich p. o. oder Diazepam 2 bis 10 mg p. o. zur Nacht [17]. In diesem Zeitraum stellen Toleranzentwicklung und Abhängigkeit kein Problem dar. Bei längerer Prognose (> 2–4 Wochen) stellt, neben der Medikation mit Benzodiazepinen, der Einsatz von Antidepressiva, z. B. selektiven Serotonin-Reuptake-Inhibitoren (SSRI) oder selektive Serotonin-Noradrenalin-Wiederaufnahmehemmern (SSNRI), eine Therapiemöglichkeit dar [14, 17, 21] (Tab. 1). Hierbei erfolgt der Wirkeintritt erst nach mehreren Wochen [4]. Auch Pregabalin und Quetiapin als Vertreter anderer Substanzklassen (Gabapentinoide und Antipsychotika der zweiten Generation) sind in der Therapie von Angst einsetzbar [17]. Aufgrund des raschen Wirkungseintritts kann die zusätzliche Gabe von Pregabalin bei begrenzter Prognose erwogen werden. Quetiapin sollte wegen der eingeschränkten Verträglichkeit eingesetzt werden, wenn unter Kombination von Antidepressivum +/– Benzodiazepin +/– Pregabalin kein ausreichendes Ansprechen erzielt wird [2].
Tab. 1. Überblick über die medikamentöse Therapie bei Angst und Panikattacken
|
Medikament |
Applikation |
HWZ |
Einzeldosis |
Maximaldosis pro Tag |
|
|
Akut |
Lorazepam |
s. l. |
11–18 h |
1,0–2,5 mg |
7,5 mg |
|
Oxazepam |
p. o. |
5–15 h |
10–40 mg |
150 mg |
|
|
Midazolam (Off-Label) |
p. o., s. c., i. v. |
1,5–2,5 h |
2,5–5 mg |
15 mg |
|
|
Rezidivierend |
Citalopram |
p. o. |
35 h |
10–20 mg |
40 mg |
|
Escitalopram |
p. o. |
30 h |
5–10 mg |
20 mg |
|
|
Sertralin |
p. o. |
22–36 h |
50 mg |
200 mg |
|
|
Venlafaxin |
p. o. |
5 h (Metabolit 11 h) |
37,5 mg |
150 mg |
HWZ: Halbwertszeit
Substanzklassen
Benzodiazepine sind GABAA-Modulatoren und führen über eine allosterische Modulation zu einer erhöhten Rezeptoraffinität für Gamma-Aminobuttersäure (GABA). Je nach Rezeptorsubtyp werden verschiedene Wirkungen hervorgerufen [16]. Hierzu gehören: Schlaf, antiepileptische Wirkung, Amnesie, Abhängigkeit, Anxiolyse, Antihyperalgesie, Muskelrelaxation. Die verschiedenen Substanzen werden meist gut resorbiert, meist über Cytochrom P450 (CYP) 3A4 metabolisiert, unterscheiden sich jedoch in Bezug auf Wirkstärke und Pharmakokinetik, sodass die zum Teil langen Halbwertszeiten beachtet werden sollten. Sie differieren mit zum Beispiel einer bis vier Stunden für Midazolam i. v. und 25 bis 50 Stunden für Diazepam p. o. deutlich. Dies ist besonders im Hinblick auf mögliche Kumulation und Gefahr der Atemdepression bei i. v-Nutzung relevant. Letztere ist insbesondere bei bestehender Leber- und Niereninsuffizienz und immer in der Kombination mit anderen potenziell atemdepressiven Medikamenten zu beachten. Die Kombination mit Opioiden zur Analgesie und/oder Linderung von Atemnot ist in der Palliativmedizin häufig, bedarf aber einer engmaschigen Patientenbeobachtung. Häufige Nebenwirkungen sind Müdigkeit bis zur Benommenheit, eingeschränkte psychomotorische Fähigkeiten und Hypotonie. Hier sollte in der Eindosierungsphase besonders bei älteren, immobilen und sturzgefährdeten Patienten ebenfalls eine klinische Beobachtung erfolgen. Paradoxe Reaktionen kommen in weniger als 10 % der Fälle vor, sind nicht selten durch Unterdosierung bedingt und gehen mit Agitiertheit und gegebenenfalls aggressivem Verhalten einher [17]. Eine Überdosierung durch Benzodiazepine kann mit Flumazenil i. v. antagonisiert werden. Weitere Anwendungsgebiete in der Palliativmedizin stellen das hyperaktive Delir sowie Agitation in der Finalphase dar (s. u.) [17]. Die SSRI bzw. SSNRI werden weiter unten behandelt.
Depression
Ein weiteres Symptom, das gegebenenfalls psychopharmakologischer Intervention bedarf, ist die Depression bzw. depressive Episode. Hier muss zunächst die Depression von einer situativ adäquaten herabgesetzten Stimmungslage differenziert werden. Andere Differenzialdiagnosen sind die Anpassungsstörung, Dysthymie, eine organisch depressive Störung sowie eine von der Depression gegebenenfalls schwierig abzugrenzende Trauerreaktion. Zunächst wird in der S3-Leitlinie Palliativmedizin der Einsatz eines Screeningverfahrens empfohlen, bei auffälligen Werten im Anschluss auch eine Erfassung der klassischen Haupt- und Zusatzsymptome nach ICD-10-Kriterien [4, 14]. Wird eine leichte, mittelgradige oder schwere depressive Episode diagnostiziert, erfolgt eine Therapie angepasst an den Schweregrad der Erkrankung, an den Patientenwunsch und in Abhängigkeit der Prognose der Patienten. Immer ist die Evaluation von möglichen Suizidgedanken obligat. Hier muss zwischen Todeswünschen, die in aller Ambivalenz ein häufiges Phänomen in der palliativmedizinischen Versorgung darstellen, und Suizidgedanken auf dem Boden einer nicht- oder unzureichend behandelten Depression unterschieden werden.
Nichtmedikamentöse Therapie
Allen Palliativpatienten wird im Rahmen des ganzheitlichen Therapieansatzes eine psychologische bzw. psychoonkologische Therapie durch Mitarbeitende des Teams angeboten. Dies bedeutet, dass ein psychotherapeutisches bzw. supportives Gesprächsangebot auch unabhängig vom Vorliegen einer etwaigen Depression besteht. Bei unklarer Diagnose, psychiatrischen Vorerkrankungen, Suizidgedanken auf dem Boden der Depression oder psychotischen Symptomen ist zusätzliche psychiatrische bzw. psychosomatische Expertise hilfreich. In der psychotherapeutischen Therapie kommen dann, zugeschnitten auf die individuellen Bedürfnisse der Patienten, verhaltenstherapeutische Verfahren, Verfahren der interpersonellen Psychotherapie sowie Akzeptanz- und Commitment-Therapie zur Anwendung, die fakultativ durch Kreativtherapien ergänzt werden.
Medikamentöse Therapie der Depression
Die medikamentöse Therapie richtet sich grundsätzlich nach den Empfehlungen der S3-Leitlinie Palliativmedizin sowie der Nationalen Versorgungs-Leitlinie Unipolare Depression. Dabei existieren keine Daten für die Überlegenheit einer spezifischen Substanz oder Substanzklasse für die Therapie von Palliativpatienten. Zu beachten sind hier Nebenwirkungsprofile, Handhabbarkeiten und gegebenenfalls Vortherapien. Bei Vorliegen einer depressiven Episode orientiert sich die Therapie, medikamentös wie nichtmedikamentös, am Schweregrad der Symptomatik [4, 19]. Relevant im klinischen Alltag ist die Abwägung medikamentöser Therapien bei absehbar kurzer Prognose, da unter Umständen die Patienten den positiven Effekt durch ein Antidepressivum nicht mehr erleben. Sind Patienten in die Sterbephase eingetreten, ist eine Fortführung einer oralen antidepressiven Therapie weder indiziert noch bei Unmöglichkeit einer oralen Tabletteneinnahme umsetzbar. Wenn möglich, sollten Antidepressiva in dieser Situation ausgeschlichen werden, häufig ist dies jedoch bei rascher Verschlechterung des Allgemeinzustands nicht mehr möglich. Die häufig einzig orale Verfügbarkeit stellt generell ein Problem dar für Patienten, die eine Dysphagie aufweisen und vor dem Hintergrund der palliativen Grunderkrankung keine Magensonde erhalten oder unter starker Übelkeit und Erbrechen mit konsekutiv unsicherer Resorption leiden. Hier kann unter Umständen Esketamin, das auch als transnasale Formulierung zur Verfügung steht, Off-Label eingesetzt werden. Seit Dezember 2019 von der Europäischen Kommission für die therapieresistente Major Depression als Kombinationstherapeutikum zugelassen [15], liegen derzeit noch wenige Daten für den Einsatz in der Palliativmedizin vor [8, 10]. Günstig sind aus palliativmedizinischer Perspektive die Applikationsform sowie der rasche Wirkeintritt, der eine Zulassung für den psychiatrischen Notfall nach sich zog. Aufgrund der jedoch hohen Rate an Nebenwirkungen (neuro- und hepatotoxisch, Tachykardie, erhöhter intrakranieller Druck, Halluzinationen u. a.) sollte von Esketamin nur kurzzeitig Gebrauch gemacht werden. In einer retrospektiven Analyse konnte gezeigt werden, dass schon der einmalige Gebrauch von Esketamin bei Palliativpatienten einen positiven Effekt auf Symptome wie Angst und depressive Verstimmung haben kann. Zudem findet Esketamin bei therapierefraktären Schmerzen, wie sie bei Tumorpatienten in der Palliativmedizin häufig vorkommen, in einer Dosierung von 0,25 mg/kg i. v. über 45 Minuten Anwendung [8].
Substanzklassen
Aufgrund der Fülle der Antidepressiva werden im weiteren Verlauf nur Substanzklassen dargestellt, die im palliativmedizinischen Kontext häufig eingesetzt werden. Für umfassende Information sei hier auf die Leitlinie Unipolare Depression verwiesen.
Verwendet werden SSRI, SSNRI, noradrenerge spezifische serotonerge Antidepressiva (NaSSA) und trizyklische Antidepressiva (TZA), wie beispielhaft in Tabelle 2 aufgeführt. Generell führen herkömmliche Antidepressiva zu einer Erhöhung der Monoaminkonzentration im synaptischen Spalt, die über nachgeschaltete Effekte zu einer antidepressiven Wirkung führt. Dabei wirken Antidepressiva je nach Präparat an verschiedenen Rezeptoren, die zum Teil erwünschte, aber auch unterwünschte Wirkungen nach sich ziehen. Als Nebenwirkungen sind besonders kardiovaskuläre Nebenwirkungen sowie die Gefahr eines serotonergen Syndroms zu beachten. Außerdem sollte eine medikamentöse Therapie bei Beendigung ausgeschlichen werden, um Absetzsymptome zu vermeiden.
Tab. 2. Überblick über die medikamentöse Therapie bei Depression
|
Medikament |
Applikation |
Einzeldosis |
Maximaldosis pro Tag |
|
|
SSRI |
Citalopram |
p. o., i. v. |
10–20 mg |
40 mg |
|
Sertralin |
p. o. |
50 mg |
200 mg |
|
|
NaSSA |
Mirtazapin |
p. o. |
15 mg |
45 mg |
|
TZA |
Amitriptylin |
p. o. |
25–50 mg |
150 mg (stationär bis 300 mg) |
|
SSNRI |
Duloxetin |
p. o. |
60 mg |
120 mg |
|
Venlafaxin |
p. o. |
37,5–75 mg |
375 mg |
NaSSA: noradrenerge spezifische serotonerge Antidepressiva; SSNRI: selektive Serotonin-Noradrenalin-Wiederaufnahmehemmer; SSRI: selektive Serotonin-Wiederaufnahmehemmer; TZA: trizyklische Antidepressiva
Ein häufig genutzter Vertreter der SSRI ist Citalopram. Die eher antriebssteigernde Wirkung bedingt eine morgendliche Gabe. Neben einer oralen Gabe ist eine i. v. Applikation möglich. Citalopram birgt wie auch Sertralin, das ebenfalls in die Gruppe der SSRI fällt, ein eher geringes Potenzial von Absetzerscheinungen. Im Gegensatz zu Sertralin kann Citalopram jedoch zu einer QT-Zeit-Verlängerung führen. Hier sollte eine Kombination mit anderen Substanzen, die ebenfalls zu einer Verlängerung des QT-Intervalls führen (z. B. Antiarrhythmika, Erythromycin, Ketoconazol, Haloperidol) [23], vermieden werden. Bei kardialen Vorerkrankungen ist eine EKG-Kontrolle vor Therapiebeginn obligat sowie ein Absetzen der Medikation bei Auftreten von Rhythmusstörungen wie einer QTc-Verlängerung auf mehr als 500 ms. Als weitere Nebenwirkungen werden besonders Schlaflosigkeit, Schwindel, Diarrhö, Kopfschmerzen Übelkeit und Mundtrockenheit erwähnt. Beide Präparate werden in der Palliativmedizin auch bei Angst- und Panikstörungen eingesetzt (Tab. 1).
Mirtazapin führt sowohl zu einer Serotonin- und Noradrenalinfreisetzung als auch zu einer Dopaminfreisetzung. Außerdem zeigte es über Antagonismus an Histamin-H1-Rezeptoren eine sedierende Wirkung, sodass eine abendliche Gabe erfolgt und es in einer niedrigen Dosierung von 7,5 mg auch als schlafanstoßendes Präparat verwendet wird. Die antidepressive Wirkung tritt schneller ein als unter SSRI [22] und es besteht nicht die Gefahr von kardiovaskulären Nebenwirkungen. Zusätzlich zeigt es antiemetische Effekte. Aufgrund dieses Wirkprofils findet Mirtazapin häufig Anwendung in der Palliativmedizin, in der Praxis zeigt sich eine rasche Symptomkontrolle und Besserung der Lebensqualität. Eine Kombination mit Monoaminoxidase-(MAO-)Hemmern ist aufgrund der Gefahr eines serotonergen Syndroms kontraindiziert, Medikamenteninteraktion sind aufgrund des Metabolisierungswegs (u. a. CYP3A4) zu beachten. Die bekannte Nebenwirkung der Appetitsteigerung ist in der Palliativmedizin zweitranging oder sogar eher von Nutzen bei häufiger bestehender Inappetenz durch die Grunderkrankung.
Amitriptylin führt zu einer Serotonin- und Noradrenalin-Wiederaufnahmehemmung und wirkt darüber hinaus auch antagonistisch an Muscarin-, H1- sowie Serotonin-(5-HT-)Rezeptoren. Es wird ebenfalls eingesetzt bei der Therapie von Panikstörungen und insbesondere bei neuropathischen Schmerzen. Der analgetische Effekt durch die Noradrenalin-Wiederaufnahmehemmung wird durch einen Antagonismus am NMDA-Glutamat-Rezeptor unterstützt. Außerdem wirkt es antitussiv und ist bei einer Dranginkontinenz einsetzbar. Amitriptylin führt häufig zu anticholinergen Nebenwirkungen wie Mundtrockenheit, Müdigkeit, orthostatischer Hypotonie. Daher erfolgt eine abendliche Gabe, wobei hier auf eine vermehrte Sturzgefahr bei älteren Patienten geachtet werden muss. Mundtrockenheit spielt bei Palliativpatienten, die oftmals nicht mehr genug trinken und essen können, eine große Rolle. Wird diese durch Nebenwirkungen von Arzneimitteln verstärkt, sollten allgemeine Maßnahmen mit Befeuchtungssprays (z. B. Mischung aus Wasser, Orangenöl und Honig) und Lippenpflege regelmäßig durchgeführt werden. Als Folge von Arzneimittelinteraktionen muss auf das Risiko eines serotonergen Syndroms besonders in der Kombination mit anderen fördernden Präparaten geachtet werden, daher ist die Kombination mit MAO-Hemmern kontraindiziert. Weiterhin kann auch Amitriptylin zu einer QTc-Verlängerung führen.
Venlafaxin gehört zu der Gruppe der SSNRI und wird neben der Therapie der Depression auch zur Behandlung von Angststörungen eingesetzt. Die Inhibition der Noradrenalin-Wiederaufnahme nimmt mit steigender Dosierung zu und es kommt zusätzlich zu einer Dopamin-Wiederaufnahmehemmung. Es wird als Mittel der zweiten Wahl eingesetzt, da es eher schlechter verträglich ist. Als Nebenwirkungen treten sehr häufig Mundtrockenheit, Übelkeit, Kopfschmerzen und vermehrtes Schwitzen auf, des Weiteren Schwindel, Verwirrtheit und andere mehr. Die Anwendung von Venlafaxin kann zu einer QT-Intervall-Verlängerung führen, die Interaktion mit anderen Arzneimitteln zudem zu einem erhöhten Risiko eines serotonergen Syndroms. Auch hier ist die gleichzeitige Therapie mit MAO-Hemmern kontraindiziert.
Für Patienten unter 25 Jahren wurde ein Zusammenhang von Einsatz von Antidepressiva mit Suizidgedanken und nichttödlichen Selbstverletzungen beschrieben [6, 17]. Zudem besteht bei allen Patienten das Risiko der Entstehung von Suizidgedanken bis zur Remission der Depression fort. Daher sollte regelmäßig eine multiprofessionelle Evaluation von bereits existierenden oder neu auftretenden Suizidgedanken erfolgen.
Delir
Delir ist gekennzeichnet durch eine veränderte Bewusstseinslage, Verwirrung, Unruhe, gestörten Tag-Nacht-Rhythmus und Störungen in der Wahrnehmung bis hin zu Halluzinationen [3, 11, 14]. Die Unterteilung erfolgt in eine hypoaktive und hyperaktive Form, zudem existieren gemischte Formen [5]. Im palliativmedizinischen Setting finden sich oft gemischte Formen wieder [5, 11].
Bei bis zu 50 % der Patienten mit fortgeschrittenem Tumorleiden auf Palliativstationen kommt es zu deliranten Zuständen, in der Phase kurz vor dem Tod sogar bei bis zu 93 % [11, 14]. Ätiologisch sind paraneoplastische Syndrome, Anämie, Dehydrierung, zerebrale Filiae, metabolische Entgleisungen, Sepsis und die regelmäßige Einnahme von Opioiden anzuführen [3, 5]. Daher sind vor einer medikamentösen Therapie unbedingt möglich reversible Ursachen auszuschließen [11].
In der Behandlung des Delirs spielen allen voran allgemeine Maßnahmen eine zentrale Rolle [5]. Es ist wichtig, eine ruhige und vertraute Umgebung herzustellen, für eine Sturzprophylaxe zu sorgen, die Kommunikation ruhig zu gestalten und eine Kontinuität in der Betreuung zu gewährleisten [5, 14].
Erst nach Versagen dieser Maßnahmen und bei Vorliegen eines schweren Delirs mit zum Beispiel Halluzinationen kann eine medikamentöse Therapie der Symptomkontrolle dienen [9, 11]. Hierbei ist die Studienlage zum Einsatz von Antipsychotika heterogen, es gibt nur wenige randomisierte kontrollierte Studien, die einen Nutzen von Antipsychotika oder eine Überlegenheit einzelner Substanzen bestätigen [5, 9, 11, 14]. Eine jüngst veröffentlichte randomisierte kontrollierte Studie im Setting der Intensivstation zeigte keine Überlegenheit in Überleben und Hospitalisierungsdauer von Haloperidol im Vergleich zu Placebo [1].
Die vergleichsweise breiteste Datenlage liegt für den Einsatz von Haloperidol vor, aufgrund dessen kommt dieses Antipsychotikum beim Delir häufig zum Einsatz [5, 14]. Die Gabe sollte hierbei auf einen kurzen Zeitraum von nur wenigen Tagen angelegt sein [5]. Um eine Überdosierung zur vermeiden, sollte Haloperidol langsam titriert werden und eine Tagesgesamtdosis von 10 mg nicht überschreiten [24].
Substanzklassen
Man teilt Antipsychotika in drei Gruppen ein: Antipsychotika der ersten (früher typische Antipsychotika, z. B. Haloperidol, Levomepromazin, Pipamperon, Melperon), zweiten (früher atypische Antipsychotika, z. B. Olanzapin) und dritten (Aripiprazol) Generation [5]. Patienten in der Palliativmedizin mit oftmals fortgeschrittenem Tumorleiden haben ein durchaus höheres Risiko, unter Nebenwirkungen zu leiden. Dies liegt an bestehenden Komorbiditäten, Polypharmazie, Kachexie und bisweilen fortgeschrittenem Alter sowie Organdysfunktion. Weitere Gründe sind ein reduzierter Stoffwechsel und eine verringerte Eliminationsleistung. In der Palliativmedizin häufig eingesetzt werden die Substanzen Haloperidol, Olanzapin und Levomepromazin, zum Schlafanstoß auch Melperon und Pipamperon. Tabelle 3 zeigt einen Überblick über gängige Antipsychotika, die in der Palliativmedizin Verwendung finden.
Tab. 3. Überblick über die medikamentöse Therapie bei Delir
|
Medikament |
Applikation |
Einzeldosis |
Maximaldosis pro Tag |
|
|
Monotherapie |
Haloperidol |
p. o., s. c. |
0,5–2 mg |
10 mg |
|
Olanzapin |
s. l. |
5 mg |
15 mg |
|
|
Melperon |
p. o. |
25 mg |
150 mg |
|
|
Pipamperon |
p. o. |
12 mg |
80 mg |
|
|
Additive Therapie |
Lorazepam |
i. v. |
0,5–1 mg |
3 mg |
|
Levomepromazin |
p. o. |
15–30 mg |
90 mg |
Die Halbwertszeit von Haloperidol beträgt 13 bis 23 Stunden [20]. Haloperidol hat eine hohe Affinität zum D2-Rezeptor, was die Nebenwirkung der extrapyramidal-motorischen Symptome (EPMS) erklärt [7, 20, 24]. Aber auch QTc-Verlängerungen und Hypotension können auftreten, weshalb bei intravenöser Gabe ein EKG-Monitoring gefordert wird [14, 23]. In der Palliativmedizin wird daher in aller Regel auf eine intravenöse Applikation verzichtet und andere Formen, zum Beispiel eine subkutane Gabe, werden bevorzugt. Weitere unerwünschte Wirkungen wie Tremor, Insomnie, herabgesetzte Krampfschwelle und Akinesie wurden beschrieben [5]. Das Auftreten dieser Nebenwirkungen wird zudem bei Patienten mit fortgeschrittenem Tumorleiden durch eine reduzierte Stoffwechselleistung mit kompromittierter Elimination begünstigt [20, 24]. Aber auch bei älteren Patienten mit Demenz führt Haloperidol zu einer erhöhten Mortalität, weshalb hier eine Dosisreduktion gefordert wird [5, 24]. Aufgrund der zentralnervösen Wirkung wirkt Haloperidol antiemetisch, sedierend und antipsychotisch [24].
Pro Tag kann Haloperidol in einer Dosierung von 0,5 mg bis 2 mg p. o./s. c. bis zu drei Mal gegeben werden [11]. Im Delir bei Finalphase kann Haloperidol subkutan alle zwei bis vier Stunden gegeben werden, in einer Dosierung von 1 bis 2 mg bis zum Erreichen einer suffizienten Symptomkontrolle [24]. Das erhöhte Mortalitätsrisiko und die Veränderungen im EKG sind in dieser Phase zu vernachlässigen, da die Symptomkontrolle Vorrang hat. Daher kann auf ein EKG-Monitoring verzichtet werden [9].
Sollten die Symptome des Delirs persistieren, kann die Dosis gesteigert werden oder eine medikamentöse Kombinationstherapie etabliert werden. Alternativ ist die Rotation auf ein anderes Antipsychotikum denkbar. Hierbei wäre die Gabe von Olanzapin in einer Dosis von 5 mg s. l. alle acht Stunden möglich [11].
Eine Kombination mit Lorazepam (bis zu 3 mg i. v.) kann das Delir bei Therapieversagen einer Monotherapie mit Haloperidol bessern. Wenn auch die potenziell delirogene und zum Teil paradoxe Wirkung bekannt ist, findet diese Kombination in der Palliativmedizin im klinischen Alltag ihre Relevanz. Weiterhin ist eine Kombination mit Midazolam möglich, da dies im Rahmen einer kontinuierlichen Gabe gut steuerbar ist. Außerdem ist auch eine Kombination mit Levomepromazin möglich [12, 14]. Levomepromazin sollte hierbei in einer Startdosis von 15 bis 30 mg bis zu drei Mal am Tag gegeben werden [20].
Weitere Medikamente, die zur Behandlung des Delirs zum Einsatz kommen, sind Melperon und Pipamperon. Pipamperon hat eine hohe Affinität zu D4-Rezeptoren und 5-HT2A-Rezeptoren, wirkt aber auch an anderen Serotonin- und Dopaminrezeptoren. Die Halbwertszeit beträgt 17 bis 22 Stunden, wichtige Nebenwirkungen sind extrapyamidal-motorische Störungen (CAVE: Parkinson-Patienten), QT-Verlängerung, Kopfschmerzen und Krampfanfälle. In der Palliativmedizin sind Patienten oft aufgrund eines gestörten Tag-Nacht-Rhythmus belastet. Hier zeigt die klinische Erfahrung in Konkordanz zur Literatur unter Pipamperon einen guten Schlafanstoß und Rhythmisierung des Nachtschlafs. Melperon wirkt vor allem an D2-Rezeptoren, die Halbwertszeit beträgt sechs bis acht Stunden. Zu Nebenwirkungen gehören auch EPMS, wobei diese selten auftreten, sowie Hypotension. Aufgrund des geringen Nebenwirkungsspektrums wird Melperon bevorzugt im geriatrischen Bereich verabreicht. Melperon sollte dabei in einer Initialdosis von 25 mg verabreicht werden, eine Steigerung auf 50 mg bis zu drei Mal pro Tag ist möglich. Pipamperon sollte in einer Initialdosis von 12 mg verabreicht werden, eine Gabe bis zu 40 mg zweimal pro Tag ist möglich [17].
Levomepromazin ist ein Vertreter der ersten Generation von Antipsychotika und kommt in der Palliativmedizin in der Behandlung von psychomotorischer Unruhe und akuten Erregungszuständen zum Einsatz [20]. Es zeigt eine Affinität zu D2-, H1- und 5-HT2-Rezeptoren und besitzt zudem eine anti-muskarinerge Wirkung [7, 14, 20]. Levomepromazin senkt die Krampfschwelle, führt zu orthostatischer Dysregulation und kann bisweilen zu Müdigkeit und einer Vigilanzminderung führen. Die Halbwertszeit ist mit bis zu 30 Stunden lang, sodass in der Regel eine Einmalgabe suffizient ist [14, 20]. Aufgrund des breiten Wirkspektrums machen Palliativteams im ambulanten Bereich (spezialisierte, ambulante Palliativversorgung [SAPV]) immer wieder von Levomepromazin Gebrauch, da neben einer Symptomkontrolle bei Erregungszuständen in der Finalphase auch Symptome wie Übelkeit gut therapiert werden.
Olanzapin ist ein Vertreter der Antipsychotika der zweiten Generation. Aufgrund der antagonisierenden Wirkung an muskarinergen Rezeptoren wird das Risiko für EPMS im Vergleich zu Antipsychotika der ersten Generation gesenkt [18]. Als typische Nebenwirkung wird Schläfrigkeit beschrieben [18]. Auch Olanzapin hat eine lange HWZ von etwa 30 Stunden, sodass eine Einmalgabe oft ausreichend ist. Neben der Behandlung des Delirs findet Olanzapin auch im Bereich der Antiemese und Anxiolyse in der Palliativmedizin immer wieder Anwendung [18].
Zusammenfassung
Neben der rein somatischen Behandlung von Symptomen wird in der Palliativmedizin Symptomlast auch auf der psychischen, sozialen und spirituellen Ebene erfasst und behandelt. Daher spielen allgemeine Maßnahmen allen voran eine entscheidende Rolle. Hierdurch kann Leid oftmals gelindert werden und die Lebensqualität der Patienten wiederhergestellt werden. Ist eine suffiziente Symptomkontrolle so nicht zu erreichen, spielen im Bereich der psychischen Ebene zur Behandlung von Depressionen, Angst und Delir psychopharmazeutische Substanzen eine wichtige Rolle. Aber auch hierbei ist eine holistische Betrachtung der Patienten und ihrem Leiden wichtig, um Medikamente bedarfsgerecht zu applizieren. In der Palliativmedizin kommt so zum Beispiel dem Off-Label-Use eine wichtige Rolle zu. Mit einem Repertoire an entscheidenden Medikamenten sind Symptome auf der psychischen Ebene zielgerichtet therapierbar, um somit eine Verbesserung der Lebensqualität unter Minimieren des Nebenwirkungsspektrums zu erreichen.
Interessenkonflikterklärung
Es bestehen keine Interessenkonflikte seitens der Autoren.
Literatur
1. Andersen-Ranberg NC, Poulsen LM, Perner A, Wetterslev J, et al. Haloperidol for the treatment of delirium in ICU patients. N Engl J Med 2022;387:2425–35.
2. Baldwin DS, Anderson IM, Nutt DJ, Allgulander C, et al. Evidence-based pharmacological treatment of anxiety disorders, post-traumatic stress disorder and obsessive-compulsive disorder: A revision of the 2005 guidelines from the British Association for Psychopharmacology. J Psychopharmacol 2014;28:403–39.
3. Bruera E, Neumann C. Management of specific symptom complexes in patients receiving palliative care. CMAJ 1998;158:1717–26.
4. Bundesärztekammer (BÄK), Kassenärztliche Bundesvereinigung (KBV), Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF). Nationale Versorgungs-Leitlinie Unipolare Depression – Langfassung, Version 3.0. [Internet]. 2022. Available from: https://register.awmf.org/de/leitlinien/detail/nvl-005 (Zugriff am 25.10.2022).
5. Bush SH, Tierney S, Lawlor PG. Clinical assessment and management of delirium in the palliative care setting. Drugs 2017;77:1623–43.
6. Cleare A, Pariante C, Young A, Anderson I, Christmas D, et al. Evidence-based guidelines for treating depressive disorders with antidepressants: A revision of the 2008 British Association for Psychopharmacology guidelines. J Psychopharmacol 2015;29:459–525.
7. Clemens K, Klaschik E. Übelkeit, Erbrechen und Obstipation in der palliativen Situation. Dtsch Arztebl 2007;104:A269–78.
8. Falk E, Schlieper D, van Caster P, Lutterbeck MJ, et al. A rapid positive influence of S-ketamine on the anxiety of patients in palliative care: a retrospective pilot study. BMC Palliat Care 2020;19:1.
9. Gaertner J, Eychmueller S, Leyhe T, Bueche D, et al. Benzodiazepines and/or neuroleptics for the treatment of delirium in palliative care? A critical appraisal of recent randomized controlled trials. Ann Palliat Med 2019;8:504–15.
10. Goldman N, Frankenthaler M, Klepacz L. The efficacy of ketamine in the palliative care setting: A comprehensive review of the literature. J Palliat Med 2019;22:1154–61.
11. Hui D, Dev R, Bruera E. Neuroleptics in the management of delirium in patients with advanced cancer. Curr Opin Support Palliat Care 2016;10:316–23.
12. Hui D, Frisbee-Hume S, Wilson A, Dibaj SS, Nguyen T, et al. Effect of lorazepam with haloperidol vs haloperidol alone on agitated delirium in patients with advanced cancer receiving palliative care. JAMA 2017;318:1047–56.
13. Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): Psychoonkologische Diagnostik, Beratung und Behandlung von erwachsenen Krebspatienten, Langversion 1.1 [Internet]. 2014. Available from: www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Psychoonkologie/Psychoonkologieleitlinie_1.1/LL_PSO_Langversion_1.1.pdf (Zugriff am 25.10.2022).
14. Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): Palliativmedizin für Patienten mit einer nicht-heilbaren Krebserkrankung, Langversion 2.2, AWMF-Registernummer: 128/001OL [Internet]. 2020. Available from: https://www.leitlinienprogramm-onkologie.de/leitlinien/palliativmedizin/ (Zugriff am 25.10.2022).
15. McIntyre RS, Rosenblat JD, Nemeroff CB, Sanacora G, et al. Synthesizing the evidence for ketamine and esketamine in treatment-resistant depression: An international expert opinion on the available evidence and implementation. Am J Psychiatry 2021;178:383–99.
16. Möhler H. The rise of a new GABA pharmacology. Neuropharmacology 2011;60:1042–9.
17. Rémi C, Bausewein C, Twycross R, Wilcock A, Howard P. Arzneimitteltherapie in der Palliativmedizin. 3. Aufl. München: Elsevier, 2018.
18. Saudemont G, Prod’Homme C, da Silva A, Villet S, et al. The use of olanzapine as an antiemetic in palliative medicine: a systematic review of the literature. BMC Palliat Care 2020;19:56.
19. Schwartz J, Neukirchen M, Hornemann B, Gärtner J, et al. Depression in der Palliativmedizin. Onkologie 2022;28:931–6.
20. Stübner S, Grohmann R, Eckermann G, Hiemke C, Lorenzl S. Psychopharmaka in der Palliativmedizin: Diskussionswürdige Praxis. Dtsch Arztebl 2018;115:A868–71.
21. The diagnosis of and treatment recommendations for anxiety disorders, Langversion 2, AWMF Registernummer: 051–028 [Internet]. 2021. Available from: https://www.awmf.org/uploads/tx_szleitlinien/051-028l_S3_Behandlung-von-Angststoerungen_2021-06.pdf (Zugriff am 26.10.2022).
22. Watanabe N, Omori IM, Nakagawa A, Cipriani A, et al. Mirtazapine versus other antidepressive agents for depression. Cochrane Database Syst Rev 2011;(12):CD006528.
23. Yap YG. Drug induced QT prolongation and torsades de pointes. Heart 2003;89:1363–72.
24. Zaporowska-Stachowiak I, Stachowiak-Szymczak K, Oduah MT, Sopata M. Haloperidol in palliative care: Indications and risks. Biomed Pharmacother 2020;132:110772.
Dr. med. Yann-Nicolas Batzler, Dr. med. Jaqueline Schwarz, Interdisziplinäres Zentrum für Palliativmedizin, Medizinische Fakultät und Universitätsklinikum Düsseldorf, Heinrich-Heine-Universität Düsseldorf, Moorenstraße 5, 40225 Düsseldorf, E-Mail: yannic.batzler@med.uni-duesseldorf.de
Priv.-Doz. Dr. med. Martin Neukirchen, Interdisziplinäres Zentrum für Palliativmedizin und Klinik für Anästhesiologie, Medizinische Fakultät und Universitätsklinikum Düsseldorf, Heinrich-Heine-Universität Düsseldorf
Psychopharmacotherapy in palliative medicine. Clinically relevant problems from the perspective of palliative care medicine
In palliative care psychotropic drugs are frequently used. Palliative care is defined by a holistic approach in determining symptoms and controlling those symptoms. Symptoms are assessed and treated on somatic, psychic, spiritual and social dimensions. The goal is to ameliorate quality of life. On the psychic level symptoms such as anxiety and agitation, depressions and delirium are frequent. This review aims to give an overview over the common medications used treating those conditions from the perspective of palliative care. It is important to note that treatments are embedded within a multiprofessional approach through specially trained physicians, nurses and psychologists.
Key words: Palliative care, delirium, anxiety, depression
Psychopharmakotherapie 2023; 30(02):40-46
