Siegfried Kasper, Wien
Es gibt Hinweise, dass bereits die Neandertaler vor 50 000 Jahren Pflanzen zur Behandlung von Krankheiten verwendeten [25]. In Indien, China, Mesopotamien und Ägypten wurden mehrere tausend Jahre alte Aufzeichnungen über die Anwendung von Heilpflanzen gefunden [74]. In Europa begannen die Benediktiner etwa im 8. Jahrhundert n. Chr., Überlieferungen zur therapeutischen Anwendung von Pflanzen zu sammeln. Im Mittelalter hüteten vor allem Klöster wie die Abtei der Hildegard von Bingen (1098–1179) die Heilgeheimnisse der Kräuter und Pflanzen. Die wissenschaftliche Auseinandersetzung mit pflanzlichen Zubereitungen als Therapeutika geht im Wesentlichen auf Hippokrates (ca. 460–370 v. Chr.) zurück. Den Grundstein für die moderne Phytotherapie legte Paracelsus (1493–1541), indem er Extraktionsverfahren einsetzte, um „der Pflanze die Seele zu entlocken“. Er beschrieb Johanniskraut als Kraut gegen „Geister und tolle Phantasien, die den Menschen in Verzweiflung bringen“ [52]. Die Verwendung von Arzneipflanzen, die die Psyche und das Nervensystem beruhigen und ausgleichen, hat eine lange Tradition und ist heute aufgrund der vielfältigen psychischen Belastungen möglicherweise so aktuell wie nie zuvor. Pflanzliche Arzneimittel werden in der Regel gut vertragen.
In den Vereinigten Staaten ergab eine nationale Haushaltsbefragung, dass pflanzliche Arzneimittel und Nahrungsergänzungsmittel die am häufigsten verwendeten komplementären Therapien für psychische Störungen sind, wobei unter anderem Johanniskraut-Präparate (Hypericum perforatum L.) bei depressiver Verstimmung am häufigsten verwendet werden [68]. Für Deutschland zeigte eine repräsentative Stichprobe Präferenzen für die Behandlung depressiver Symptome mit Phytotherapeutika [5]. Die Akzeptanzrate war im Vergleich zu synthetischen Antidepressiva etwa sechsmal höher, sodass die Autoren von einer besseren Compliance bei pflanzlichen Präparaten ausgehen. Es ist davon auszugehen, dass hierzu auch das gegenüber synthetischen Substanzen oft günstigere Risikoprofil beiträgt [40, 82].
Die rationale Phytotherapie integriert jahrhundertealtes Erfahrungswissen in die moderne, evidenzbasierte Medizin und bedient sich dabei der gleichen wissenschaftlichen Methoden, die auch bei der Prüfung chemisch-synthetischer Wirkstoffe zur Anwendung kommen [73]. Dies schließt die Verifizierung der Wirksamkeit und Verträglichkeit mithilfe kontrollierter klinischer Studien ein. Den hohen Stellenwert von evidenzbasierten Phytopharmaka zur Behandlung von psychischen Erkrankungen tragen die Empfehlungen der aktuellen Leitlinie der World Federation of Societies of Biological Psychiatry (WFSBP) und des Canadian Network for Mood and Anxiety Treatments (CANMAT) Rechnung [69]. Präparate, die im Rahmen einer rationalen, evidenzbasierten Phytotherapie infrage kommen, müssen daher definierten Anforderungen genügen (Kasten 1).
Kasten 1. Anforderungen an Präparate für die evidenzbasierte Phytotherapie
- Definierter Extrakt in nachweislich gleichbleibender Qualität
- Klinische Wirksamkeit in randomisierten, kontrollierten Doppelblindstudien belegt; vorzugsweise Vorliegen von systematischen Reviews und Metaanalysen (Evidenzgrad 1 oder 2, vgl. Tab. 1)
- In der Europäischen Union als Arzneimittel zugelassen
Tab. 1. Kriterien für den Evidenzgrad von Arzneimitteln [66]
|
Evidenzgrad |
Kriterien |
|
1 |
Metaanalyse mit „schmalen“ Konfidenzintervallen und/oder mindestens zwei RCTs mit ausreichender Fallzahl, vorzugsweise Placebo-kontrolliert |
|
2 |
Metaanalyse mit „weiten“ Konfidenzintervallen und/oder mindestens ein RCT mit ausreichender Fallzahl |
|
3 |
RCTs mit geringer Fallzahl, oder nicht randomisierte, kontrollierte, prospektive Studien, oder Fallserien, oder qualitativ hochwertige, retrospektive Studien |
|
4 |
Expertenmeinung/Konsens |
RCT: randomisierte, kontrollierte Studie (randomized, controlled trial)
Die vorliegende Übersichtsarbeit präsentiert vier pflanzliche Zubereitungen (Lavendelöl Silexan®, Ginkgo-biloba-Spezialextrakt EGb 761®, methanolischer Johanniskraut-Extrakt wie WS® 5570 und Rhodiolaextrakt), die die Anforderungen an eine evidenzbasierte Phytotherapie erfüllen (Tab. 2).
Für weitere Pflanzenextrakte, die ebenfalls bei psychischen Beschwerden und Erkrankungen weltweit zum Einsatz kommen, ist trotz teilweise guter Datenlage bislang noch keine einheitliche Evidenzbeurteilung verfügbar (Kasten 2).
Tab. 2. Überblick der beschriebenen Wirkstoffe und der zugehörige Evidenzgrad
|
Wirkstoff |
Indikation |
Evidenzgrad# |
Empfehlung$ |
Referenz |
|
Lavendelöl Silexan® |
Angststörungen und Komorbiditäten |
1 |
B |
[69] |
|
Unruhe |
2 |
I |
||
|
Depressionen |
2 |
C |
[69] |
|
|
Ginkgo-biloba-Spezialextrakt EGb 761® |
Demenz |
1 |
B, C, I |
[14, 32] |
|
BPSD |
1 |
0 |
||
|
MCI |
2 |
0 |
||
|
Begleitend bei Schizophrenie |
2 |
C |
[69] |
|
|
Methanolischer Hypericumextrakt (u. a. WS 5570) |
Leichte bis mittelschwere Depression |
1 |
A, C, I |
[8, 69] |
|
Rhodiolaextrakt SHI |
Mentaler Stress |
3 |
I |
|
|
Mentale Schwäche |
3 |
I |
# Vgl. Kasten 1
$ A: „Soll“; B: „Sollte“; C: „Kann“; I: Indikation im Rahmen der Zulassung als Arzneimittel; 0: keine Leitlinien-Empfehlung verfügbar
BPSD: Behavioural and Psychological Symptoms of Dementia; MCI: Mild Cognitive Impairment
Kasten 2. Bei psychischen Beschwerden und Erkrankungen eingesetzte Pflanzenextrakte ohne einheitliche Evidenzbeurteilung
Für Extrakte aus der Baldrianwurzel, Passionsblume und Melissenblätter [55], auch in Kombination [17], liegen Daten für Patienten mit Schlafstörungen sowie für hyperaktive Kinder [24] vor. Die Bewertung der Evidenz ist jedoch uneinheitlich.
Metaanalysen überwiegend kleinerer Studien weisen auf einen antidepressiven Effekt von Safran (Crocus sativus) hin [62, 81]. Safran-Extrakte sind jedoch bislang weder im Iran, wo die meisten der Studien durchgeführt wurden, noch in der EU als Arzneimittel zugelassen.
Für Cannabis und Cannabinoide liegen klinische Studien für mehrere Krankheitsbilder wie Depression, Angst, Tourette-Syndrom oder ADHS vor; ein systematischer Review fand jedoch lediglich eingeschränkte Evidenz für eine mögliche Wirksamkeit bei Angststörungen [7].
Zu Curcuma, Galphimia, Ashwagandha existieren in der aktuellen WFSBP/CANMAT Phytopharmaka-Leitlinie schwache oder vorläufige Empfehlungen bei Stimmungs- bzw. Angststörungen [69]; solche Präparate sind in Deutschland jedoch bislang wegen der fehlenden Standardisierung nicht als Arzneimittel zugelassen.
Evidenzbasierte Phytopharmaka
Lavendelöl Silexan® (Lavandula angustifolia/ officinalis)
Wirksamkeit
Lavendelöl ist ein ätherisches Öl das derzeit als einziger pflanzlicher Wirkstoff in der anatomisch-therapeutisch-chemischen (ATC) Klassifikation der WHO als „Anxiolytikum“ geführt wird. Dies leitet sich aus kontrollierten klinischen Studien ab, von denen viele mit Silexan® durchgeführt wurden, das in Deutschland als Arzneimittel zur Behandlung von Unruhezuständen bei ängstlicher Verstimmung zugelassen ist. Randomisierte, Placebo-kontrollierte Doppelblindstudien weisen die Wirksamkeit bei syndromalen (ICD-10-Code F41.1) und subsyndromalen (F41.9) Angststörungen nach [41, 42], des Weiteren bei Unruhezuständen mit Schlafstörungen (R45.1) [37]. In einer Metaanalyse von fünf randomisierten Doppelblindstudien über zehn Wochen nahm der Gesamtwert der Hamilton-Angstskala bei mit Silexan® behandelten Patienten im Mittel um 2,93 Punkte (95%- Konfidenzintervall [KI] 1,08; p < 0,01) stärker ab als unter Placebo [15]. Weitere Metaanalysen bestätigten mit höchstem Evidenzgrad die anxiolytische Wirkung von Silexan® [22, 44, 58, 89].
Angst- und depressive Störungen besitzen eine hohe Komorbidität und sind wechselseitige Risikofaktoren. Bei Patienten mit gemischter Angst und Depression bewirkte Silexan® eine gegenüber Placebo auch signifikant stärkere Reduktion der depressiven Symptomatik, wie eine randomisierte, Placebo-kontrollierte Studie zeigte [46]. Dies bestätigte eine Metaanalyse bei Patienten mit subsyndromalen Angststörungen, da hier ebenfalls eine signifikante Reduktion komorbider depressiver Symptome unter Behandlung mit Silexan® eintrat [4].
Eine weitere Metaanalyse zeigte eine günstige Wirkung von Silexan® auf somatische Komorbiditäten von Angsterkrankungen, wobei insbesondere eine Besserung der kardiovaskulären, urogenitalen und muskulären Begleitsymptome sowie von Schmerzzuständen nachweisbar war [84]. Diese ergab sich sowohl aus der Selbstbeurteilung der Patienten als auch aus der Beurteilung durch den Therapeuten.
Empfehlungen
Die WFSBP/CANMAT Guideline [69] spricht für Lavandula officinalis L. (syn. Lavandula angustifolia) eine vorläufige Empfehlung für die Behandlung von generalisierten Angststörungen aus sowie eine schwache Empfehlung für die Behandlung der Major Depression. Beide Empfehlungen gelten für die Monotherapie oder als ergänzende Behandlung, jeweils in der Dosierung 80 bis 160 mg/Tag ätherisches Öl in Weichgelatinekapseln oder 500 mg bis 15 g getrocknete Blüten/Tag. Die Leitlinie empfiehlt jedoch klar, die standardisierte Kapsel Teezubereitungen unbekannter Qualität vorzuziehen. Silexan® ist in Deutschland derzeit das einzige Lavendelöl, das als Arzneimittel in einer Kapsel verfügbar ist und eine einfache Handhabung und einheitliche Dosierung erlaubt. Zwei der drei Studien, auf denen diese Empfehlung beruht, wurden damit durchgeführt [37, 41]. Weitere inzwischen publizierte randomisierte Doppelblindstudien mit Silexan® [42, 44, 46] und Metaanalysen blieben noch unberücksichtigt.
Wirkungsmechanismen und Inhaltsstoffe
Silexan® wird durch Dampfdestillation aus den Blüten von Lavandula angustifolia Mill. gewonnen. Der Extrakt entspricht in allen Qualitätsparametern den Vorgaben der Monographie zu Lavendelöl im Europäischen Arzneibuch und besitzt einen besonders hohen Anteil der für die Wirkung relevanten Inhaltsstoffe Linalool und Linalylacetat.
Die pharmakologischen Grundlagen der therapeutischen Anwendung von Silexan® wurden in Studien aufgeklärt und in der Literatur ausführlich beschrieben [45, 60, 61]. Es bewirkt eine Blockade spannungsabhängiger Calciumkanäle (VOCC [voltage-operated calcium channels]) und reduziert dadurch den Calciumeinstrom unter anderem im Hippocampus. Silexan® hat jedoch keine Affinität zu den Zielstrukturen anderer Anxiolytika wie dem GABA(Gamma-Aminobuttersäure)-A-Rezeptor [75]. Silexan® reduziert zudem signifikant das Bindungspotenzial der Serotonin-1A-Rezeptoren im Gehirn (Abb. 1). Dies legt nahe, dass die anxiolytische Wirkung auch auf einem veränderten Bindungsverhalten des Neurotransmitters Serotonin beruhen könnte [3].
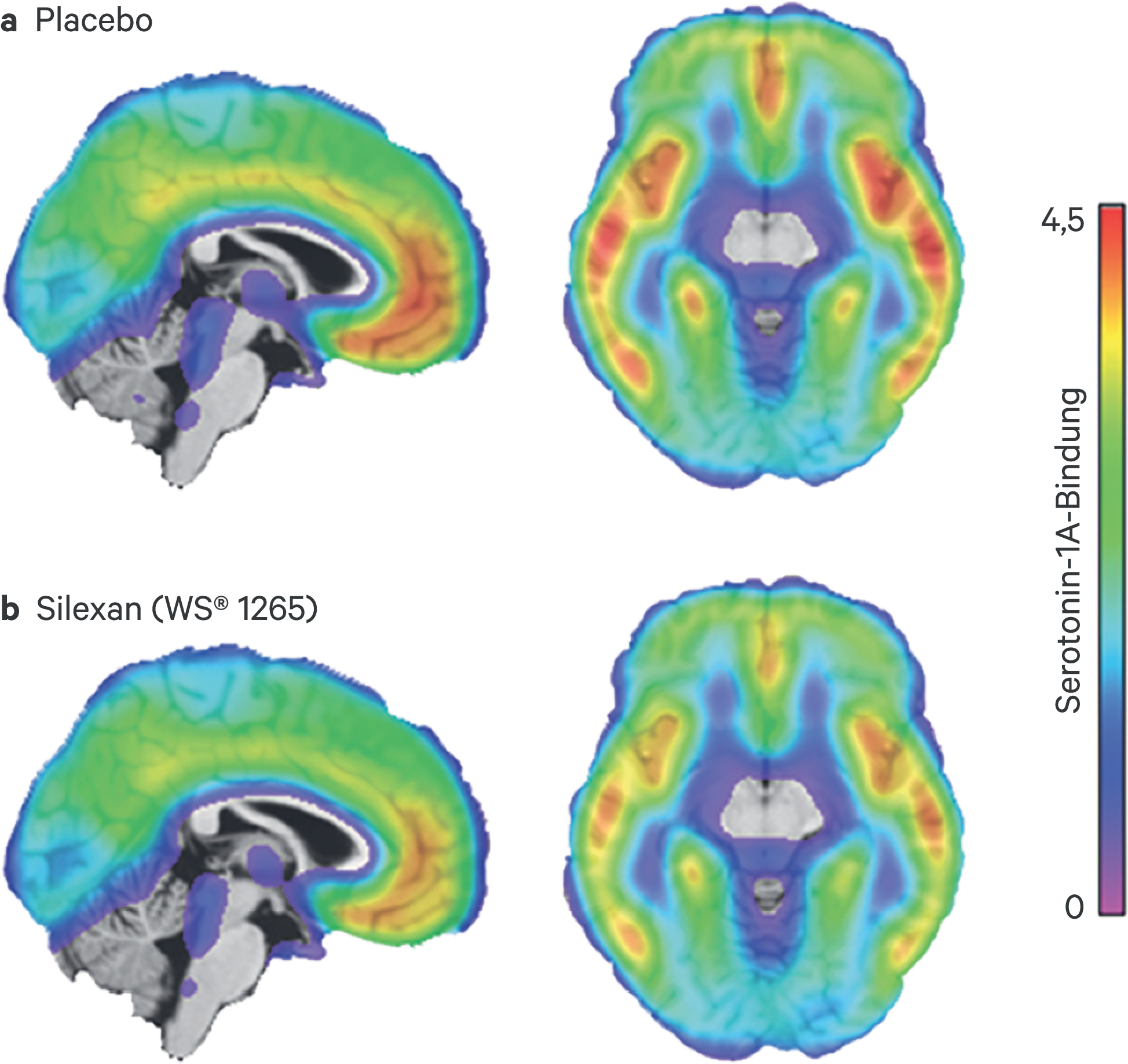
Abb. 1. Durchschnittliches Serotonin-1A-Rezeptor-Potenzial (5-HT1A) bei gesunden Probanden nach chronischer Einnahme von (a) Placebo und (b) Silexan. Mithilfe der Positronen Emissionstomographie ist eine reduzierte 5-HT1A-Rezeptorbindung nach der Einnahme von Silexan in mehreren Gehirnregionen festzustellen. Die Abbildung wurde bereits publiziert [aus 3] und dankenswerterweise von Pia Baldinger et al. zum erneuten Abdruck überlassen.
Sicherheit und Verträglichkeit
In klinischen Studien beschränkten sich unerwünschte Wirkungen, die Silexan® zugeschrieben wurden, auf gastrointestinale Probleme wie Übelkeit, Aufstoßen, Atemgeruch (nach Lavendel) oder Diarrhö [89]. Im Gegensatz zu Benzodiazepinen weist das Präparat weder das Potenzial für Abhängigkeit auf [76], noch zeigten sich Anhaltspunkte für einen sedierenden Effekt. Die Einnahme von Silexan® beeinträchtigt auch nicht die Fahrtüchtigkeit, wie eine kontrollierte Studie zeigte [59]. Aus einer Metaanalyse geht hervor, dass Silexan® weder direkt schlafinduzierend noch sedierend wirkt. Vielmehr ist die günstige Beeinflussung der Schlafqualität als indirekte Folge der Anxiolyse erklärbar [77].
Silexan® zeigt keine Interaktionseffekte mit Kontrazeptiva [27] und führt weder zu einer Induktion noch zu einer Inhibition der Cytochrom-P450-Enzyme CYP1A2, 2C9, 2C19, 2D6, and 3A4 [16], sodass Interaktionen mit anderen Arzneimitteln nicht zu erwarten sind.
Ginkgo-biloba-Spezialextrakt EGb 761®
Wirksamkeit
Der Ginkgo-Baum (Ginkgo biloba L.) ist in China heimisch und wurde im 18. Jahrhundert von holländischen Seefahrern nach Europa gebracht. Gemäß ATC-Klassifikation der WHO gehören Extrakte aus Ginkgo-Blättern zu den Antidementiva.
Der Spezialextrakt EGb 761® ist in Deutschland als Arzneimittel zur Verbesserung einer altersbedingten kognitiven Beeinträchtigung und der Lebensqualität bei leichter Demenz zugelassen. Bei Patienten mit leichter bis mittelschwerer Demenz verbesserten sich unter Behandlung mit EGb 761® die kognitiven Fähigkeiten [28, 33] sowie neuropsychiatrische Symptome [70]. Eine Metaanalyse zeigte die Wirksamkeit von EGb 761® speziell bei der Behandlung von Auffälligkeiten des Verhaltens und der Psyche bei Demenzpatienten (Behavioral and psychological symptoms of dementia [BPSD]) [31]. Mehrere randomisierte, kontrollierte Doppelblindstudien wiesen die Wirkung bei leichter bis mittelschwerer Demenz nach, was durch Metaanalysen unabhängig voneinander bestätigt wurde [20, 26, 80]. Die Überlegenheit von EGb 761® gegenüber Placebo war bei Tagesdosen von 240 mg insgesamt stärker ausgeprägt als bei 120 mg pro Tag [80]; die ausreichende Dosierung ist somit essenziell für die Wirksamkeit. Im prädemenziellen Frühstadium, das heißt bei leichter kognitiver Beeinträchtigung (Mild cognitive impairment [MCI]), erwies sich der pflanzliche Extrakt ebenfalls als wirksam [21, 23].
Empfehlungen
Bei Alzheimer-Demenz empfehlen die WFSBP Guidelines for the Biological Treatment of Alzheimer’s Disease and Other Dementias EGb 761® gleichrangig mit Acetylcholinesterase-Hemmern [32]. Für diese Indikation gibt es für EGb 761® auch eine positive Nutzenbewertung durch das Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG) [34]. Die aktuelle S3-Leitlinie „Demenzen“ der Deutschen Gesellschaft für Psychiatrie und der Deutschen Gesellschaft für Neurologie attestiert EGb 761® bei einer Tagesdosis von 240 mg positive Effekte auf die Kognition bei Patienten mit leichter bis mittelgrader Alzheimer-Demenz oder vaskulärer Demenz und spricht eine „Kann“-Empfehlung aus [14]. Die aktuelle WFSBP/CANMAT Guideline [69] behandelt die Indikation Demenz nicht, gibt aber für Ginkgo-biloba-Extrakt eine schwache Empfehlung für die begleitende Behandlung bei Schizophrenie. Auch das Committee on Herbal Medicinal Products (HMPC) der European Medicines Agency (EMA) bestätigt die Wirksamkeit zur Verbesserung einer altersbedingten kognitiven Beeinträchtigung und der Lebensqualität bei leichter Demenz [10].
Wirkungsmechanismen und Inhaltsstoffe
EGb 761® ist ein Spezialextrakt, der die Vorgaben des Europäischen Arzneibuchs für die Bestandteile Flavonoidglykoside, Bilobalid und die Ginkgolide A, B und C übererfüllt [71]. Als wesentlicher Wirkungsmechanismus gilt heute eine verbesserte mitochondriale Funktion durch direkt antioxidative Effekte (Polyphenole) und eine direkte Beeinflussung der Mitochondrien (Bilobalid, Ginkgolide), die die meisten anderen Effekte wie verbesserte Kognition und Effekte auf die Neuroplastizität erklärt [59a]. Effekte auf die Blutvikosität und die Mikrozirkulation im Gehirn, die vor Jahren auch für Nootropika wie Piracetam beschrieben wurden [79], gelten heute als nicht mehr relevant. Im Tiermodell begrenzt EGb 761® die stressinduzierte Hypersekretion von Corticosteron [91]. EGb 761® reduziert die Produktion freier Radikale im präfrontalen Kortex, wirkt als Radikalfänger und schützt dadurch Neuronen vor oxidativen Schäden und Apoptose. Der Extrakt verbessert somit das Kurzzeitgedächtnis und beugt altersbedingten oxidativen Schäden und neuronalem Zelltod vor [57].
Sicherheit und Verträglichkeit
In einer Metaanalyse von 44 randomisierten Doppelblindstudien mit insgesamt rund 6400 Patienten zeigten sich unter EGb 761® leicht erhöhte Inzidenzen von gastrointestinalen Beschwerden, allergischen Hautreaktionen und Kopfschmerzen, jedoch kein erhöhtes Blutungsrisiko (Abb. 2) [72]. Eine Metaanalyse [47] sowie eine Auswertung von Daten einer klinischen Prüfung [48] erbrachten keine Hinweise auf eine Beeinflussung der Gerinnungsmarker durch EGb 761®. Der Extrakt zeigt keine Effekte auf das Cytochrom-P450-Enzymsystem und lässt daher keine relevanten Interaktionen mit anderen Arzneimitteln erwarten [90]. In einer kürzlich publizierten Interaktionsstudie ergaben sich auch keine Hinweise auf Interaktionen mit dem direkten Faktor-Xa-Inhibitor Rivaroxaban [29] als Vertreter für direkte orale Antikoagulanzien. Auf der Grundlage von Einzelfallberichten finden sich in einigen Packungsbeilagen zugelassener Präparate dennoch Warnhinweise bezüglich Wechselwirkungen mit gerinnungshemmenden Stoffen.
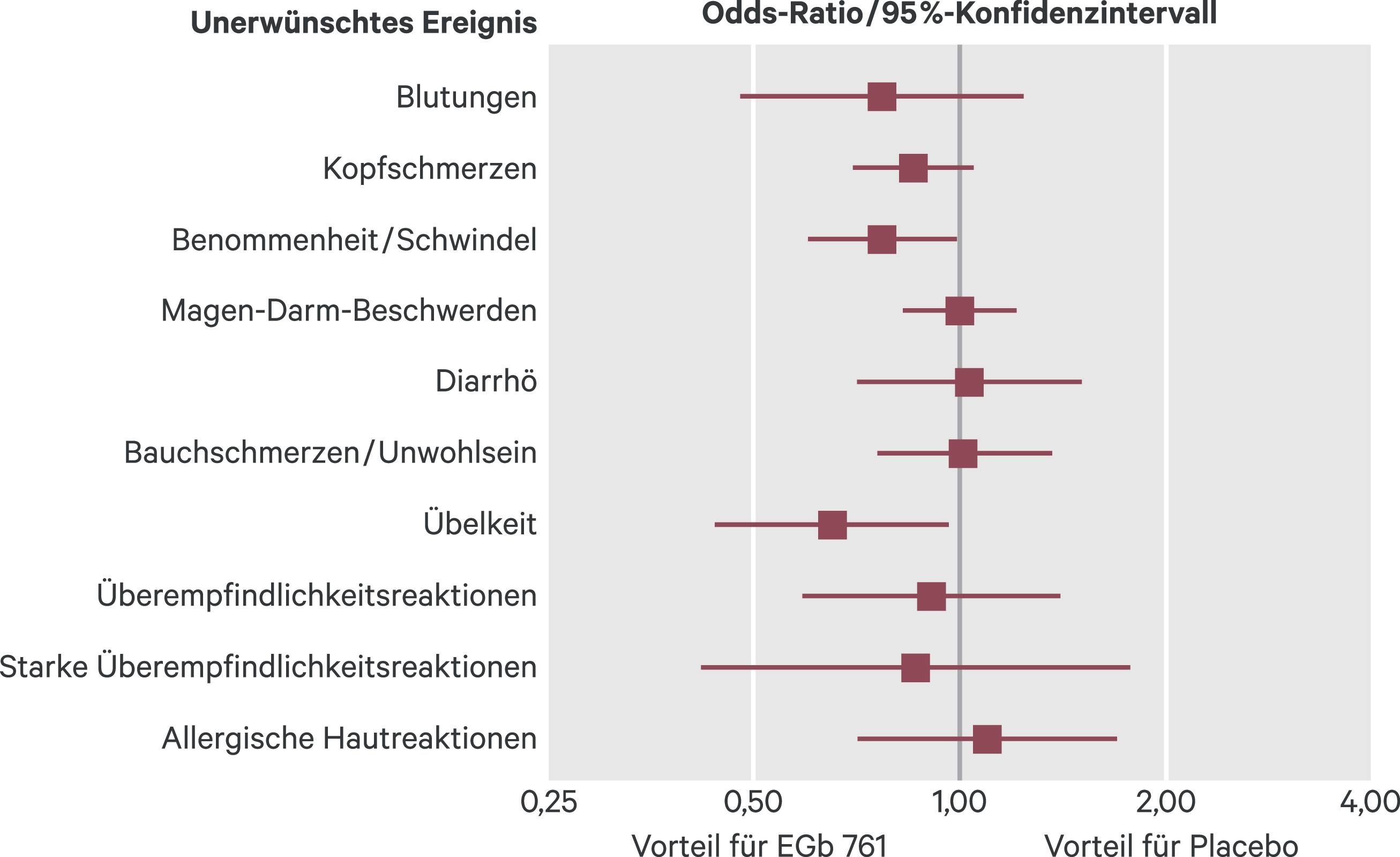
Abb. 2. Auftreten unerwünschter Ereignisse unter EGb 761 und Placebo in 44 randomisierten Doppelblindstudien – Ergebnisse einer Metaanalyse (Odds-Ratios und 95%-Konfidenzintervalle) [72]
Extrakt aus den Blättern von Hypericum perforatum
Wirksamkeit
Wie bereits einleitend beschrieben, gehört Johanniskraut (Hypericum perforatum L.) zu den in der europäischen Medizin am längsten gebräuchlichen Heilpflanzen. Einige ethanolische und methanolische Extrakte sind in Deutschland als Arzneimittel zur Behandlung von leichten bis mittelschweren depressiven Episoden zugelassen.
Johanniskrautextrakte gehören zu den am besten untersuchten, rationalen Phytotherapeutika. Ein Cochrane-Review kommt auf der Basis von 29 klinischen Prüfungen mit insgesamt knapp 5500 Patienten zu dem Ergebnis, dass hochwertige ethanolische und methanolische Johanniskrautextrakte wie WS® 5570 bei leichten bis mittelschweren Depressionen gegenüber Placebo überlegen und ebenso wirksam sind wie selektive Serotonin-Wiederaufnahmehemmer (SSRI) und Trizyklika (TCA). Im Vergleich zu diesen chemischen Antidepressiva werden sie jedoch besser vertragen [56]. Die Ergebnisse werden durch neuere Metaanalysen bestätigt [2, 64]. Eine Übersichtsarbeit, ausschließlich auf der Grundlage von Studien mit WS® 5570, bestätigt diese Resultate ebenfalls [19]. Dabei wirkt der Extrakt positiv auf die Kernsymptome der Depression und reduziert komorbide Beschwerden wie Schlaf- oder somatische Befindlichkeitsstörungen [38].
Empfehlungen
Die aktuelle WFSBP/CANMAT-Leitlinie [69] spricht eine starke Empfehlung für Hypericumextrakt als Mittel der ersten Wahl bei leichten bis mittelschweren Depressionen aus. Grundlage dafür sind verschiedene Metaanalysen zur Wirksamkeit [2]. Dies gilt jedoch nur für Präparate wie u. a. WS® 5570, die einen definierten Gehalt an Hypericin und Hyperforin enthalten. Auch die deutsche S3-Leitlinie zu unipolaren Depressionen [8] gibt eine „Kann“-Empfehlung für apothekenpflichtige Präparate.
Wirkungsmechanismus und Inhaltsstoffe
Hypericumextrakt ist ein Gemisch aus mehr als 150 Inhaltsstoffen, von denen insbesondere Hypericin, Hyperforin, Pseudohypericin, Hyperosid und Amentoflavon für die antidepressive Wirkung verantwortlich gemacht werden [63]. Der methanolische Hypericum-Extrakt WS 5570 ist auf einen Gehalt von 3 bis 6 % Hyperforin, 0,1 bis 0,3 % Hypericin, ≥ 6 % Flavonoide und ≥ 1,5 % Rutin eingestellt.
An seiner pharmakologischen Wirkung sind verschiedene Mechanismen beteiligt. Johanniskrautextrakt modifiziert die Wiederaufnahme von Serotonin (5-HT), Dopamin und Noradrenalin aus dem synaptischen Spalt und blockiert die neuronale Aufnahme von GABA. Ein weiterer Mechanismus besteht in einer Erhöhung der Anzahl oder der Dichte der 5-HT2-Rezeptoren im frontalen Kortex. Schließlich hemmt Johanniskrautextrakt in einem geringen Ausmaß die Enzymaktivität von Monoaminoxidase (MAO) und Catechol-O-Methyltransferase (COMT) sowie die Freisetzung von Interleukin 6 [9, 67].
Eine entscheidende Rolle scheint Hyperforin zu spielen [18, 59b], wie eine vergleichende Studie zeigte. Ein Extrakt mit einem Hyperforin-Gehalt von 0,5 % entfaltete keine relevante antidepressive Wirkung, während ein ansonsten gleicher Extrakt mit 5 % Hyperforin einen signifikanten antidepressiven Effekt besitzt (Abb. 3) [54].
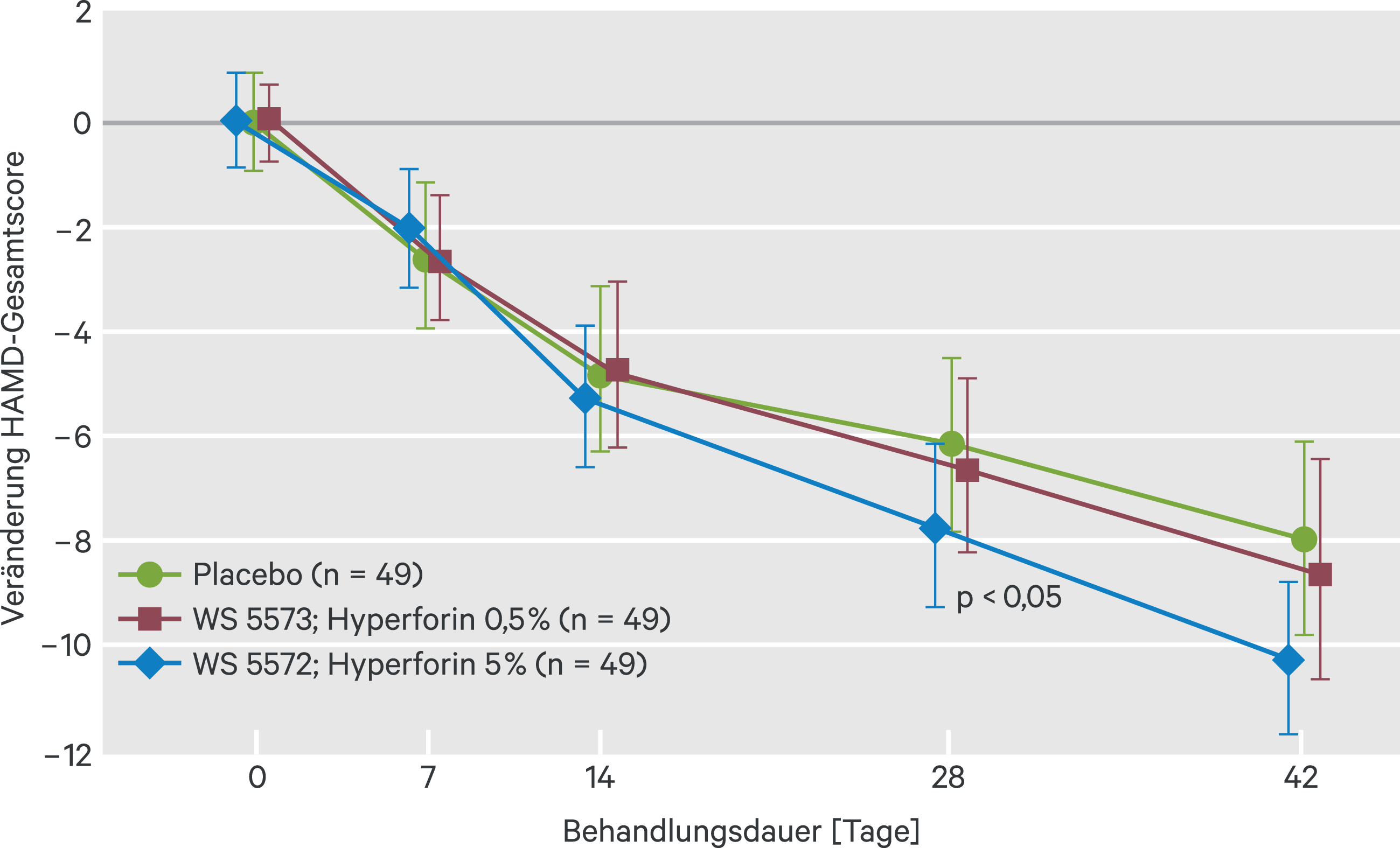
Abb. 3. Veränderung des Gesamtscores der Hamilton-Depressionsskala (HAMD) gegenüber der Baseline bei Behandlung mit einem Hyperforin-reichen und einem Hyperforin-armen Hypericumextrakt oder Placebo [nach 54]. Mittelwerte und 95%-Konfidenzintervalle.
Sicherheit und Verträglichkeit
Für Hypericumextrakte allgemein sind als mögliche Begleiterscheinungen Photosensibilisierung, seltene allergische Hautreaktionen, Müdigkeit oder Unruhe sowie ebenfalls seltene gastrointestinale Beschwerden bekannt. In klinischen Prüfungen lag die Rate unerwünschter Ereignisse unter WS® 5570 durchgängig auf Placebo-Niveau sowie signifikant niedriger als bei SSRI und anderen synthetischen Antidepressiva [40]. Johanniskrautextrakt ist ein potenter Induktor des Transmembran-Transporters P-Glykoprotein und des Cytochrom-P450-Enzymsystems, über das etwa zwei Drittel aller verschreibungspflichtigen Medikamente, u. a. Immunsuppressiva oder synthetische Antidepressiva, metabolisiert werden. Da deren Plasmaspiegel durch die gleichzeitige Einnahme von Hypericumextrakt erniedrigt werden kann, ist wie bei allen Antidepressiva eine sorgfältige Beachtung möglicher Wechselwirkungen notwendig [67].
Extrakt aus den Wurzeln von Rhodiola rosea
Wirksamkeit
Rosenwurz (Rhodiola rosea L.) ist eine in arktischen Gebieten und Gebirgsregionen Eurasiens und Nordamerikas vorkommende Pflanze, die vor allem in Nordeuropa seit Jahrhunderten als Heilpflanze angewandt wird. In Deutschland ist der Extrakt Rosalin® als Arzneimittel zur vorübergehenden Linderung von Stress-Symptomen wie Müdigkeits- und Schwächegefühl zugelassen.
In Übersichtsarbeiten mit randomisierten, kontrollierten Studien mit Rhodiolaextrakten wurde über eine Wirksamkeit bei stressinduzierten, geistigen Erschöpfungszuständen, Depressionen, Angstsymptomen sowie bei Stresssymptomen und zur Steigerung der geistigen Leistungsfähigkeit berichtet [30, 35]. Für Rosalin® geben exploratorische, nicht kontrollierte Studien Hinweise auf eine Besserung der Symptomatik bei Burnout-Patienten [39] sowie auf eine Verbesserung der mentalen Schnelligkeit bei gesunden Probanden [50]. In einer offenen, kontrollierten Studie mit Patienten mit Angstsymptomen zeigten sich unter Rosalin® in der Selbsteinschätzung eine Abnahme von Angst- und Stresssymptomen sowie von Verwirrtheit und Depressivität [13]. Eine mögliche stressreduzierende Wirkung von Rosalin® wurde auch in einem In-vitro-Modell an Humanzellen gezeigt [1].
Empfehlungen
Zu Rhodiolaextrakten liegen derzeit noch keine spezifischen Leitlinien-Empfehlungen vor. Die Zulassung von Rosalin® in Deutschland beruht auf einer seitens des HMPC bestätigten Wirkplausibilität aus der traditionellen Anwendung. Das HMPC kommt zu dem Schluss, dass die Anwendung des Extrakts als sogenanntes Adaptogen durch klinische Daten gestützt wird [11, 12].
Wirkungsmechanismus und Inhaltsstoffe
Rhodiolaextrakte aus der Wurzel der Pflanze enthalten als wirksame Inhaltsstoffe Phenylpropanoide (Rosavin, Rosin und Rosarin – zusammenfassend Rosavine) und das Phenylethanolderivat Salidrosid im ungefähren Verhältnis von 3 : 1. Rosalin® ist auf einen Gehalt von 3 bis 8 % an Rosavinen und > 1 % Salidrosid eingestellt.
Pharmakologische Untersuchungen geben Hinweise, dass die adaptogenen Effekte von Rhodiolaextrakten auf einen modulierenden Einfluss auf die hormonelle Stressachse sowie auf die Stärkung des Energiestoffwechsels zurückzuführen sind [85]. Für Rosalin® konnten nach Stressinduktion im Tiermodell eine dosisabhängige Normalisierung der Noradrenalin-, 5-HT- und Dopaminspiegel im Gehirn sowie ZNS-stimulierende Effekte nachgewiesen werden [53]. Rhodiolaextrakt zeigt im Tier- und Zellmodell auch antioxidative, antiinflammatorische und neuroprotektive Wirkungen, fördert das Wachstum von Neuriten und bewirkt einen Anstieg des Spiegels des Wachstumsfaktors Brain-derived neurotrophic Factor [1]. Dies wird im Zusammenhang mit einer emotionalen Beruhigung und einer kognitiven Stimulation diskutiert.
Sicherheit und Verträglichkeit
In klinischen Studien traten vereinzelt Ereignisse wie Schwindel und Mundtrockenheit auf, die allerdings auch durch die Grunderkrankung verursacht worden sein könnten. Spezifische Nebenwirkungen sind bislang nicht bekannt. Für besondere Populationen (z. B. Kinder, geriatrische Patienten, Schwangere) liegen allerdings bislang keine Daten vor [11].
Zusammenfassende Bewertung
Die moderne Psychopharmakologie geht auf den Psychiater Emil Kraepelin zurück, der 1883 seine wegweisende Schrift „Über die Einwirkung einiger medikamentöser Stoffe auf die Dauer einfacher psychischer Vorgänge“ publizierte. Meilensteine in der Entwicklung synthetischer Psychopharmaka waren unter anderem die Entdeckung der antimanischen Wirkung von Lithium und des antipsychotischen Effekts von Chlorpromazin, die Entwicklung von Imipramin und der Benzodiazepine in den 1950er- und 1960er-Jahren sowie der SSRI und anderer Antidepressiva der zweiten und dritten Generation ab den 1980er-Jahren.
Gerade Letzteres führte zu einem sprunghaften Anstieg von Antidepressiva-Verordnungen, da diese Substanzen mit weniger gravierenden Nebenwirkungen verbunden waren als die vorher gebräuchlichen Antidepressiva [43, 49].
Es ist jedoch auch bei neuesten synthetischen Antidepressiva mit belastenden Begleiterscheinungen zu rechnen. Hierzu gehören – je nach Substanz – Sedierung oder auch innere Unruhe, Suizidalität, und Störungen der Sexualfunktionen [z. B. 65, 78]. Solche Effekte können zu einer Einschränkung der Alltagskompetenz und zu einer negativen Beeinflussung der Lebensqualität führen.
Nicht zuletzt wegen der Bedenken von Patienten bezüglich möglicher Nebenwirkungen synthetischer Psychopharmaka besteht ein Interesse an pflanzlichen Präparaten als gut verträglichen Alternativen. Die vorliegende Übersichtsarbeit zeigt, dass für Angststörungen und Depressionen, neuropsychiatrische Symptome von Demenzerkrankungen und Stresssymptome qualitativ hochwertige Phytotherapeutika verfügbar sind, die – bei vergleichbarer Wirksamkeit (siehe z B. [40, 41]) – gegenüber synthetischen Präparaten eine teilweise bessere Verträglichkeit aufweisen und die sich daher als wichtige therapeutische Optionen anbieten.
Einschränkend ist anzumerken, dass nicht für alle interessierenden Patientengruppen Daten zur Verfügung stehen – so fehlt beispielsweise Evidenz zur Anwendung bei Schwangeren und Stillenden oder bei Kindern und Jugendlichen. Andererseits zeigt die Übersichtsarbeit von Kasper [36], dass Silexan®, WS® 5570 und EGb 761® auch bei Patienten über 60 Jahren wirksam und gut verträglich sind. Dies ist auch insofern von besonderem Interesse, als ältere Patienten häufig besonders empfindlich auf Nebenwirkungen reagieren können.
Moderne Phytopharmaka sind Naturprodukte, aber auch Arzneimittel, die im Rahmen der guten pharmazeutischen Herstellungspraxis nach streng standardisierten Prozessen unter engmaschiger Qualitätskontrolle und behördlicher Überwachung hergestellt und für eine spezifische therapeutische Anwendung optimiert werden. Zwar unterliegt ihr Ausgangsmaterial einer natürlichen Variabilität, jedoch lässt sich durch definierte Herstellungsprozesse das erforderliche Maß an Gleichförmigkeit erzielen [86, 87]. Dabei ist jedoch zu beachten, dass sich unterschiedliche Extrakte in ihren Inhaltsstoffen zum Teil ganz erheblich voneinander unterscheiden [88], sodass sie keineswegs untereinander austauschbar sind. Daten zur Wirksamkeit und Verträglichkeit aus Studien sind nicht ohne Weiteres auf anders hergestellte Extrakte übertragbar. Nach Expertenmeinung gibt es bei pflanzlichen Wirkstoffen im Gegensatz zu chemisch definierten keine „Phytogenerika“ [83].
Von Bedeutung ist auch die Unterscheidung zwischen Phytopharmaka einerseits und Nahrungsergänzungsmitteln (NEM) andererseits. Bedauerlicherweise wird im europäischen Markt bis heute eine einheitliche, klare, Abgrenzung zwischen den unterschiedlichen Produktkategorien von den Behörden nicht durchgesetzt, sodass NEM teilweise ebenfalls mit Heilaussagen beworben werden und vom Patienten von Phytopharmaka kaum zu unterscheiden sind [6]. Während pflanzliche Arzneimittel zur Heilung, Linderung, Verhütung bzw. Diagnose von Erkrankungen vorgesehen sind, sind NEM Bestandteil einer gesunden Ernährung und Lebensführung, das heißt, solche Produkte sollen der Gesunderhaltung dienen [51]. Eine gleichbleibende, standardisierte und regulatorisch überwachte Qualität kann jedoch nur bei Arzneimitteln sichergestellt werden, da bei NEM nur der Hersteller für die Qualität verantwortlich ist. Von den pflanzlichen Präparaten kommen daher nur Phytopharmaka zur evidenzbasierten Therapie von psychischen Erkrankungen infrage.
Interessenkonflikterklärung
Siegfried Kasper erhielt Forschungsförderung bzw. -unterstützung und Honorare für Berater- und Vortragstätigkeiten während der letzten drei Jahre von Abbott, Angelini, Aspen Farmaceutica S.A., Biogen, Eisai, Janssen, IQVIA, Lundbeck, Mylan, Recordati, Sage, Sanofi, Schwabe, Servier, Sun Pharma and Vifor.
Literatur
1. Agapouda A, Grimm A, Lejri I, Eckert A. Rhodiola rosea extract counteracts stress in an adaptogenic response curve manner via elimination of ROS and induction of neurite outgrowth. Oxid Med Cell Longev 2022;2022:5647599.
2. Apaydin EA, Maher AR, Shanman R, Booth MS, et al. A systematic review of St. John’s wort for major depressive disorder. Syst Rev 2016;5:148.
3. Baldinger P, Höflich AS, Mitterhauser M, Hahn A, et al. Effects of Silexan on the serotonin-1A receptor and microstructure of the human brain: a randomized, placebo-controlled, double-blind, cross-over study with molecular and structural neuroimaging. Int J Neuropsychopharmacol 2014;18:pyu063.
4. Bartova L, Dold M, Volz HP, Seifritz E, et al. Beneficial effects of silexan on co-occurring depressive symptoms in patients with subthreshold anxiety and anxiety disorders: randomized, placebo-controlled trials revisited. Eur Arch Psychiatry Clin Neurosci 2022. doi: 10.1007/s00406-022-01390-z. Online ahead of print.
5. Berner MM, Kriston L, Sitta P, Harter M. Treatment of depressive symptoms and attitudes towards treatment options in a representative German general population sample. Int J Psychiatry Clin Pract 2008;12:5–10.
6. Bilia AR, Costa MDC. Medicinal plants and their preparations in the European market: Why has the harmonization failed? The cases of St. John’s wort, valerian, ginkgo, ginseng, and green tea. Phytomedicine 2021;81:153421.
7. Black N, Stockings E, Campbell G, Tran LT, et al. Cannabinoids for the treatment of mental disorders and symptoms of mental disorders: a systematic review and meta-analysis. Lancet Psychiatry 2019;6:995–1010.
8. Bundesärztekammer (BÄK), Kassenärztliche Bundesvereinigung (KBV), Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF). Nationale VersorgungsLeitlinie Unipolare Depression – Langfassung. 2022. www.leitlinien.de/depression.
9. Butterweck V. Mechanism of action of St John’s wort in depression: what is known? CNS Drugs 2003;17:539–62.
10. Committee on Herbal Medicinal Products (HMPC). Assessment report on Ginkgo biloba L., folium. London: European Medicines Agency, Committee on Herbal Medicinal Products (HMPC), 2012. https://www.ema.europa.eu/documents/herbal-report/final-assessment-report-ginkgo-biloba-l-folium_en.pdf (Zugriff am 5.10.2022).
11. Committee on Herbal Medicinal Products (HMPC). Assessment report on Rhodiola rosea L., rhizoma et radix. London: European Medicines Agency, Committee on Herbal Medicinal Products (HMPC), 2012. https://www.ema.europa.eu/documents/herbal-report/final-assessment-report-rhodiola-rosea-first-version_en.pdf (Zugriff am 7.10.2022).
12. Committee on Herbal Medicinal Products (HMPC). Community herbal monograph on Rhodiola rosea L., rhizoma et radix. London: European Medicines Agency, Committee on Herbal Medicinal Products (HMPC), 2012. https://www.ema.europa.eu/en/documents/herbal-monograph/final-community-herbal-monograph-rhodiola-rosea-first-version_en.pdf (Zugriff am 28.04.2021).
13. Cropley M, Banks AP, Boyle J. The effects of Rhodiola rosea L. Extract on anxiety, stress, cognition and other mood symptoms. Phytother Res 2015;29:1934–9.
14. Deutsche Gesellschaft für Psychiatrie, Psychotherapie und Nervenheilkunde (DGPPN), Deutsche Gesellschaft für Neurologie (DGN). S3-Leitlinie „Demenzen“. Köln, Bonn: Deutsche Gesellschaft für Psychiatrie und Psychotherapie, Psychosomatik und Nervenheilkunde, Deutsche Gesellschaft für Neurologie, 2016 (Zugriff am 06.10.2022).
15. Dold M, Bartova L, Volz H-P, Seifritz E, et al. Efficacy of Silexan in patients with anxiety disorders – a meta-analysis of randomized, placebo-controlled trials. Eur Arch Psychiatry Clin Neurosci [in press].
16. Doroshyenko O, Rokitta D, Zadoyan G, Klement S, et al. Drug cocktail interaction study on the effect of the orally administered lavender oil preparation silexan on cytochrome P450 enzymes in healthy volunteers. Drug Metab Dispos 2013;41:987–93.
17. Dreßing H, Koehler S, Mueller WE. Verbesserung der Schlafqualität mit einem hochdosierten Baldrian-Melisse-Präparat. Eine plazebokontrollierte Doppelblindstudie. Psychopharmakotherapie 1996;3:123–30.
18. Friedland K, Harteneck C. Hyperforin: To be or not to be an activator of TRPC(6). Rev Physiol Biochem Pharmacol 2015;169:1–24.
19. Gastpar M. Hypericum extract WS® 5570 for depression – an overview. Int J Psychiatry Clin Pract 2013;17(Suppl 1):1–7.
20. Gauthier S, Schläfke S. Efficacy and tolerability of Ginkgo biloba extract EGb 761® in dementia: a systematic review and meta-analysis of randomized placebo-controlled trials. Clin Interv Aging 2014;9:2065–77.
21. Gavrilova SI, Preuss UW, Wong JW, Hoerr R, et al. Efficacy and safety of Ginkgo biloba extract EGb 761 in mild cognitive impairment with neuropsychiatric symptoms: a randomized, placebo-controlled, double-blind, multi-center trial. Int J Geriatr Psychiatry 2014;29:1087–95.
22. Generoso MB, Soares A, Taiar IT, Cordeiro Q, Shiozawa P. Lavender oil preparation (Silexan) for treating anxiety: An updated meta-analysis. J Clin Psychopharmacol 2017;37:115–7.
23. Grass-Kapanke B, Busmane A, Lasmanis A, Hoerr R, et al. Effects of Ginkgo biloba special extract EGb 761® in very mild cognitive impairment (vMCI). Neuroscience and Medicine 2011;02:48–56.
24. Gromball J, Beschorner F, Wantzen C, Paulsen U, et al. Hyperactivity, concentration difficulties and impulsiveness improve during seven weeks’ treatment with valerian root and lemon balm extracts in primary school children. Phytomedicine 2014;21:1098–103.
25. Hardy K, Buckley S, Collins MJ, Estalrrich A, et al. Neanderthal medics? Evidence for food, cooking, and medicinal plants entrapped in dental calculus. Naturwissenschaften 2012;99:617–26.
26. Hashiguchi M, Ohta Y, Shimizu M, Maruyama J, et al. Meta-analysis of the efficacy and safety of Ginkgo biloba extract for the treatment of dementia. J Pharm Health Care Sci 2015;1:14.
27. Heger-Mahn D, Pabst G, Dienel A, Schlafke S, et al. No interacting influence of lavender oil preparation silexan on oral contraception using an ethinyl estradiol/levonorgestrel combination. Drugs R D 2014;14:265–72.
28. Herrschaft H, Nacu A, Likhachev S, Sholomov I, et al. Ginkgo biloba extract EGb 761® in dementia with neuropsychiatric features: a randomised, placebo-controlled trial to confirm the efficacy and safety of a daily dose of 240 mg. J Psychiatr Res 2012;46:716–23.
29. Hoerr R, Zimmermann A, Seitz F, Dienel A. Single and repeated doses of EGb 761® do not affect pharmacokinetics or pharmacodynamics of rivaroxaban in healthy subjects. Front Pharmacol 2022;13:868843.
30. Hung SK, Perry R, Ernst E. The effectiveness and efficacy of Rhodiola rosea L.: A systematic review of randomized clinical trials. Phytomedicine 2011;18:235–44.
31. Hyde AJ, May BH, Dong L, Feng M, et al. Herbal medicine for management of the behavioural and psychological symptoms of dementia (BPSD): A systematic review and meta-analysis. J Psychopharmacol 2017;31:169–83.
32. Ihl R, Frölich L, Winblad B, Schneider L, et al. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for the biological treatment of Alzheimer’s disease and other dementias. World J Biol Psychiatry 2011;12:2–32.
33. Ihl R, Tribanek M, Bachinskaya N, Group GS. Efficacy and tolerability of a once daily formulation of Ginkgo biloba extract EGb 761® in Alzheimer’s disease and vascular dementia: results from a randomised controlled trial. Pharmacopsychiatry 2012;45:41–6.
34. Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen (IQWiG). Ginkgohaltige Präparate bei Alzheimer Demenz. Cologne, Germany: Institut für Qualität und Wirtschaftlichkeit im Gesundheitswesen, 2008. https://www.iqwig.de/download/a05-19b_abschlussbericht_ginkgohaltige_praeparate_bei_alzheimer_demenz.pdf (Zugriff am 30.06.2022).
35. Ishaque S, Shamseer L, Bukutu C, Vohra S. Rhodiola rosea for physical and mental fatigue: a systematic review. BMC Complement Altern Med 2012;12:70.
36. Kasper S. Phytopharmaceutical treatment of anxiety, depression, and dementia in the elderly: evidence from randomized, controlled clinical trials. Wien Med Wochenschr 2015;165:217–28.
37. Kasper S, Anghelescu I, Dienel A. Efficacy of orally administered Silexan in patients with anxiety-related restlessness and disturbed sleep – A randomized, placebo-controlled trial. Eur Neuropsychopharmacol 2015;25:1960–7.
38. Kasper S, Dienel A. Cluster analysis of symptoms during antidepressant treatment with Hypericum extract in mildly to moderately depressed out-patients. A meta-analysis of data from three randomized, placebo-controlled trials. Psychopharmacology (Berl) 2002;164:301–8.
39. Kasper S, Dienel A. Multicenter, open-label, exploratory clinical trial with Rhodiola rosea extract in patients suffering from burnout symptoms. Neuropsychiatr Dis Treat 2017;13:889–98.
40. Kasper S, Gastpar M, Möller HJ, Müller WE, et al. Better tolerability of St. John’s wort extract WS 5570 compared to treatment with SSRIs: a reanalysis of data from controlled clinical trials in acute major depression. Int Clin Psychopharmacol 2010;25:204–13.
41. Kasper S, Gastpar M, Müller WE, Volz HP, et al. Lavender oil preparation Silexan is effective in generalized anxiety disorder – a randomized, double-blind comparison to placebo and paroxetine. Int J Neuropsychopharmacol 2014;17:859–69.
42. Kasper S, Gastpar M, Müller WE, Volz HP, et al. Silexan, an orally administered Lavandula oil preparation, is effective in the treatment of ‘subsyndromal’ anxiety disorder: a randomized, double-blind, placebo controlled trial. Int Clin Psychopharmacol 2010;25:277–87.
43. Kasper S, Heiden A. Do SSRIs differ in their antidepressant efficacy. Hum Psychopharmacol 1995;10(Suppl 3):S163–72.
44. Kasper S, Möller HJ, Volz HP, Schläfke S, Dienel A. Silexan in generalized anxiety disorder: investigation of the therapeutic dosage range in a pooled data set. Int Clin Psychopharmacol 2017;32:195–204.
45. Kasper S, Müller WE, Volz HP, Möller HJ, et al. Silexan in anxiety disorders: Clinical data and pharmacological background. World J Biol Psychiatry 2018;19:412–20.
46. Kasper S, Volz HP, Dienel A, Schlafke S. Efficacy of silexan in mixed anxiety-depression – A randomized, placebo-controlled trial. Eur Neuropsychopharmacol 2016;26:331–40.
47. Kellermann AJ, Kloft C. Is there a risk of bleeding associated with standardized Ginkgo biloba extract therapy? A systematic review and meta-analysis. Pharmacotherapy 2011;31:490–502.
48. Kloft C, Hoerr R. EGb 761® does not affect blood coagulation and bleeding time in patients with probable Alzheimer’s dementia – secondary analysis of a double-blind placebo-controlled trial. Submitted for publication at MDPI Healthcare in August 2021.
49. Konstantinidis A, Papageorgiou K, Grohmann R, Horvath A, et al. Increase of antipsychotic medication in depressive inpatients from 2000 to 2007: Results from the AMSP International Pharmacovigilance Program. Int J Neuropsychopharmacol 2012;15:449–57.
50. Koop T, Dienel A, Heldmann M, Münte TF. Effects of a Rhodiola rosea extract on mental resource allocation and attention: An event-related potential dual task study. Phytother Res 2020;34:3287–97.
51. Kraft K, Kelber O, Armbrüster N, Nauert C, et al. Pflanzliche Arzneimittel versus Botanicals: Klare Abgrenzung notwendig. Zeitschr Phytother 2013;34:P03.
52. Kremp D. Herz-Jesu-Blut im Johanniskraut – Balsam für die Seele. Leipzig: Engelsdorfer Verlag, 2011.
53. Kumar V, Husain G, Nöldner M, Koch E. Adaptogenic Activity of WS® 1375, a proprietary dry extract from Rhodiola rosea roots and rhizomes 2019;2018: 129–36.
54. Laakmann G, Schüle C, Baghai T, Kieser M. St. John’s wort in mild to moderate depression: The relevance of hyperforin for the clinical efficacy. Pharmacopsychiatry 1998;31:54–9.
55. Leach MJ, Page AT. Herbal medicine for insomnia: A systematic review and meta-analysis. Sleep Med Rev 2015;24:1–12.
56. Linde K, Berner MM, Kriston L. St John’s wort for major depression. Cochrane Database of Systematic Reviews 2008;Issue 4.:Art. No.: CD000448.
57. Liu Q, Jin Z, Xu Z, Yang H, et al. Antioxidant effects of ginkgolides and bilobalide against cerebral ischemia injury by activating the Akt/Nrf2 pathway in vitro and in vivo. Cell Stress Chaperones 2019;24:441–52.
58. Möller HJ, Volz HP, Dienel A, Schläfke S, et al. Efficacy of Silexan in subthreshold anxiety: meta-analysis of randomised, placebo-controlled trials. Eur Arch Psychiatry Clin Neurosci 2019;269:183–93.
59. Möller HJ, Volz HP, Seifritz E, Müller H, et al. Silexan does not affect driving performance after single and multiple dose applications: Results from a double-blind, placebo and reference-controlled study in healthy volunteers. J Psychiatr Res 2021;136:543–51.
59a. Müller WE, Eckert A, Eckert G, Fink H, et al. Ginkgo-Spezialextrakt 761® (Tebonin®): Ein präklinisches und klinisches Update im Wandel klinischer und ätiopathogenetischer Konzepte der Alzheimer-Demenz. Psychopharmakotherapie 2016;23:102–17.
59b. Müller WE, Schubert-Zsilavecz M. Friedland K. Der feine Unterschied. Johanniskrautextrakte in der Therapie von Depressionen. Dtsch Apoth Ztg 2020;160(27):70–6.
60. Müller WE, Schuwald AM, Nöldner M, Kasper S, et al. Pharmakologische Grundlagen der therapeutischen Anwendung von Silexan (Lasea®) Psychopharmakotherapie 2015;22:3–14.
61. Müller WE, Sillani G, Schuwald A, Friedland K. Pharmacological basis of the anxiolytic and antidepressant properties of Silexan®, an essential oil from the flowers of lavender. Neurochem Int 2021;143:104899.
62. Musazadeh V, Zarezadeh M, Faghfouri AH, Keramati M, et al. Saffron, as an adjunct therapy, contributes to relieve depression symptoms: An umbrella meta-analysis. Pharmacol Res 2022;175:105963.
63. Nahrstedt A, Butterweck V. Biologically active and other chemical constituents of the herb of Hypericum perforatum L. Pharmacopsychiatry 1997;30 Suppl 2:129–34.
64. Ng QX, Venkatanarayanan N, Ho CY. Clinical use of Hypericum perforatum (St John’s wort) in depression: A meta-analysis. J Affect Disord 2017;210;211–21.
65. Panariello F, Kasper S, Zohar J, Souery D, et al. Characterisation of medication side effects in patients with mostly resistant depression in a real-world setting. World J Biol Psychiatry (in press) 2022.
66. Ravindran AV, Balneaves LG, Faulkner G, Ortiz A, et al. Canadian Network for Mood and Anxiety Treatments (CANMAT) 2016 Clinical guidelines for the management of adults with major depressive disorder: Section 5. Complementary and alternative medicine treatments. Can J Psychiatry 2016;61:576–87.
67. Russo E, Scicchitano F, Whalley BJ, Mazzitello C, et al. Hypericum perforatum: pharmacokinetic, mechanism of action, tolerability, and clinical drug-drug interactions. Phytother Res 2014;28:643–55.
68. Sarris J, Marx W, Ashton MM, Ng CH, et al. Plant-based Medicines (Phytoceuticals) in the treatment of psychiatric disorders: A meta-review of meta-analyses of randomized controlled trials: Les médicaments à base de plantes (phytoceutiques) dans le traitement des troubles psychiatriques: une méta-revue des méta-analyses d’essais randomisés contrôlés. Can J Psychiatry 2021;66:849–62.
69. Sarris J, Ravindran A, Yatham LN, Marx W, et al. Clinician guidelines for the treatment of psychiatric disorders with nutraceuticals and phytoceuticals: The World Federation of Societies of Biological Psychiatry (WFSBP) and Canadian Network for Mood and Anxiety Treatments (CANMAT) Taskforce. World J Biol Psychiatry 2022:1–32.
70. Savaskan E, Müller H, Hoerr R, von Gunten A, et al. Treatment effects of Ginkgo biloba extract EGb 761® on the spectrum of behavioral and psychological symptoms of dementia: meta-analysis of randomized controlled trials. Int Psychogeriatr 2018;30:285–93.
71. Schäfer B. Ginkgolide. Chemie in unserer Zeit 2015;49:410–20.
72. Schulz M, Hoerr R, Mueller H. Ginkgo biloba extract EGb 761: A meta-analysis of adverse event rates from randomized, placebo-controlled, double-blind clinical trials. Int J Clin Pharm 2018;40:203–317.
73. Schulz V, Hänsel R. Rationale Phytotherapie – Ratgeber für Ärzte und Apotheker. 5. Aufl. Berlin: Springer, 2013.
74. Schunder-Tatzber S. Phytotherapie – von Urzeiten bis heute. Die wissenschaftliche Schwester der Volksmedizin. Journal für Ernährungsmedizin 2012;14:18–20.
75. Schuwald AM, Nöldner M, Wilmes T, Klugbauer N, et al. Lavender oil-potent anxiolytic properties via modulating voltage dependent calcium channels. PLoS One 2013;8:e59998.
76. Seifritz E, Möller HJ, Volz HP, Müller WE, et al. No abuse potential of Silexan in healthy recreational drug users: A randomized controlled trial. Int J Neuropsychopharmacol 2021;24:171–80.
77. Seifritz E, Schläfke S, Holsboer-Trachsler E. Beneficial effects of Silexan on sleep are mediated by its anxiolytic effect. Journal of Psychiatric Research 2019;115:69–74.
78. Stubner S, Grohmann R, Greil W, Zhang X, et al. Suicidal ideation and suicidal behavior as rare adverse events of antidepressant medication: Current report from the AMSP multicenter drug safety surveillance project. Int J Neuropsychopharmacol 2018;21:814–21.
79. Stücker O, Pons C, Duverger JP, Drieu K. Effects of Ginkgo biloba extract (EGb 761) on capillary red blood cell velocity. Advances in Ginkgo biloba Research 1994;3:31–4.
80. Tan MS, Yu JT, Tan CC, Wang HF, et al. Efficacy and adverse effects of ginkgo biloba for cognitive impairment and dementia: a systematic review and meta-analysis. J Alzheimers Dis 2015;43:589–603.
81. Toth B, Hegyi P, Lantos T, Szakacs Z, et al. The efficacy of saffron in the treatment of mild to moderate depression: A meta-analysis. Planta Med 2019;85:24–31.
82. Trautmann-Sponsel RD, Dienel A. Safety of Hypericum extract in mildly to moderately depressed outpatients: a review based on data from three randomized, placebo-controlled trials. J Affect Disord 2004;82:303–7.
83. Veit M. Gleiche Quelle, gleiche Wirkung? Zur Frage der Austauschbarkeit von pflanzlichen Arzneimitteln. Deutsche Apotheker Zeitung 2014;(33):62.
84. von Känel R, Kasper S, Bondolfi G, Holsboer-Trachsler E, et al. Therapeutic effects of Silexan on somatic symptoms and physical health in patients with anxiety disorders: A meta-analysis. Brain Behav 2021;11:e01997.
85. Wegener T. Rosenwurz – Arzneipflanze mit hohem adaptogenen Potenzial. Phytokompass 2021:26–30.
86. Wurglics M, Schubert-Zsilavecz M. Qualität pflanzlicher Arzneimittel. Chargenkonformität und biopharmazeutische Charakterisierung von Johanniskraut-Präparaten. Zeitschrift für Phytotherapie 2004;25:S35–S40.
87. Wurglics M, Westerhoff K, Kaunzinger A, Wilke A, et al. Batch-to-batch reproducibility of St. John’s wort preparations. Pharmacopsychiatry 2001;34(Suppl 1):S152–6.
88. Wurglics M, Westerhoff K, Kaunzinger A, Wilke A, et al. Comparison of German St. John’s wort products according to hyperforin and total hypericin content. J Am Pharm Assoc (Wash) 2001;41:560–6.
89. Yap WS, Dolzhenko AV, Jalal Z, Hadi MA, Khan TM. Efficacy and safety of lavender essential oil (Silexan) capsules among patients suffering from anxiety disorders: A network meta-analysis. Sci Rep 2019;9:18042.
90. Zadoyan G, Rokitta D, Klement S, Dienel A, et al. Effect of Ginkgo biloba special extract EGb 761® on human cytochrome P450 activity: a cocktail interaction study in healthy volunteers. Eur J Clin Pharmacol 2012;68:553–60.
91. Zhang L, Li D, Cao F, Xiao W, et al. Identification of human acetylcholinesterase inhibitors from the constituents of EGb 761 by modeling docking and molecular dynamics simulations. Comb Chem High Throughput Screen 2018;21:41–9.
Em. O. Univ.-Prof. Dr.h.c. mult. Dr.med. Siegfried Kasper, Center for Brain Research, Medizinische Universität Wien, Spitalgasse 4, 1090 Wien, Österreich, E-Mail: siegfried.kasper@meduniwien.ac.at
Evidence base of herbal medicinal products in psychopharmacotherapy – overview of active substances
The use of herbal preparations for the treatment of mental disorders has a long tradition. According to the principle of rational phytotherapy, centuries-old empirical knowledge is transferred into modern, evidence-based medicine. Traditional empiricism has to be confirmed by clinical trials. The lavender oil Silexan® for the treatment of anxiety disorders, Ginkgo biloba special extract EGb 761® for neuropsychiatric symptoms in dementia, alcoholic hypericum extracts such as WS® 5570 for mild to moderate depression, and with lower evidence rhodiola extract for stress-related mental and physical complaints meet these requirements and are approved as medicinal products in EU countries.
The paper presents the main results of clinical studies and reviews as well as treatment guideline recommendations. Statements apply only to the defined extracts and their specification and are not readily transferable to other preparations from the same plant. In psychiatric disorders, the use of phytopharmaceuticals often corresponds to patient preference for a treatment with few unwanted effects and therefore has a positive effect on compliance. In medical hands, these products represent a n integral part of psychopharmacotherapy.
Key words: Evidence based phytotherapy, psychic disorders, lavender oil, ginkgo biloba extract, hypericum extract
Psychopharmakotherapie 2023; 30(01):11-20
