Dr. Matthias Herrmann, Berlin
Bei Patienten mit schubförmiger multipler Sklerose (MS) bilden sich die Symptome nach einem Schub oft weitgehend oder sogar vollständig wieder zurück. Anders die deutlich selteneren NMOSD, die zu den wichtigsten Differenzialdiagnosen der MS zählen: Bei ihnen kann schon der erste Schub schwerste bleibende Schäden wie ein deutlich reduziertes Sehvermögen am betroffenen Auge zur Folge haben. Unbehandelt sind fünf Jahre nach Krankheitsbeginn 41 % der Betroffenen auf mindestens einem Auge blind und 8 % auf einen Rollstuhl angewiesen
Es ist deshalb entscheidend, schon nach der ersten Attacke mit einer präventiven Immuntherapie zu beginnen. Hier steht mit dem Antikörper Inebilizumab (Uplizna®) nach Zulassung durch die Europäische Kommission seit Anfang Mai 2022 eine neue Option zur Verfügung. Inebilizumab ist indiziert als Monotherapie zur Behandlung von erwachsenen Patienten mit NMOSD, die AQP4-Immunglobulin-G(IgG)-seropositiv sind [2]. Der Einsatz ist gleich nach dem ersten Schub möglich. Bei nur zweimal jährlicher Verabreichung als intravenöse Infusion bewirkt der monoklonale Antikörper eine nachhaltige Depletion CD19-positiver B-Zellen, die eine maßgebliche Rolle in der NMOSD-Pathogenese spielen.
Schubrate um 77 % reduziert
Basis der Zulassung bildet die Phase-II/III-Studie N-MOmentum mit 230 Patienten, von denen 213 seropositiv für AQP4-Antikörper waren [1]. Bis Tag 197 blieben 87,6 % der mit Inebilizumab behandelten seropositiven Patienten gegenüber 56,6 % der Placebo-Patienten anfallsfrei (Abb. 1). Dies entspricht einer Reduktion des relativen Risikos um 77,3 % (p < 0,0001). Unter Inebilizumab wurden die Schübe mit 29 % zudem seltener als schwer eingestuft als unter Placebo mit 45 %.
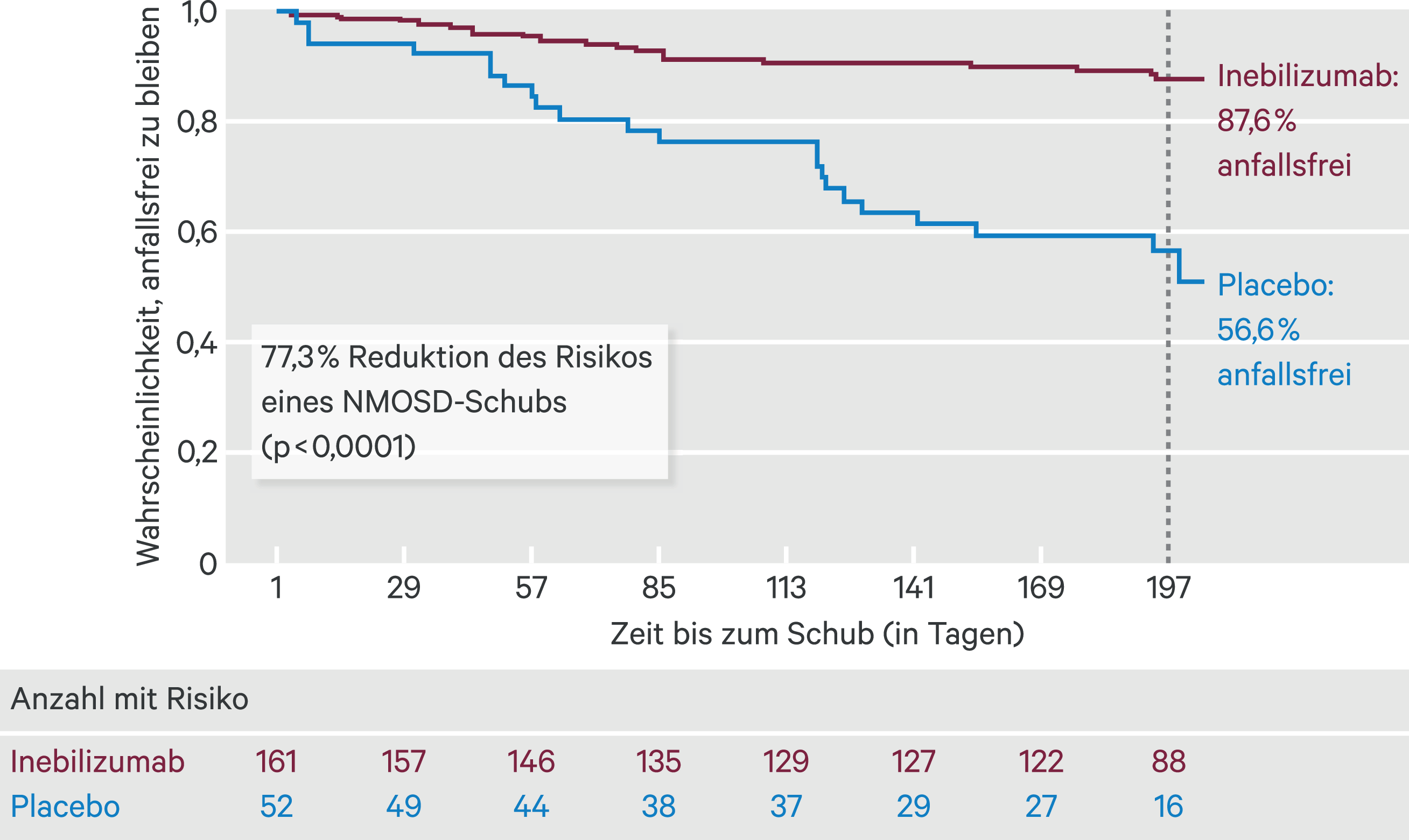
Abb. 1. Zeit bis zum ersten bestätigten NMOSD-Schub während der randomisierten kontrollierten Studienphase bei AQP4-IgG-seropositiven Patienten (primärer Endpunkt) (nach [1]).
Hinsichtlich der Verträglichkeit zeigte Inebilizumab ein ähnliches Nebenwirkungsprofil wie Placebo [1]. In beiden Gruppen traten Harnwegsinfektionen und Arthralgien sowie Kopf- und Rückenschmerzen am häufigsten auf. Bei weniger als 5 % der mit Inebilizumab behandelten Studienteilnehmer wurde ein Abfall der IgG-Titer auf sehr niedrige Werte von weniger als 300 mg/dl beobachtet. In der offenen Verlängerungsphase der N-MOmentum-Studie waren niedrigere IgG-Werte unter Inebilizumab bei einer Beobachtungsdauer von mehr als vier Jahren mit keinem erhöhten Infektionsrisiko assoziiert [3].
Fazit
Mit Inebilizumab steht eine interessante Therapieoption zur viele Patienten mit früher NMOSD zur Verfügung.
Quelle
Prof. Dr. Orhan Aktas, Düsseldorf, Launch-Pressegespräch von Uplizna® (Inebilizumab) zur Behandlung von Erwachsenen mit Neuromyelitis-optica-Spektrum-Erkrankungen (NMOSD), Berlin, 10. Juni 2022, veranstaltet von Horizon.
Literatur
1. Cree BA, et al. Inebilizumab for the treatment of neuromyelitis optica spectrum disorder (N-Momentum): a double-blind, randomised placebo-controlled phase 2/3 trial. Lancet 2019;394:1352–63.
2. Fachinformation Uplizna®, aktueller Stand.
3. Greenberg BE, et al. Immunoglobulin kinetics and infection risk after long-term inebilizumab treatment for neuromyelitis optica spectrum disorder. 7. Kongress der European Academy of Neurology EAN), 19.–22. Juni 2021 (virtuell), Poster A-21–00372.
Psychopharmakotherapie 2022; 29(05):192-203
