Pierre Baumann, Prilly-Lausanne/Schweiz, Martina Hahn, Sibylle C. Roll, Frankfurt/Main, und Dominik Stämpfli, Zürich/Schweiz*
Patienten, welche wegen eines psychischen Leidens bei einem Psychiater1 in Behandlung sind, leiden häufig auch an somatischen Komorbiditäten [9]. Dieser Umstand muss vom Arzt mit Spezialisierung in Psychiatrie und Psychotherapie bei einer Psychopharmakotherapie berücksichtigt werden, um beim Patienten pharmakokinetische und pharmakodynamische Interaktionen zu vermeiden und das Risiko für ein Nichtansprechen auf die Therapie oder für ein Auftreten von unerwünschten Arzneimittelwirkungen zu reduzieren. Der Psychiater kann beim Verordnen einer Psychopharmakotherapie auf drei wichtige Partner zählen: im stationären Setting auf den Arzt mit Spezialisierung in klinischer Pharmakologie und Toxikologie oder auf klinische Pharmazeuten, im ambulanten Setting auf den Apotheker, der den Patienten in seiner Offizin empfängt und berät sowie die vom Psychiater und gegebenenfalls von einem weiteren Partner, dem somatischen Arzt, verschriebenen Rezepte überprüft und abgleicht (Abb. 1). Dabei evaluiert der Apotheker die Risiken der Psychopharmakotherapie nochmals, um situationsabhängig mit den behandelnden Ärzten Rücksprache zu halten und den Patienten gegebenenfalls über Vorsichtsmaßnahmen zu informieren.
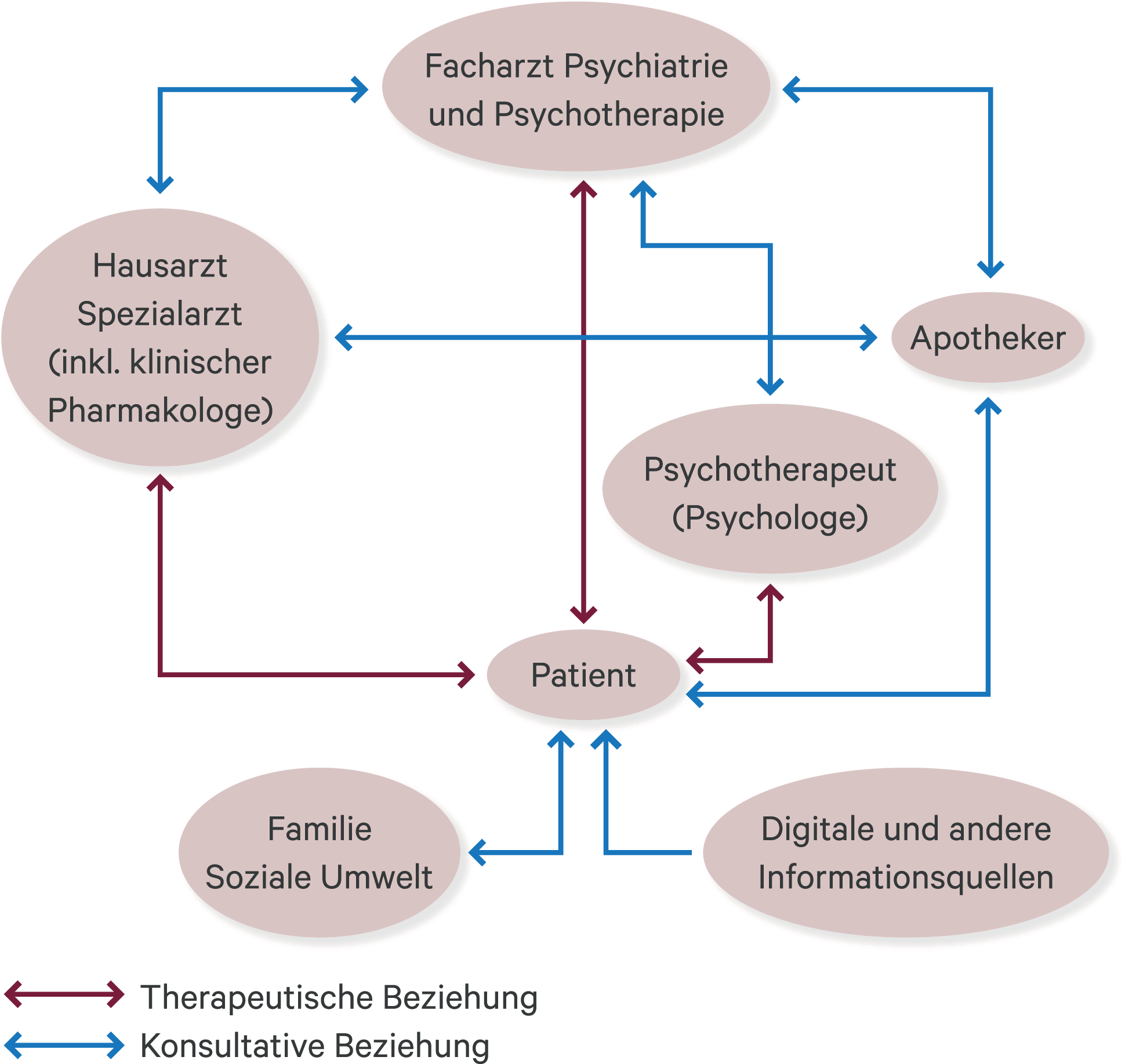
Abb. 1. Therapeutische und konsultative Beziehungen zwischen dem Patienten und Fachleuten der Medizin und Pharmazie im Rahmen einer psychopharmakotherapeutischen Behandlung
Im stationären Setting funktioniert die Kooperation oftmals sehr gut, weil allen Beteiligten über das Krankenhausinformationssystem umfassende Patienteninformationen zur Verfügung stehen und alle beim selben Arbeitgeber angestellt sind. Probleme gibt es insbesondere im ambulanten Setting, wo oftmals sehr unterschiedliche und unvollständige Patienteninformationen zur Verfügung stehen. Da Arzt und Apotheker bei der Evaluation der Arzneimitteltherapiesicherheit so auf unterschiedliche Ergebnisse kommen können, kann sich der Patient nach dem Besuch der öffentlichen Apotheke verunsichert fühlen, gerade wenn die Medikamente nicht ohne weitere Rücksprache mit dem Arzt dispensiert werden konnten. Es besteht deshalb die Forderung nach einem optimalen Zusammenwirken zwischen diesen verschiedenen Heilberuflern, sodass durch eine zielführende Kommunikation eine Verunsicherung des Patienten wegen widersprüchlicher Signale vermieden werden kann.
Dieses Zusammenwirken kann auch den zunehmenden Mangel an Fachärzten in Psychiatrie und Psychotherapie lindern, wie er in Deutschland besteht [6, 21] – aber auch in der Schweiz werden demnächst 1000 Psychiater fehlen [11]. So geht die Psychiatrie als Disziplin gemäß dem früheren Präsidenten der World Psychiatric Assocation (WPA), Dinesh Bhugra, und anderen Autoren der WPA-Lancet Psychiatry Commission allgemein größeren Änderungen und Herausforderungen entgegen [5]. Eine Revolution zeichne sich ab, wobei die Psychiater hier die Führung übernehmen sollen, indem sie mit Interessengruppen, Entscheidungsträgern und Patienten so zusammenarbeiten, dass diese die beste Unterstützung finden, welche im Rahmen der möglichen Ressourcen realisiert werden kann.
Dieser Beitrag ist das Ergebnis einer Zusammenarbeit zwischen deutschen und schweizerischen Autoren, weshalb darauf hingewiesen wird, dass jeweils länderspezifische behördliche Verordnungen erwähnt werden.
Die Situation des Patienten
Im Regelfall wird der Patient vom behandelnden Arzt auf Risiken und unerwünschte Arzneimittelwirkungen der ihm verschriebenen Medikamente aufmerksam gemacht. Nach dieser Aufklärung entscheidet der Patient im Rahmen der partizipativen Entscheidungsfindung (shared decision making) idealerweise über die Auswahl des geeigneten Präparats mit [8]. Beim Einlösen des Rezepts in der Apotheke werden dann nochmals Informationen vermittelt. Auch können weitere, zu klärende Fragen aufkommen. Anekdotisch wird berichtet, dass die Medikation gegenüber dem Patienten kommentiert oder gar kritisiert wird, bevor das Rezept schließlich umfassend evaluiert und ausgeführt wird. Unterschiede in all diesen mitgeteilten Informationen zur Psychopharmakotherapie können Unsicherheiten aufseiten des Patienten auslösen, die durch eine standardisierte transparente Kommunikation zwischen Arzt und Apotheker vermieden werden können [14].
Ein Fallbeispiel: Rezepte für eine kombinierte Behandlung mit Citalopram plus Trazodon (z. B. 20 mg/Tag Citalopram + 100 bis 150 mg/Tag Trazodon; 40 mg/Tag Citalopram + 100 mg/Tag Trazodon) lösen in Interaktionsdatenbanken einen Alert zu additiver QT-Verlängerung und additiven serotonergen Effekten aus. Trazodon in einer verhältnismäßig geringen Dosis und in Kombination mit einem selektiven Serotonin-Wiederaufnahmehemmer (SSRI) als Antidepressivum wird allerdings oft wegen seiner sedierenden und schlaffördernden Eigenschaften verordnet [24]. Auch schätzen Leitlinien und Originalliteratur die Kombination Citalopram plus Trazodon generell als nicht so risikoreich ein [26]. Während für Citalopram das Risiko für das Auftreten von Torsades de pointes anerkannt ist, besteht dieses Risiko für Trazodon nur unter gewissen Bedingungen (https://crediblemeds.org/pdftemp/pdf/CombinedList.pdf, 9. Januar 2020). Trazodon wird unter die Antidepressiva mit geringem Risiko, die QTc-Zeit zu verlängern, eingereiht [7, 33], was kürzlich in einer Studie mit älteren Patienten bestätigt wurde [1]. Der Apotheker steht bei der Rezeptvalidierung nun vor einem Dilemma: Gemäß Fachinformation und Interaktionsdatenbanken ist die Kombination formal kontraindiziert und verlangt nach weiteren Abklärungen. Der Psychiater hat diese Kombination jedoch unter sorgfältiger Nutzen-Risiko-Abwägung und Gründen wie Unverträglichkeit oder Unwirksamkeit anderer Präparate und individuellem Risikoprofil des Patienten bewusst und bestenfalls transparent gewählt. Leitlinien und klinische Praxis zeigen also in eine andere Richtung als die Interaktionsdatenbanken. Fragen für die eigene Risikoabschätzung des Apothekers können den Patienten verunsichern und ihn zusätzlich sich unwohl fühlen lassen, falls in der Apotheke kein separater Beratungsraum oder keine geeignete Diskretzone genutzt wird. Hätte dieses Dilemma vermieden werden können, indem dem Apotheker pro-aktiv Informationen zur Wahl der Kombination mitgeteilt werden?
Die Situation und Rolle des Psychiaters bei der Psychopharmakotherapie
Beim Entscheid für eine psychopharmakotherapeutische Behandlung eines Patienten stützt sich der Psychiater auf eine Anamnese, auf klinisch-psychiatrische und somatische Untersuchungen inklusive Laboruntersuchungen, test- und neuropsychologische Diagnostik sowie Bildgebung, welche ihm erlauben, eine klinische Diagnose zu stellen. Er berücksichtigt dabei den familiären Hintergrund des Patienten, seine Lebensgewohnheiten, sein Risikoprofil und seine soziale Umwelt (Abb. 1), aber er stützt sich auch auf eine konstruktive Zusammenarbeit mit dem Hausarzt und anderen Fachärzten. Entscheidend ist, den Patienten im Sinne der partizipativen Entscheidungsfindung (shared decision making) frühestmöglich auf den gleichen Kenntnisstand über die gestellte Diagnose und die möglichen pharmakotherapeutischen Behandlungsoptionen zu bringen, um ihm damit zu ermöglichen, gemeinsam mit dem Psychiater zu entscheiden, welches Arzneimittel geeignet ist. Im Laufe der pharmakotherapeutischen Behandlung, die allgemein durch eine vom Facharzt für Psychiatrie und Psychotherapie persönlich oder gegebenenfalls von einem Psychologen in Delegation ausgeführte Psychotherapie begleitet wird, wird die Medikation je nach Ansprechen und Verträglichkeit, wieder unter Beteiligung des Patienten im Sinne des „shared decision making“, angepasst. Dabei werden auch Laboruntersuchungen und gegebenenfalls pharmakogenetische Diagnostik [2] einbezogen (z. B. Lithiumspiegel bei einer Behandlung mit Lithium, Blutbild bei einer Behandlung mit Clozapin, Schilddrüsenfunktionstests, Genotypisierung zur prospektiven Einschätzung von Wirksamkeit und Verträglichkeit eines Präparats). Der behandelnde Arzt stützt die Therapie auf Fähigkeiten und Erfahrungen, die er im Laufe seiner Aus- und Weiterbildung und danach gewonnen hat (Tab. 1). Begrenzend gilt, dass international die Fächer Pharmakotherapie/Psychopharmakologie einen relativ bescheidenen Platz während der gesamten Ausbildungszeit zum Facharzt für Psychiatrie und Psychotherapie einnehmen, nämlich 24 bis 48 Stunden in fünf Jahren [4, 18].
Tab. 1. Facharzt für Psychiatrie und Psychotherapie: Basis der Entscheidung für eine Psychopharmakotherapie
|
|
|
|
|
Die Situation und Rolle des Apothekers bei der Psychopharmakotherapie
Apotheker sind das letzte Glied in der Kette von Heilberuflern und markieren mit der Überreichung des Arzneimittels an die Patienten die Startlinie in die pharmakotherapeutische Behandlung. Als die abgebende Instanz tragen sie dabei im Sinne der pharmazeutischen Sorgfaltspflicht Mitverantwortung, dass die verordnete Dosierung im gebräuchlichen Bereich ist und, dass keine potenziell schwerwiegenden Interaktionen vorliegen. Wird die pharmazeutische Sorgfaltspflicht nun verletzt, wenn das Rezept ohne Rücksprache und ohne Hinweis an den Patienten abgegeben wird? Geregelt wird diese Beratungspflicht des Apothekers in § 20 der Apothekenbetriebsordnung und in der Berufsordnung der Apothekerkammern (Schweiz: Medikamenten-Check in der Tarifstruktur für Apothekerleistungen, LOA IV). Diese Mitverantwortung wird auch in einer Richtlinie zur guten pharmazeutischen Praxis („good pharmacy practice“) der WHO angesprochen, welche unter anderem von der Sicherstellung der medikamentösen Wirksamkeit und dem Verhindern von Schäden durch eine Pharmakotherapie spricht [34].
Zur Förderung von Wirksamkeit und Sicherheit einer pharmakologischen Therapie gehört auch die Verordnungsvalidierung. Beispielsweise muss in der Schweiz vor Ausführung eines Rezepts dieses logistisch (Identität) als auch pharmazeutisch und pharmakologisch, wie in Tabelle 2 dargestellt, überprüft werden. In Deutschland gibt es eine Leitlinie der Bundesapothekerkammer, die detailliert jeden Schritt bei der Abgabe und Beratung des Patienten beschreibt (Kommentar zur Leitlinie der Bundesapothekerkammer zur Qualitätssicherung, Information und Beratung des Patienten bei der Abgabe von Arzneimitteln auf ärztliche Verordnung, Stand der Revision: 13.11.2019).
Tab. 2. Überprüfung eines Rezepts vor seiner Ausführung in der Schweiz im Sinne einer Verordnungsvalidierung*
|
|
|
|
|
|
|
|
*Positionspapier H010.02, Kantonsapotheker-Vereinigung Nordwestschweiz; 1. November 2018; https://www.kantonsapotheker.ch/de/leitlinien-positionspapiere/kav-nwch-positionspapiere; konsultiert am 15. Januar 2020)
In einer Stammapotheke können verschiedene Behandlungsstränge zusammenlaufen, wodurch die Verordnungsvalidierung auch weitere involvierte Ärzte (Hausarzt, Facharzt Krankenhaus) und die Selbstmedikation einschließen kann. So wird eine umfassende Überprüfung der gesamten Pharmakotherapie ermöglicht. Bestehen Unklarheiten oder Zweifel betreffend Angaben auf dem Rezept, vermutet der Apotheker mögliche relevante Interaktionen mit anderen Arzneimitteln oder identifiziert er einen potenziellen Irrtum seitens des verschreibenden Arztes, so muss er unverzüglich mit diesem Rücksprache halten. Ein Fallbeispiel für einen solchen Irrtum ist die Verwechslung des pharmakologisch aktiven Enantiomers Escitalopram mit dem bereits länger verfügbaren Racemat Citalopram: Die Dosierung von Citalopram wird für Escitalopram teils direkt übernommen und führt so zu einer Verdoppelung der eigentlich vorgesehenen Dosierung. Auch wird Kontakt zur verordnenden Person aufgenommen und die Verschreibungen werden vorerst nicht ausgeführt, wenn seitens Apotheker eine Fälschung oder Verfälschung der Verordnung vermutet wird.
Beim Wahrnehmen seiner Aufgaben in der öffentlichen Apotheke stützt sich der Apotheker mit Weiterbildung in Offizinpharmazie (CH) bzw. Allgemeinpharmazie (D) auf die in Tabelle 3 dargestellten Fähigkeiten und Grundlagen. Um die pharmazeutisch-pharmakologische Kompetenz von Ärzten zu stärken, wurden in Deutschland in den letzten Jahren – angelehnt an das Eichberger Modell® [13, 28] – vereinzelt klinische Pharmazeuten im Klinikteam psychiatrischer Kliniken zur Verbesserung der Arzneimitteltherapie durch standardisierte Kooperation und Kommunikation zwischen Arzt, Apotheker, Patient und Angehörigen eingestellt. Stationsapotheker werden ab dem 1. Januar 2022 zumindest im Bundesland Niedersachsen verpflichtend für alle Kliniken eingesetzt. Dies gilt es in den kommenden Jahren flächendeckend zu erweitern. Im ambulanten Sektor sollten sich dringend ähnliche Kooperationen zwischen niedergelassenen Psychiatern und Apotheken entwickeln [15]. Die hoffentlich bald flächendeckendere Kooperation von Arzt und Apotheker im stationären Setting könnte sich mit jungen Ärzten, die es dann gewöhnt wären, mit Stationsapothekern und klinischen Pharmazeuten zu arbeiten, auch begünstigend auf die Kooperation im ambulanten Setting auswirken. Hierdurch würde nicht nur die Adhärenz des Patienten gefördert und die Arzneimitteltherapiesicherheit verbessert, sondern es würden auch die Kenntnisse von Ärzten in den Bereichen Pharmazie und Pharmakologie relevant erweitert. In den USA wurde sogar eine Spezialisierung für Apotheker geschaffen, nämlich der „Psychiatric Pharmacist“, die eine vierjährige Weiterbildung umfasst und bei welcher ein tiefes Wissen rund um die Psychopharmakotherapie aufgebaut wird.
Tab. 3. Apotheker mit Weiterbildung in Offizinpharmazie: Basis für das Wahrnehmen seiner Aufgaben in einer öffentlichen Apotheke in der Schweiz
|
|
|
|
|
1 Seit 2018 bedingt die Berufsausübung in eigener fachlicher Verantwortung einen eidgenössischen Weiterbildungstitel (Bundesgesetz über die universitären Medizinalberufe, SR 811.11 Art. 36)
Leider können in der öffentlichen Apotheke zusätzliche Informationen zur Krankengeschichte für eine eigenständige Bewertung des Risikos bei ausgelösten Interaktionsalarmen fehlen. In Krankenhäusern tätige Apotheker (Schweiz: Klinische Pharmazeuten, Spitalapotheker; Deutschland: Klinische Pharmazeuten, Stationsapotheker, Krankenhausapotheker) können bei Medikationsanalysen aufgedeckte Hinweise, beispielsweise zu additiven QT-verlängernden Effekten, bequem selbst im letzten EKG kontrollieren. Elektronische Patientendossiers versprechen dabei auch ambulant den nötigen Informationsaustausch, lassen allerdings seit mehreren Jahren und mit noch ungewisser Implementierungsrate auf sich warten. So bleiben in der öffentlichen Apotheke die anwesenden Patienten und Angehörigen als schnell verfügbare Informationsquellen übrig, wobei Rückfragen die Gefahr bergen, zu verunsichern und sich damit negativ auf Therapieadhärenz und -effektivität auszuwirken.
Beitrag des Klinischen Pharmakologen zur Patientensicherheit
Als weiterer Partner im stationären Setting ist der Klinische Pharmakologe zu nennen, welcher Ärzte, aber auch Patienten direkt bei der Polypharmazie unterstützt.
Medikationsprobleme manifestieren sich insbesondere als zu geringe gewünschte Wirkung oder als vermehrtes oder verstärktes Auftreten von unerwünschten Wirkungen. Für beide Arten der inadäquaten Arzneimittelwirkung gibt es genetische und nichtgenetische Einflüsse. Durch pharmakogenetische Untersuchungen, die mittlerweile auch in der klinischen Routine unter bestimmten Bedingungen verfügbar sind, kann das individuelle Ansprechen eines Patienten in gewissen Situationen vorhergesagt bzw. erklärt werden. Pharmakogenetische Untersuchungen können hilfreiche Informationen bei Patienten bieten, bei denen eine Besonderheit im Arzneimittelstoffwechsel oder -transport vermutet wird, zum Beispiel:
- Unerwünschte Effekte bei normalen Dosierungen
- Wirkungslosigkeit bei gesicherter Einnahme bei normalen Dosierungen
- Notwendigkeit deutlich erhöhter Dosen zum Erreichen des gewünschten Effekts
- Beginn einer Therapie, bei der pharmakogenetische Einflüsse klinisch relevant sind
In der Realität mangelt es an klinischen Pharmakologen. Wie in den meisten europäischen Ländern sind klinische Pharmakologen auch in der Schweiz eine rare Spezies. In vielen Kantonen gibt es keine solche Spezialärzte, und jährlich erhalten nur zwei bis fünf Ärzte ein entsprechendes Facharztdiplom [2a]. Für medikamentöse Probleme bieten die Abteilungen für Klinische Pharmakologie und Toxikologie an den Schweizer Universitätsspitälern Konsiliardienste und Sprechstunden an. In diesem Rahmen wird unter anderem überprüft, ob eine pharmakogenetische Untersuchung nützliche Informationen zur Arzneimitteltherapie beitragen kann. In der Schweiz ist die Rückvergütung von pharmakogenetischen Tests nur für einige wenige Medikamenten-Gen-Paare von der Grundversicherung gesetzlich vorgeschrieben. Für darüber hinaus gehende Tests erfolgt die Rückvergütung nur, wenn der Test von einem Facharzt für klinische Pharmakologie und Toxikologie verschrieben wird [3].
Der Klinische Pharmakologe beurteilt medikamentöse Probleme immer „personalisiert“, also unter Berücksichtigung der Komedikation sowie weiterer individueller Einflüsse wie Begleiterkrankungen, der Funktionen von Niere und Leber und von Plasmakonzentrationen der verabreichten Medikamente, sodass eine individuelle Empfehlung zur Optimierung der Pharmakotherapie abgegeben werden kann, die in ihrer Komplexität die Informationen aus elektronischen Interaktionsprüfprogrammen übersteigt. Hierdurch wird auch der Beitrag der klinischen Pharmakologie und Toxikologie bei komplexen Fragestellungen zur Therapie, zur Patientensicherheit und als Bindeglied im Medikationsprozess deutlich.
Forschung zur Zusammenarbeit zwischen Arzt und Apotheker
Eine harmonische Zusammenarbeit zwischen Ärzten (Psychiater, somatische Ärzte, klinische Pharmakologen) und Apotheker zur Optimierung der pharmakologischen Behandlung des Patienten ist Bedingung. Probleme können aber auch durch Verordnungen von Heilpraktikern entstehen, welche nicht gemeldet oder eruiert werden und zu Interaktionen mit Nebenwirkungen führen können.
Es gibt wenige Studien zur Zusammenarbeit zwischen verordnendem Arzt und Apotheker, insbesondere fehlen sie auf dem Gebiet der Psychiatrie. Studien dokumentieren medizinische [17, 19, 20] und pharmazeutische [29] Irrtümer bei der Verschreibung und Dispensierung. Sie weisen aber auch auf Bemühungen hin, diese zu vermeiden. Critical Incident Reporting System (CIRS) (deutsch: Berichtssystem über kritische Vorkommnisse) ist ein Berichtssystem zur anonymisierten Meldung von kritischen Ereignissen (englisch: critical incident) und Beinahe-Schäden (englisch: near miss). Sie wurden in Einrichtungen des Gesundheitswesens vor vielen Jahren eingeführt, um Fehler zu erfassen, zu analysieren und aus den Erkenntnissen dann Prozesse zu verbessern. Bemerkenswert ist der Beitrag des renommierten Pharmakologen Jeffrey K. Aronson, der fordert, dass dem Patienten eine aktivere Rolle zugesprochen werden sollte, da dieser sich selbst und seine Medikation evaluiert und für eine vertrauensvolle Partnerschaft mit dem Arzt und Apotheker zufriedenstellende Erklärungen braucht [23].
Eine ältere Untersuchung von 2003 [25] hatte das Ziel, in England schwerwiegende Verschreibungsirrtümer bis 2005 um 40 % zu verringern. Ein Netzwerk von in der Psychiatrie tätigen Pharmazeuten nahm an der Studie teil, indem sie mittels Fragebögen Irrtümer in der Verschreibung von Medikamenten durch Psychiater aus 12 verschiedenen „Mental Health Trusts“ notierten. Es stellte sich heraus, dass 155 (27 %) von 579 Interventionen notwendig waren, um Irrtümer zu korrigieren. In 65 % der Fälle waren psychotrope Medikationen betroffen, bei den Restlichen waren es Somatika. Durch die Interventionen konnten in 63 (11 %) der Fälle schwerwiegende Folgen vermieden werden.
In einer weiteren Studie hatten 14 Offizin-Apotheker aus fünf verschiedenen Ortschaften in England während jeweils einer Woche pro Monat über ein Jahr jede klinisch-pharmazeutische Intervention dokumentiert [16]. Ergab sich die Notwendigkeit, einen verschreibenden Arzt zu kontaktieren, wurden kurze Einzelheiten über den Patienten, die verschriebene Pharmakotherapie, die Indikation, das Outcome sowie die dafür verwendete Zeit notiert. Eine Expertengruppe schätzte dann unter anderem das Potenzial jeder Intervention, eine Hospitalisierung des Patienten zu vermeiden. Es wurden 1503 klinisch-pharmazeutische Interventionen bei insgesamt 201 000 Abgaben durchgeführt. Die Expertengruppe schloss, dass 19 bis 242 Interventionen dazu beigetragen hatten, eine mit der Pharmakotherapie zusammenhängende Hospitalisierung zu vermeiden. Weiter halfen 71 bis 483 Interventionen, gesundheitliche Schäden zu vermeiden; 103 bis 364 Interventionen trugen zur Verbesserung des ursprünglich etablierten Behandlungsplans bei, und 748 Interventionen verbesserten den Outcome und vermieden wahrscheinlich einen Hausarztbesuch.
Als Pionierarbeit muss die kürzlich publizierte, allerdings nicht Psychiatrie-nahe Studie bezeichnet werden, bei der Patienten mit chronischer Herzinsuffizienz in zwei Gruppen eingeteilt wurden [32]. Die eine Gruppe erhielt während eines Jahres die übliche Betreuung, die andere eine spezielle pharmazeutische Betreuung. Die Patienten suchten alle 14 Tage die Apotheke auf. Bei diesen Besuchen wurde der Behandlungsplan verifiziert und die Medikation für die nächste Behandlungsperiode dispensiert. Des Weiteren wurden die Patienten zu ihrer Medikation beraten und es wurden Blutdruck und Puls gemessen. Falls es sich als notwendig erwies (Hinweise auf arzneimittelbezogene Probleme, deutliche Veränderungen der Vitalzeichen), wurde der Arzt kontaktiert. Bei den pharmazeutisch betreuten Patienten war am Ende der Beobachtungszeit nicht nur die Adhärenz signifikant höher als bei der Kontrollgruppe, sondern auch die Lebensqualität nach zwei Jahren. Hingegen unterschieden sich die Endpunkte nicht in Bezug auf die Anzahl Hospitalisierungen und Todesfälle.
Vorschläge
Das Collaborative-Working-Relationship-(CWR-)Modell unterscheidet in der Zusammenarbeit zwischen Ärzte- und Apothekerschaft fünf verschiedene Stufen (Abb. 2) [12, 22]. Rückfragen zu Rezepten werden in Stufe 0 eingeordnet: Es sind minimale und diskrete unilaterale Interaktionen. So kann der Vermerk „sic“ („so!“) darauf hinweisen, dass potenziell interagierende Kombinationen oder Off-Label-Dosierungen bewusst so verordnet und aufs Rezept geschrieben wurden. In Stufe 1 des CWR-Modells haben die Apotheker neue Dienstleistungen entwickelt und suchen weitere Kontakte auf. In späteren Stufen wird die Zusammenarbeit bilateral und es etabliert sich ein wahres Miteinander. Beeinflussende Faktoren für die Zusammenarbeit sind dabei unter anderem das Alter, die Berufserfahrung und die Bereitschaft der Partner zur Zusammenarbeit, das Umfeld und die Art der Kommunikation. Grundsätzlich sollten möglichst höhere Stufen der Zusammenarbeit angestrebt werden, doch kann die Qualität der Kommunikation bereits in tieferen Stufen unterstützt werden: Die ABDA – Bundesvereinigung Deutscher Apothekerverbände – hat zu verschiedenen Interaktionen Faxvorlagen entwickelt (www.abda.de/fuer-apotheker/qualitaetssicherung/leitlinien/leitlinien-und-arbeitshilfen/, Zugriff: 5. Mai 2020). Reichen die Rezeptzeilen zur Kommunikation nicht mehr aus, könnten solche Faxvorlagen für die eigenen Zwecke und in Absprache mit umliegenden Partnern adaptiert verwendet werden. Höhere Stufen der Zusammenarbeit wurden beispielsweise in Deutschland in den Athina- [27] und Armin-Projekten (https://www.aerzteblatt.de/archiv/172811/Arzneimittelinitiative-Sachsen-Thueringen-Der-Patient-gewinnt-ganz-klar) und Apo-AMTS in Westfalen-Lippe erreicht, bei denen gezielt Medikationsanalysen durchgeführt werden und Kontaktaufnahme mit dem verschreibenden Arzt über die aufgedeckten arzneimittelbezogenen Probleme stattfindet. Bei einer Medikationsanalyse im weiter verbreiteten Athina-Projekt werden mit dem Patienten zwei Termine vereinbart. Zunächst bringt der Patient alle seine Arzneimittel in die Apotheke. Die Präparate werden durch den Apotheker erfasst und die Medikation strukturiert analysiert. Beim zweiten Termin erhält der Patient einen übersichtlichen Medikationsplan und Informationen zu seinen Arzneimitteln. Der Apotheker prüft auch, ob die Präparate zueinander passen. Häufig kommt es beispielsweise vor, dass Patienten fast identische Arzneimittel gleichzeitig einnehmen. Der Apotheker macht Vorschläge, wie sich die Wirkung der Arzneimittel optimieren lässt, wie sich unerwünschte Wirkungen vermeiden lassen und sogar, welche Arzneimittel nach Rücksprache mit dem Arzt abgesetzt werden könnten. Patienten profitieren von der Medikationsanalyse durch ein größeres Wohlbefinden und ein besseres Verständnis für ihre Medikation. Das Projekt ist mittlerweile in fast allen Bundesländern etabliert. Die Teilnahme der Apotheken ist freiwillig und erfordert das Besuchen von Fortbildungskursen. Die ersten Fälle werden durch erfahrene Tutoren mitbegutachtet, bevor Kontakt zum Arzt aufgenommen wird. Eine Medikationsanalyse bedeutet für die Apotheke großen Aufwand. Für die Durchführung einer Medikationsanalyse nach Athina hält die Landesapothekerkammer einen Betrag von etwa 69 Euro für angemessen. Derzeit bezahlen die Krankenkassen noch nicht für diese wichtige pharmazeutische Dienstleistung.
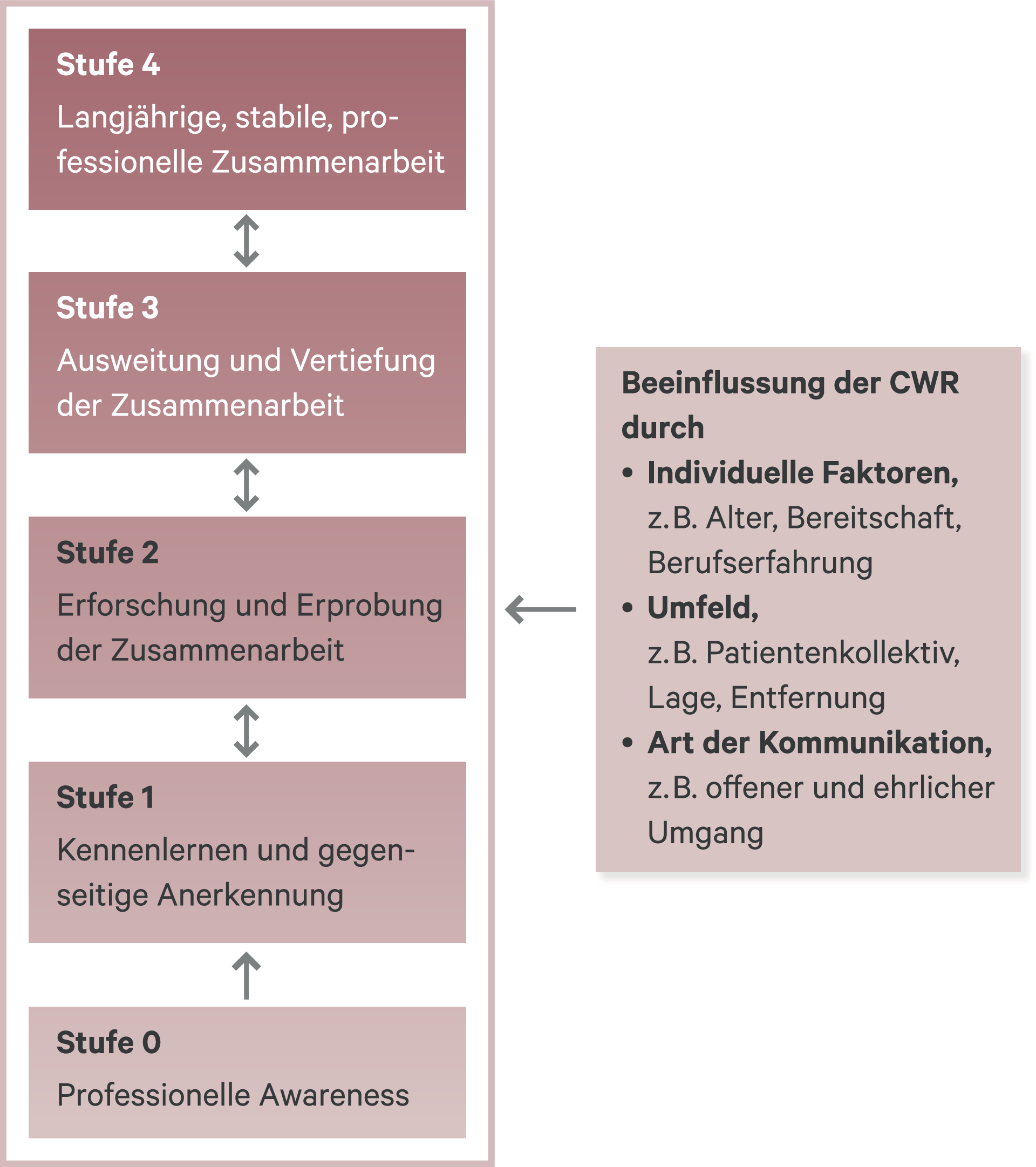
Abb. 2. Das Collaborative-Working-Relationship-(CWR-)Modell (nach Mc Donough et al., 2001 [22], adaptiert durch Haefeli et al., 2015 [12])
Qualitätszirkel zwischen Ärzten und Apothekern bieten eine weitere Möglichkeit, sich intensiver zur Behandlungsqualität auszutauschen (https://www.pharmasuisse.org/de/1246/Qualitätszirkel.htm; Zugriff: 16. Juni 2020).
Zusammenarbeit zwischen verschiedenen Heilberuflern will geübt sein und sollte nicht erst im Berufsalltag verlangt oder erwartet werden. Interprofessionelle Ausbildungsblöcke sollten entsprechend Platz in den Curricula finden [10]. An den Universitäten Tübingen und Frankfurt am Main gibt es solche Ansätze bereits. In gemeinsamen aktiven Lernsequenzen können Studierende der Pharmazie und der Medizin ein Verständnis für die jeweiligen späteren Rollen und Kompetenzen erlernen. Die Schweizer Universitäten Basel, Zürich, Genf und ETH Zürich haben interprofessionelle Ausbildungsblöcke aufgenommen. Die Lernsequenz aus Basel wurde 2017 mit dem Award „Interprofessionalität“ der Schweizerischen Akademie der Medizinischen Wissenschaften prämiert (https://www.samw.ch/dam/jcr:8dba5f64-bf9b-4f47-bcf1-d5afa39b0e56/award2017_interprofess_samw_uebersicht.pdf, Zugriff: 31. Januar 2020).
In naher Zukunft wird sich ein weiterer Partner am Prozess der Verschreibung von Medikamenten beteiligen. In einigen Ländern verfügen Pflegeexperten APN (Advanced Practice Nurse) bereits über die Kompetenz, Medikamente zu verschreiben, aber noch nicht allgemein in den deutschsprachigen Ländern [30, 31]; eine Ausnahme bildet der Kanton Waadt (Schweiz), wo APN über diese Kompetenz verfügen. Diese Pflegeperson muss über einen Masterabschluss in Pflege (Nursing Science) verfügen (http://icn-apnetwork.org/).
Um eine seitens des Patienten gefühlte Indiskretion zu vermeiden, sollten in den Apotheken für die Verordnungsvalidierung und Beratung zu psychopharmakologischen Therapien zunehmend die separaten Beratungsräume benutzt werden. Beim Psychiater in der Praxis, aber auch inzwischen zunehmend bei der Aufnahme in Kliniken, wo eine angestellte Person in für diese Zwecke errichteten Kabinen die administrativen Daten notiert, kann der Patient darauf trauen, dass die Kommunikation diskret erfolgt. Eine solche Umgebung, die für Entspannung sorgt, ist in den meisten Apotheken nicht von Beginn des Kontakts garantiert. Der Patient ist umgeben von anderen Klienten, die mehr oder weniger neugierig dem Gespräch zwischen dem Apotheker oder seinem Angestellten folgen können. Gerade bei einer Überprüfung durch den Apotheker, ob der Patient sichere Medikamentenkombinationen erhält, ist es möglich, dass Letzterer auch Einzelheiten über seine Krankheit und andere heikle Informationen mitteilt. Dies sollte er in einer geschützten Umgebung tun können. Die Apothekenbetriebsordnung schreibt dies auch vor: „Die Offizin muss so eingerichtet sein, dass die Vertraulichkeit der Beratung, insbesondere an den Stellen, an denen Arzneimittel an Kunden abgegeben werden, so gewahrt wird, dass das Mithören des Beratungsgesprächs durch andere Kunden weitestgehend verhindert wird.“ (§ 4, Abs. 2a, Satz 3). Aufgrund baulicher Gegebenheiten ist dies aber nur vereinzelt realisierbar, sodass Beratungsräume nur in wenigen Apotheken zu finden sind.
Ein verstärktes, kommunikatives Miteinander zwischen Apotheker und Arzt mit Spezialisierung in Psychiatrie und Psychotherapie bei der Behandlung von psychiatrischen Patienten würde die (vermittelte) Sicherheit der Psychopharmakotherapie fördern und optimieren. Dieses Miteinander würde sich auch in die Vorschläge der eingangs erwähnten WPA-Lancet-Psychiatry-Commission über die Zukunft der Psychiatrie (Future of Psychiatry) einreihen.
Interessenkonflikterklärung
PB: Honorare für die Beratung oder Teilnahme an einem Expertenbeirat von Janssen und Lundbeck; Honorare für Vorträge, Stellungnahmen oder Artikel von Janssen, Lundbeck, Recordati, Schwabe, Servier, Vifor und Zeller; Aktien von Novartis und Roche
MH: Keine Interessenkonflikte
SR: Mitgliedschaft bei ECNP, DGPPN, DBT-Dachverband, Deutsche Balintgesellschaft, Werkgemeinschaft Rehabilitation Wiesbaden, Lebensraum Eltville, Landesarbeitsgemeinschaft Psychiatrie-Erfahrene Hessen
DS: Mitgliedschaft beim Schweizerischen Apothekerverband pharmaSuisse, bei der European Society of Clinical Pharmacy (ESCP), beim Schweizerischen Verein der Amts- und Spitalapotheker (GSASA), Vorstandsmitglied beim Pharmaceutical Care Network Switzerland (PCN-S)
Literatur
1. Armstrong SEM, Brown HK, Shorey C, Madan R, et al. No association between trazodone and corrected-QT prolongation in older adults. J Clin Psychopharmacol 2019;39:528–30.
2. Battig VAD, Roll SC, Hahn M. Pharmacogenetic testing in depressed patients and interdisciplinary exchange between a pharmacist and psychiatrists results in reduced hospitalization times. Pharmacopsychiatry 2020;53:185–92.
2a. Baumann P. Clinical Psychopharmacology in Switzerland. J Clin Psychopharmacol 2019;39(1):5–8.
3. Baumann P, Amstutz U, Jetter A, Samer C, et al. Personalisierte Therapie bei Psychopharmaka: Grundlagen und praktische Hinweise für pharmakogenetische Tests. InFo Neurologie und Psychiatrie 2017;15:21–30.
4. Baumann P, Spies M, Moller HJ, Kasper S, et al. A proposal for a psychopharmacology-pharmacotherapy catalogue of learning objectives and a curriculum in Europe. World J Biol Psychiatry 2017;18:29–38.
5. Bhugra D, Tasman A, Pathare S, Priebe S, et al. The WPA-Lancet Psychiatry Commission on the future of psychiatry. Lancet Psychiatry 2017;4:775–818.
6. Blum K, Löffert S, Offermanns M, Steffen P. Psychiatrie Barometer. Umfrage 2017/2018. Deutsches Krankenhausinstitut, 2018.
7. Dietle A. QTc prolongation with antidepressants and antipsychotics. US Pharmacist 2015;40:HS34–40.
8. Elwyn G, Frosch D, Thomson R, Joseph-Williams N, et al. Shared decision making: a model for clinical practice. J Gen Intern Med 2012;27:1361–7.
9. Firth J, Siddiqi N, Koyanagi A, Siskind D, et al. The Lancet Psychiatry Commission: a blueprint for protecting physical health in people with mental illness. Lancet Psychiatry 2019;6:675–712.
10. Gallagher RM, Gallagher HC. Improving the working relationship between doctors and pharmacists: is inter-professional education the answer? Adv Health Sci Educ Theory Pract 2012;17:247–57.
11. Giacometti-Bickel G, Landolt K, Bernath C, Seifritz E, et al. In 10 Jahren werden 1000 Psychiaterinnen und Psychiater fehlen. Schweizerische Ärztezeitung 2103;94:302–5.
12. Haefeli WE, Seidling H, Weissenborn M. Serie AMTS: Interprofessionelle Zusammenarbeit. Pharm Ztg 2015;160:26–8.
13. Hahn M, Ritter C, Roll SC. Validation of pharmacist-physician collaboration in psychiatry: ‚the Eichberger-model‘. Int J Clin Pharm 2018;40:1001–4.
14. Hahn M, Roll S. Welche Patienteninformationen sollten Heilberuflern zur Verfügung stehen, um die Arzneimitteltherapiesicherheit nicht zu gefährden? Versicherungsmedizin 2018;71:173–5.
15. Hahn M, Roll SC, Klein J. [Drug therapy safety at the transition from hospital to community medicine]. Nervenarzt 2018;89:796–800.
16. Hawksworth GM, Corlett AJ, Wright DJ, Chrystyn H. Clinical pharmacy interventions by community pharmacists during the dispensing process. Br J Clin Pharmacol 1999;47:695–700.
17. Jayaram G, Doyle D, Steinwachs D, Samuels J. Identifying and reducing medication errors in psychiatry: creating a culture of safety through the use of an adverse event reporting mechanism. J Psychiatr Pract 2011;17:81–8.
18. Laux G. Proposal for a model psychopharmacology curriculum for psychiatric residents in Germany. Psychopharmakotherapie 2014;21:64–8.
19. Likic R, Maxwell SR. Prevention of medication errors: teaching and training. Br J Clin Pharmacol 2009;67:656–61.
20. Mann K, Rothschild JM, Keohane CA, Chu JA, et al. Adverse drug events and medication errors in psychiatry: methodological issues regarding identification and classification. World J Biol Psychiatry 2008;9:24–33.
21. Martin W. Ärztemangel: Einzelne Fachgebiete stark unter Druck. Dtsch Ärztebl 2019;116:2–4.
22. McDonough R, Doucette W. Developing collaborative working relationships between pharmacists and physicians. J Am Pharm Assoc 2001;41:682–92.
23. Members of EMERGE, Erice Medication Errors Research Group; Agrawal A, Aronson JK, Britten N, Ferner RE, et al. Medication errors: problems and recommendations from a consensus meeting. Br J Clin Pharmacol 2009;67:592–8.
24. Moret C. Combination/augmentation strategies for improving the treatment of depression. Neuropsychiatr Dis Treat 2005;1:301–9.
25. Paton C, Gill-Banham S. Prescribing errors in psychiatry. Psychiatr Bull 2003;27:208–10.
26. Prapotnik M, Waschgler R, Konig P, Moll W, et al. Therapeutic drug monitoring of trazodone: are there pharmacokinetic interactions involving citalopram and fluoxetine? Int J Clin Pharmacol Ther 2004;42:120–4.
27. Renner K. Mit Athina in die Praxis. Pharm Ztg 2014;159:32–3.
28. Roll SC, Hahn M. Das Eichberger Modell. Hessisches Ärzteblatt 2017;9:485–8.
29. Samsiah A, Othman N, Jamshed S, Hassali MA. Perceptions and attitudes towards medication error reporting in primary care clinics: A qualitative study in Malaysia. PLoS One 2016;11:e0166114.
30. Schober M. Introduction to Advanced Nursing Practice. An International Focus. Paris, France: Springer, 2016.
31. Schober M. Guidelines on advanced practice nursing 2020. Geneva: International Council of Nurses; 2020
32. Schulz M, Griese-Mammen N, Anker SD, Koehler F, et al. Pharmacy-based interdisciplinary intervention for patients with chronic heart failure: results of the PHARM-CHF randomized controlled trial. Eur J Heart Fail 2019;21:1012–21.
33. Wenzel-Seifert K, Wittmann M, Haen E. QTc prolongation by psychotropic drugs and the risk of Torsade de Pointes. Dtsch Arztebl Int 2011;108:687–93.
34. World Health Organization. WHO Technical Report Series, No. 961, 2011, Annex 8: Joint FIP/WHO guidelines on good pharmacy practice: standards for quality of pharmacy services; https://apps.who.int/medicinedocs/documents/s18676en/s18676en.pdf (Zugriff am 29.01.2020).
1 Die Begriffe Psychiater, Apotheker und Patienten beziehen sich auch auf weibliche Personen (Psychiaterinnen, Apothekerinnen, Patientinnen)
*Nach einem Symposium der Jahrestagung der Schweizerischen Gesellschaft für Psychiatrie und Psychotherapie (SGPP) (2019) vorgeschlagen von der Schweizerischen Gesellschaft für Arzneimittelsicherheit in der Psychiatrie (SGAMSP)
Prof. hon. Dr. rer. nat. Pierre Baumann, Département de Psychiatrie (DP-CHUV), Université de Lausanne, Site de Cery, 1008 Prilly-Lausanne, Schweiz, E-Mail: pierre.baumann@chuv.ch
Prof. Dr. Martina Hahn, Klinik für Psychiatrie, Psychosomatik und Psychotherapie, Klinikum der Goethe-Universität Frankfurt; Privatklinik Dr. Amelung, Königstein im Taunus
Prof. Dr. med. Sibylle C. Roll, Facharztzentrum Frankfurt Westend
Dr. Dominik Stämpfli, Institut für Pharmazeutische Wissenschaften, Eidgenössische Technische Hochschule ETH Zürich; Spitalapotheke, Kantonsspital Baden AG, Schweiz
Psychiatric patients ask their physician and pharmacist – how to optimize ambulant care?
When psychopharmacotherapy is implemented, different specialists including psychiatrists, psychotherapists, pharmacists, clinical pharmacologists and somatic physicians, and other partners work together. Training, adapted to the individual profession, and the use of different sources of information can lead to differences in the information provided, which can unsettle patients. Preventing this uncertainty requires effective communication between prescribing specialists and issuing authorities. Renewed continuing education also enables new forms of interaction and could counteract a shortage of skilled specialists. New communication channels should also be opened away from the usual prescription notices (e.g. sic, aut idem) lines and practiced in cooperation in training. Models, templates and working groups provide the necessary foundation for this.
Key words: psychopharmacotherapy, physician–patient–pharmacist, optimization of care
Psychopharmakotherapie 2020; 27(06):270-277
