Holger Petri, Bad Wildungen*
Selegilin
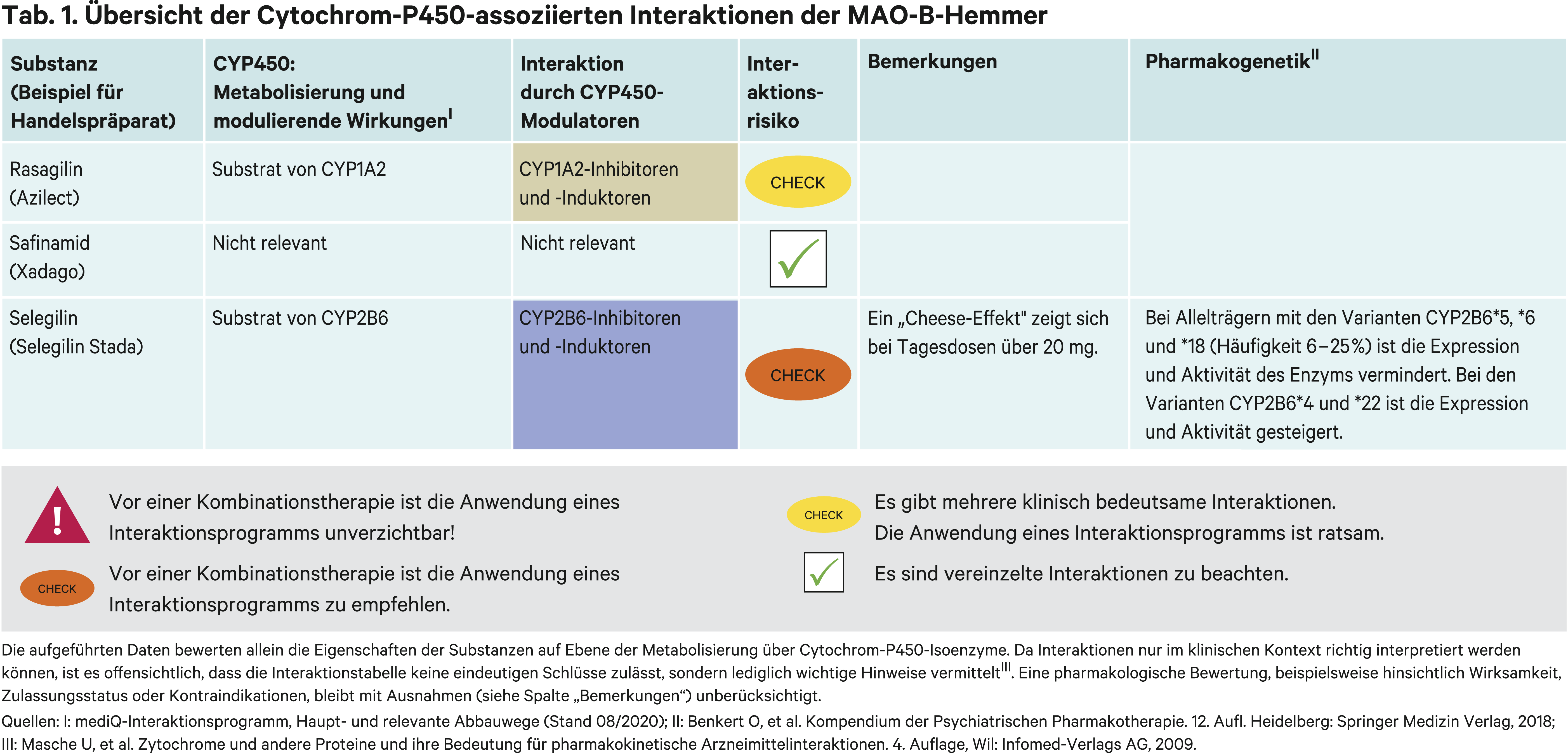
Bei der Entwicklung von Monoaminoxidase-(MAO-)Hemmern zur Behandlung von Depressionen wurde in den 60er-Jahren Selegilin (R-Deprenyl) synthetisiert. Es unterschied sich von anderen Wirkstoffkandidaten aufgrund des fehlenden „Cheese-Effekts“ [15]. Dieses durch potenziell lebensbedrohliche hypertensive Krisen gekennzeichnete Phänomen kommt durch die Verstärkung der sympathomimetischen Wirkung von Tyramin bei gleichzeitiger Gabe eines nichtselektiven Monoaminoxidase-Hemmers zustande. Selegilin wirkt in niedrigen Dosen selektiv auf die Monoaminoxidase Typ B. In Tagesdosen von über 20 mg oral hemmt Selegilin aber auch die Monoaminoxidase Typ A [5]. Selegilin unterliegt einem ausgeprägten First-Pass-Effekt. Als transdermales System angewendet, steigt die Bioverfügbarkeit von 4 % auf 73 %. Dadurch verliert sich die MAO-B-selektive Hemmwirkung im zentralen Nervensystem und Selegilin wirkt über zusätzliche MAO-A-Inhibition antidepressiv. Das transdermale System hat 2006 von der FDA die Zulassung als Antidepressivum erhalten. Da der Magen-Darm-Trakt umgangen wird, werden intestinale MAO-A-Enzyme kaum gehemmt und somit ist das Risiko für einen „Cheese-Effekt“ gering [15]. Der Metabolismus erfolgt primär über das polymorph exprimierte Cytochrom-P450(CYP)-Isoenzym 2B6 [2]. Als Abbauprodukte entstehen Desmethylselegilin und R-Amphetamine. Letztere sind anders als die S-Enantiomere nur wenig psychotrop aktiv, können aber in Dopingtests zu einem positiven Ergebnis führen [5, 10, 15]. Desmethylselegilin zeigt wie die Muttersubstanz MAO-B-Effekte, diese sind aber deutlich geringer ausgeprägt [15].
In einer klinischen pharmakokinetischen Interaktionsstudie wurde der Einfluss von Ethinylestradiol-haltigen hormonellen Kontrazeptiva auf den Metabolismus von Selegilin untersucht. Dabei zeigten sich 20-fach höhere Selegilin-Plasmaspiegel bei den Probandinnen [9]. Die Hemmung des Estrogens auf CYP-Enzyme erfolgt wahrscheinlich nicht durch direkten Angriff am Enzym, da hierfür supratherapeutische Konzentrationen erforderlich sind. Wahrscheinlicher scheint eine transkriptionelle Hemmung der Genexpression relevant zu sein. Über einen Estrogenrezeptor-vermittelten Mechanismus wird für CYP2C9 und CYP2C19 berichtet [12, 13]. Wie sich andere CYP2B6-Inhibitoren auf den Stoffwechsel von Selegilin auswirken, wurde in In-vivo-Studien nicht untersucht. Homozygote Allelträger des Allels CYP2B6*6 haben eine verminderte Stoffwechselkapazität [7, 16]. Das HIV-Arzneimittel Efavirenz wird primär über CYP2B6 metabolisiert. Die mittleren Spitzenspiegel lagen in einer Studie bei homozygoten Trägern des *6-Allels um das 2,25-Fache höher im Vergleich zu homozygoten CYP2B6-Wildtypträgern [6]. Das gibt einen Hinweis, wie sich CYP2B6-Inhibitoren auf die Exposition von Selegilin auswirken könnten. Wenig ist auch bekannt zum Einfluss von Induktoren auf die Selegilin-Plasmaspiegel. Es kann angenommen werden, dass genetische Polymorphismen bei der Betrachtung von CYP2B6-bedingten Arzneimittelwirkungen von Bedeutung sind [7, 16].
Selegilin wird von den drei verfügbaren MAO-B-Hemmern nur noch selten angewandt [14]. Jedoch zeigen sich in In-vitro- und Tierexperimenten mögliche Therapieansätze auch in nichtneurologischen Indikationen Selegilin einzusetzen [15]. Wünschenswert wären dann auch systematische klinische Studien zu den Auswirkungen von pharmakokinetischen Wechselwirkungen.
Rasagilin
Rasagilin ist ein Substrat von CYP1A2. Unter Einnahme des CYP1A2-Inhibitors Ciprofloxacin (Abb. 1) nimmt die AUC (Fläche unter der Konzentrations-Zeit-Kurve) von Rasagilin um 83 % zu [4]. In einem Fallbericht werden die dyskinetischen Nebenwirkungen eines Parkinsonpatienten auf erhöhte Dopaminspiegel zurückgeführt. Zu der bestehenden Grundmedikation mit Rasagilin und Levodopa wurde eine antiinfektive Therapie mit dem Fluorchinolon begonnen. Nach Absetzen des Antibiotikums sistierten die Symptome in kurzer Zeit. Die Autoren empfehlen daher bei Kombination mit potenten CYP1A2-Inhibitoren eine Halbierung der Rasagilin-Dosis [3].
Polyzyklische Kohlenwasserstoffe im Zigarettenrauch induzieren die Bildung von CYP1A2 [8]. Wie sich dies zusammen mit einer Komedikation mit anderen CYP1A2-Induktoren auf die Exposition von Rasagilin auswirkt, ist nicht bekannt. Mit einer Wirkungsabschwächung muss aber gerechnet werden [4].
Safinamid
Der MAO-B-Hemmer Safinamid kann wie Zonisamid über spannungsabhängige Natrium-Kanäle die bei parkinsonerkrankten Patienten relativen hohen Glutamatspiegel senken [1]. Anders als beim Antikonvulsivum ist der Metabolismus von Safinamid CYP-unabhängig und deshalb können diesbezüglich Wechselwirkungen ausgeschlossen werden [11].
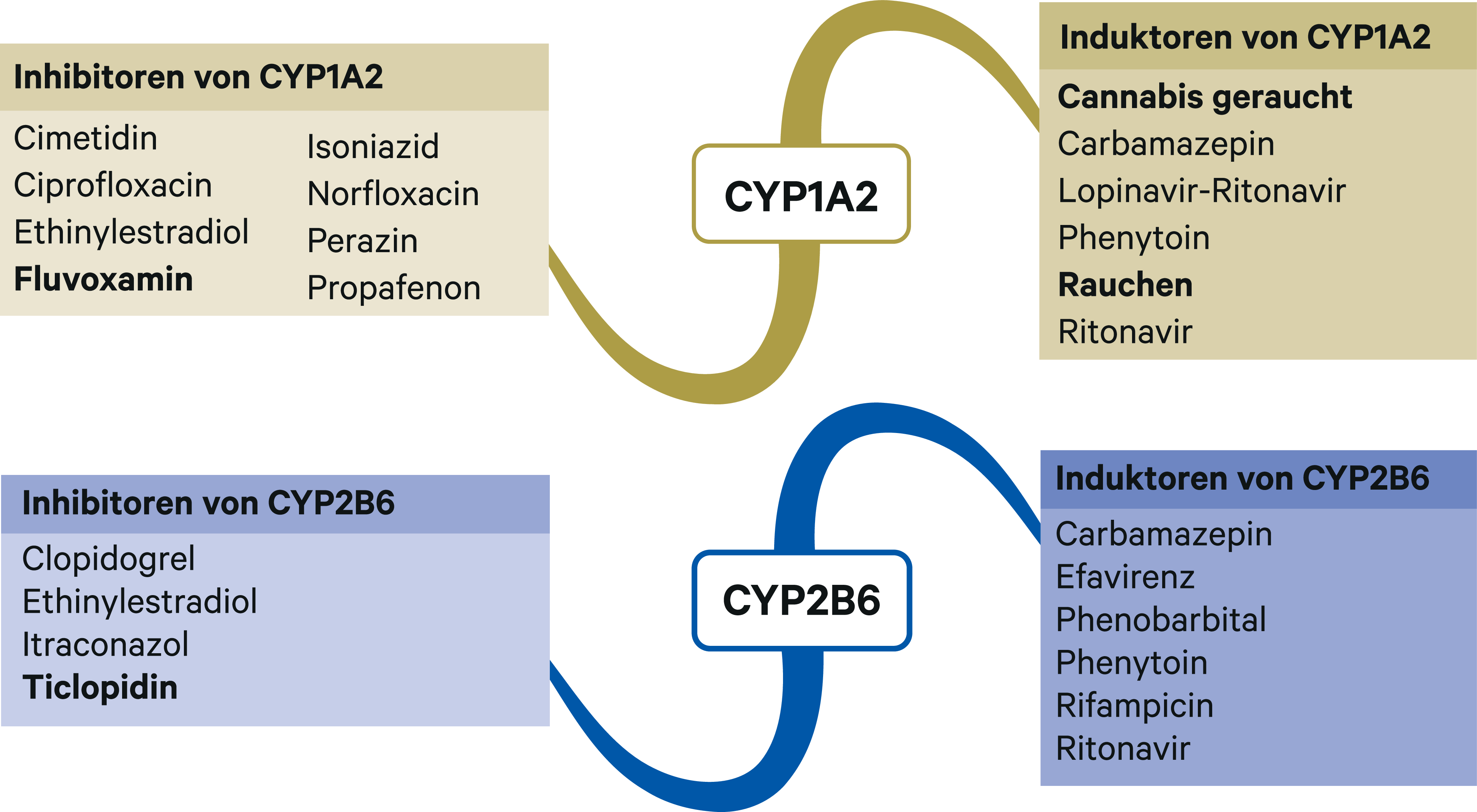
Abb. 1. Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450 (CYP) 1A2 und 2B6 (Stand 08/2020) [Quelle: mediQ-Interaktionsprogramm]
Literatur
1. Alborghetti M, Nicoletti F. Different generations of type-B monoamine oxidase inhibitors in Parkinson’s disease: From bench to bedside. Curr Neuropharmacol 2019;17:861–73.
2. Benetton SA, Fang C, Yang YO, et al. P450 phenotyping of the metabolism of selegiline to desmethylselegiline and methamphetamine. Drug Metab Pharmacokinet 2007;22:78–87.
3. Chappell KB, Shah SP, Cutshall BT, et al. Ciprofloxacin-rasagiline drug interaction leading to dopaminergic effects. Nurse Pract 2020;45:11–2.
4. Fachinformation Azilect®. Stand: Juni 2018.
5. Fachinformation Selegilin Stada®. Stand: Dezember 2016.
6. Fachinformation Sustiva®. Stand: Februar 2015.
7. Hedrich WD, Hassan HE, Wang H. Insights into CYP2B6-mediated drug-drug interactions. Acta Pharm Sin B 2016;6:413–25.
8. Kroon LA, Drug interactions with smoking. Am J Health Syst Pharm 2007;64:1971–21.
9. Laine K, Anttila M, Helminen A, Karnani H, Huupponen R. Dose linearity study of selegiline pharmacokinetics after oral administration: evidence for strong drug interaction with female sex steroids. Br J Clin Pharmacol 1999;47:249–54.
10. Mahmood, I. Clinical pharmacokinetics and pharmacodynamics of selegiline. Clin Pharmacokinet 1997;33:91–102.
11. Müller T, Foley P. Clinical pharmacokinetics and pharmacodynamics of safinamide. Clin Pharmacokinet 2017;56:251–61.
12. Mwinyi J, Cavaco I, Pedersen RS, et al. Regulation of CYP2C19 expression by estrogen receptor α: implications for estrogen-dependent inhibition of drug metabolism. Mol Pharmacol 2010;78:886–94.
13. Mwinyi J, Cavaco I, Yurdakok B, et al. The ligands of estrogen receptor α regulate cytochrome P4502C9 (CYP2C9) expression. J Pharmacol Exp Ther 2011;338:302–9.
14. Schwabe U, Paffrath D, Ludwig WD, et al. Arzneiverordnungs-Report 2019. Berlin, Heidelberg: Springer, 2019.
15. Tábi T, Vécsei L, Youdim MB, et al. Selegiline: a molecule with innovative potential. J Neural Transm (Vienna) 2020;127:831–42.
16. Wang H, Tompkins LM. CYP2B6: new insights into a historically overlooked cytochrome P450 isozyme. Curr Drug Metab 2008;9:598–610.
*Nachdruck aus Krankenhauspharmazie 2020;41:348–50.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2020; 27(05):255-257
