Holger Petri, Bad Wildungen*
Benzodiazepine
Benzodiazepine sind hochwirksame Substanzen. Sie wirken im Gegensatz zu anderen Anxiolytika schnell und zuverlässig, haben eine gute Verträglichkeit und große therapeutische Breite. Wegen des Abhängigkeitsrisikos ist ihre Anwendung jedoch zeitlich begrenzt [1]. Diazepam ist nur für einen kurzfristigen Einsatz als Anxiolytikum geeignet, da sein aktiver Hauptmetabolit N-Desmethyldiazepam mit einer Halbwertszeit von 30 bis 100 Stunden schlecht steuerbar ist und ein Kumulationsrisiko besteht. Zudem birgt Diazepam als CYP2C19- und CYP3A4-Substrat ein Interaktionspotenzial [14]. Vom pharmakokinetischen Profil sind Lorazepam und Oxazepam die zu bevorzugenden Benzodiazepine. Beide werden direkt glucuronidiert, wodurch Plasmaspiegelveränderungen durch die Komedikation wenig wahrscheinlich sind [1, 2, 6]. Die Glucuronidierung von Lorazepam wird durch Valproat gehemmt [15]. Deshalb werden 50 % niedrigere Lorazepam-Dosen bei Kombination mit dem Antikonvulsivum empfohlen [6].
Buspiron
Buspiron wird primär über CYP3A4 metabolisiert. Die pharmakologisch aktiven Hauptmetaboliten sind 6-Hydroxybuspiron und 1-Pyrimidinylpiperazin (1-PP) [1, 3, 16]. Es wird gemäß Konsensus-Leitlinien für therapeutisches Drug-Monitoring in der Neuropsychopharmakologie empfohlen, den Summenspiegel der aktiven Fraktion zu bestimmen [8].
Der Einfluss von CYP3A4-Modulatoren auf die Exposition wurde in verschiedenen pharmakokinetischen Studien mit gesunden Probanden untersucht. Die starken CYP3A4-Inhibitoren Erythromycin und Itraconazol (Abb. 1) erhöhten die Buspiron-Exposition um das 6-Fache bzw. das 19-Fache [10]. Die beiden Calciumkanalblocker Diltiazem und Verapamil, beide moderate CYP3A4-Hemmer (Abb. 1), erhöhten die Bioverfügbarkeit des Anxiolytikums um das 4- bzw. 3,4-Fache [12]. Der Konsum größerer Mengen Grapefruitsaft führte zu einem durchschnittlich 9,2-fach höheren AUC(Fläche unter der Konzentrations-Zeit-Kurve)-Wert [13]. Es werden daher in Kombination mit starken CYP3A4-Hemmern (Abb. 1) deutlich niedrigere Tagesdosen empfohlen. Dosissteigerungen sind nur nach klinischem Ansprechen vorzunehmen. Zu den möglichen unerwünschten Arzneimittelwirkungen, besonders in Kombination mit anderen serotonergen Arzneimitteln wie SSRI-Antidepressiva, gehört das Serotonin-Syndrom [3]. Mit mittelstarken CYP3A4-Hemmern wie Diltiazem und Verapamil (Abb. 1) braucht die Dosis nicht reduziert zu werden, jedoch kann das Therapieansprechen verändert sein [3].
Der starke CYP3A4-Induktor Rifampicin senkte in einer Untersuchung die Buspiron-Exposition um 90 % [11]. Vom Hersteller werden keine Vorgaben zur Dosissteigerung gegeben [3]. Bei An- und Absetzen von starken CYP3A4-Induktoren sollten die Dosisanpassungen unter Plasmaspiegelkontrolle vorgenommen werden.
Auf die Exposition des aktiven Metaboliten 1-Pyrimidinylpiperazin haben die starken CYP3A4-Modulatoren Itraconazol und Rifampicin nur einen geringfügigen Effekt [9].
Opipramol
Opipramol hat chemisch Ähnlichkeit mit den trizyklischen Antidepressiva, weist aber eine gänzlich andere Pharmakodynamik auf [7]. Der Metabolismus ist abhängig von der CYP2D6-Enzymaktivität. Bei Personen mit CYP2D6-Poor-Metabolizer-Phänotyp kann die maximale Plasmakonzentration cmax von Opipramol bis zu 2,5-mal höher sein als bei Personen mit normalem Metabolisierungsstatus (Extensive Metabolizer, EM) [4]. Pharmakokinetische klinische Studien mit CYP2D6-Inhibitoren sind nicht bekannt. Es kann erwartet werden, dass CYP2D6-Hemmer zu einem ähnlichen Anstieg der maximalen Plasmaspiegel führen, wie es bei Personen mit einem Poor-Metabolizer-Status beobachtet wurde. Hierdurch sollte auch eine erhöhte Exposition folgen. Der Primärmetabolit Deshydroxyethyl-Opipramol zeigt keine klinische Wirksamkeit [7].
Pregabalin
Pregabalin wird größtenteils unverändert renal ausgeschieden. Dosisanpassungen sind bei eingeschränkter Nierenfunktionsleistung notwendig [5].
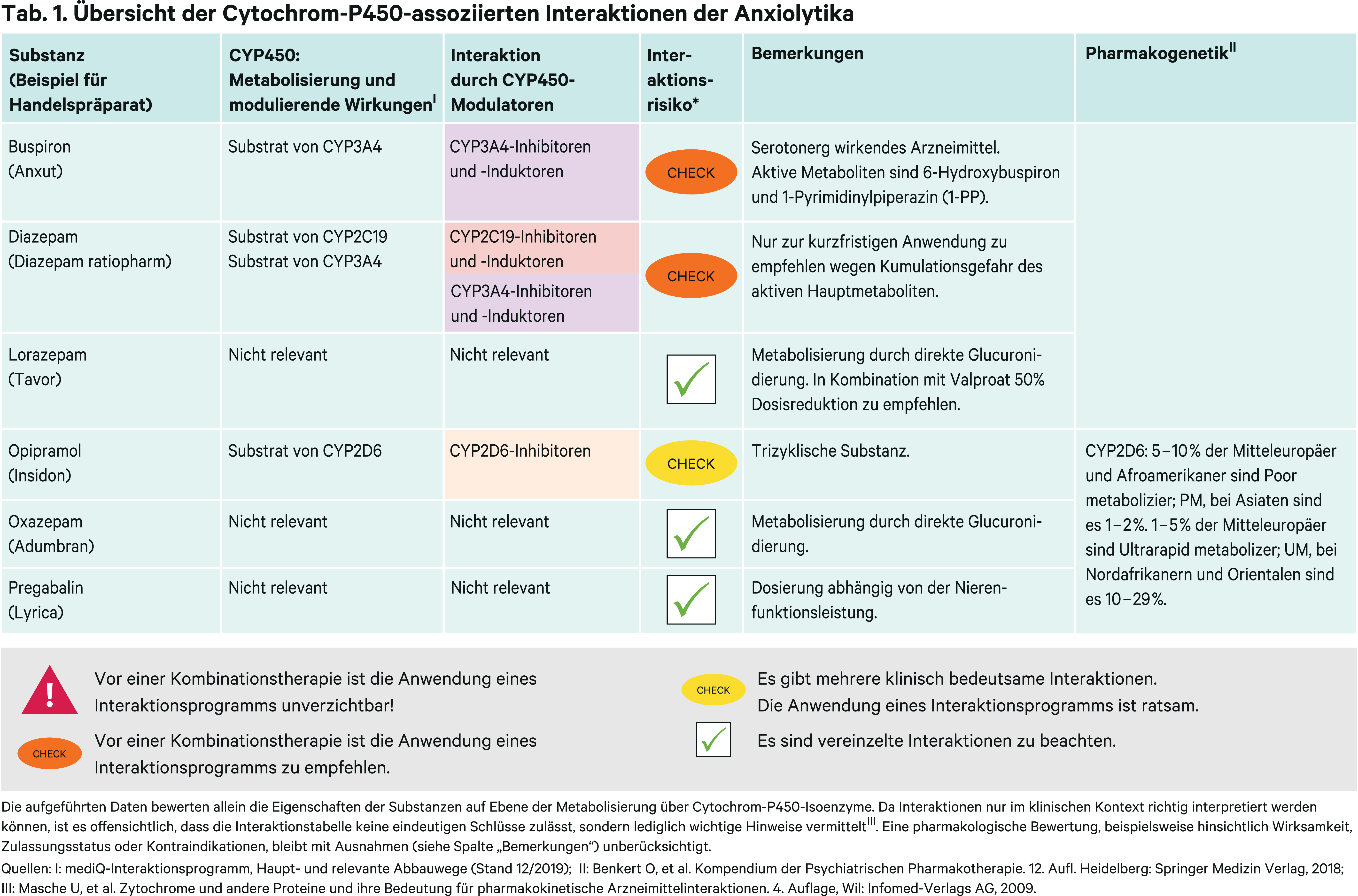
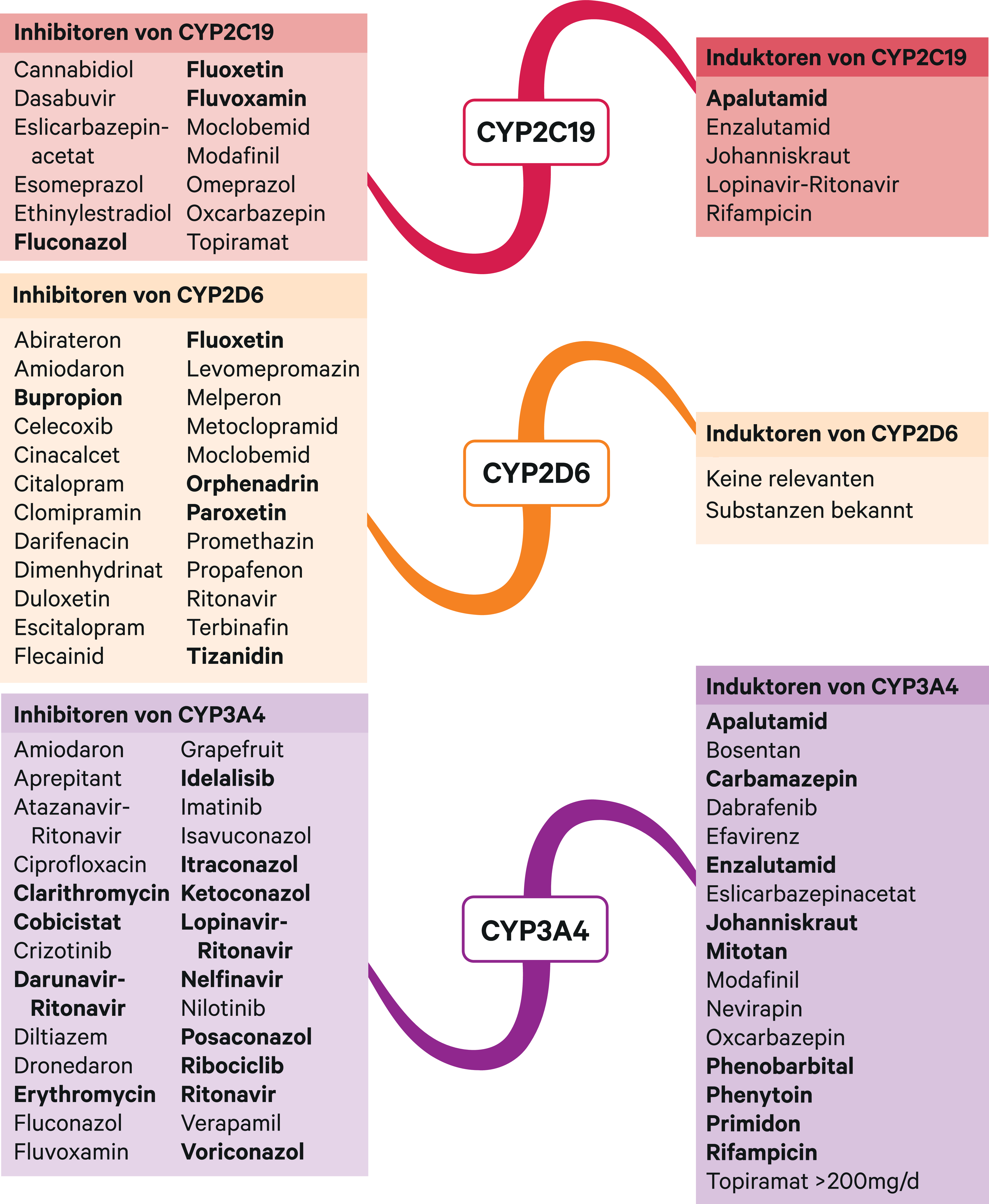
Abb. 1. Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450 (CYP) 2C19, 2D6 und 3A4 (Stand 12/2019) [Quelle: mediQ-Interaktionsprogramm]
Literatur
1. Benkert O, Hippius H. Kompendium der Psychiatrischen Pharmakotherapie. 12. Aufl. Heidelberg: Springer Medizin Verlag 2018.
2. Fachinformation Adumbran®. Stand: Juni 2019.
3. Fachinformation Anxut®. Stand: August 2016.
4. Fachinformation Insidon®. Stand: August 2015.
5. Fachinformation Lyrica®. Stand: Mai 2019.
6. Fachinformation Tavor®. Stand: Februar 2019.
7. Gahr M, Hiemke C , Connemann BJ. Update Opipramol. Fortschr Neurol Psychiatr 2017;85:139–45.
8. Hefner G, Laux, G, Baumann P, et al. Konsensus-Leitlinien für therapeutisches Drug-Monitoring in der Neuropsychopharmakologie: Update 2017. Psychopharmakotherapie 2018;25:92–140.
9. Kivistö KT, Lamberg TS, Neuvonen PJ. Interactions of buspirone with itraconazole and rifampicin: effects on the pharmacokinetics of the active 1-(2-pyrimidinyl)-piperazine metabolite of buspirone. Pharmacol Toxicol 1999;84:94–7.
10. Kivistö KT, Lamberg TS, Kantola T, et al. Plasma buspirone concentrations are greatly increased by erythromycin and itraconazole. Clin Pharmacol Ther 1997;62:348–54.
11. Lamberg TS, Kivistö KT, Neuvonen PJ. Concentrations and effects of buspirone are considerably reduced by rifampicin. Br J Clin Pharmacol 1998;45:381–5.
12. Lamberg TS, Kivistö KT, Neuvonen PJ. Effects of verapamil and diltiazem on the pharmacokinetics and pharmacodynamics of buspirone. Clin Pharmacol Ther 1998;63:640–5.
13. Lilja JJ, Kivistö KT, Backman JT, et al. Grapefruit juice substantially increases plasma concentrations of buspirone. Clin Pharmacol Ther. 1998;64:655–60.
14. Petri H. Das Interaktionspotenzial der zentralen Muskelrelaxanzien. Krankenhauspharmazie 2019;40:520–3.
15. Samara EE, Granneman RG, Witt GF, et al. Effect of valproate on the pharmacokinetics and pharmacodynamics of lorazepam. J Clin Pharmacol 1997;37:442–50.
16. Wong H, Dockens RC, Pajor L, et al. 6-Hydroxybuspirone is a major active metabolite of buspirone: assessment of pharmacokinetics and 5-hydroxytryptamine1A receptor occupancy in rats. Drug Metab Dispos 2007;35:1387–92.
*Nachdruck aus Krankenhauspharmazie 2020;41:25–8.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2020; 27(01)
