Abdol A. Ameri, Weidenstetten
Motorische Komplikationen wie On/Off-Fluktuationen gehören zu den am belastendsten und schwierigsten zu behandelnden Problemen im mittleren und fortgeschrittenen Stadium der Parkinson-Krankheit. Seit der Zulassung von Safinamid (Xadago®) im Mai 2015 als Add-on-Therapie zu Levodopa oder weiteren Parkinson-Medikamenten haben sich die Möglichkeiten zur Kontrolle der Fluktuationen erweitert. Die Substanz hat einen dualen Wirkungsmechanismus [10]: Über eine selektive und reversible Hemmung der MAO-B wird die dopaminerge Neurotransmission verstärkt. Darüber hinaus führt der Wirkstoff zu einer spannungsabhängigen Blockade von Natrium- und Calciumkanälen, was wiederum die glutamaterge Überaktivität verringern kann.
Der Nutzen der Add-on-Therapie mit Safinamid (50 und 100 mg/Tag) wurde in den drei Placebo-kontrollierten Phase-III-Studien, (Studien 016/018 und SETTLE) bei insgesamt mehr als 1200 Parkinson-Patienten im mittleren bis späten Krankheitsstadium mit motorischen Fluktuationen nachgewiesen [2, 3, 8]. Durch die Zugabe von Safinamid zur Standardtherapie wurde eine im Vergleich zu Placebo signifikante Verlängerung der On-Zeit (ohne beeinträchtigende Dyskinesien) erreicht. Die Wirkung setzte innerhalb der ersten vier Wochen ein und blieb über insgesamt 24 Monate erhalten [2, 3]. Ein zusätzlicher Nutzen zeigte sich im Rahmen einer Post-hoc-Analyse bei Patienten (n = 242), die bei Einschluss in die Studie 016 mäßige bis schwere Dyskinesien aufwiesen (DRS[Dyskinesia rating scale]-Gesamtscore > 4) [3]. In dieser Subgruppe kam es nach 24 Monaten unter Safinamid 100 mg zu einer signifikanten Abnahme des DRS-Gesamtscores während der On-Zeit (p = 0,0317 vs. Placebo) [3].
Vielversprechende Effekte auf nichtmotorische Symptome
Weitere Post-hoc-Analysen der Phase-III-Studien weisen auf potenzielle Effekte von Safinamid auf die mit dem Parkinson’s Disease Questionnaire – PDQ-39 erfasste Lebensqualität und auf nichtmotorische Symptome hin [1, 5, 6]. In einer aktuellen Post-hoc-Analyse der Langzeitstudie 018 zeigten sich unter Safinamid 100 mg/Tag signifikante Verbesserungen im PDQ-39-Item 37 „Muskelkrämpfe“ und Item 39 „Hitze-/Kältegefühl“ im Vergleich zu Placebo sowie eine leichte, aber nicht signifikante Verbesserung von Gelenkschmerzen (Item 38) (Abb. 1) [6]. Außerdem war der Anteil der Patienten, die keine Schmerzmittel benötigten, im Safinamid-Arm höher als im Placebo-Arm (50,9 % vs. 61,1 %; p = 0,0476) [6]. Weiterhin zeigte sich, dass unter der Add-on-Therapie auch die Schwere von Depressionen, gemessen anhand der Hamilton Rating Scale for Depression (GRID-HAMD), abnahm – sowohl in Woche 24 (–1,06 vs. –0,49; p = 0,0408) als auch in Woche 102 (–0,76 vs. +0,11; p = 0,0027) [5].
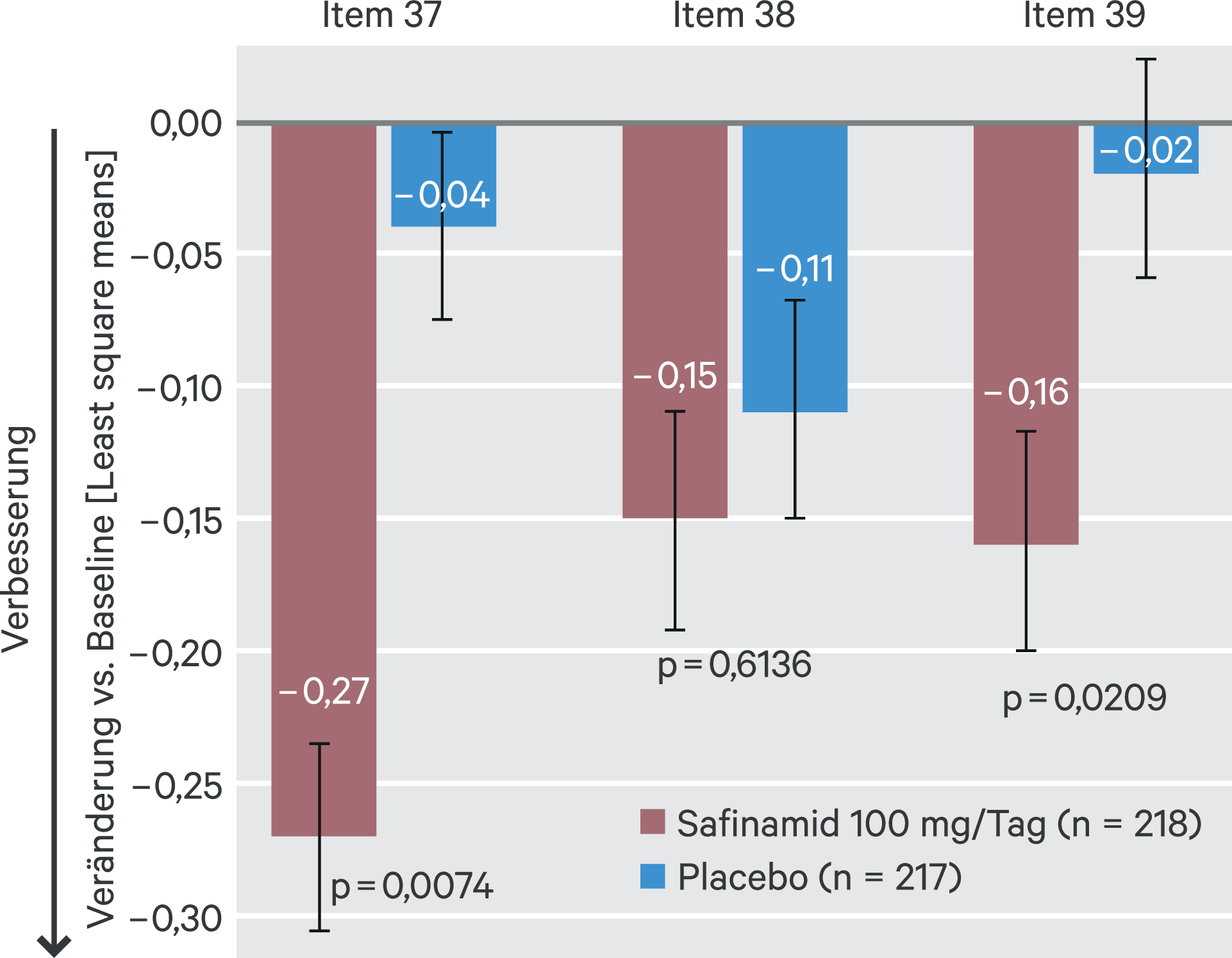
Abb. 1. Post-hoc-Analyse der Studie 018: Veränderung in den PDQ-39-Items 37 (Muskelkrämpfe), 38 (Gelenkschmerzen) und 39 (Hitze-/Kältegefühl) von Baseline bis Woche 102 (mod. nach [6])
Erfahrungen aus dem klinischen Alltag
Die Evidenz aus klinischen Studien wird ergänzt durch neue Daten der prospektiven, nichtinterventionellen Studie X-TRA [7]. An der Beobachtungsstudie nahmen 299 unselektierte Parkinson-Patienten (Alter: 72,7 ± 9,0 Jahre, Krankheitsdauer 7,8 ± 5,9 Jahre) aus Deutschland teil, die zusätzlich zu ihrer bisherigen Medikation auf Safinamid (50–100 mg/Tag) eingestellt wurden. Während der sechsmonatigen Studie wurde ein deutlicher Rückgang bei verschiedenen Symptom-Scores beobachtet, der auf eine Verbesserung motorischer und nichtmotorischer Symptome sowie der gesundheitsbezogenen Lebensqualität schließen ließ. Bei den mit der Non-Motor Symptoms Scale (NMSS) erfassten nichtmotorischen Symptomen zeigten sich unter der Zusatztherapie mit Safinamid die stärksten Verbesserungen gegenüber Baseline in den NMSS-Bereichen Stimmung/Kognition, Schlaf/Müdigkeit und Sexualfunktion. Wie bereits in den Phase-III-Studien war Safinamid auch in dieser breiten Kohorte im Allgemeinen gut verträglich [7].
Quelle
Prof. Dr. Karla Eggert, Marburg; Prof. Dr. Thomas Müller, Berlin; Satellitensymposium „Therapeutisches Potenzial von Safinamid und Verbesserung der Lebensqualität von Parkinson-Patienten“, veranstaltet von Zambon im Rahmen des Deutschen Kongresses für Parkinson und Bewegungsstörungen, Düsseldorf, 8. März 2019.
Literatur
1. Barone P, et al. Significant reductions of pain treatments with safinamide administered as add-on therapy to levodopa in patients with Parkinson’s disease and fluctuations. Eur J Neurol 2015;22(Suppl 1):293; P.2240.
2. Borgohain R, et al. Randomized trial of safinamide add-on to levodopa in Parkinson’s disease with motor fluctuations. Mov Disord 2014;29:229–37.
3. Borgohain R, et al. Two-year, randomized, controlled study of safinamide as add-on to levodopa in mid to late Parkinson’s disease. Mov Disord 2014;29:1273–80.
4. Caccia C, et al. Safinamide: from molecular targets to a new anti-Parkinson drug. Neurology 2006;67(Suppl 2):S1823.
5. Cattaneo C, et al. Long-term effects of safinamide on mood fluctuations in Parkinson’s disease. J Parkinson Dis 2017;7:629–34.
6. Cattaneo C, et al. Long-term efficacy of safinamide on Parkinson’s disease chronic pain. Adv Ther 2018;35:515–22.
7. Jost W, et al. Wirksamkeit und Sicherheit von Safinamid als Zusatztherapie zu Levodopa bei Parkinson-Patienten: eine nicht-interventionelle Beobachtungsstudie. Fortschr Neurol Psychiatry 2018;86:624–34.
8. Schapira AH, et al. Assessment of safety and efficacy of safinamide as a levodopa adjunct in patients with Parkinson disease and motor fluctuations: A randomized clinical trial. JAMA Neurol 2017;74:216–24.
Psychopharmakotherapie 2019; 26(03):165-173
