Daniel Reker, Michael Schneider, Timo Greiner, Rüdersdorf/Neuruppin, Detlef Degner, Göttingen, Sermin Toto, Stefan Bleich, Hannover, Renate Grohmann, München, und Martin Heinze, Rüdersdorf/Neuruppin
Kasuistik
Es erfolgte eine stationäre Aufnahme des seit über 30 Jahren alkoholabhängigen und komorbid rezidivierend depressiven 57-jährigen Patienten bei akutem Suchtdruck und wiederholter Exazerbation einer depressiven Episode (ICD 10: F33.2). Zum Aufnahmezeitpunkt währte die Abstinenz seit etwa 19 Monaten, wobei neun Monate zuvor ein Umzug in eine sozialtherapeutische Wohnform im Einzugsgebiet unserer Klinik erfolgt war. Der Suchtdruck hatte sich nach Angaben des Patienten infolge einer Umstellung der antidepressiven Medikation eingestellt. Im Verlauf der etwa zehn Monate andauernden depressiven Episode waren neben der ambulanten Behandlung in der Psychiatrischen Institutsambulanz (PIA) unseres Hauses bereits drei Aufenthalte auf verschiedenen Stationen unserer Abteilung erfolgt.
Der Patient war vor dem Umzug längere Zeit unter anderem auf Mirtazapin eingestellt, hatte es gut vertragen und war stabil. Unter dieser Einstellung hatte er in zeitlichem Zusammenhang mit seinem Umzug eine depressive Symptomatik entwickelt. Im ersten stationären Aufenthalt wurde die Mirtazapin-Medikation wegen mutmaßlich ungenügender Wirksamkeit beendet. Die in den weiteren Aufenthalten angewandten Antidepressiva zeigten keine ausreichende Wirksamkeit. Kurz nach der dritten Entlassung erfolgte im Rahmen einer Hausarztkonsultation die erneute Verordnung von Mirtazapin mit einer ungewöhnlich hohen Startdosis von 45 mg/Tag. Abbildung 1 zeigt eine Übersicht der medikamentösen Behandlungsversuche.
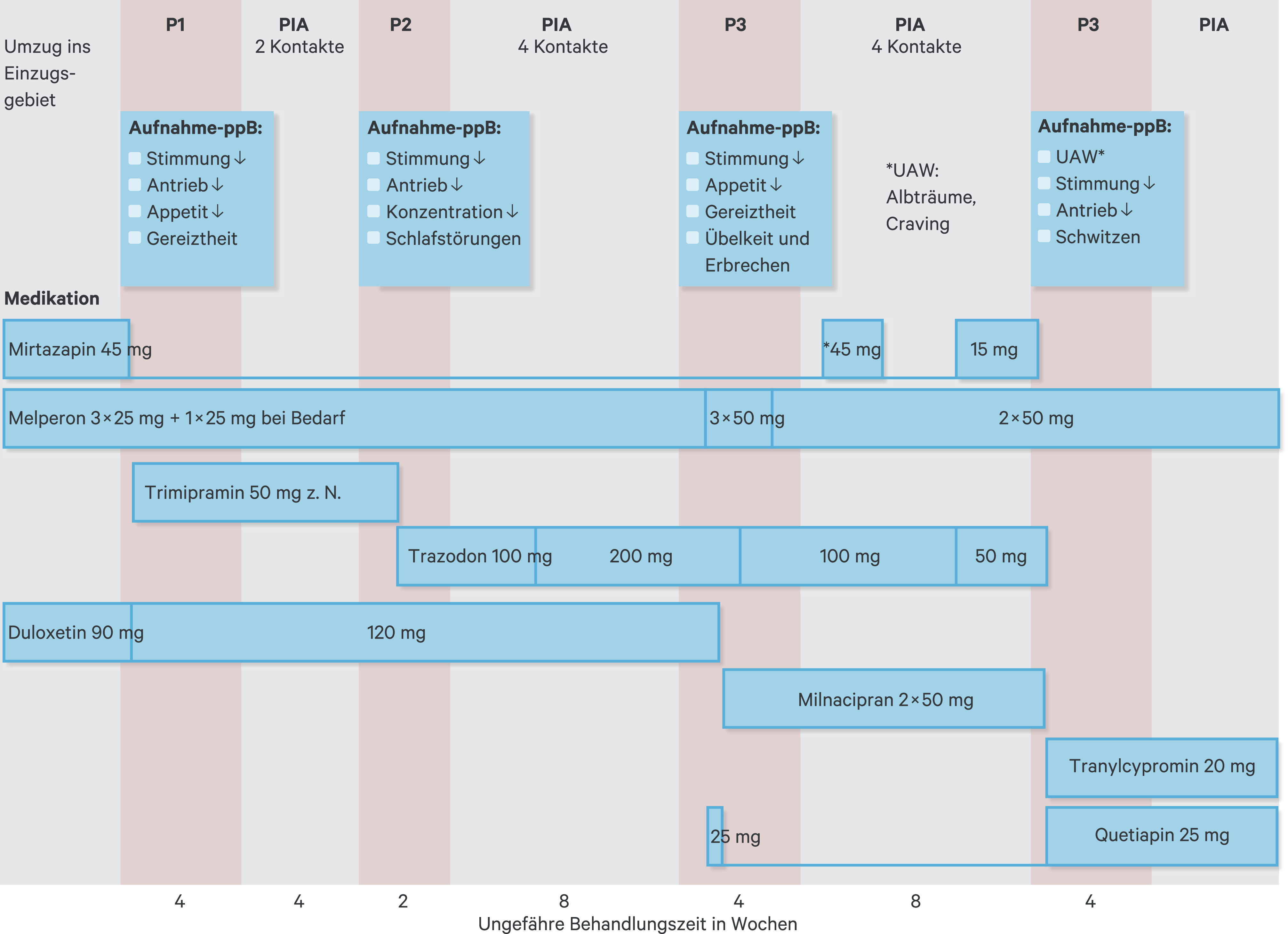
Abb. 1. Übersicht zum Verlauf der medikamentösen Behandlung im dargestellten Fall Alle Dosisangaben beziehen sich auf die Erhaltungsdosen ohne Berücksichtigung schrittweiser Dosissteigerung bei Verordnungsbeginn * Verordnung durch die Hausärztin; UAW: unerwünschte Arzneimittelwirkung; ppB: psychopathologischer Befund; ↓: Minderung; Übelk.: Übelkeit; Erbr.: Erbrechen; PIA: psychiatrische Institutsambulanz; P1: allgemeinpsychiatrische Station 1; P2: allgemeinpsychiatrische Station 2; P3: Suchtstation
Die neuerliche Einnahme einer unmittelbaren Tagesdosis von 45 mg Mirtazapin führte bei dem Patienten zu einem ausgeprägten Suchtdruck sowie zu Albträumen und vermehrtem Schwitzen, sodass er die Einnahme unterbrach und mit einigen Wochen Verzögerung die PIA aufsuchte. Dort wurde mit ihm besprochen, die ehemals guten antidepressiven Erfahrungen mit Mirtazapin noch einmal aufzugreifen und die erlebten unerwünschten Arzneimittelwirkungen (UAW) durch eine geringere Einstiegsdosis von 15 mg täglich zu vermeiden. Ferner wurde das vom Patienten als wirkungslos erlebte Trazodon herunterdosiert, mit dem Ziel, es bald gänzlich zu beenden.
Es stellten sich jedoch auch unter 15 mg/Tag Mirtazapin erneut Suchtdruck und Albträume ein. Hierdurch zeigte sich der Patient stark verunsichert und auf Unterstützung bei der Abstinenzaufrechterhaltung angewiesen, sodass die hier betreffende Aufnahme erfolgte.
Auf der Station wurde die antidepressive Medikation auf Tranylcypromin als Monotherapie umgestellt, wovon der Patient auch subjektiv deutlich profitierte. Zu Craving oder einem Trinkrückfall kam es in diesem Zeitraum nicht.
Diskussion
Craving, der Drang oder intensive Wunsch, Alkohol zu trinken stellt ein wichtiges Kriterium zur Diagnose einer Alkoholabhängigkeit dar. Es ist in seinen biologischen Mechanismen sowie in der Genese bzw. Etablierung als Symptom bei Suchtkranken nicht vollständig verstanden. Verschiedene kognitionspsychologische Modelle werden schon lange diskutiert. Sie erstrecken sich von klassischer Konditionierung verknüpft mit anschließender kognitiver Bewertung bis hin zu komplexen Prozessen paralleler emotionaler Besetzung oder Bewusstwerdung von Craving einzig bei Unterdrückung automatischer Verhaltensmuster [10]. In den jüngeren Modellen wird dabei die Beobachtung berücksichtigt, dass Craving unabhängig vom Konsum auftritt und auch Konsum ohne vorheriges Craving von Suchtkranken beschrieben wird. In empirischen Zusammenhängen, in denen es als ein Prädiktor der Rückfallwahrscheinlichkeit untersucht wurde, zeigten sich korrespondierende Ergebnisse [11].
Diverse aktuelle Untersuchungen geben einen Überblick über die Induktion bzw. die Auftrittswahrscheinlichkeit von Craving. Untersuchungen zur Erfassung von Craving in Zusammenhang mit Medikamenten bzw. als UAW sind dabei nicht sehr häufig. Eine Zusammenfassung findet sich in einem Review, in welchem der Zusammenhang zwischen verschiedenen Stressoren – darunter auch pharmakologischen – und Alkoholkonsum beschrieben wurden [9]. Hier finden sich auch Ansätze, in denen der Craving-induzierende Effekte des alpha-2-adrenergen Antagonisten Yohimbin und des als Partydroge bekannten Meta-Chlorophenylpiperazin (mCPP) genutzt werden, um dieses Phänomen eingehender zu erforschen. Hierbei konnte ein Zusammenhang zwischen dem Schweregrad der Alkoholabhängigkeit und der Intensität des medikamentös induzierten Cravings festgestellt werden [12]. Ausgehend von der Vermittlung von Stress über die Hypothalamus-Hypophysen-Nebennierenrinden-Achse werden in der Übersicht auch Arbeiten aufgezählt, in denen beispielsweise Insulin, 2-Deoxyglucose, Nicotin, serotonerg wirkende Psychopharmaka wie Citalopram oder auch Alkohol selbst als Trigger für Craving untersucht werden.
Mirtazapin ist ein zugleich noradrenerg und serotonerg wirkendes Antidepressivum. Es blockiert präsynaptische adrenerge Alpha-2A/C-Autorezeptoren und Serotoninrezeptoren vom Subtyp 5-HT2A. Zusätzlich besteht eine ausgeprägt antihistaminerge Komponente [2]. Im klinischen Alltag wird die gute Wirksamkeit hinsichtlich begleitender Schlafstörungen geschätzt, während unerwünschte Wirkungen wie eine häufig auftretende Gewichtszunahme oder die nicht seltene Induktion von Albträumen den Gebrauch limitieren.
Es gibt Hinweise dafür, dass in der Pathophysiologie von Suchterkrankungen Serotoninrezeptor-Untergruppen beteiligt sind. Darauf beruhend wurde Mirtazapin als vielversprechend in der Suchtbehandlung angesehen, wobei in der jüngsten diesbezüglichen Übersichtsarbeit bereits 2012 ein Mangel an großen randomisierten und kontrollierten klinischen Studien beschrieben wurde [7].
Eine aktuelle Suchanfrage zur Rückfallhäufigkeit für Alkoholkonsum oder Steigerungsraten für Craving nach Alkohol durch Mirtazapin erbrachte eine geringe Anzahl an Studien. Einige werden in einem Review zusammengefasst, dessen Autoren vier der sechs dort eingeschlossenen Studien selbst durchgeführt hatten [6]. Die Autoren kamen zu dem Urteil, dass die offenen und teils ohne Kontrollgruppen angesetzten Studiendesigns sowie die Fallzahlen der aktuellen Arbeiten bisher keine Nachweise für Trinkmengenreduktion durch Mirtazapin liefern konnten. Für die symptomatische Behandlung von Craving wurden jedoch in drei der sechs Studien Hinweise auf einen mindernden Effekt durch Mirtazapin beschrieben, wenn auch gegenwärtig nicht ausreichend belastbar. Ferner bleiben Fragen zur Aussagekraft der Studienlage in Bezug auf ältere Patienten mit Suchterkrankung und Depression zu beachten. Zu diesem Schluss kommen auch Cornelius et al. in ihrem Review mit Verweis auf eine kurz zuvor veröffentlichte Studie, in der sowohl in der Wirksamkeit als auch in der Verträglichkeit für Mirtazapin bessere Werte bei jüngeren Probanden im Vergleich mit älteren Probanden gefunden wurden [3]. Dies könnte für den eher älteren Patienten im vorliegenden Fall von Bedeutung sein.
Auf Grundlage des Reviews wird eine umfangreichere Studie durch die Autoren selbst angekündigt, die aktuell in der Durchführungsphase ist. Im Review selbst wurde die Pilotstudie dazu eingeschlossen. In dieser wurde Craving mittels der Obsessive Compulsive Drinking Scale erhoben. Daran gemessen reduzierte sich das Craving um etwa 47 % bei allen 14 Teilnehmern nach 12 Wochen. Es zeigte sich kein signifikanter Unterschied der Verum- zur Placebo-Gruppe bei niedriger Fallzahl [5]. Ähnliche Ergebnisse zeigten sich auch bei den beiden im Review hinzugezogenen Studien von anderen Arbeitsgruppen außerhalb der USA. Altintoprak et al. stellten eine Abnahme des Cravings, gemessen an einem bisher und selbst für diese Studie nicht veröffentlichten Fragebogen mit 24 Fragen fest [1]. Es wurden keine signifikanten Unterschiede nach symptomadaptierter Behandlung sowohl mit 45 bis 60 mg Mirtazapin pro Tag (durchschnittlich 45,0 ± 17,55 mg/Tag) als auch mit 125 bis 150 mg Amitriptylin (durchschnittlich 125,0 ± 20,4 mg/Tag) über 54 Tage ersichtlich. Eine Placebo-Kontrolle wurde nicht durchgeführt.
Yoon et al. kamen in ihrer offenen Studie an 128 koreanischen Probanden unter Verwendung der Obsessive Compulsive Drinking Scale und der visuellen Analogskala für Craving ebenfalls zu dem Ergebnis einer deutlichen Symptomreduktion, wobei keine Kontrolle gegen Placebo stattfand und die zusätzliche Einnahme anderer Antidepressiva sowie Anti-Craving-Medikamente gestattet wurde [13].
Neben dem bis hierhin dargestellten Review findet sich eine weitere offene Pilotstudie [4]. Dabei wurden 45 mg Mirtazapin in einem zweiten Studienabschnitt zusätzlich verordnet, nach einer ersten Behandlungsperiode mit durchschnittlich 298 mg (SD ±137 mg) Quetiapin als Monotherapie über acht Wochen. Von den 20 initial eingeschlossenen Probanden fielen vier bereits während der Quetiapin-Monotherapie aus. Weitere fünf Probanden verließen die Studie in der zweiten Phase der Quetiapin-Mirtazapin-Kombinationstherapie, sodass elf Probanden letztlich den gesamten 16-wöchigen Behandlungsplan mit Quetiapin und Mirtazapin abschlossen. Die Arbeitsgruppe berichtete über einen Craving-reduzierenden Effekt der Kombinationstherapie verglichen mit der Quetiapin-Monotherapie und gemessen an der Penn Alcohol Craving Scale (PACS) von 3,2 ± 1,2 auf 2,5 ± 1,4 (p = 0,04).
Zusammengefasst lässt sich für den hier vorgestellten Fall feststellen, dass es in der Literatur keine sicheren Hinweise auf vermehrtes Craving durch Mirtazapin gibt. Eher wurden die Hinweise auf einen mindernden Effekt auf Craving für Mirtazapin untersucht.
Nun entwickelte unser Patient nach Reexposition erneut eine vergleichbare Symptomatik. Somit ist eine Induktion des Cravings durch Mirtazapin nicht ohne weiteres von der Hand zu weisen. Lässt man den Blick hierdurch auf die bestehenden Unterschiede unseres Falls zu den Studienverhältnissen leiten, fällt zum einen das höhere Alter unseres Patienten auf. Die begrenzte Aussagekraft von Studien für ältere Patienten wurde weiter oben im Text bereits angemerkt.
Zum anderen ist die Komedikation im vorliegenden Fall zu beachten. Nicht nur fand durch eine gleichzeitige Einnahme von Milnacipran zum betreffenden Zeitpunkt eine additive serotonerge Aktivierung statt, auch die gleichzeitig bestehende bedarfsweise Verordnung des Cytochrom-P450-Enzym-CYP2D6-Inhibitors Melperon kann von Bedeutung sein. Die Metabolisierung von Mirtazapin erfolgt in erster Linie über die Cytochrom-P450-Isoenzyme CYP2D6 und CYP3A4. Milnacipran wird kaum in der Leber verstoffwechselt. Leider bleibt offen, wie oft der Patient ambulant von Melperon Gebrauch gemacht hat, sodass hier über die Bemerkung eines denkbaren Zusammenhangs hinaus keine weiteren Ausführungen gemacht werden können. In der Klinik forderte er sich den Bedarf nur etwa ein- bis zweimal in Einzeldosen von 25 bis 50 mg je stationärem Aufenthalt ab.
Die veränderte Komedikation bildet womöglich auch den entscheidenden Unterschied in der Frage, warum der Patient unter der ehemaligen Einstellung auf Mirtazapin vor seinem Umzug kein Craving entwickelt hatte. Da jedoch die oben bereits genannten Annahmen zu serotonerg vermitteltem Stress und Craving als Folge [9] bisher nur wenig untersucht sind, erschöpft sich die Argumentation an dieser Stelle.
Anamnestisch waren dem Patienten selbst neben der Mirtazapin-Einnahme keine weiteren situativen Stressoren bewusst. Auch ein Zusammenhang mit den zugleich aufgetretenen Albträumen kann allenfalls vermutet werden, da ihm keine Inhalte der Träume erinnerlich waren. Albträume sind eine bekannte UAW unter Mirtazapin. Zwar war der Patient hiervon in der Vergangenheit nicht betroffen gewesen, jedoch lässt uns allein die Tatsache des Auftretens der UAW Craving hier nach Unterschieden in den Gegebenheiten zu den verschiedenen Zeitpunkten suchen, was in den oben bereits aufgeführten Betrachtungen münden muss.
In der AMSP-internen Fallbewertung [8] wurde der Zusammenhang des Cravings mit Mirtazapin mit der schwächeren Wahrscheinlichkeitsstufe W1 (möglicher Zusammenhang) eingestuft. Dies deckt sich mit unserer nicht über Hinweise und spekulative Überlegungen hinausreichenden Betrachtung hier.
Einen vergleichbaren Fallbericht konnten wir in PubMed nicht finden, in der AMSP-Datenbank finden sich zum Thema Craving zwei weitere Fälle. In einem Fall entwickelte eine Patientin mit agitierter Depression ohne Abhängigkeitsanamnese im Rahmen einer symptomatischen Therapie mit Olanzapin ein ihr vorher unbekanntes Verlangen nach Alkohol. Im anderen Fall zeigte ein multisubstanzabhängiger Patient ausgeprägtes Craving nach Ansetzen von Reboxetin. Bei beiden Fällen wurde der Zusammenhang nur als möglich eingestuft, da es insgesamt als unerwünschte Arzneimittelwirkung (UAW) unbekannt war und Alternativerklärungen plausibel erschienen.
Alternativerklärungen ergeben sich im vorliegenden Fall, wie bereits angesprochen, nicht hinreichend, zumal das zweimalige zeitlich mit der Einnahme von Mirtazapin assoziierte Auftreten der Symptomatik zu berücksichtigen ist. Die Laborwerte des Patienten zum Zeitpunkt der stationären Aufnahme direkt nach der zweiten Craving-Episode zeigten keine akuten pathologischen Veränderungen. Ferner war während des dritten der vier stationären Aufenthalte eine bildgebende Diagnostik mittels kranialer Kernspintomographie erfolgt, bei der sich ebenso keine akuten pathologischen Veränderungen gezeigt hatten.
Eine Liquorpunktion oder eine EEG-Untersuchung wurde während der stationären Aufenthalte nicht durchgeführt. Im Labor fanden sich keine wegweisenden pathologischen Befunde. Das Gewicht des Patienten war weitestgehend stabil. Hinweise für ein Kohlenhydrat-Craving fanden sich in der Dokumentation nicht, es lässt sich jedoch auch nicht ausschließen.
Letzthin können noch die Exazerbation der depressiven Symptomatik sowie die veränderte Lebenssituation des Patienten nach dem Umzug in eine betreute Wohngemeinschaft mit anderen Alkoholabhängigen in Zusammenhang mit dem Craving betrachtet werden. Sowohl psychische als auch soziale Faktoren werden als Auslöser für Stress und dadurch angestoßenes Craving untersucht. Der Patient berichtete sowohl bezüglich der Symptomatik als auch im Rahmen der alltäglichen Interaktionen im neuen Umfeld keine zusätzlichen bewussten auslösenden Ereignisse in zeitlichem Zusammenhang mit dem Craving. Unbewusste depressive Konfliktdynamiken wurden nicht exploriert und können hier somit nicht detailliert betrachtet werden. Sie können jedoch auch nicht ausgeschlossen werden. Insgesamt erscheinen beide Belastungsfelder – sowohl das depressive Erleben als auch die sozialen Veränderungen – in ihrem eher schwelend wirkenden Charakter als eher bahnende bzw. begünstigende Faktoren für Stress im vorliegenden Fall und damit plausibel als Triggerfaktoren für Craving, wie in dem Review von 2012 um Thomas et al. zusammengefasst [9].
Für uns ist der vorliegende Fall ein anschauliches Beispiel für die komplexen Schwierigkeiten in der Behandlung von komorbid erkrankten Suchtpatienten, wobei psychotrope Substanzen, worunter Psychopharmaka ja letztlich auch einzustufen sind, exklusive und eigendynamisch wirksame Symptome erzeugen können. Wie bereits einleitend erwähnt, ist oftmals eine individuelle Rationale als Basis eines symptomorientierten Behandlungsansatzes gefragt, um allen klinischen Notwendigkeiten gerecht zu werden. Schlafanstoßende Substanzen wie Mirtazapin als „Ersatz“ der sedativen Alkohol-Komponente bzw. als Behelf gegen Schlafstörungen im Rahmen des Entzugs haben dabei eine eigene Bedeutung, müssen jedoch mit Bedacht und in engem Kontakt mit dem Patienten angewandt werden.
Im vorliegenden Fall gefährdeten die depressiven Symptome eine Abstinenz derart, dass eine stufenweise eskalierte medikamentöse Intervention notwendig wurde. Letztlich konnte die Abstinenz jedoch vorwiegend gesichert werden, indem der Patient ernst genommen und eine niederschwellige stationäre Aufnahme ermöglicht wurde, nachdem – zumindest in seinem Erleben – die Medikation selbst die Abstinenz gefährdete.
Interessenkonflikterklärung
DR, MS, TG, MH, SB, DD, RG: Keine Interessenkonflikte
ST: Vortragshonorare Janssen-Cilag GmbH, Otsuka/Lundbeck und Servier, Advisory Board Otsuka
Literatur
1. Altintoprak AE, Zorlu N, Coskunol H, Akdeniz F, et al. Effectiveness and tolerability of mirtazapine and amitriptyline in alcoholic patients with co-morbid depressive disorder: a randomized, double-blind study. Hum Psychopharmacol 2008;23:313–9.
2. Benkert O, Hippius H (Hrsg.). Kompendium der Psychiatrischen Pharmakotherapie. 11., vollständig überarbeitete und aktualisierte Auflage. Berlin, Heidelberg: Springer-Verlag, 2017.
3. Bridge JA, Iyengar S, Salary CB, et al. Clinical response and risk for reported suicidal ideation and suicide attempts in pediatric antidepressant treatment: a meta-analysis of randomized controlled trials. JAMA 2007;297:1683–96.
4. Brunette MF, Akerman SC, Dawson R, O’Keefe CD, Green AI. An open-label pilot study of quetiapine plus mirtazapine for heavy drinkers with alcohol use disorder. Alcohol 2016;53:45–50.
5. Cornelius JR, Chung T, Douaihy AB, et al. Mirtazapine in comorbid major depression and an alcohol use disorder: A double-blind placebo-controlled pilot trial. Psychiatry Res 2016;242:326–30.
6. Cornelius JR, Chung TA, Douaihy AB, Kirisci L, et al. (2016): A Review of the literature of mirtazapine in co-occurring depression and an alcohol use disorder. J Addict Behav Ther Rehabil 2016;5:159.
7. Graves SM, Rafeyan R, Watts J, Napier TC. Mirtazapine, and mirtazapine-like compounds as possible pharmacotherapy for substance abuse disorders: evidence from the bench and the bedside. Pharmacol Ther 2012;136:343–53.
8. Grohmann R, Engel RR, Rüther E, Hippius H. The AMSP drug safety program: methods and global results. Pharmacopsychiatry 2004;37(Suppl 1):S4–11.
9. Thomas S, Bacon AK, Sinha R, Uhart M, et al. Clinical laboratory stressors used to study alcohol-stress relationships. Alcohol Res 2012;34:459–67.
10. Tiffany ST, Carter BL. Is craving the source of compulsive drug use? J Psychopharmacol 1998;12:23–30.
11. Tiffany ST. Cognitive concepts of craving. Alcohol Res Health 1999;23:215–24.
12. Umhau JC, Schwandt ML, Usala J, Geyer C, et al. Pharmacologically induced alcohol craving in treatment seeking alcoholics correlates with alcoholism severity, but is insensitive to acamprosate. Neuropsychopharmacology 2011;36:1178–86.
13. Yoon S-J, Pae C-U, Kim D-J, et al. Mirtazapine for patients with alcohol dependence and comorbid depressive disorders: a multicentre, open label study. Prog Neuropsychopharmacol Biol Psychiatry 2006;30:1196–201.
Daniel Reker, Dr. med. Michael Schneider, Dr. rer. nat. Timo Greiner, Prof. Dr. Martin Heinze, Hochschulklinik für Psychiatrie und Psychotherapie, Immanuel Klinik Rüdersdorf, Seebad 82/83, 15562 Rüdersdorf bei Berlin, Medizinische Hochschule Brandenburg Theodor Fontane, Fehrbelliner Straße 38, 16816 Neuruppin, E-Mail: D.Reker@immanuel.de
Prof. Dr. Detlef Degner, Klinik für Psychiatrie und Psychotherapie der Universitätsmedizin Göttingen, Von-Siebold-Straße 5. 37075 Göttingen
Dr. Sermin Toto, Prof. Dr. med. Stefan Bleich, Medizinische Hochschule Hannover, Klinik für Psychiatrie, Sozialpsychiatrie und Psychotherapie, Carl-Neuberg-Straße 1, 30625 Hannover
Dr. Renate Grohmann, Klinik für Psychiatrie und Psychotherapie, Ludwig-Maximilians-Universität, Nussbaumstraße 7, 80336 München
Craving associated with mirtazapine
Craving is described as the urgent desire for alcohol or psychotropic drugs by patients who suffer from addiction. For people with psychiatric co-morbidities it could also be a possible and presumably rare adverse drug reaction (ADR). Here we present a case in which the introduction of mirtazapine was repeatedly associated with the occurrence of craving in a patient with alcohol dependence and depression. Interestingly, there is some evidence that mirtazapine has the opposite effect, i. e., it reduces craving.
The presented case has been documented by the drug safety program in psychiatry (AMSP) and it has been evaluated in national conferences. Since 1993 AMSP systematically monitors the occurrence of severe, new and unusual ADRs of psychopharmaceuticals in the treatment of inpatients.
Key words: mirtazapine, antidepressant, alcohol dependence, craving, depression, comorbidity, AMSP
Psychopharmakotherapie 2019; 26(03):156-160
