Karin Thume, Christoph Kindler, Julia Reiff, Dieter F. Braus, Wiesbaden, Renate Grohmann, München, Detlef Degner, Göttingen, und Sermin Toto, Hannover
Der folgende Fallbericht illustriert das Auftreten eines serotonergen Syndroms unter der Kombination von Duloxetin mit Tramadol, einen inadäquaten Spiegelverlauf von Duloxetin sowie die kritische Bewertung eines ausschließlich spiegelkontrollierten Medikamentenmonitorings.
Fallbericht
Die Aufnahme der 55-jährigen Patientin erfolgte wegen einer schweren depressiven Episode mit drängenden Suizidgedanken und Schlafstörungen. Depressive Phasen bestanden seit etwa zehn Jahren und wurden zuletzt vor fünf Jahren mit Doxepin in unklarer Dosierung behandelt; dies wurde von der Patientin bei Gewichtszunahme abgesetzt.
Als Begleiterkrankungen lagen seit Längerem ein chronisches Schmerzsyndrom im Sinne einer Fibromyalgie, eine arterielle Hypertonie, eine Hyperurikämie sowie eine Hyperlipoproteinämie vor, die mit Tramadol 75 mg/Tag, Bisoprolol 10 mg/Tag, Hydrochlorothiazid 12,5 mg/Tag sowie Atorvastatin 40 mg/Tag behandelt wurden. In der Vorgeschichte war kein schädlicher Gebrauch von Alkohol, Drogen oder Nikotin bekannt.
Die Patientin wies einen guten Allgemein- und Ernährungszustand auf (163 cm, 76 kg), zeigte eine auffallend eingeschränkte Konzentrationsfähigkeit, einen formal eingeengten Gedankengang, deutlich depressive Stimmung mit aufgehobener affektiver Schwingungsfähigkeit und Eigengefährdung bei Suizidalität. Es wurde eine diffuse Schmerzsymptomatik mit Triggerpunkten angegeben, eine sichtbare Einschränkung des Bewegungsapparats oder fokalneurologische Defizite lagen nicht vor, der Blutdruck lag im Normbereich (120/80 mmHg).
Bei vorbestehender Fibromyalgie wurde leitliniengerecht eine antidepressive Therapie mit dem selektiven Serotonin- und Noradrenalin-Wiederaufnahmehemmer (SSNRI) Duloxetin bis 90 mg/Tag eingeleitet. Schlafanstoßend wurde zusätzlich zu Beginn Mirtazapin 7,5 mg/Tag, im Verlauf probatorisch Agomelatin 25 mg/Tag und zuletzt Pipamperon 20 mg/Tag gegeben. Bei Unruhe erhielt die Patientin bis 100 mg Quetiapin fraktioniert pro Tag. Die analgetische Vormedikation mit Tramadol 75 mg/Tag wurde bei langjähriger Einnahme zunächst beibehalten. Die antihypertensive Therapie konnte bei anfänglich hypotonen Werten auf 2,5 mg Bisoprolol/Tag und Atorvastatin leitliniengerecht auf 20 mg/Tag reduziert werden.
Die ergänzend durchgeführten Untersuchungen (cMRT, Routinelabor, EKG) waren unauffällig, insbesondere lagen keine Zeichen einer Mikroangiopathie im cMRT vor. In der neuropsychologischen Untersuchung zeigten sich mit der klinischen Diagnose vereinbare kognitive Defizite.
Der klinische Verlauf gestaltete sich zunächst im Rahmen der schrittweisen Dosiserhöhung des Duloxetins bis 90 mg/Tag positiv mit Besserung der depressiven Symptomatik. In Folge traten jedoch eine zunehmende psychomotorische Unruhe, hypomanische Symptome, beschleunigter Gedankengang, teilweise Enthemmung, tachykarde Herzfrequenz sowie vermehrtes Schwitzen im Sinne eines serotonergen Syndroms auf.
Die kurzfristige Kontrolle des Duloxetin-Spiegels (jeweils Talspiegel) ergab deutlich erhöhte Werte (148 µg/l, therapeutisch 20–80 µg/l), sodass eine unmittelbare Dosisreduktion auf 60 mg Duloxetin/Tag vorgenommen wurde. Bei Kontrolle des Spiegels drei Tage später unter 60 mg Duloxetin/Tag ergab sich ein Wert von 163 µg/l (Eliminationshalbwertszeit von 8–17 Stunden; Mittelwert 12 Stunden [6]).
Nach erneuter Analyse der Medikation bei bekannter serotonerger Interaktion zwischen Tramadol und Duloxetin [2, 4, 12, 20] wurde Duloxetin pausiert und Tramadol abgesetzt. Die klinische Symptomatik sistierte nach dieser Maßnahme zeitnah. Eine Woche nach Absetzen der Medikation lag der Duloxetin-Spiegel bei 10 µg/l.
Angesichts der deutlichen Besserung der depressiven Symptomatik bei der erstmaligen Gabe wurde in Folge Duloxetin mit 30 mg/Tag wieder eindosiert und es konnte ein adäquater Duloxetin-Spiegel (28 µg/l) nach etwa zehn Tagen Therapie nachgewiesen werden (Abb. 1). Unterstützend wurde bei chronischem Schmerzsyndrom erfolgreich Pregabalin 100 mg/Tag verabreicht.
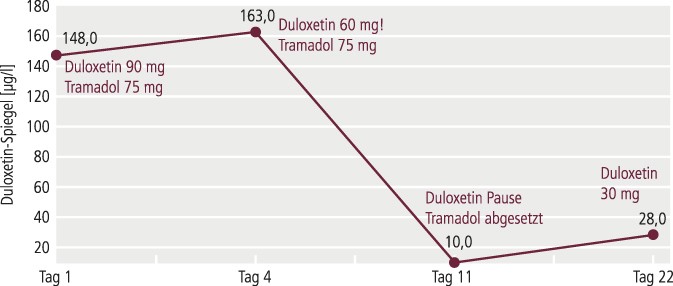
Abb. 1. Duloxetin-Spiegelverlauf
Angesichts des ungewöhnlichen Verlaufs des Duloxetin-Spiegels und der beabsichtigten Reexposition wurde ergänzend eine Genotypisierung bezüglich eines Cytochrom-P45-(CYP-)2D6-Polymorphismus durchgeführt, die einen normalen Metabolisierungsstatus entsprechend einem CYP2D6-Extensive-Metabolizer-Status ergab [11, 13, 14].
Diskussion
Bei der Behandlung von chronischen Schmerzpatienten mit depressiver Störung ist die Kombination aus dualen Antidepressiva und Opioiden häufig geübte Praxis. Dabei ist bekannt, dass die Kombination von Tramadol mit SSNRI, wie Duloxetin, insbesondere bei CYP2D6-Gering-Metabolisierern, älteren Patienten und höheren Dosierungen die Gefahr eines serotonergen Syndroms birgt. Hierzu liegen bereits Daten und Fallberichte vor [1, 3, 5, 8, 12, 16, 19, 20, 21, 23].
Im vorliegenden Fall ist von einem serotonergen Syndrom unter Komedikation von Duloxetin und Tramadol bei einer Patientin im mittlerem Lebensalter und üblichen Medikamentendosierungen [6, 7] auszugehen. Das Vollbild eines Serotoninsyndroms [2, 15, 17, 24] lag hier noch nicht vor, jedoch wies die Symptomkonstellation auf serotonerge unerwünschte Effekte im Sinn eines „serotonergen Syndroms“ hin. Dabei fand sich eine ungewöhnliche Spiegelerhöhung des Duloxetins bei normalem Genotyp entsprechend einem Extensive-Metabolizer-Status [11, 13, 14] bezüglich CYP2D6, das allerdings nicht den Hauptweg der Metabolisierung von Duloxetin darstellt; die Metabolisierung von Duloxetin geschieht hauptsächlich über CYP1A2 [6, 18]. Duloxetin hemmt die CYP2D6-aktivitätsabhängige Metabolisierung von Tramadol zum aktiven (analgetisch wirksamen) Hauptmetaboliten O-Desmethyltramadol, was möglicherweise die analgetische Wirkung etwas einschränken kann, die proserotonerge Wirkung aber nicht. Es besteht ein erhöhtes Risiko für Serotonintoxizität aufgrund additiver Verstärkung der Serotonin- und Noradrenalin-Wiederaufnahme. Bei gleichzeitiger Anwendung beider Substanzen wird ein periodisches Screening nach Zeichen der serotonergen Überstimulation (z.B. Hyperreflexie/Klonus, Agitation, Schwitzen, Fieber) empfohlen [18]. Eine kinetische Interaktion mit Spiegelerhöhung von Duloxetin durch Tramadol ist bisher nicht bekannt [18].
Deshalb wurde dieser Fall im Rahmen des AMSP-Projekts vorgestellt, diskutiert und als wahrscheinliche UAW gewertet. Die Schilderung des Ablaufs zeigt, dass die ausschließlich spiegelüberwachte Therapieadaptation unzureichend ist, da die reaktive Dosisreduktion des Duloxetins bei nachgewiesener Spiegelerhöhung angesichts des additiven Effekts von Tramadol das Gesamtproblem nicht lösen konnte [11].
Inwieweit das Kontrollintervall von nur drei Tagen, das eine weitere Spiegelzunahme trotz Dosisreduktion zeigte, im Hinblick auf die Eliminationszeit von durchschnittlich 12 Stunden zu kurz gewählt war, ist sicherlich zu diskutieren. Dennoch blieb der Serumspiegel in Bezug auf die verabreichte Dosis von 60 mg/Tag unerwartet hoch.
Im Bereich des CYP2D6-Systems und der bekannten Inhibitorfunktion des Duloxetins ist eine Wechselwirkung der beiden Substanzen mit potenzieller Wirkabschwächung des Tramadols vorbeschrieben und wird daher neben dem Risiko eines serotonergen Syndroms schmerztherapeutisch kritisch bewertet [9, 21]. Als Alternative zu Tramadol würde sich unter Berücksichtigung der analgetischen Potenz Hydromorphon anbieten, das nicht über das Cytochrom-System metabolisiert wird und auch nur eine geringe renale Elimination aufweist [10].
Eine mögliche prolongierte Halbwertszeit bei Verabreichung dieser Kombination von renal zu eliminierenden serotonerg wirkenden Medikamenten, die bei Drugs.com [1, 4] beschrieben ist, könnte zum einen den Spiegelverlauf des Duloxetins als auch die fehlende Schmerzzunahme bei potenzieller Wirkabschwächung des mit 75 mg niedrig dosierten Tramadols erklären. Die laborchemischen Kontrollen der Nierenfunktion lagen bei der Patientin allerdings unverändert im Normbereich. Abschließend bleibt der Duloxetin-Spiegelverlauf unzureichend geklärt.
Vor allem aber mahnt dieser Fall erneut zu besonderer Vorsicht bei der Kombination von Duloxetin mit Tramadol, das ohnehin eher kein geeignetes Analgetikum in der Polymedikation darstellt [22], aufgrund des pharmakodynamisch additiven serotonergen Effekts mit hier resultierendem serotonergen Syndrom.
Interessenkonflikterklärung
K. Thume, C. Kindler, J. Reiff : keine Interessenkonflikte
D. F. Braus : kein Interessenskonflikt im Zusammenhang mit dem geschilderten Fall. In den letzten zwei Jahren neurowissenschaftliche Vorträge für Lilly, Janssen-Cilag, Lundbeck, Pfizer, Servier, Novartis, Allalgan, Shire und TAD Pharma.
R. Grohmann: keine Interessenkonflikte
S. Toto: kein Interessenskonflikt im Zusammenhang mit dem geschilderten Fall. In den letzten zwei Jahren neurowissenschaftliche Vorträge/Workshops für Janssen-Cilag, Lundbeck, Otsuka, Servier.
D. Degner: keine Interessenkonflikte
Literatur
1. Barann M, Stamer UM, Lyutenska M, et al. Effects of opioids on human serotonin transporters. Naunyn-Schmiedeberg’s Arch Pharmacol 2015;388:43–9.
2. Boyer EW, Shannon M. The serotonin syndrome. N Engl J Med 2005;352:1112–20.
3. Chan BSH, Graudins A, Whyte IM, Dawson AH, et al. Serotonin syndrome resulting from drug interactions. Med J Aust 1998;169:523–5.
4. drugs.com/_interactions checker / Duloxetine Tramadol
5. Enggaard TP. The analgesic effect of tramadol after intravenous injection in healthy volunteers in relation to CYP2D6. Anesth Analg 2006;102:146–50.
6. Fachinformation Cymbalta, Firma Lilly GmbH.
7. Fachinformation Tramal, Firma Grünenthal GmbH.
8. Gnanadesigan N. Interaction of serotonergic antidepressants and opioid analgesics: Is serotonin syndrome going undetected. J Am Med Dir Assoc 2005;6:265–9.
9. Haefeli WE. Forum Schmerz, Wechselwirkung in der Schmerztherapie mit Opioiden. Bulletin 2011.
10. Herdt R. Hydromorphon hat geringes Interaktionspotenzial. Dtsch Apo Ztg 2006;43:60.
11. Hiemke C, et al. AGNP consensus guidelines for therapeutic drug monitoring in psychiatry: update 2011. Pharmacopsychiaty 2011;44:195–235.
12. Houlihan DJ. Serotonin syndrome resulting from coadministration of tramadol, venlafaxine, and mirtazapine. Ann Pharmacother 2004;38:411–3.
13. Ingelmann-Sundberg M. Genetic polymorphisms of cytochrome P4502D6 (CYP2D6): clinical consequences, evolutionary aspects and functional diversity. Pharmacogenomics J 2005;5:6–13.
14. Kirchheiner J, Nickchen K, Bauer M, Wong ML, et al. Pharmacogenetics of antidepressants and antipsychotics: the contribution of allelic variations to the phenotype of drug response. Mol Psychiatry 2004;9:442–73.
15. Kitson R, Carr B. Tramadol and severe serotonin syndrome. Anaesthesia 2005;60:934–5.
16. Köberle U, Bschor T. Dysarthrie als serotonerge Nebenwirkung durch Interaktion zwischen Duloxetin und Tramadol. Psychopharmakotherapie 2007;14:82–4.
17. Martin TG. Serotonin syndrome. Ann Emerg Med 1996;28:520–6.
18. mediq.ch / Medikationscheck Duloxetin/Tramadol
19. Overholser BR. Opioid pharmacokinetic drug-drug-interactions. Am J Manag Care 2011;17(Suppl 11):S276–87.
20. Park SH. Serotonin syndrome: is it a reason to avoid the use of tramadol with antidepressants? J Pharm Pract 2014;27:71–8.
21. Petri H. Das Interaktionspotenzial niederpotenter Opioide. Krankenhauspharmazie 2014;35:161–3.
22. Petri H, Grandt D. Interaktionen der Opioidanalgetika auf Ebene der Biotransformation. Schmerz 2016;30:519–25.
23. Poulsen L. The hypoalgesic effect of tramadol in relation to CYP2D6. Clin Pharmacol Ther 1996;60:636–44.
24. Sternbach H. The serotonin syndrome. Am J Psychiatry 1991;148:705–13.
Karin Thume, FÄ für Innere Medizin, Klinik für Psychiatrie und Psychotherapie, Helios Dr. Horst Schmidt Kliniken, Ludwig-Erhard-Straße 100, 65199 Wiesbaden, E-Mail: karin.thume@helios-kliniken.de
Dr.med. Christoph Kindler, Dr.med. Julia Reiff, Prof. Dr.med. Dieter F. Braus, Klinik für Psychiatrie und Psychotherapie, Helios Dr. Horst Schmidt Kliniken, Ludwig-Erhard-Straße 100, 65199 Wiesbaden
Dr.med. Renate Grohmann, Psychiatrische Klinik der LMU, Nussbaumstraße 7, 80336 München
Priv.-Doz. Dr. med. Detlef Degner, Psychiatrische Klinik der Universität, von-Siebold-Straße 5, 37075 Göttingen
Dr.med. Sermin Toto, Medizinische Hochschule Hannover, Klinik für Psychiatrie, Sozialpsychiatrie und Psychotherapie, Carl-Neuberg-Straße 1, 30625 Hannover
Serotonin syndrome under treatment with duloxetine and tramadol and unexpected high drug level of duloxetine
A 55-year-old female patient developed a serotonin syndrome with tachycardia, increased transpiration and psychomotor agitation during treatment with tramadol und duloxetine. We detected an increased serum concentration of duloxetine. Reduction of duloxetine dose showed no improvement of clinical symptoms or duloxetine blood levels. After stopping tramadol treatment and pausing duloxetine medication, symptoms of serotonin syndrome declined and duloxetine drug level dropped. Genotypical evidence for a CYP2D6 slow metabolizer could not be detected. Because the initial response to duloxetine was positive, we started a second treatment with duloxetine with adequate drug levels. The case was reported within the AMSP project (AMSP e.V.), analyzed and classified as a probable adverse drug reaction/interaction (ADR). Duloxetine is an inhibitor of cytochrome P450–2D6 and thus inhibits tramadol metabolism. In addition, a pharmacodynamic serotonergic interaction is known for this combination. The abnormal high drug level of duloxetine under simultaneous treatment with tramadol was discussed without a final conclusion.
Key words: duloxetine, tramadol, depression, chronic pain syndrome (fibromyalgia), serotonin syndrome, adverse drug reaction (ADR) and interaction, increased duloxetine concentration, AMSP project (AMSP e.V.)
Psychopharmakotherapie 2017; 24(04)
