Tillmann H.C. Krüger*, Stefanie Jung*, Hannover, und M. Axel Wollmer, Hamburg
Historischer Hintergrund von Botulinumtoxin
Botulinumtoxin ist ein neurotoxisches Protein, das vom Bakterium Clostridium botulinum synthetisiert und ausgeschieden wird [30]. Das Exotoxin Botulinumtoxin hemmt in der präsynaptischen Nervenendigung die Ausschüttung des Neurotransmitters Acetylcholin [18], verhindert damit die Signalübertragung von Nervenzellen an Muskelzellen und wirkt infolge der dadurch aussetzenden Muskelkontraktion paralysierend. Die physiologischen Auswirkungen dessen wurden erstmals im Jahr 1817 durch den Arzt Dr.Justinus Christian Kerner beschrieben [20]. Erst um 1868 erhielten die Vergiftungssymptome von den Medizinern Rupprecht und Müller den Namen „Botulismus“ [2]. Dieser leitet sich aus dem Lateinischen (botulus =Wurst) ab, da mit den Symptomen des Botulismus assoziierte Vergiftungen in der Vergangenheit häufig auf den Verzehr verdorbener Wurstwaren zurückzuführen waren [7]. Da Clostridium zum Auskeimen eine sauerstoffarme und nichtsaure Umgebung bevorzugt, stellten Wurstkonserven eine ideale Umgebung für das Bakterium dar. Die historischen Beschreibungen von Botulinumtoxin-Vergiftungsfällen deuten auf den Schrecken hin, den sie damals ausgelöst haben müssen: Bereits etwa 1793 kam es den Aufzeichnungen von Dickson zufolge zu einer auf den Verzehr ungekochter Blutwurst zurückzuführenden Epidemie in Süddeutschland, bei der über die Hälfte der Betroffenen an den Vergiftungssymptomen starben [6]. Knapp 100 Jahre später ist es bei einer Beerdigung in Belgien zu einer Massenvergiftung gekommen, nachdem die Trauergäste ungekochten Schinken gegessen hatten [38]. Die durch das hochpotente Toxin hervorgerufenen Symptome deuten auf die Potenz des Giftes hin: Etwa 12 bis 36 Stunden nach dem Verzehr betroffener Nahrung kommt es zunächst zu Erbrechen, Kopf- und Gliederschmerzen sowie zu Mundtrockenheit. Die anschließenden Lähmungserscheinungen betreffen erst die Augenmuskeln, dann die Rachen- und Mundmuskulatur und später die Darm- und Blasenmuskulatur. Dabei kommt es nach anfänglichen Seh-, Sprech- und Schluckbeschwerden zu Blasenentleerungsproblemen und Verstopfung [21]. Letztlich kann das Toxin durch Lähmung der Atem- oder Herzmuskulatur zum Tode führen, wenn nicht rechtzeitig eine intensivmedizinische Versorgung erfolgt.
Trotz der verheerenden Auswirkungen sah Dr. Kerner neben seiner massiven Toxizität für den Menschen schon sehr früh den potenziellen Nutzen des neu entdeckten Giftes und stellte Überlegungen zum therapeutischen Einsatz bei Muskeltonuserhöhungen an [27]. Bis zur gezielten Anwendbarkeit des Stoffes sind jedoch noch einmal etwa 150 Jahre vergangen.
Im Jahr 1897 konnte der Erreger des Botulismus vom Bakteriologen und Robert-Koch-Schüler Pierre Marie van Ermengen isoliert werden [39]. Weitere 23 Jahre später wurde das Botulinumtoxin vom Typ A erstmalig vom Mediziner Hermann Sommer in gereinigter Form gewonnen [15]. Durch die Hoffnung, das Botulinumtoxin als chemische Waffe einsetzen zu können, wurde die Forschung zu dem Giftstoff im zweiten Weltkrieg intensiviert und ausgedehnt. Erst 1959 lag das Botulinumtoxin in kristalliner Form vor. Die Herstellung von größeren Mengen des Toxins gelang allerdings trotz der verstärkten Forschungsbemühungen seit dem zweiten Weltkrieg erst später [31].
Klinischer Nutzen von Botulinumtoxin
Der erste gezielte Einsatz von Botulinumtoxin fand 1973 durch den Arzt Dr. Alan Scott statt, der Botulinumtoxin bei schielenden Affen einsetzte und damit die Behandlung von Strabismus testete [34]. Im Jahre 1978 erhielt er von der FDA (Food and Drug Administration) die Erlaubnis, seine Befunde am Menschen zu überprüfen. Die erste erfolgreiche Botulinumtoxin-Behandlung am Menschen [35] bahnte daraufhin den Weg für weitere Indikationen. Heute wird Botulinumtoxin A bei einer Reihe von Erkrankungen, die mit einem erhöhten Muskeltonus einhergehen, und neurologischen Störungsbildern eingesetzt. Dazu zählen neben dem Strabismus der hemifaziale Spasmus [4], der Blepharospasmus [14], Torticollis [24], Hyperhidrosis [32], Harninkontinenz [28] und chronische Migräne [23]. Aber auch zur Milderung einzelner Symptome im Rahmen neurologischer Erkrankungen (z.B. übermäßiger Speichelfluss; [12]) kommt Botulinumtoxin heutzutage zum Einsatz. Die bekannteste Indikation für Botulinumtoxin dürfte jedoch die in Deutschland seit 2006 zugelassene Behandlung von Falten in der Glabella-Region in der ästhetischen Medizin sein, welche auf Jean und Alastair Carruthers zurückgeht [3].
Aktuelle Befunde zur Wirksamkeit von Botulinumtoxin bei Depressionen
Vor knapp zehn Jahren wurde erstmals ein antidepressiver Effekt einer Botulinumtoxin-Therapie der Glabella-Region im Rahmen einer Fallserie von dem Dermatologen Eric Finzi beschrieben [9]. Wie auch bei der Entdeckung von Botulinumtoxin zur Anwendung gegen chronischen Kopfschmerz [16] entstammte die Beobachtung einem in der Dermatologie aufgetretenen und von Patienten berichteten Nebeneffekt. Mittlerweile konnten drei randomisiert-kontrollierte Studien und eine Metaanalyse der individuellen Patientendaten diesen Effekt bestätigen [8, 25, 26, 40]. Wollmer et al. konnten im Jahr 2012 in einer ersten randomisiert-kontrollierten Studie anhand von 30 Patienten zeigen, dass Botulinumtoxin bei teilweise chronifiziert und therapieresistent depressiven Patienten zu einer signifikanten Besserung der depressiven Symptome führt (Abb. 1) [40]. Finzi und Rosenthal konnten diesen Befund 2014 anhand einer größeren Fallzahl (n=74) replizieren [8]. Anders als bei Wollmer et al. (2012) war das Vorliegen einer ausgeprägten Glabella-Falte in dieser Studie kein Einschlusskriterium und der antidepressive Effekt zeigte sich unabhängig von der Ausprägung der Glabella-Falte. Ebenfalls im Jahr 2014 konnten Magid et al. mithilfe einer Crossover-Studie anhand von 30 Patienten weitere Nachweise für den Effekt von Botulinumtoxin bei Depressionen erbringen [25]. Dabei wurden die Patienten in zwei Gruppen aufgeteilt. Eine Gruppe erhielt zu Beginn der Studie ein Placebo und nach zwölf Wochen Botulinumtoxin, die andere Gruppe erhielt zu Beginn Botulinumtoxin und im zweiten Abschnitt ein Placebo. Mit diesem Studiendesign war eine Beobachtung des Verlaufs der Depression unter Botulinumtoxin über fast ein halbes Jahr möglich. In der von Anfang an mit Botulinumtoxin behandelten Gruppe betrug die Symptomreduktion (gemessen anhand des Beck-Depressions-Inventars [BDI]) nach sechs Wochen 42% und nahm bis Ende der 24. Woche auf 57% zu. Diese Werte verdeutlichen, dass der antidepressive Effekt der Behandlung die paralytische Wirkung des Botulinumtoxins überdauert.
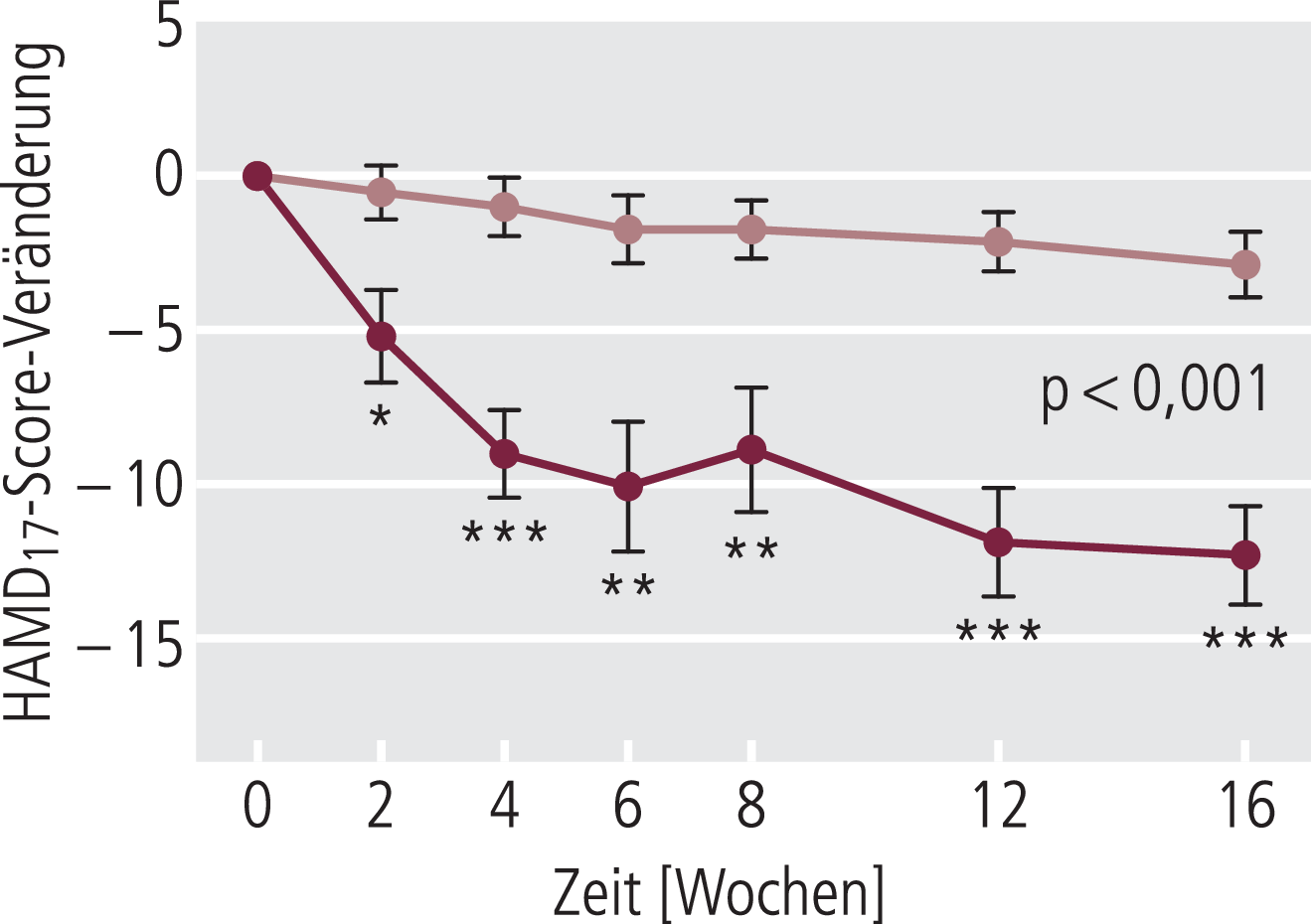
Abb. 1. Erster Nachweis unter randomisiert-kontrollierten Bedingungen einer antidepressiven Wirkung von Botulinumtoxin – Verlauf anhand der Hamilton-Depressionsskala (HAMD17) [nach 40]; *p ≤0,05; **p ≤ 0,01; ***p ≤0,001 vs.Placebo
Magid et al. (2015) analysierten die gebündelten Datensätze (n=134) der drei randomisiert-kontrollierten Studien [26]. Zum gemeinsamen primären Endpunkt nach sechs Wochen zeigte sich unter Botulinumtoxin – anhand einer Fremdbeurteilung mithilfe der Hamilton-Depressionsskala (HAMD) und der Montgomery-Åsberg Depression Rating Scale (MADRS) – eine Reduktion der depressiven Symptomatik um 45,7% gegenüber 14,6% unter Placebo. Ein ähnliches Bild ergab sich in der Selbsteinschätzung der Patienten anhand des BDI. Patienten, die Botulinumtoxin erhalten hatten, gaben eine Besserung der depressiven Symptome von durchschnittlich 47,4% an, während die empfundene Besserung nach Kochsalz-Injektion lediglich bei 16,2% lag. Insgesamt sprachen 54,2% auf die Botulinumtoxin-Therapie an und 30,5% zeigten eine vollständige Remission (vs. 10,7% Response und 6,7% Remission in der Placebo-Bedingung). Das Ansprechen war unabhängig davon, ob die Patienten Botulinumtoxin als Monotherapie oder adjunktiv zu einer konstanten Medikation mit einem Antidepressivum erhalten hatten. Zudem befanden sich unter den Probanden großenteils chronisch und teilweise therapieresistent depressive Patienten.
„Facial Feedback“ als Wirkungsmechanismus
Die aktuelle Datenlage zeigt, dass Botulinumtoxin das Potenzial hat, sich zu einer weiteren Therapieoption in der Behandlung der Depressionen zu entwickeln (Tab.1).
Tab. 1. Studien zur Anwendung von Botulinumtoxin (BT) in der Depressionsbehandlung
|
Jahra |
Studieb |
Autoren |
Patienten |
Interventionc |
Ziel-Parameter |
|
2006 |
Finzi & Wasserman |
N=10 weiblich |
29 E Onabotulinumtoxin A; Glabella |
Erste Studie, welche gezeigt hat, dass BTA depressive Symptome verbessern kann. Response wurde von 90%, Remission von 80% aller Patienten erreicht |
|
|
2012 |
RCT NCT00934687 |
Wollmer et al. |
N=30 |
29/40 E Onabotulinumtoxin A oder Kochsalzlösung (Placebo); Glabella |
Erste randomisiert-kontrollierte Studie, die eine signifikante Verbesserung der Depression (47,1%) und höhere partielle Response- und Responseraten nach adjunktiver BTA-Injektion (86,7%, 60%, resp.) verglichen mit Placebo (26,7%, 13,3%, resp.) zeigte |
|
2013 |
RCT NCT01556971 |
Finzi & Rosenthal |
N=74 |
29/40 E Onabotulinumtoxin A oder Kochsalzlösung (Placebo); Glabella |
Signifikante Verbesserung der Depression (47%), höhere Response- und ebenfalls höhere Remissionsraten nach einer alleinigen oder adjunktiven BTA-Injektion (52%, 27%, resp.) verglichen mit Placebo (15%, 7%, resp.) |
|
2013 |
NCT01004042 |
Hexsel et al. |
N=25 |
20–40 E Onabotulinumtoxin A |
Verbesserung der depressiven Symptome (54,38%) nach Injektion von BTA |
|
2014 |
RCT NCT01392963 |
Magid et al. |
N=30 |
29/40 E Onabotulinumtoxin A oder Kochsalzlösung (Placebo); Glabella |
Signifikante Verbesserung der Depression (42%), höhere Response- und ebenfalls höhere Remissionsraten nach BTA-Injektion (45%, 27%, resp.) verglichen mit Placebo (5%, 5%, resp.), welche über den Effekt muskulärer Paralyse und kosmetischer Veränderung hinaus anhielt |
|
2015 |
Boudreau et al. |
N=32 |
155 E Onabotulinumtoxin A; Kopf und Nacken |
Verbesserung der mit chronischer Migräne assoziierten depressiven Symptome (ca. 45%) |
|
|
k. A. |
RCT NCT02116361 |
Allergan |
N=248 |
Zwei verschiedene Dosierungen Onabotulinumtoxin A oder Kochsalzlösung (Placebo) |
k. A. |
a Jahr der ersten Online- oder Print-Veröffentlichung; b Nummer im Studienregister ClinicalTrials.gov; c mit „/“ getrennte Dosierungen gelten jeweils für Frauen bzw.Männer; RCT: randomisiert-kontrollierte Studie
Doch wie erklärt sich die antidepressive Wirkung von Botulinumtoxin? Die beschriebenen Studien stützen sich alle auf die sogenannte „Facial-Feedback-Hypothese“. Diese beschreibt den Zusammenhang zwischen mimischem Emotionsausdruck und emotionalem Empfinden. Der Evolutionsbiologe Charles Darwin (1809–1882) und der Psychologe William James (1842–1910) beschrieben im 19. Jahrhundert erstmals diesen Mechanismus. In seinem Werk „Der Ausdruck der Gemütsbewegungen bei dem Menschen und den Tieren“ schreibt Darwin 1872: „Der freie Ausdruck […] einer Emotion intensiviert sie. Auf der anderen Seite schwächt die Unterdrückung aller äußeren Anzeichen unsere Emotionen ab. Wer seiner Wut durch heftige Gebärden nachgibt, wird sie vergrößern; wer die äußeren Anzeichen der Furcht nicht kontrolliert, wird intensivere Furcht empfinden; und wer in Passivität verharrt, wenn er von Kummer überwältigt wird, verliert die beste Chance, die Elastizität des Geistes wiederzuerlangen“ [5]. 1890 wiederum erkannte James in seinem Werk „Die Prinzipien der Psychologie“ ebenfalls, dass die Unterdrückung einer emotionalen Regung zu ihrer Abflachung führt: „Refuse to express a passion, and it dies“ [13]. Diese Beobachtungen wurden 1988 vom deutschen Sozialpsychologen Fritz Strack und seinen Kollegen in einer Studie getestet [37]. Dabei sollten die Probanden einen Stift mit dem Mund festhalten und dabei Comics hinsichtlich ihrer Lustigkeit bewerten. Ein Teil der Probanden erhielt die Instruktion, den Stift mit den Lippen fest zu umschließen. Dadurch wurden die für das Lächeln zuständigen Muskeln gehemmt. Der andere Teil der Probanden wurde angewiesen, den Stift mit den Zähnen zu halten und Kontakt der Lippen mit dem Stift zu vermeiden. Dadurch wurden die für das Lächeln zuständigen Muskeln automatisch kontrahiert. Entsprechend der Facial-Feedback-Hypothese fanden die Forscher heraus, dass die Probanden die Comics unter der zweiten Bedingung als lustiger bewerteten. Auch für negative Emotionen konnte dieser Effekt vom Psychologen Randall Larsen und seinen Kollegen 1992 experimentell bestätigt werden [22]. Ziel der Untersuchung war es, die Probanden zum Zusammenziehen der Augenbrauen zu bewegen, ohne dass diese speziell zu diesem Zweck instruiert werden mussten. Dazu wurden den Probanden in der Augenbrauen-Region zwei Golf-Tees angebracht. Die Probanden wurden gebeten, die Spitzen der beiden Golf-Tees zusammenzuführen. Dieses Zusammenführen konnte nur erreicht werden, indem wie beim Stirnrunzeln die Augenbrauen zusammengezogen wurden. Die für das Runzeln verantwortlichen Muskeln stehen in Verbindung mit negativen Emotionen. Gemäß der Facial-Feedback-Hypothese bewerteten die Probanden ihnen präsentiertes aversives Bildmaterial negativer, wenn die beiden Golf-Tees zusammengeführt wurden und dadurch ein Stirnrunzeln erzwungen wurde (Abb. 2).
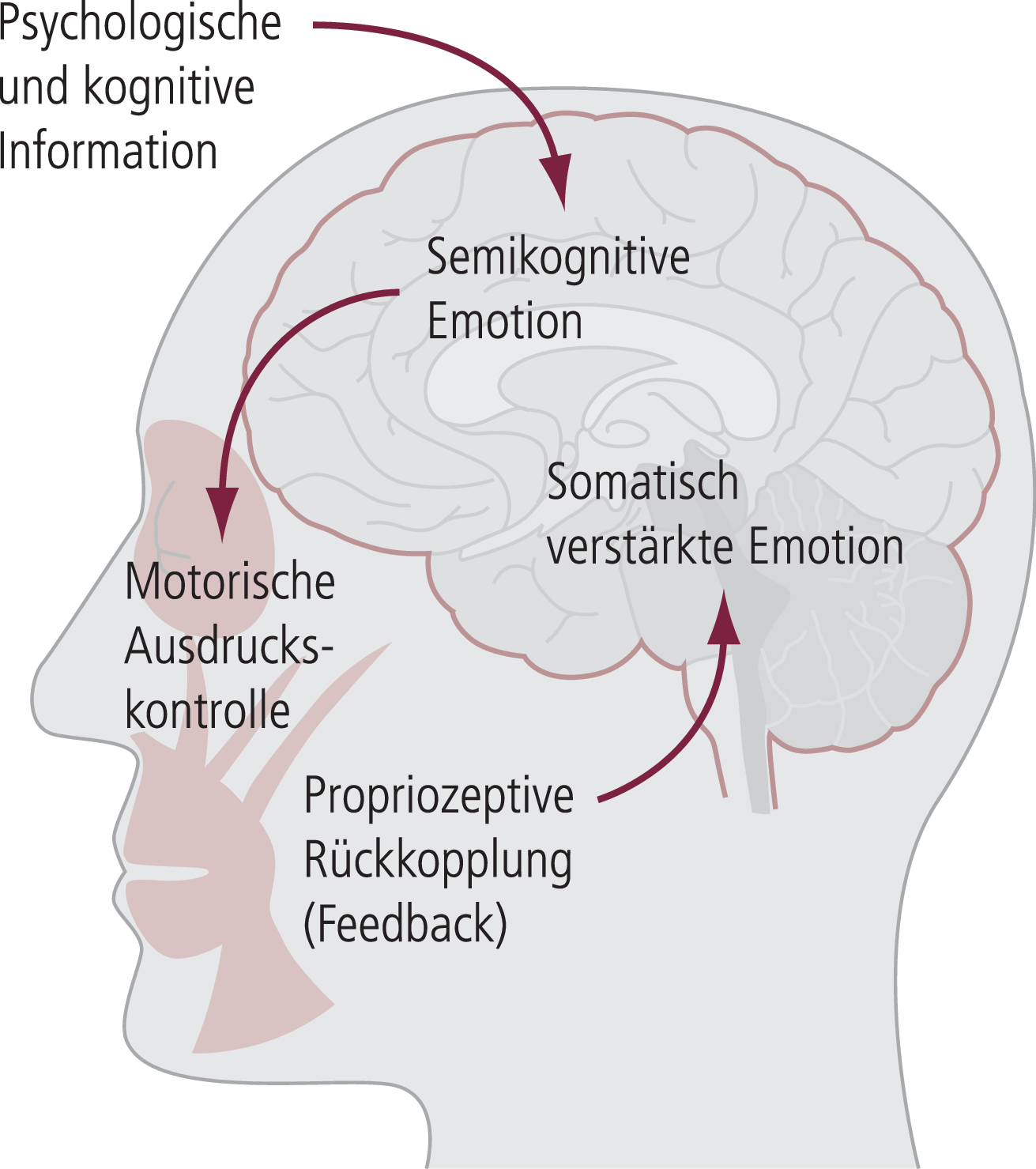
Abb. 2. Verbindung von Emotionsempfinden und -ausdruck
Die Aktivierung der Gesichtsmuskulatur trägt offenbar über propriozeptive Afferenzen zur Aufrechterhaltung und Verstärkung der durch sie ausgedrückten Emotionen bei. Für die häufig bei Patienten mit agitiert-depressiven Zustandsbildern sichtbare Faltenkonfiguration in der Glabella-Region prägte Heinrich Schüle den Ausdruck „omega melancholicum“ (Abb. 3). Es ist gut vorstellbar, dass der Ausdruck der Depression zu ihrer Aufrechterhaltung beiträgt und dass die Behandlung mit Botulinumtoxin diesen Kreislauf durch die Lähmung der am negativen Emotionsausdruck beteiligten Gesichtsmuskeln (Musculi corrugatores supercilii und Musculus procerus in der Glabella-Region; [33]) unterbrechen und somit antidepressiv wirken kann.
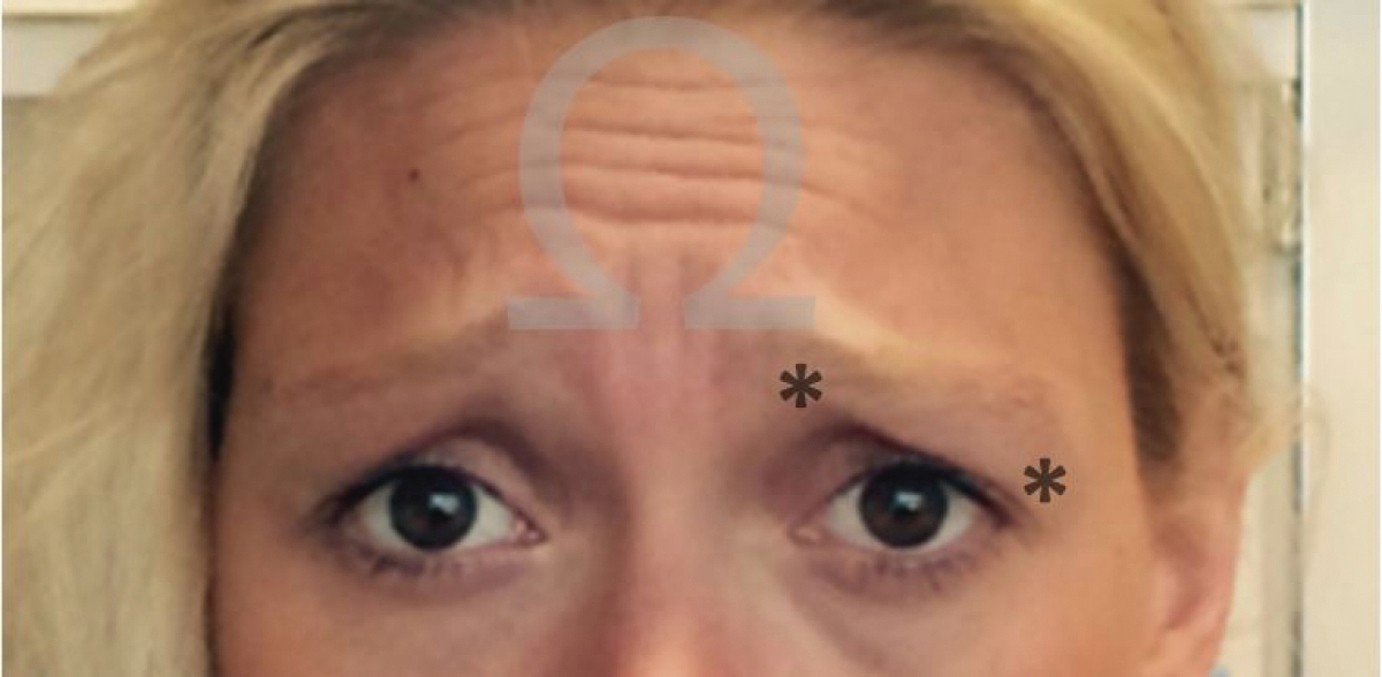
Abb. 3. Omega melancholicum und Veraguth-Falte (*) [Foto: S. Jung]
Praxisaspekte
Während viele Antidepressiva für die Patienten unangenehme Nebenwirkungen haben (z.B. Benommenheit [19], Gewichtszunahme [29] oder Libido-Verlust [10]), sind die Nebenwirkungen der Botulinumtoxin-Behandlung gering [11]. Bei der zur Behandlung der Depression eingesetzten Anwendung in der Glabella-Region können vorübergehend Kopfschmerz sowie leichte Schwellungen, Hämatome oder Rötungen in der behandelten Region oder Schmerzen in der Einstichstelle auftreten [36]. Komplikationen, wie etwa eine Ptose, können durch die richtige Injektionstechnik in der Regel vermieden werden und sind mit abklingender Wirkung des Toxins reversibel [1]. Ein positiver Aspekt von Botulinumtoxin ist die relativ lang anhaltende Wirkung (3 bis 6 Monate) einer einzigen Behandlung. Dadurch können, ähnlich wie bei einer Depot-Behandlung, Adhärenzprobleme vermieden werden. Wiederholte Applikationen von Botulinumtoxin im Sinne einer Erhaltungstherapie oder Rezidivprophylaxe sind noch nicht Gegenstand von randomisiert-kontrollierten Studien gewesen. Klinische Erfahrungen der Autoren sprechen jedoch für eine Wirksamkeit auch über längere Zeiträume und bei wiederholter Anwendung. Die Tagesbehandlungskosten der Behandlung entsprechen etwa denen für die Behandlung mit einem modernen Antidepressivum.
Nicht alle Patienten sprechen auf eine Behandlung mit Botulinumtoxin an. Mit motorischer Unruhe (Agitation) ist bereits ein möglicher Prädiktor für den Behandlungserfolg beschrieben worden [41]. Es ist denkbar, dass mithilfe geeigneter Instrumente [17] Patientengruppen identifiziert werden können, die im Sinne einer stratifizierten Medizin besonders gut von der Botulinumtoxin-Therapie profitieren können.
Obwohl die Befundlage zur Anwendung von Botulinumtoxin in der Behandlung der Depression ermutigend ist, bedarf sie einer weiteren Verbreiterung und Bestätigung. Eine Herausforderung ist dabei die Optimierung der Kontrollbedingungen, da der offensichtliche kosmetische Effekt von Botulinumtoxin im Rahmen randomisiert-kontrollierter Studien eine Verblindung der Patienten nur eingeschränkt möglich macht.
Ausblick
Botulinumtoxin hat in den vergangenen knapp 200 Jahren in der Medizin eine beachtliche Entwicklung genommen. Zunächst gefürchtet als Auslöser mitunter tödlich verlaufender Vergiftungen, hat es aufgrund seiner paralysierenden Eigenschaften in der Behandlung von Erkrankungen, die mit einem erhöhten Muskeltonus einhergehen, einen festen Platz eingenommen. Vergleichbar mit vielen heute in der Medizin angewandten Wirkstoffen (z.B. das 1928 durch den schottischen Bakteriologen Alexander Fleming entdeckte Penicillin) geht die Entdeckung seines Nutzens auf glückliche Zufälle und aufmerksame Forscher zurück. Trotz seiner enormen toxischen Potenz kann das Nervengift heute in der Medizin segensreich angewandt werden. Schon sehr früh bemerkte schließlich der Schweizer Arzt Paracelsus (1493–1541): „Alle Dinge sind Gift, und nichts ist ohne Gift; allein die Dosis machts, dass ein Ding kein Gift sei.“ Vor allem für den Bereich psychiatrischer Krankheitsbilder und assoziierter Grundlagenforschung sehen wir für Botulinumtoxin ein großes Entwicklungs- und Forschungspotenzial für die kommenden Jahre.
Interessenkonflikterklärung
THCK hat Honorare für Beratung oder Teilnahme am Advisory Board von Allergan und Lundbeck sowie für Vorträge, Stellungnahmen oder Artikel von Allergan, Lundbeck, Otsuka, Schwabe, Servier und Trommsdorf erhalten.
Für SJ bestehen keine Interessenkonflikte.
MAW hat Honorare für Beratung oder Teilnahme am Advisory Board von Allergan sowie für Vorträge, Stellungnahmen oder Artikel von Ipsen, Merz, Lilly und Novartis erhalten. Drittmittel erhält er von der Asklepios Hamburg GmbH.
Literatur
1. Alderson K, Holds J, Alderson R. Botulinum induces alteration of nerve muscle interactions in the human orbicularis oculi following treatment for blepharospasm. Neurology 1991;41:1800–5.
2. Aus der Natur: die neuesten Entdeckungen auf dem Gebiet der Naturwissenschaften. Band 31–34. Leipzig: Gebhardt & Reisland, 1868.
2a. Boudreau GP, Grosberg BM, McAllister PJ, Lipton RB, et al. Prophylactic botulinumtoxin A in patients with chronic migraine and comorbid depression: An open-label, multicenter, pilot study of efficacy, safety and effect on headache-related disability, depression, and anxiety. Int J Gen Med 2015;9:79–86.
3. Carruthers J, Carruthers A. Botox: beyond wrinkles. Clin Dermatol 2004;22:89–93.
4. Costa J, Espírito-Santo C, Borges A, Ferreira JJ, et al. Botulinum toxin type A therapy for blepharospasm. Cochrane Database Syst Rev 2005;25(1):CD004900.
5. Darwin CR. The expression of emotions in man and animals. 1st edition. London: John Murray, 1872.
6. Dickson EC. Botulism: a clinical and experimental study. New York: Rockefeller Institute for Medical Research Monograph No. 8, 1918.
7. Erbguth FJ, Naumann M. Historical aspects of botulinum toxin: Justinus Kerner (1786–1862) and the „sausage poison“. Neurology 1999;53:1850.
8. Finzi E, Rosenthal N. Treatment of depression with onabotulinumtoxin A: a randomized, double-blind, placebo controlled trial. J Psychiatr Res 2014;52:1–6.
9. Finzi E, Wasserman E. Treatment of depression with botulinum toxin A: A case series. Dermatol Surg 2006;32:645–50.
10. Grant JE, Potenza MN (editors). The Oxford handbook of impulse control disorders. Oxford: Oxford University Press, 2012.
11. Guo Y, Lu Y, Liu T, Zhou Y, et al. Efficacy and safety of botulinum toxin type A in the treatment of glabellar lines: A meta-analysis of randomized, placebo-controlled, double-blind trials. Plast Reconstr Surg 2015;136:310e–8e.
11a. Hexsel D, Brum C, Siega C, Schilling-Souza J, et al. Evaluation of self-esteem and depression symptoms in depressed and nondepressed subjects treated with onabotulinumtoxinA for glabellar lines. Dermatol Surg 2014;39:1088–96.
12. Jackson CE, Gronseth G, Rosenfeld J, Barohn RJ, et al. Randomized double-blind study of botulinum toxin type B for sialorrhea in ALS patients. Muscle Nerve 2009;39:137–43.
13. James W. The principles of psychology. New York: Holt, 1890.
14. Jankovic J. Blepharospasm and oromandibular-laryngeal-cervical dystonia: a controlled trial of botulinum A toxin therapy. Adv Neurol 1988;50:583–91.
15. Jankovic J, Albanese A, Atassi MZ, Hallett M, et al. Botulinum toxin: Therapeutic clinical practice and science. 1st edition. Oxford: Elsevier Ltd, 2009.
16. Jost W. Botulinumtoxin A bei der Migräne. Neuro aktuell 2014;7:1–6.
17. Jung S, Wollmer MA, Krüger THC. The Hamburg-Hannover Agitation Scale (H2A): Development and validation of a self-assessment tool for symptoms of agitation. J Psychiatr Res 2015;69:158–65.
18. Kao I, Drachman DB, Price DL. Botulinum toxin: mechanism of presynaptic blockade. Science 1976;193:1256–8.
19. Kelly K, Posternak M, Jonathan EA. Toward achieving optimal response: understanding and managing antidepressant side effects. Dialogues Clin Neurosci 2008;10:409–18.
20. Kerner JC. Vergiftung durch verdorbene Würste. Tübinger Blätter für Naturwissenschaften und Arzneykunde 1817;3:1–45.
21. Kreyden OP, Geiges ML, Böni R, Burg G. Botulinumtoxin: Vom Gift zum Medikament. Ein historischer Rückblick. Hautarzt 2000;51:733–7.
22. Larsen RJ, Kasimatis M, Frey K. Facilitating the furrowed brow: An unobtrusive test of the facial feedback hypothesis applied to unpleasant affect. Cogn Emot 1992;6:321–38.
23. Lipton RB, Varon SF, Grosberg B, McAllister PJ, et al. Onabotulinumtoxin A improves quality of life and reduces impact of chronic migraine. Neurology 2011;77:1465–72.
24. Lorentz IT, Subramaniam SS, Yiannikas C. Treatment of idiopathic spasmodic torticollis with botulinum toxin A: a double-blind study on twenty-three patients. Mov Disord 1991;6:145–50.
25. Magid MR, Reichenberg JS, Poth PE, Robertson HT, et al. Treatment of major depressive disorder using botulinum toxin A: A 24-week randomized, double-blind, placebo-controlled study. J Clin Psychiatry 2014;75: 837–44.
26. Magid M, Finzi E, Krüger THC, Robertson HT, et al. Treating depression with botulinum toxin: A pooled analysis of randomized controlled trials. Pharmacopsychiatry 2015;48:205–10.
27. Moore P, Naumann M (editors). Handbook of botulinum toxin treatment. 2nd edition. Wiley-Blackwell, 2003.
28. Morrisroe SN, Chancellor MB. Botulinum toxin A in the treatment of neurogenic and idiopathic urinary incontinence. Rev Urol 2007;9:44–5.
29. Papakostas GI. Tolerability of modern antidepressants. J Clin Psychiatry 2008;69(Suppl E1):8–13.
30. Schantz EJ, Johnson EA. Properties and use of botulinum toxin and other microbial neurotoxins in medicine. Microbiol Rev 1992;56:80–99.
31. Schantz EJ, Johnson EA. Botulinum toxin: the story of its development of human disease. Perspect Biol Med 1997;40:317–27.
32. Schnider P, Binder M, Kittler H, Birner P, et al. A randomized, double-blind, placebo-controlled trial of botulinum A toxin for severe axillary hyperhidrosis. Br J Dermatol 1999;(4):677–80.
33. Schwartz GE, Fair PL, Salt P, Mandel MR, et al. Facial expression and imagery in depression: An electromyographic study. Psychosom Med 1976;38:337–47.
34. Scott AB, Rosenbaum A, Collins CC. Pharmacologic weakening of extraocular muscles. Invest Ophthalmol 1973;12:924–7.
35. Scott AB. Botulinum toxin injection of eye muscles to correct strabismus. Trans Am Ophthalmol Soc 1981;79:734–70.
36. Sommer B, Sattler G (editors). Botulinumtoxin in der ästhetischen Medizin. 3rd edition. Stuttgart: Georg Thieme Verlag, 2006.
37. Strack F, Martin LL, Stepper S. Inhibiting and facilitating conditions of the human smile: A nonobtrusive test of the facial feedback hypothesis. J Pers Soc Psychol 1988;54: 768–77.
38. Tölzel S, Hajak G. Botulinumtoxin – ein Neuromodulator zur effektiven Therapie von Depression? DNP 2015;16:24–30.
39. Van Ermengen E. Über einen neuen anaeroben Bazillus und seine Beziehung zum Botulismus. J Hyg Infektionskrankh 1897;26:1–56.
40. Wollmer MA, de Boer C, Kalak N, Beck J, et al. Facing depression with botulinum toxin: A randomized controlled trial. J Psychiatr Res 2012;46:574–81.
41. Wollmer MA, Kalak N, Jung S, de Boer C, et al. Agitation predicts response of depression to botulinum toxin treatment in a randomized controlled trial. Front Psychiatry 2014;5:36.
* Geteilte Erstautorenschaft
Prof. Dr. Tillmann H.C. Krüger, Stefanie Jung, Klinik für Psychiatrie, Sozialpsychiatrie und Psychotherapie, Medizinische Hochschule Hannover, Carl-Neuberg-Straße 1, 30625 Hannover, E-Mail: krueger.tillmann@mh-hannover.de
Priv.-Doz. Dr. M. Axel Wollmer, Klinik für Gerontopsychiatrie, Asklepios Klinik Nord, Standort Ochsenzoll, Langenhorner Chaussee 560, 22419 Hamburg
Botulinum toxin – a new agent in psychoparmacotherapy?
Botulinum toxin is a neurotoxin that inhibits signal transmission from nerve cells to the muscles and thereby works through paralysis. Although it is highly toxic for humans it has been used therapeutically in medicine for years. After its use was first recognized in treatment of neurological diseases and malfunctions of the muscle tone, novel findings suggest its potentially highly efficient use in treatment of depression. For this purpose botulinum toxin is injected into the glabella region of the forehead. This effect can presumably be explained with the facial feedback theory. It states that mimic expression of emotion and proprioception of expression strengthen the underlying emotion. Paralysis of muscles involved in expression of negative emotions leads to a marked improvement of depressive mood (50% reduction). Current studies show that the mood lifting effect has also been found for chronically depressive and therapy-resistant patients and without presence of visible frown lines in the forehead. Moreover the mood lifting effect seems to persist beyond the time period of botulinum toxin’s physiological effectiveness (6 months). For consolidation of the existing findings and extensive exploration of this novel promising approach, further studies with a higher number of participants are encouraged.
Key words: Botulinum toxin, depression, treatment, facial feedback hypothesis
Psychopharmakotherapie 2016; 23(01)
