Friedhelm C. Schmitt*, Lars Büntjen*, Magdeburg, und Hermann Stefan, Erlangen
Mit einer Prävalenz von etwa 0,7 bis 0,8% ist Epilepsie nach Migräne und M. Alzheimer die häufigste chronische Erkrankung in der Neurologie [32, 42]. Im Vergleich zu anderen chronischen Erkrankungen wie Bluthochdruck, Diabetes mellitus, koronaren Herzerkrankungen und chronischer Depression haben betroffene Patienten, solange sie noch epileptische Anfälle haben, eine insgesamt schlechtere Lebensqualität [91]. Zudem hat die Diagnose erhebliche Auswirkungen auf Berufswahl bzw. -ausübung, Mobilität [31, 34] und die Inzidenz von beispielsweise psychischen Erkrankungen [77]. Ziel einer Behandlung sollte also immer Anfallsfreiheit sein.
Die Diagnose Epilepsie ist dann zulässig, wenn „ein Zustand des Gehirns, der gekennzeichnet ist durch eine andauernde Prädisposition, epileptische Anfälle zu generieren“, vorliegt [42]. Der epileptische Anfall ist somit nur ein Symptom, und die Ursachen der „Prädisposition“ sind vielfältig [9, 42]. Auch die syndromale Einteilung und das Erscheinungsbild dieser Erkrankung sind mannigfaltig und müssen dem aktuellen wissenschaftlichen Kenntnisstand regelmäßig angepasst werden [9, 59]. Die genaue Bestimmung des Epilepsiesyndroms hat für den einzelnen Patienten eine besondere Bedeutung, da das Syndrom die pharmakologische oder auch die chirurgische Epilepsiebehandlung bestimmt. Bezüglich der medikamentösen Behandlung gibt es – trotz der Entwicklung neuer Antiepileptika in den letzten zehn Jahren – keine wesentliche Veränderung: Der Anteil der Patienten, die das Ziel der Anfallsfreiheit nicht erreichten, blieb trotz neu verfügbaren Antiepileptika nahezu konstant bei rund 35% [12, 41]. Eine fachgerechte medikamentöse Behandlung in einer spezialisierten Epilepsieambulanz kann nochmals für maximal 16% der Patienten Anfallsfreiheit für mindestens ein Jahr erreichen [14, 44]. Wird nach fünf Jahren oder nach zwei adäquat dosierten Antiepileptika (im Falle einer im MRT diagnostizierten Hippocampussklerose sogar nach dem Versagen nur eines Medikaments) keine Anfallsfreiheit erreicht, empfiehlt die Leitlinie der Deutschen Gesellschaft für Neurologie die Zuweisung in ein Spezialzentrum, um die Frage der Operabilität des Anfallsleidens zu prüfen. Hierzu gehört unter anderem die Durchführung eines diagnostischen bzw. prächirurgischen Video-EEG-Monitorings zur Sicherung der Diagnose und zur Lokalisierung der epileptogenen Zone (Abb. 1) [7, 8, 42, 71].
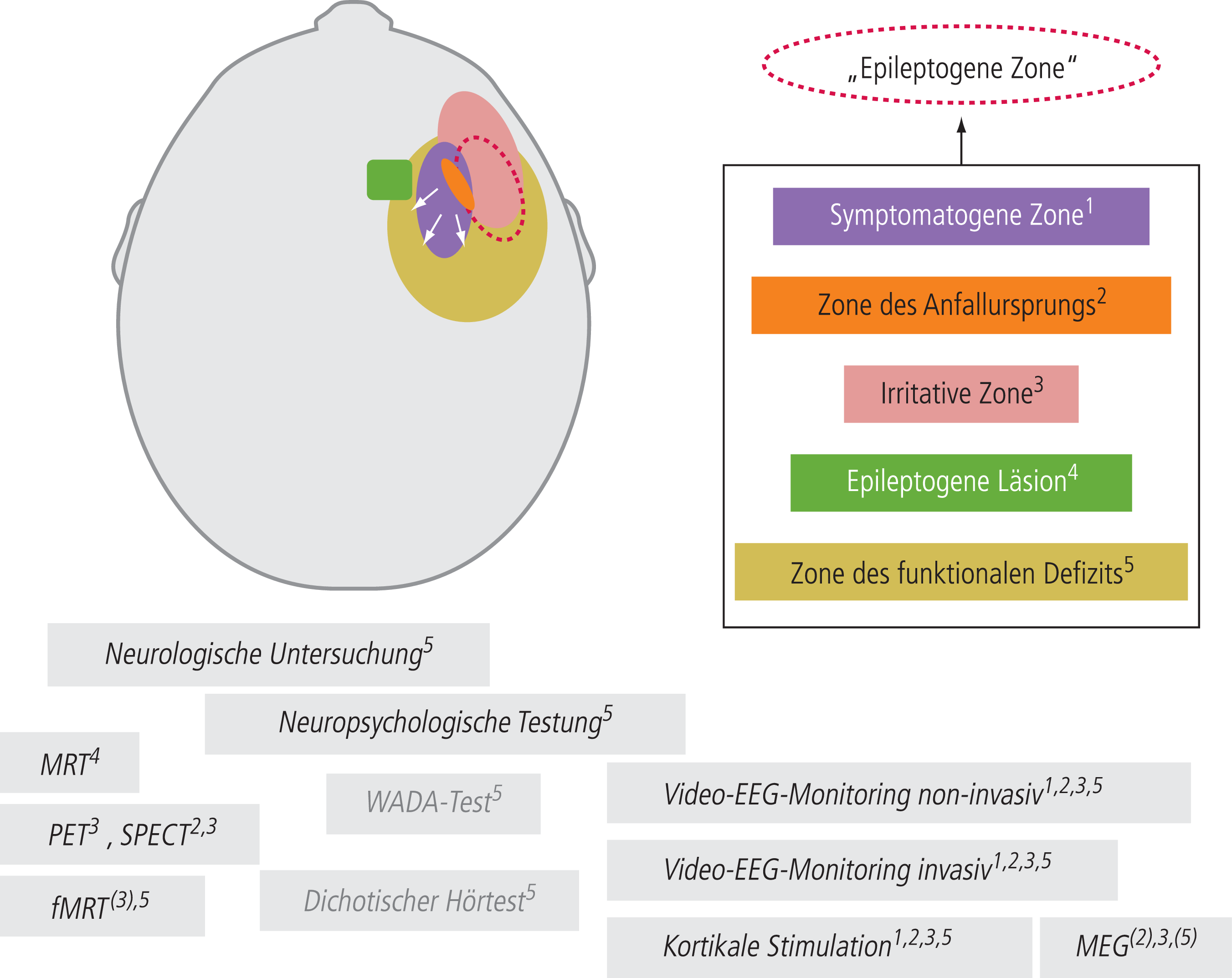
Abb. 1. Konzept der prächirurgischen Epilepsiediagnostik. Schematische Darstellung der verschiedenen Zonen, aus deren Gesamtheit sich eine Hypothese für die epileptogene Zone ergibt. In kursiver Schrift sind die in der prächirurgischen Evaluierung zur Verfügung stehenden diagnostischen Methoden dargestellt (in grau zunehmend weniger benutzte Verfahren; die kleinen Zahlen drücken die mögliche Bestimmung der entsprechenden Zonen durch das jeweilige Verfahren aus). Definitionen [71]: Epileptogene Zone (gestrichelte Linie): Areal, das chirurgisch entfernt werden muss, um Anfallsfreiheit zu erreichen (konzeptionelle Definition, denn dies ist die einzige Zone, die ausschließlich post-operativ bestimmt werden kann). Zone des Anfallsursprung (orange): kortikale Region, von der aus die klinischen Anfälle generiert werden. Irritative Zone (rosa): kortikales Areal, das interiktale Spikes generiert. Epileptogene Läsion (grün): bildmorphologisch darstellbare Läsion, die Ursache der epileptischen Anfälle ist. Zone des funktionellen Defizits: kortikales Areal, das interiktal funktionell eingeschränkt ist.
Im Folgenden soll auf die gängigsten chirurgischen Verfahren, Konzepte und Prognosen der gängigen Behandlungsalternativen für pharmakoresistente Patienten eingegangen werden.
Invasive Verfahren
Resektive Verfahren
Irreversible Entfernung des epileptogenen Herdes
Wenn eine plausible Hypothese bezüglich der epileptogenen Zonen durch eine Bestimmung der Zone des Anfallsursprungs, der irritativen Zone (durch die elektro-klinischen Befunde des Video-EEG-Monitorings), der epileptogenen Läsion (durch eine adäquate epilepsiespezifische Bildgebung) und der funktionellen Zone (z.B. neuropsychologische Testung, Sprachlateralisation bzw. -regionalisierung) vorliegt, kann dem Patienten möglicherweise ein resektiver Eingriff empfohlen werden [7, 8, 60, 71, 72]. Bei Vorliegen konkordanter Befunde ist eine epilepsiechirurgische Entfernung der epileptogenen Zone potenziell kurativ, vorausgesetzt dass die Entfernung komplett ist und angrenzende eloquente Kortexareale geschont werden. In Abgrenzung zu medikamentösen und einigen der minimal-invasiv-epilepsiechirurgischen Verfahren (tiefe Hirnstimulation und in der Regel Vagus-Nerv-Stimulation) ist die Resektion ein irreversibler Vorgang und nur begrenzt wiederholt anwendbar. Deshalb wird auf Vermeidung von unerwünschten Wirkungen besonderer Wert gelegt. In Kenntnis des individuellen Patienten kann dann in enger Zusammenarbeit eines erfahrenen multidisziplinären Teams – bestehend aus Epileptologen, Neurochirurgen, Neuropsychologen und Neuroradiologen – unter Berücksichtigung der psychiatrischen und sozialmedizinischen Zusammenhänge ein resektiver Eingriff empfohlen werden [39].
Prognostische Aussagen vor dem Eingriff
Die Prognose bezüglich einer mindestens einjährigen Anfallsfreiheit variiert in Abhängigkeit von zahlreichen Faktoren, wie der Gehirnregion, in der der epileptogene Herd liegt (z.B. temporal [2, 10, 15, 16, 21, 27, 38, 51, 52, 53, 87] vs. extratemporalen Epilepsien [2, 6, 16, 21, 38, 53, 87]), dem Propagationsverhalten [35, 79], der räumlichen Verteilung von interiktalen Spikes [79], der Ätiologie [10, 82], dem Nachweis einer Läsion in einer epilepsiespezifischen MRT-Bildgebung [5, 10, 22, 53, 57, 84, 97], dem Alter des Patienten [38, 85], dem Vorliegen einer geistigen Behinderung [50], der Dauer [22, 69] bzw. der Schwere [22, 38] der Epilepsie-Erkrankung. Grundsätzlich gilt, dass die Rate der Anfallsfreiheit durch ein resektives Verfahren – unter der Voraussetzung einer fachgerechten prächirurgischen Diagnostik – immer höher liegt (zwischen 30 und 90%) [5, 15, 21, 27, 51, 52, 87, 98] als bei einer Beibehaltung oder Veränderung der medikamentösen Therapie (zwischen 3 und 16%) [15, 44, 98]. Dies ist auch der Grund für die strenge Forderung der Deutschen Gesellschaft für Neurologie nach Durchführung dieses aufwendigen Verfahrens bei nachgewiesener Pharmakoresistenz [42]. Erstaunlicherweise wird eine prächirurgische Diagnostik bei pharmakoresistenten Epilepsie-Patienten aber immer noch häufig erst nach langer Verzögerung von bis zu 20 Jahren durchgeführt [20, 72].
Eine Herausforderung besteht in manchen Fällen darin, das Ausmaß der epileptogenen Zone exakt festzulegen. Ferner erhöht sich der chirurgische Schwierigkeitsgrad bei Zweiteingriffen oder nach invasiver prächirurgischer Diagnostik. Oberste Prämisse für einen epilepsiechirurgischen Eingriff ist die Schonung von eloquentem Kortex. Zu diesem Zweck muss gegebenenfalls präoperativ in Abhängigkeit von der Befundkonstellation ein invasives Monitoring durchgeführt werden [71]. Zunehmend finden berechtigterweise Studien Beachtung, die einen längeren Verlauf (z.B. 5 oder besser 10 Jahre [21, 22, 53] nach einem Eingriff verfolgen und so eine bessere prognostische Einschätzung bezüglich des Behandlungsergebnisses nicht nur hinsichtlich der Anfallsfrequenz [2, 22, 53], sondern auch in Bezug auf die sozialmedizinischen [2, 89] und neuropsychologischen Konsequenzen [26, 81] eines resektiven Eingriffs ermöglichen.
Verschiedene resektive Verfahren – Abhängigkeit vom individuellen Patienten
Den größten Anteil der invasiven epilepsiechirurgischen Eingriffe stellen entsprechend ihrer Häufigkeit die mesialen Temporallappen-Epilepsien. Zwei operative Vorgehensweisen können unterschieden werden. Die Amygdalohippokampektomie erfolgt über einen transsylvischen, einen subtemporalen oder transkortikalen Zugang. Alternativ hierzu kommt die vordere Temporalpolresektion häufig in Kombination mit einer Hippokampektomie [17] zum Einsatz. Ein klassisches Beispiel für die Anwendung dieser beiden Verfahren ist die mesiale Temporallappenepilepsie (mTLE), beispielsweise auf dem Boden einer Hippocampussklerose (Abb. 2). Die mTLE sind die bestuntersuchten Epilepsiesyndrome. In einer randomisierten, kontrollierten Studie konnte bei diesem Syndrom die Überlegenheit der Resektion (Anfallsfreiheit nach einem Jahr von 58% aller Patienten) gegenüber einer medikamentösen Therapie (Anfallsfreiheit nach einem Jahr von 8% aller Patienten) belegt werden [98]. Eine mögliche Komplikation bei der Temporallappenteilresektion ist eine vorübergehende kontralaterale obere Quadrantenanopsie, die im Verlauf zumeist rückläufig ist, sodass nur selten ein relevantes funktionales Defizit verbleibt. Andere Verfahren sind – analog zur Temporallappenteilresektion – Teil-Lobektomien in anderen Kortexarealen (an 2. Stelle der Frontallappen) oder beispielsweise Läsionektomien. Die Wahl des Verfahrens hängt vom individuellen elektro-klinischen Befund des prächirurgischen Monitorings und von der Ätiologie der Epilepsie ab.
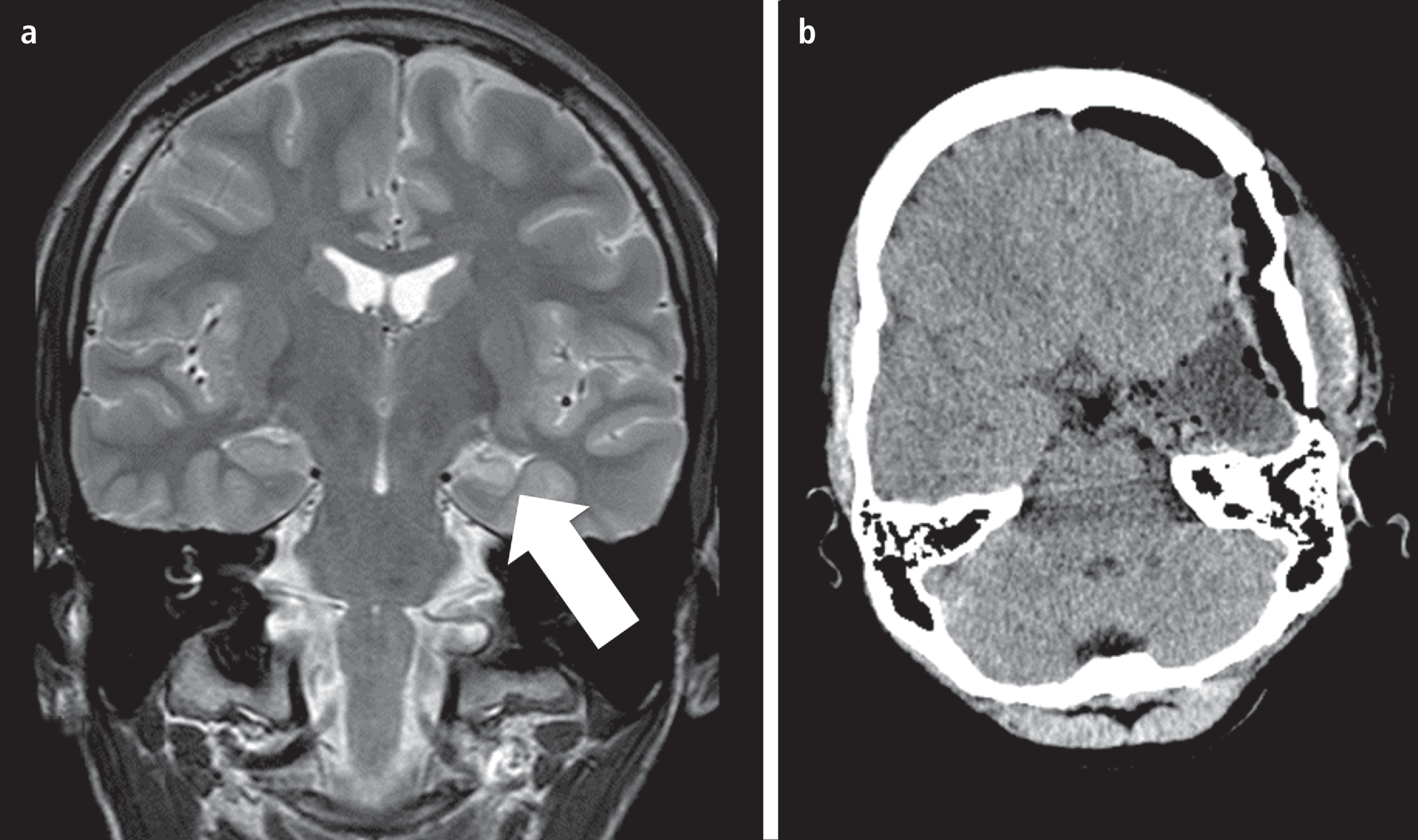
Abb. 2. Illustratives Fallbeispiel. Patientin mit fokaler Epilepsie (unspezifischen Auren und komplex-motorischen Anfällen; relevante Vorerkrankungen: Meningitis im 1. Lebensjahr) seit dem 8. Lebensjahr. MRT-Diagnose einer linksseitigen Hippocampussklerose im 12. Lebensjahr und pharmakoresistent gegen zwei Antiepileptika seit mindestens dem 14. Lebensjahr. Prächirurgisches Video-EEG-Monitoring im Alter von 17 (konkordante Befunde). a) Präoperatives MRT mit linksseitiger Hippocampussklerose (weißer Pfeil). b) Perioperative CT-Aufnahme des Operationssitus (18. Lebensjahr). Seit zwei Jahren ist die Patientin mit unveränderter medikamentöser Therapie anfallsfrei; sie befindet sich zurzeit in Abiturvorbereitung.
In der Kinderepileptologie werden im Verhältnis weniger Temporallappen- oder Frontallappen-Operationen und stattdessen mehr Hemisphärotomien [37, 70] und multilobäre Resektionen [30] (zusammen ein Drittel der Operationen) durchgeführt. Bei beiden Verfahren geht es in der Regel um die Entfernung oder Verkleinerung eines mehr diffus ausgeprägten epileptischen Herdes. Das Behandlungskonzept differiert bei einigen zusätzlichen, vorwiegend bei Kindern, angewandten Verfahren von den klassischen resektiven Methoden: Durch Kallosotomien und multiple, subpiale Transsektionen (MST) soll die Propagationsfähigkeit epileptischer Anfälle so gestört werden, dass es zur Reduktion der Anfallsschwere und idealerweise auch der Anfallsfrequenz kommt. MST haben nur in beschränktem Maße zur Anfallsreduktion geführt und eine komplette Anfallskontrolle ist sehr selten [78], sodass dieses Verfahren zunehmend verlassen wurde, obwohl der Ansatz eine Störung des epileptogenen Herdes unter gleichzeitiger Schonung des eloquenten Kortex initial sehr attraktiv schien und teilweise gute Ergebnisse erbrachte [61]. Für Kallosotomien konnte ein positiver Effekt im Langzeitverlauf für eine spezielle und besonders beeinträchtigende Sorte von Anfällen – die atonischen Sturzanfälle – belegt werden [86].
Die Leitlinien der Neuropädiatrischen Gesellschaft [3] setzen – besonders im Hinblick auf jüngere Kinder – einen anderen Akzent. So sollten auch Patienten, bei denen noch keine formale Pharmakoresistenz besteht, grundsätzlich in ein tertiäres Epilepsiezentrum überwiesen werden. Ein frühes Vorgehen empfehle sich insbesondere für Patienten, bei denen ein Stilstand oder eine Regression der mentalen Entwicklung festzustellen ist. Typischerweise trifft das auf Ätiologien zu, die mit Epilepsie assoziiert sind und häufig in der Kindheit klinisch manifest werden, wie beispielsweise das Sturge-Weber-Syndrom, hypothalamische Tumoren [64, 67], tuberöse Sklerose [45], Rasmussen-Enzephalitis [11] oder neuro-ektodermale Tumoren [69]. Auch finden sich bei diesen Kindern häufiger fokal-kortikale Dysplasien [4] und andere kortikale Entwicklungsstörungen (z.B. Polymikrogyrien) als im Erwachsenenalter.
Grundsätzlich gelten alle der oben genannten epilepsiechirurgischen Konzepte für Kinder und Erwachsene gleichermaßen. Durch die altersabhängige Verteilung der verschiedenen Ätiologien [28, 30], die bei Kindern vermehrt im Fokus stehende Gefahr der Entwicklungsverzögerung [36, 37, 69], das vorwiegend im Kindesdesalter gehäufte Auftreten von „schweren“ Epilepsien und die erhöhte Plastizität des Kortex im frühen Kindesalter ergibt sich aber eine andere Betonung der gewählten operativen Verfahren.
Ausblick
Unabhängig vom Alter der Patienten wird auch nach neuen diagnostischen Verfahren gesucht, um eine Reduktion der invasiven Diagnostik zu erreichen, zum Beispiel durch eine verfeinerte Steuerung der invasiven Elektrodenimplantation mittels MEG-Quellenlokalisation [1] oder die nichtinvasive Zuordnung fokaler epileptischer Aktivität zu Läsionen [40, 56, 83]. So können weniger invasive epilepsiechirurgische Eingriffe mittels umschriebener Ablationen angestrebt werden.
Minimal-invasive Verfahren
Thermoablation – Verkleinerung oder Zerstörung des epileptogenen Herdes
Diese Methode kann bezüglich der neurochirurgischen Technik ebenfalls auf einen langen Erfahrungszeitraum und technische Weiterentwicklungen zurückgreifen [25, 62]. Im unmittelbaren Vergleich mit dem resektiven Vorgehen bietet die Thermoablation mehrere konzeptionelle Vorteile:
- Es besteht eine geringere perioperative Belastung
- Der Eingriff kann im Bedarfsfall problemlos wiederholt werden
- Die Möglichkeit eines anschließenden resektiven Vorgehens wird in keiner Weise eingeschränkt (Eskalationsprinzip oder „Step-by-Step“-Prinzip)
Theoretisch beruht die Wirkung dieses stereotaktischen Eingriffs auf einer Zerstörung des epileptogenen Herdes, allerdings wurde in der Vergangenheit [29, 63] auch eine Verhinderung oder Einschränkung der Propagation epileptischer Aktivität diskutiert. Anfang der 50er-Jahre fand dieses neurochirurgische Verfahren zunehmende Anwendung bei einer Vielzahl von Indikationen insbesondere bei Bewegungsstörungen und psychiatrischen Erkrankungen, aber auch bei Patienten mit einer medikamentös unzureichend behandelbaren Epilepsie [23, 76]. Aus heutiger Sicht muss für die beiden zuletzt genannten Fachgebiete die Indikationsstellung kritisch hinterfragt werden, weil eine Erfassung der epileptogenen Zone seinerzeit technischen Begrenzungen unterworfen war.
Für die Indikation der mesialen Temporallappenepilepsien sind in den letzten fünf Jahren mehrere Arbeiten von einer Arbeitsgruppe aus der Tschechischen Republik erschienen, die bezüglich einer Anfallsfreiheit und des neuropsychologischen Outcomes über einen Zeitraum von zwei Jahren ein mit resektiven Verfahren vergleichbares Ergebnis erbrachten [43, 46–49]. Die Autoren selbst führen ihre guten Ergebnisse auf ihre zunehmende Erfahrung mit dem Verfahren zurück [47]. Eine Replikation dieser monozentrisch generierten Ergebnisse steht noch aus.
Kürzlich wurden erste Behandlungsergebnisse zweier weiterer Indikationen aus dem epileptischen Formenkreis berichtet. Diese Beobachtungen betreffen einerseits die periventrikulären nodulären Heterotopien, andererseits die fokalen kortikalen Dysplasien. Durch die Zerstörung von im prächirurgischen Monitoring nachgewiesenen epileptogenen singulären periventrikulären nodulären Heterotopien (Abb. 3a) mittels stereotaktisch geführter Thermoablation konnte in insgesamt sechs von sieben Fällen Anfallsfreiheit während einer Nachbeobachtungszeit von 12 bis 60 Monaten erreicht werden [18, 68, 73]. Der einzige therapierefraktäre Patient konnte durch ein anschließendes resektives Verfahren ebenfalls Anfallsfreiheit (nach 2-jährigem Beobachtungszeitraum) erreichen [18] – ein gutes Beispiel für die Anwendung des Eskalationsprinzips.
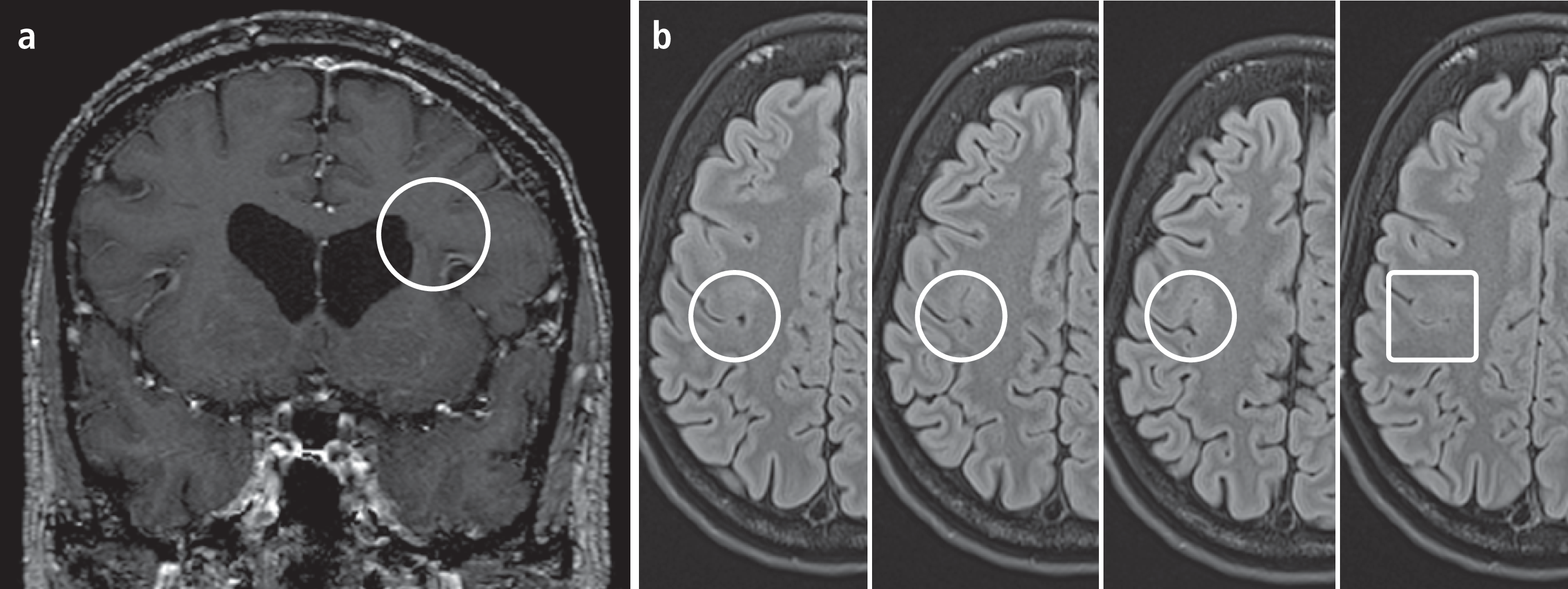
Abb. 3. a) Koronare T2-gewichtete MRT-Aufnahme einer singulären periventrikulären Heterotopie (weißer Kreis). b) Axiale T2-gewichtete MRT-Aufnahmen mit fokaler kortikaler Dysplasie Typ 2b (weißer Kreis: verschwommene Mark-Rindengrenze; Quadrat: Anschnitt einer typischen T2-Hyperintensität vom Kortex in Richtung Seitenventrikel)
Immer häufiger werden fokale kortikale Dysplasien (Abb. 3b) in tertiären Epilepsiezentren im Rahmen standardisiert durchgeführter spezieller MRT-Technik [80] und gegebenenfalls anschließenden Post-Processing-Methoden [33, 65, 100] erkannt. Fokale kortikale Dysplasien sind in fachgerecht durchgeführten MRT-Aufnahmen [97] für den geübten Untersucher [94] anhand einer charakteristischen, zum Kortex ziehenden Hyperintensität oft gut zu erkennen (siehe Quadrat in Abb. 3b). Eine komplette Resektion des gesamten epileptogenen Kortex – und nicht allein der oben genannten pathognomonischen subkortikalen Veränderung – ist Voraussetzung für ein gutes Outcome (Engel-Klasse 1) [95]. In diesem Fall scheint also eine bildmorphologische Charakteristik eine unmittelbare Aussage über die Lokalisation und das Ausmaß des epileptischen Herds zuzulassen. Somit wurde auch die Anwendung der Läsionektomie mittels Thermokoagulation möglich. Kürzlich wurde dieses Verfahren für die ersten zwei Patienten publiziert [96]: von inzwischen insgesamt sechs durchgeführten Operationen (persönliche Kommunikation) erreichten die oben genannten zwei Patienten einen Nachbeobachtungszeitraum von mehr als einem Jahr und sind weiter anfallsfrei (12 Monate bzw. 18 Monate).
Eine aus Autorensicht vielversprechende technische Erweiterung stellt die gerade in den USA und Kanada bereits seit einigen Jahren in Erprobung befindliche „MRI-guided Laserablation“ dar, bei der mittels stereotaktischer Technik nicht durch elektrisch induzierte Hitze, sondern durch einen Laser der epileptische Herd verkleinert oder zerstört wird. Die Anwender weisen auf gute Erfahrungen bei verschiedenen Ätiologien und unter anderem auf die mittels des MRT mögliche Steuerbarkeit der Läsionsgröße [19, 99] hin. In Europa ist dieses Verfahren (noch) nicht zugelassen.
Vagus-Nerv-Stimulation – Modulierung der Propagation 1
In den letzten 20 Jahren hat sich die Vagus-Nerv-Stimulation (VNS) in der Behandlung therapierefraktärer Epilepsien etabliert. Sie ist – unter den neuromodulativen Verfahren – das Verfahren mit dem größten Erfahrungshintergrund. Obwohl eine große Menge an tierexperimentellen Daten über physiologische Effekte der VNS vorliegen, sind die für den Therapieerfolg relevanten Mechanismen oder prognostische Faktoren nicht abschließend geklärt.
Das Stimulationssystem besteht aus einem Impulsgeber, der über einen linksaxillären Hautschnitt eingebracht und auf dem M. pectoralis fixiert wird, sowie einem Kabel, an dessen Ende sich zwei Elektroden befinden, die mittels Kunststoffhelices am Nervus vagus fixiert werden. Die Patienten erhalten zusätzlich einen Magneten, mit dem die durch den Neurologen vorgegebene Stromstärke der Intervallstimulation vor dem Auftreten eines größeren epileptischen Anfalls (z.B. bei Auftreten einer Aura) vorübergehend um 0,25 mA überschritten werden bzw. der Stimulator ausgeschaltet werden kann. Das Prinzip einer vorübergehenden Stromstärkenerhöhung mit dem Ziel einer Anfallsunterbrechung wird in den aktuellen Weiterentwicklungen der Firma automatisiert: durch die über den Nervus vagus vermittelte erhöhte Pulsrate erhöht der Stimulator vorübergehend den Stromimpuls. Inwieweit dieses Prinzip die Wirksamkeit der VNS erweitern kann, sollte aus Sicht der Autoren unter kontrollierten Bedingungen, beispielsweise im Rahmen einer doppel-verblindeten Studie, und ohne Veränderung der antiepileptischen Zusatztherapie untersucht werden.
Die VNS wurde 1988 [66] erstmals zur Behandlung therapierefraktärer Epilepsie eingesetzt und ist seit 1994 in Europa zur Behandlung von Epilepsie zugelassen. Die FDA-Zulassung erfolgte 1997. Zwei Jahre zuvor wurde eine randomisierte kontrollierte Studie mit 114 Patienten durch die VNS-Study-Group [88] veröffentlicht. Eine Gruppe erhielt eine effektive Stimulation, die Kontrollgruppe eine Sham-Stimulation mit sehr niedriger und somit ebenfalls vom Patienten bemerkter, aber nicht effektiver Stromstärke. Nach 14 Wochen zeigte sich ein signifikanter Abfall der Anfallsfrequenz in der effektiv stimulierten Gruppe. 31% der Patienten unter Verum-Stimulation zeigten eine Reduktion der Anfallsfrequenz von über 50%. Eine evidenzbasierte Überarbeitung [55] des amerikanischen Einsatzes der VNS zieht nach Auswertung von 13 Class-III-Studien den Schluss, dass in 55% der pädiatrischen Fälle über 12 Jahren mit fokaler oder (primär) generalisierter Epilepsie eine Reduktion der Anfälle von über 50% erreicht wird. Die gleichen Reduktionsraten werden beim sogenannten Lennox-Gastaut-Syndrom beobachtet. Die Autoren schlussfolgern, die VNS könne bei diesen Indikationen zum Einsatz kommen (Evidenz-Klasse C). Sie fanden eine erhöhte Ansprechrate nach längerem Therapieintervall sowie Stimmungsaufhellung bei Erwachsenen mit Epilepsie. Bei Kindern fand sich perioperativ eine erhöhte Infektionsrate der Operations-Situs.
Für alle neuromodulativen Verfahren gilt generell, dass der Therapieeffekt erst mit einer Verzögerung von einigen Monaten klinisch erkennbar wird. Dieser Zeitraum ist bei der VNS leider nochmals verlängert, weil die Eindosierung der Stromstärke besonders langsam erfolgen muss, um den Stromstärken-abhängigen, aber einem Gewöhnungseffekt unterliegenden Nebenwirkungen Hustenreiz und Dysphonie zu begegnen: die Stromstärke wird langsam individuell in 0,25-mA-Schritten auf die in der Regel wirksame Stromstärke von mindestens 1,0 bis 1,5 mA aufdosiert.
Ein weiterer Nachteil der VNS ist die eingeschränkte Durchführbarkeit moderner MRT-Verfahren: mit jeder Weiterentwicklung des MRT hinkt die Zulassung der Implantate für kranielle MRT-Untersuchung hinterher; diese Einschränkung spricht für die Durchführung eines prächirurgischen Monitorings – zumindest aber ein unter epilepsiespezifischen Richtlinien durchgeführtes 3-Tesla-MRT [97] – vor der VNS-Implantation.
Tiefe Hirnstimulation – Modulierung der Propagation 2
Die im Jahre 2010 veröffentlichte randomisierte, kontrollierte SANTE-Studie (SANTE =Stimulation of the anterior nuclei of thalamus for epilepsy) (Evidenz-Klasse A) mit dem Nachweis der Effektivität einer tiefen Hirnstimulation (THS) des anterioren Thalamus [24] führte zu einer Zulassung dieses Verfahrens in Europa. Konzeptionell handelt es sich um ein neuromodulatives Verfahren, bei dem durch eine chronische Stimulation von intrazerebralen, bei der Propagation epileptischer Aktivität beteiligten Relais-Stationen diese derart moduliert werden sollen, dass die epileptischen Anfälle sich nicht weiterentwickeln können und klinisch blander (Anfallsschwere wird geringer) oder im Idealfall gar nicht manifest (Reduktion der Anfallsfrequenz) werden. Das Verfahren bietet im Vergleich zu einem resektiven Verfahren den Vorteil der Reversibilität und zeigt niedrige perioperative Komplikationsraten [93]. Allerdings bleiben – ähnlich zur VNS – die genauen pathophysiologischen Zusammenhänge ungeklärt und ist eine differenzierte, postoperative MRT-Bildgebung des Kopfes postoperativ deutlich erschwert. Für die THS kommen daher nur Patienten infrage, bei denen eine fachgerechte, prächirurgische Evaluation bereits erfolgt ist. Ähnlich wie bei der Thermoablation besteht bezüglich der chirurgischen Methode eine langjährige Erfahrung bei der Behandlung anderer Indikationen (Bewegungsstörungen).
In Deutschland sind – nach Angaben des Arbeitskreises Tiefe Hirnstimulation der Deutschen Gesellschaft für Epileptologie – inzwischen über 50 Patienten mit einer pharmakoresistenten fokalen Epilepsie mit THS des anterioren Thalamus (ANT) behandelt worden. Für diesen Eingriff werden in Deutschland zwei verschiedene neurochirurgische Zugänge (transventrikulär und bzw. unter Umgehung des Ventrikels) angewandt (Abb. 4); für beide werden die sich aus den anatomischen Gegebenheiten ergebenden Vor- und Nachteile diskutiert, verlässliche Daten hierzu fehlen allerdings bislang. Neuerdings kann der anteriore Thalamus auch mit geringen Veränderungen eines standardisierten, klinischen Protokolls im 3-Tesla-MRT dargestellt werden, sodass eine Optimierung der stereotaktischen Planung möglich wird [13].
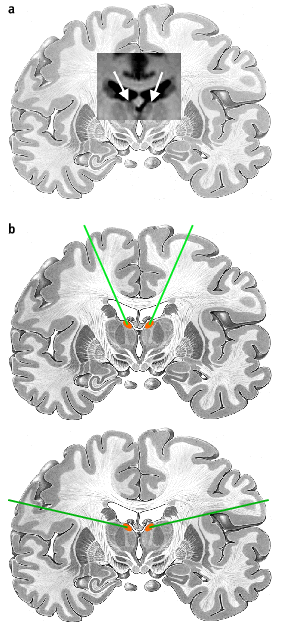
Abb. 4. Tiefe Hirnstimulation des anterioren Thalamus. a) Darstellung des anterioren Thalamus in T2-gewichteten MRT-Aufnahmen (kleine weißen Pfeile) [13] auf einen anatomischen Schnitt [58] projiziert. b) Skizzenhafte Darstellung der verschiedenen Zugangswege zum anterioren Thalamus
Die SANTE-Studie konnte – insbesondere bei Patienten mit Temporallappenepilepsie – nach drei Monaten chronischer Stimulation eine im Vergleich zur Plazebo-stimulierten Patientengruppe eine signifikante erhöhte Anfallsreduktion von durchschnittlich 40,4% erreichen. Jeder achte Patient beklagte jedoch auch Gedächtnisstörungen oder eine depressive Stimmung. Möglicherweise werden diese Störungen durch Stimulus-abhängige Arousals erklärbar, wie kürzlich vom Epilepsiezentrum Hamburg berichtet wurde [92].
2013 wurde für den zentromedianen Thalamus für eine kleine Patientengruppe (n=9) eine über 50%ige Anfallsreduktion in einem einfach-verblindeten Studiendesign gefunden [90]. In einer Kooperation zwischen der Universitätsklinik Magdeburg, der Neurologischen Klinik der Charité und des Epilepsiezentrums Berlin-Brandenburg [74, 75] konnte ebenfalls für eine kleine Gruppe von Patienten (z. Zt. n=9) bei fünf Patienten eine Reduktion der Anfallsfrequenz über 50% durch Stimulation des Nucleus accumbens erreicht werden. Bei dieser Patientenkohorte waren weder psychiatrische noch kognitive Veränderungen objektivierbar.
Responsive Stimulation – Modulierung der Propagation 3
Bei diesem Verfahren wird mittels einer im parietalen Schädelknochen untergebrachten Stimulations- und Ableiteinheit interiktale bzw. iktal abgeleitete EEG-Aktivität gemessen und daraufhin (responsiv) eine elektrische Stimulation in der zuvor im prächirurgischen Monitoring diagnostizierten epileptogenen Zone elektrisch appliziert. Der Nachweis einer Effektivität wurde in diesem recht komplexen und aufwendigen Verfahren ebenfalls in einer randomisiert kontrollierten Studie [54] erbracht. Das Verfahren ist im November 2013 in den Vereinigten Staaten zugelassen worden. Für die Anlage der Ableit- und Stimulationseinheit ist eine größere parietale Trepanation notwendig, sodass dieses Verfahren per se nicht als „minimal-invasiv“ im engeren Sinne bezeichnet werden kann. Die neurochirurgische Intervention im Gehirn bleibt aber reversibel und ist prinzipiell auch in eloquenten kortikalen Arealen anwendbar. Andere theoretische Vorteile sind die patientenindividuelle Behandlungsoption und die Überprüfbarkeit des Einflusses der Stimulation auf die iktale bzw. interiktale EEG-Aktivität. Ein zumindest theoretischer Kritikpunkt ist allerdings, dass es sich aufgrund der hohen Detektionsrate von subklinischen Anfällen ebenfalls um eine chronische Stimulationsmethode handeln soll.
Zusammenfassung
Je nach Alter, Ätiologie, Schweregrad der Epilepsie, der sozialmedizinischen Situation und den elektro-klinischen Befunden kann pharmakoresistenten Patienten ein großes Armentarium verschiedener invasiver und minimal-invasiver Verfahren angeboten werden. Hierfür sind eine fachgerechte prächirurgische Evaluation und ein sorgfältiges Abwägen der Vor- und Nachteile eines jeden Verfahrens unter Berücksichtigung des individuellen Patienten notwendig. Die Auswahl an Verfahren ist inzwischen so vielfältig, dass für viele pharmakoresistente Patienten ein invasives oder minimal-invasives Verfahren in Erwägung gezogen werden kann. Vor allem die minimal-invasiven Verfahren sehen einer technischen Weiterentwicklung entgegen.
Danksagung
Herrn Prof. Dr. med. B. Hamm, Institut für Neuroradiologie, Charité – Universitätsmedizin Berlin, Frau Dr. med. J. Matzen, Universitätsklinik für Neurologie, Magdeburg, Herrn Prof. Dr. med. M. Skalej, Institut für Neuroradiologie, Magdeburg, und Herrn Prof. Dr. med. J. Voges, Universitätsklinik für Stereotaktische Neurochirurgie, Magdeburg, für Teile des hier abgedruckten, der Universitätsklinik für Neurologie, Magdeburg verfügbar gemachten Bildmaterials.
Interessenkonflikte
FCS: Honorar für die Teilnahme an einem Advisory Board sowie Vortragshonorar von Medtronic.
LB: Keine Interessenkonflikte.
HS: Keine Interessenkonflikte.
Epilepsy surgery. Concepts of invasive and minimally invasive procedures
Literatur
1. Agirre-Arrizubieta Z, Thai NJ, Valentín A, et al. The value of nagnetoencephalography to guide electrode implantation in epilepsy. Brain Topogr 2014;27:197–207.
2. Asztely F, Ekstedt G, Rydenhag B, Malmgren K. Long term follow-up of the first 70 operated adults in the Goteborg Epilepsy Surgery Series with respect to seizures, psychosocial outcome and use of antiepileptic drugs. J Neurol Neurosurg Psychiatry 2007;78:605–9.
3. Bast DT, Holthausen H, Tuxhorn I. Epilepsiechirurgische Behandlung bei Kindern und Jugendlichen. In: Leitlinien der Gesellschaft für Neuropädiatrie. 2009. www.google.de/url?sa=t&rct=j&q=&esrc=s&source=web&cd=1&ved=0CCIQFjAA&url=http%3A%2F%2Fwww.awmf.org%2Fuploads%2Ftx_szleitlinien%2F022-023_S1_Epilepsiechirurgische_Behandlung_bei_Kindern_und_Jugendlichen_05-2009_05-2014.pdf&ei=LvLoU8mqMeTj4QSR-oC4Aw&usg=AFQjCNFTXToW4BhBV8BDrQHsocLJ_5VKQQ&sig2=4bwqcUeMMuYiyoM0zSSCQg&bvm=bv.72676100,d.bGE (Zugriff am 11.08.2014).
4. Bast T, Ramantani G, Seitz A, Rating D. Focal cortical dysplasia: prevalence, clinical presentation and epilepsy in children and adults. Acta Neurol Scand 2006;113:72–81.
5. Bast T. Outcome after epilepsy surgery in children with MRI-negative non-idiopathic focal epilepsies. Epileptic Disord Int Epilepsy J Videotape 2013;15:105–13.
6. Bauer S, Hamer HM. Chapter 15 – Extratemporal epilepsies [Internet]. In: Stefan H, Theodore WH (eds.). Handbook of Clinical Neurology. 107. Epilepsy Part I: Basic principles and diagnosis. Elsevier, 2012:241–56. Available from: www.sciencedirect.com/science/article/pii/B978044452898800015X (Zugriff am 21.06.2014)
7. Baumgartner C, Lindinger G, Lurger S, et al. [Prolonged video EEG monitoring in differential diagnosis of seizures and in presurgical epilepsy diagnosis]. Wien Med Wochenschr 19461998;148:2–8.
8. Baumgartner C, Pirker S. Presurgical evaluation in adults: noninvasive. Handb Clin Neurol 2012;108:841–66.
9. Berg AT, Berkovic SF, Brodie MJ, et al. Revised terminology and concepts for organization of seizures and epilepsies: Report of the ILAE Commission on Classification and Terminology, 2005–2009. Epilepsia 2010;51:676–85.
10. Bien CG, Raabe AL, Schramm J, Becker A, et al. Trends in presurgical evaluation and surgical treatment of epilepsy at one centre from 1988–2009. J Neurol Neurosurg Psychiatry 2012;84:54–61.
11. Bien CG. Pathogenesis, diagnosis and treatment of Rasmussen encephalitis: A European consensus statement. Brain 2005;128:454–71.
12. Brodie MJ, Barry SJE, Bamagous GA, Norrie JD, et al. Patterns of treatment response in newly diagnosed epilepsy. Neurology 2012;78:1548–54.
13. Büntjen L, Kopitzki K, Schmitt F, et al. Direct targeting of the thalamic anteroventral nucleus for deep brain stimulation by T1-weighted magnetic resonance imaging at 3 T. Stereotact Funct Neurosurg 2013;92:25–30.
14. Callaghan BC, Anand K, Hesdorffer D, Hauser WA, et al. Likelihood of seizure remission in an adult population with refractory epilepsy. Ann Neurol 2007;62:382–9.
15. Choi H, Heiman GA, Munger Clary H, Etienne M, et al. Seizure remission in adults with long-standing intractable epilepsy: An extended follow-up. Epilepsy Res 2011;93:115–9.
16. Choi H, Sell RL, Lenert L, et al. Epilepsy surgery for pharmacoresistant temporal lobe epilepsy: a decision analysis. JAMA 2008;300:2497–505.
17. Clusmann H, Schramm J. Surgery in adults: temporal resections. Handb Clin Neurol 2012;108:897–913.
18. Cossu M, Fuschillo D, Cardinale F, et al. Stereo-EEG-guided radio-frequency thermocoagulations of epileptogenic grey-matter nodular heterotopy. J Neurol Neurosurg Psychiatry 2013;85:611–7.
19. Curry DJ, Gowda A, McNichols RJ, Wilfong AA. MR-guided stereotactic laser ablation of epileptogenic foci in children. Epilepsy Behav 2012;24:408–14.
20. De Flon P, Kumlien E, Reuterwall C, Mattsson P. Empirical evidence of underutilization of referrals for epilepsy surgery evaluation. Eur J Neurol Off J Eur Fed Neurol Soc 2010;17:619–25.
21. De Tisi J, Bell GS, Peacock JL, et al. The long-term outcome of adult epilepsy surgery, patterns of seizure remission, and relapse: a cohort study. Lancet 2011;378:1388–95.
22. Edelvik A, Rydenhag B, Olsson I, et al. Long-term outcomes of epilepsy surgery in Sweden. Neurology 2013;81:1244–51.
23. Faria MA. Violence, mental illness, and the brain – A brief history of psychosurgery: Part 3 – From deep brain stimulation to amygdalotomy for violent behavior, seizures, and pathological aggression in humans. Surg Neurol Int 2013;4:91.
24. Fisher R, Salanova V, Witt T, et al. Electrical stimulation of the anterior nucleus of thalamus for treatment of refractory epilepsy. Epilepsia 2010;51:899–908.
25. Gabriel EM, Nashold BS. Evolution of neuroablative surgery for involuntary movement disorders: An historical review. Neurosurgery 1998;42:575–91.
26. Grivas A, Schramm J, Kral T, et al. Surgical treatment for refractory temporal lobe epilepsy in the elderly: seizure outcome and neuropsychological sequels compared with a younger cohort. Epilepsia 2006;47:1364–72.
27. Hanáková P, Brázdil M, Novák Z, et al. Long-term outcome and predictors of resective surgery prognosis in patients with refractory extratemporal epilepsy. Seizure 2014;23:266–73.
28. Harvey AS, Cross JH, Shinnar S, Mathern GW, et al.; ILAE Pediatric Epilepsy Surgery Survey Taskforce. Defining the spectrum of international practice in pediatric epilepsy surgery patients. Epilepsia 2008;49:146–55.
29. Hassler R, Riechert T. Über einen Fall von doppelseitiger Fornicotomie bei sogenannter temporaler Epilepsie. Acta Neurochir (Wien) 1957;5:330–40.
30. Hauptman JS, Mathern GW. Epilepsy neurosurgery in children. Handb Clin Neurol 2012;108:881–95.
31. Helmstaedter C, Droege F, Witt J-A. [Assessing activities of daily living in patients with epilepsy]. Fortschr Neurol Psychiatr 2013;81:452–8.
32. Hirtz D, Thurman DJ, Gwinn-Hardy K, Mohamed M, et al. How common are the “common” neurologic disorders? Neurology 2007;68:326–37.
33. House PM, Lanz M, Holst B, Martens T, et al. Comparison of morphometric analysis based on T1- and T2-weighted MRI data for visualization of focal cortical dysplasia. Epilepsy Res 2013;106:403–9.
34. Janz D. Social prognosis in epilepsy especially in regard to social status and the necessity for institutionalization. Epilepsia 1972;13:141–7.
35. Jenssen S, Roberts CM, Gracely EJ, Dlugos DJ, et al. Focal seizure propagation in the intracranial EEG. Epilepsy Res 2011;93:25–32.
36. Jonas R, Asarnow RF, LoPresti C, et al. Surgery for symptomatic infant-onset epileptic encephalopathy with and without infantile spasms. Neurology 2005;64:746–50.
37. Jonas R, Nguyen S, Hu B, et al. Cerebral hemispherectomy: hospital course, seizure, developmental, language, and motor outcomes. Neurology 2004;62:1712–21.
38. Kanchanatawan B, Limothai C, Srikijvilaikul T, Maes M. Clinical predictors of 2-year outcome of resective epilepsy surgery in adults with refractory epilepsy: a cohort study. BMJ Open 2014;4:e004852.
39. Kellinghaus DC, Loddenkemper T, Wyllie E, et al. Vorschlag für eine neue patientenorientierte Epilepsieklassifikation. Nervenarzt 2006;77:961–9.
40. Knowlton RC. Can Magnetoencephalography aid epilepsy surgery? Epilepsy Curr 2008;8:1–5.
41. Kwan P, Brodie MJ. Early identification of refractory epilepsy. N Engl J Med 2000;342:314–9.
42. Leitlinie Erster epileptischer Anfall und Epilepsien im Erwachsenenalter. C. Baumgartner et al. unter Federführung von Christian E. Elger. In: Diener HC, Weimar C. Leitlinien zur Diagnostik und Therapie in der Neurologie. Herausgegeben von der Kommission Leitlinien der Deutschen Gesellschaft für Neurologie (DGN). 5., aktualisierte und erweiterte Auflage. Stuttgart: Thieme, 2012.
43. Liscak R, Malikova H, Kalina M, et al. Stereotactic radiofrequency amygdalohippocampectomy in the treatment of mesial temporal lobe epilepsy. Acta Neurochir (Wien) 2010;152:1291–8.
44. Luciano AL, Shorvon SD. Results of treatment changes in patients with apparently drug-resistant chronic epilepsy. Ann Neurol 2007;62:375–81.
45. Madhavan D, Schaffer S, Yankovsky A, et al. Surgical outcome in tuberous sclerosis complex: A multicenter survey: Surgical outcome in tuberous sclerosis complex. Epilepsia 2007;48:1625–8.
46. Malikova H, Kramska L, Liscak R, et al. Stereotactic radiofrequency amygdalohippocampectomy for the treatment of temporal lobe epilepsy: do good neuropsychological and seizure outcomes correlate with hippocampal volume reduction? Epilepsy Res 2012;102:34–44.
47. Malikova H, Kramska L, Vojtech Z, Lukavsky J, et al. Stereotactic radiofrequency amygdalohippocampectomy: two years of good neuropsychological outcomes. Epilepsy Res 2013;106:423–32.
48. Malikova H, Vojtech Z, Liscak R, et al. Microsurgical and stereotactic radiofrequency amygdalohippocampectomy for the treatment of mesial temporal lobe epilepsy: different volume reduction, similar clinical seizure control. Stereotact Funct Neurosurg 2010;88:42–50.
49. Malikova H, Vojtech Z, Liscak R, et al. Stereotactic radiofrequency amygdalohippocampectomy for the treatment of mesial temporal lobe epilepsy: correlation of MRI with clinical seizure outcome. Epilepsy Res 2009;83:235–42.
50. Malmgren K, Olsson I, Engman E, Flink R, et al. Seizure outcome after resective epilepsy surgery in patients with low IQ. Brain J Neurol 2008;131(Pt 2):535–42.
51. McIntosh AM, Averill CA, Kalnins RM, et al. Long-term seizure outcome and risk factors for recurrence after extratemporal epilepsy surgery. Epilepsia 2012;53:970–8.
52. McIntosh AM, Wilson SJ, Berkovic SF. Seizure outcome after temporal lobectomy: current research practice and findings. Epilepsia 2001;42:1288–307.
53. Meencke H-J, Meinken-Jaeggi D, Lehmann T, Schmitt FC. 10-year follow up after temporal lobe resection. Epilepsia 2009;50:76.
54. Morrell MJ, RNS System in Epilepsy Study Group. Responsive cortical stimulation for the treatment of medically intractable partial epilepsy. Neurology 2011;77:1295–304.
55. Morris GL, Gloss D, Buchhalter J, Mack KJ, et al. Evidence-based guideline update: Vagus nerve stimulation for the treatment of epilepsy: Report of the Guideline Development Subcommittee of the American Academy of Neurology. Epilepsy Curr 2013;13: 297–303.
56. Mu J, Rampp S, Carrette E, et al. Clinical relevance of source location in frontal lobe epilepsy and prediction of postoperative long-term outcome. Seizure 2014;23:553–9.
57. Mueller C-A, Scorzin J, von Lehe M, et al. Seizure outcome 1 year after temporal lobe epilepsy: an analysis of MR volumetric and clinical parameters. Acta Neurochir (Wien) 2012;154:1327–36.
58. Nieuwenhuys R, Voogd J, van Huijzen C. The Human Central Nervous System: A Synopsis and Atlas. 4th edition. New York: Steinkopff, 2007.
59. Noachtar PDS, Rémi J. Klassifikation epileptischer Anfälle und Syndrome. Nervenarzt 2012;83:156–61.
60. Oehl B, Altenmüller D-M, Schulze-Bonhage A. Zur Notwendigkeit prächirurgischer Video-EEG-Registrierungen bei läsionellen Epilepsiepatienten. Nervenarzt 2009;80:464–7.
61. Ogrezeanu I, Buchfelder M, Stefan H. Experience with multiple subpial transections as a unique procedure or supplement to resective surgery for epilepsy. Romanian Neurosurg 2006;13:30–6.
62. Ohye C, Fodstad H. Forty years with Professor Narabayashi. Neurosurgery 2004;55:222–6; discussion 226–7.
63. Parrent AG, Blume WT. Stereotactic amygdalohippocampotomy for the treatment of medial temporal lobe epilepsy. Epilepsia 1999;40:1408–16.
64. Parrent AG. Stereotactic radiofrequency ablation for the treatment of gelastic seizures associated with hypothalamic hamartoma. Case report. J Neurosurg 1999;91:881–4.
65. Pascher B, Kröll J, Mothersill I, Krämer G, et al. Automated morphometric magnetic resonance imaging analysis for the detection of periventricular nodular heterotopia. Epilepsia 2013;54:305–13.
66. Penry JK, Dean JC. Prevention of intractable partial seizures by intermittent vagal stimulation in humans: preliminary results. Epilepsia 1990;31(Suppl 2):S40–3.
67. Polkey CE. Resective surgery for hypothalamic hamartoma. Epileptic Disord Int Epilepsy J Videotape 2003;5:281–6.
68. Polster T, Voges J, Berhard M, et al. Erfolgreiche Thermoablation einer singulären periventrikulären nodulären Heterotopie bei pharmakoresistenten Sturzanfällen. Zeitschrift für Epileptologie 2012;25(Suppl 1):19.
69. Ramantani G, Kadish NE, Anastasopoulos C, et al. Epilepsy surgery for glioneuronal tumors in childhood: avoid loss of time. Neurosurgery 2014;74:648–57.
70. Ramantani G, Kadish NE, Brandt A, et al. Seizure control and developmental trajectories after hemispherotomy for refractory epilepsy in childhood and adolescence. Epilepsia 2013;54:1046–55.
71. Rosenow F, Lüders H. Presurgical evaluation of epilepsy. Brain J Neurol 2001;124(Pt 9):1683–700.
72. Ryvlin P, Rheims S. Epilepsy surgery: eligibility criteria and presurgical evaluation. Dialogues Clin Neurosci 2008;10:91–103.
73. Schmitt FC, Voges J, Büntjen L, et al. Radiofrequency lesioning for epileptogenic periventricular nodular heterotopia: a rational approach. Epilepsia 2011;52:e101–5.
74. Schmitt FC, Voges J, Büntjen L, et al. Tiefe Hirnstimulation des Nucleus accumbens bei fokalen Epilepsien. Zeitschrift für Epileptologie 2014;27:48–54.
75. Schmitt FC, Voges J, Heinze H-J, Zähle T, et al. Safety and feasibility of nucleus accumbens stimulation in five patients with epilepsy. J Neurol 2014 261(8):1477–84.
76. Schmitt FC, Woermann FG, Kopitzki K, Kluge C, et al. Thermoablation für fokale Epilepsien. Nervenheilkunde 2014;5:370–5.
77. Schmitz B. Psychiatrische Aspekte bei Epilepsien. Nervenarzt 2012;83:205–8.
78. Schramm J, Aliashkevich AF, Grunwald T. Multiple subpial transections: outcome and complications in 20 patients who did not undergo resection. J Neurosurg 2002;97:39–47.
79. Schulz R, Lüders HO, Hoppe M, Tuxhorn I, et al. Interictal EEG and ictal scalp EEG propagation are highly predictive of surgical outcome in mesial temporal lobe epilepsy. Epilepsia 2000;41:564–70.
80. Sisodiya SM. Surgery for malformations of cortical development causing epilepsy. Brain 2000;123:1075–91.
81. Smith ML, Olds J, Snyder T, Elliott I, et al. A follow-up study of cognitive function in young adults who had resective epilepsy surgery in childhood. Epilepsy Behav 2014;32:79–83.
82. Stefan H, Hildebrandt M, Kerling F, et al. Clinical prediction of postoperative seizure control: structural, functional findings and disease histories. J Neurol Neurosurg Psychiatry 2009;80:196–200.
83. Stefan H, Nakasato N, Papanicolaou AC. Chapter 21 – Magnetoencephalography [Internet]. In: Stefan H, Theodore WH (eds.). Handbook of Clinical Neurology. 107. Epilepsy Part I: Basic principles and diagnosis. Elsevier, 2012:347–58.
84. Stefan H. Epilepsien. Stuttgart: Thieme, 1999.
85. Stefan H. Epilepsy in the elderly: facts and challenges. Acta Neurol Scand 2011;124: 223–37.
86. Stigsdotter-Broman L, Olsson I, Flink R, Rydenhag B, et al. Long-term follow-up after callosotomy – A prospective, population based, observational study. Epilepsia 2014;55:316–21.
87. Téllez-Zenteno JF, Dhar R, Wiebe S. Long-term seizure outcomes following epilepsy surgery: a systematic review and meta-analysis. Brain J Neurol 2005;128(Pt 5): 1188–98.
88. The Vagus Nerve Stimulation Study Group. A randomized controlled trial of chronic vagus nerve stimulation for treatment of medically intractable seizures. Neurology 1995;45(2):224–30.
89. Thorbecke R, May TW, Koch-Stoecker S, Ebner A, et al. Effects of an inpatient rehabilitation program after temporal lobe epilepsy surgery and other factors on employment 2 years after epilepsy surgery. Epilepsia 2014;55:725–33.
90. Valentín A, García Navarrete E, Chelvarajah R, et al. Deep brain stimulation of the centromedian thalamic nucleus for the treatment of generalized and frontal epilepsies. Epilepsia 2013;54:1823–33.
91. Vickrey BG, Hays RD, Rausch R, Sutherling WW, et al. Quality of life of epilepsy surgery patients as compared with outpatients with hypertension, diabetes, heart disease, and/or depressive symptoms. Epilepsia 1994;35:597–607.
92. Voges J, Hilker R, Bötzel K, et al. Thirty days complication rate following surgery performed for deep-brain-stimulation. Mov Disord 2007;22:1486–9.
93. Voges B; Epilepsy Study Group Hamburg. Effect of deep brain stimulation in epilepsy on sleep quality and sleep structure of the anterior nucleus thalamicus. Epilepsia 2013;54(Suppl 3):286.
94. Von Oertzen J, Urbach H, Jungbluth S, et al. Standard magnetic resonance imaging is inadequate for patients with refractory focal epilepsy. J Neurol Neurosurg Psychiatry 2002;73:643–7.
95. Wagner J, Urbach H, Niehusmann P, von Lehe M, et al. Focal cortical dysplasia type IIb: completeness of cortical, not subcortical, resection is necessary for seizure freedom. Epilepsia 2011;52:1418–24.
96. Wellmer J, Kopitzki K, Voges J. Lesion focused stereotactic thermo-coagulation of focal cortical dysplasia IIB: A new approach to epilepsy surgery? Seizure 2014;23:475–8.
97. Wellmer J, Quesada CM, Rothe L, Elger CE, et al. Proposal for a magnetic resonance imaging protocol for the detection of epileptogenic lesions at early outpatient stages. Epilepsia 2013;54:1977–87.
98. Wiebe S, Blume WT, Girvin JP, Eliasziw M. A randomized, controlled trial of surgery for temporal-lobe epilepsy. N Engl J Med 2001;345:311–8.
99. Willie JT, Laxpati NG, Drane DL, et al. Real-time magnetic resonance-guided stereotactic laser amygdalohippocampotomy for mesial temporal lobe epilepsy. Neurosurgery 2014;74:569–85.
100.Woermann FG, Free SL, Koepp MJ, Ashburner J, et al. Voxel-by-voxel comparison of automatically segmented cerebral gray matter – A rater-independent comparison of structural MRI in patients with epilepsy. Neuroimage 1999;10:373–84.
*gleichermaßen beteiligt
Korrespondenzautor: Dr. med. Friedhelm C. Schmitt, Universitätsklinik für Neurologie, Leipziger Straße 44, 39120 Magdeburg, E-Mail: fc.schmitt@med.ovgu.de
Dr. med. Lars Büntjen, Universitätsklinik für Stereotaktische Neurochirurgie, Magdeburg
Prof. Dr. Hermann Stefan, Epilepsiezentrum Erlangen, Neurologische Klinik der Universitätsklinik Erlangen, Schwabachanlage 6, 91054 Erlangen
Epilepsy surgery. Concepts of invasive and minimally invasive procedures
Provided careful patient selection, patients with medically intractable epilepsies (defined as at least two trials of adequately dosed and selected antiepileptic drugs) have a better outcome after invasive surgical methods compared to medical treatment. Among the minimally-invasive methods – i. e. ablation or neuromodulation – ablation also has a potential for cure in selected etiologies. Neuromodulative procedures hinder the propagation of seizures and for each method a different level of experience and evidence class is available. In the following the current publications the advantages and disadvantages and of the different surgical approaches are summarized.
Key words: Epilepsy surgery, resective, palliative, pharmacoresistant, focal
Psychopharmakotherapie 2014; 21(05)
