Thomas Messer, Pfaffenhofen, und Christoph Goemann, Hamburg
Die Depression zählt zu den häufigsten psychischen Erkrankungen. Wie den meisten psychischen Störungen liegt auch der Episode einer Major Depression eine multifaktorielle Ätiologie zugrunde. Hierbei spielen biologische, psychische und soziale Faktoren eine Rolle [61].
Die Lebenszeitprävalenz depressiver Störungen schwankt in Deutschland zwischen 11,6% und 17,1% [13, 23]. Schätzungen gehen davon aus, dass in den nächsten Jahrzehnten mit einer deutlichen Zunahme depressiver Störungen zu rechnen ist [31]. Die Jahresberichte der deutschen Krankenkassen und Rentenversicherer weisen eine kontinuierliche Zunahme von Arbeitsunfähigkeits-Tagen wegen depressiver Störungen ihrer Versicherten auf. Neben den negativen Auswirkungen auf die Lebensqualität in Folge von affektiven Symptomen sind vor allem auch die Beeinträchtigung der kognitiven Funktionen, beispielsweise Arbeitsgedächtnis oder Exekutivfunktionen prognoserelevant [41].
Von rund vier Millionen betroffenen Personen in Deutschland werden nur 30 bis 35% korrekt diagnostiziert, und von diesen erhalten nur etwa 10% eine adäquate Therapie. Das mittlere Alter bei einer ersten Episode der Major Depression liegt zwischen dem 26. und 31. Lebensjahr [32], wobei der Krankheitsverlauf einer Major Depression sich individuell sehr unterschiedlich gestalten kann. Die Erkrankung verläuft häufig mit Rezidiven, die innerhalb eines Jahres bei bis zu 30% der Patienten auftreten und deren Häufigkeit mit der Dauer des Beobachtungszeitraums auf 70 bis 80% ansteigen kann [51]. Mit dem Alter steigt nicht nur die durchschnittliche Episodendauer, sondern auch der Schweregrad und die Wahrscheinlichkeit für ein Rezidiv [56]. Dabei muss hervorgehoben werden, dass im Verlauf einer depressiven Episode die Rückbildung affektiver Symptome und die Konsolidierung kognitiver Defizite keineswegs parallel, sondern häufig zeitversetzt verlaufen [49, 50]. Bei einem Teil der Betroffenen lassen sich die Beeinträchtigungen sogar in einem klinisch als Vollremission definierten Intervall nachweisen, woraus dann erhebliche negative Konsequenzen für die psychosoziale und berufliche Kompetenz drohen [16, 27, 29, 54].
Vortioxetin (Lu AA21004) ist ein modernes Antidepressivum, das von der FDA im September 2013 und von der europäischen Behörde EMA am 27.12.2013 unter dem Handelsnamen Brintellix® zugelassen wurde.
Es handelt sich um einen Wirkstoff, der ein neuartiges pharmakologisches Profil besitzt und der Klasse sogenannter multimodaler Antidepressiva angehört [1, 48]. Vortioxetin agiert über zwei pharmakologische Wirkungsmechanismen, indem es verschiedene Serotonin-Rezeptoren moduliert und zusätzlich den Serotonin-Transporter inhibiert. Es wird angenommen, dass die Affinität von Vortioxetin unter anderem zu den serotonergen Rezeptor-Subtypen 5-HT1A, 5-HT1B, 5-HT7 und 5-HT1D sowie zum Serotonin-Transporter (SERT bzw. 5-HTT) von klinischer Relevanz ist und am Wirkungsmechanismus von Vortioxetin in therapeutischen Dosen beteiligt ist [3]. Es ist zu vermuten, dass infolge dieser Effekte eine Konzentrationserhöhung mehrerer Neurotransmitter in für die Depression relevanten Hirnregionen resultiert [6, 44, 52]. Die höchste Rezeptorbindungsaffinität besitzt Vortioxetin für den 5-HT3-Rezeptor, den es antagonisiert. Dies erhöht die Freisetzung von Noradrenalin und Acetylcholin vor allem im entorhinalen Kortex, im Hippocampus und in der Amygdala [44].
Pharmakokinetik
Vortioxetin hat eine Bioverfügbarkeit von etwa 75%. Es weist eine lineare Pharmakokinetik auf. Die Plasmaspitzenkonzentration wird im Mittel nach etwa acht Stunden erreicht (Tmax), und die mittlere Eliminationshalbwertszeit liegt bei rund 57 Stunden [4]. Vortioxetin ist Substrat von Cytochrom P450-2D6 ohne signifikante inhibitorische oder induktorische Potenz, sodass in dieser Hinsicht keine klinisch relevanten Interaktionen zu erwarten sind [14].
Studien
Zu Vortioxetin wurde ein umfangreiches klinisches Entwicklungsprogramm mit zahlreichen Kurzzeit- und Langzeitstudien durchgeführt, welches zu der Indikation Behandlung von Episoden einer Major Depression bei Erwachsenen geführt hat. Tabelle 1 liefert einen Überblick über das Studienprogramm. Die Anwendungsbereiche umfassen Daten aus mehreren, unter anderem Plazebo-kontrollierten Kurzzeitstudien, inklusive einer Studie mit älteren Menschen und einer Langzeit-Rückfallpräventions-Studie. Vortioxetin wurde in mehreren Dosierungen (von 1 bis 20 mg) untersucht. In einigen Studien wurden Duloxetin oder Venlafaxin als Referenzwirkstoffe zur Studienvalidierung verwendet. Die Studien wurden weltweit durchgeführt. Die fett hervorgehobene EU-Abkürzung stellt die Beteiligung deutscher Zentren dar.
Tab. 1. Übersicht über das Studienprogramm mit Vortioxetin; Fettdruck von „EU“ =Beteiligung deutscher Zentren
|
Kurzzeitstudien |
Langzeitstudien |
||||||||||||||
|
Publikation |
Alvarez 2012 [2] |
Baldwin 2012 [5] |
Henigsberg 2012 [19] |
Boulenger 2014 [11] |
Mahabelshwarkar 2013 [37] |
Jacobsen 2013 [25] |
Jain 2013 [26] |
Mahabelshwarkar 2013 [36, 38] |
Katona 2012 [28] |
McIntyre 2014 [42] |
Häggström 2013 [17] |
EPAR |
Boulenger 2012 [10] |
4 weitere Studien |
|
|
Kürzel |
HLu 11492 |
HLu 11984 |
TAK 305 |
HLu 13267 |
TAK 315 |
TAK 316 |
TAK 303 |
TAK 304 |
TAK 317 |
HLu 12541 |
HLu 14122A |
HLu 14178A |
CCT-002 |
HLu 11985 Rückfallprävention |
|
|
Dauer |
6 Wo. |
8 Wo. |
8 Wo. |
8 Wo. |
8 Wo. |
8 Wo. |
6 Wo. |
8 Wo. |
8 Wo. |
8 Wo. |
8 Wo. |
12 Wo. |
8 Wo. |
OL: 12 Wo. DB: 24–64 Wo. |
Langzeit-Sicherheitsstudien bis 1 Jahr |
|
Therapie |
|||||||||||||||
|
Plazebo |
Plazebo |
Plazebo |
Plazebo |
Plazebo |
Plazebo |
Plazebo |
Plazebo |
Plazebo |
Plazebo |
Plazebo |
Plazebo |
Plazebo |
||
|
2,5 mg |
1 mg |
|||||||||||||
|
5 mg |
5 mg |
5 mg |
5 mg |
5 mg |
5 mg |
5 mg |
5 mg |
||||||||
|
10 mg |
10 mg |
10 mg |
10 mg |
10 mg |
10 mg |
10 mg |
10 mg |
10 mg |
|||||||
|
15 mg |
15 mg |
15 mg |
|||||||||||||
|
20 mg |
20 mg |
20 mg |
20 mg |
20 mg |
20 mg |
||||||||||
|
225 mg Venlafaxin |
60 mg Duloxetin |
60 mg Duloxetin |
60 mg |
60 mg Duloxetin |
60 mg Duloxetin |
25–50 mg Agomelatin |
||||||||
|
Region |
EU Asien Kanada |
EU Asien Kanada |
EU Südafrika Asien |
EU Südafrika |
USA |
USA |
USA |
USA |
USA |
EU Kanada USA |
EU Kanada USA u.a. |
EU Russland |
EU Asien |
EU Kanada Asien |
|
|
Studienergebnis |
Positiv |
„failed“ |
Positiv |
Positiv |
Positiv |
Positiv |
Negativ# |
Negativ# |
Negativ# |
Positiv |
Positiv |
Positiv |
Negativ# |
Positiv |
Positiv |
EPAR: European Public Assessment Report; OL: offen (open label); DB: doppelblind; # kein Unterschied zwischen Verum und Plazebo
Der überwiegende Teil von Studien war positiv. Die von Baldwin et al. 2012 publizierte Studie ist als fehlgeschlagene („failed“) Studie zu bewerten, weil auch die Aktivreferenz Duloxetin sich nicht von dem Plazebo differenzieren konnte [5]. Die Negativstudien ohne Wirksamkeitsnachweis stammen überwiegend aus den USA.
Die Ergebnisse einiger dieser Studien wurden in wissenschaftlichen Fachzeitschriften veröffentlicht. Andere wurden bei internationalen Tagungen vorgestellt oder finden sich im European Public Assessment Report (EPAR; www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Public_assessment_report/human/002717/WC500159447.pdf).
Klinische Wirksamkeit
Akutstudien
Für die Prüfung der Wirksamkeit, Sicherheit und Verträglichkeit von Vortioxetin in der Behandlung der Major Depression liegen unter anderem randomisierte Plazebo-kontrollierte Studien über sechs Wochen [2] und acht Wochen [11, 19, 28] vor. In der sechswöchigen doppelblinden, randomisierten Plazebo-kontrollierten Studie mit Venlafaxin (Retardform) als aktiver Referenzsubstanz wurden 426 Patienten eingeschlossen, die mindestens einen Schweregrad der Depression von 30 oder mehr Punkten in der Montgomery-Åsberg-Depressionsskala (MADRS) aufwiesen [2]. Vortioxetin wurde von Beginn an entweder mit 5 mg (n=108) oder 10 mg (n=100) dosiert, die Venlafaxin-Gruppe (n=113) schrittweise auf 225 mg aufdosiert. Nach sechswöchiger Behandlung ergab sich mit einem durchschnittlichen Rückgang im MADRS-Gesamtwert für Vortioxetin 5 mg von 5,9 Punkten und für Vortioxetin 10 mg von 5,7 Punkten im Vergleich zu Plazebo eine hochsignifikante Verbesserung (p<0,0001 in der Kovarianzanalyse [ANCOVA] mit den LOCF[last observation carried forward]-Daten; Abb. 1). Auch in den sekundären Effektivitätsvariablen (Hamilton-Depressionsskala [HAM-D], Clinical global impression [CGI]) ergaben sich signifikante Veränderungen. Der Anteil der Responder, definiert als ≥50%-Reduktion im MADRS-Gesamtscore oder als CGI-I (CGI-Improvement) ≤2 betrug 67% für 5 mg/Tag Vortioxetin (p<0,01) und 68% für 10 mg/Tag Vortioxetin (p<0,01) im Vergleich zu Plazebo (45%) und Venlafaxin (72%; p<0,001 vs. Plazebo). Eine Remission der depressiven Symptomatik, definiert als MADRS-Wert ≤10 oder HAM-D24 ≤7 bzw. CGI-S (CGI-Severity of illness) ≤2 erreichten in beiden Vortioxetin-Gruppen 49% (p<0,01), in der Plazebo-Gruppe 27% und in der Venlafaxin-Gruppe 55% (p<0,001).
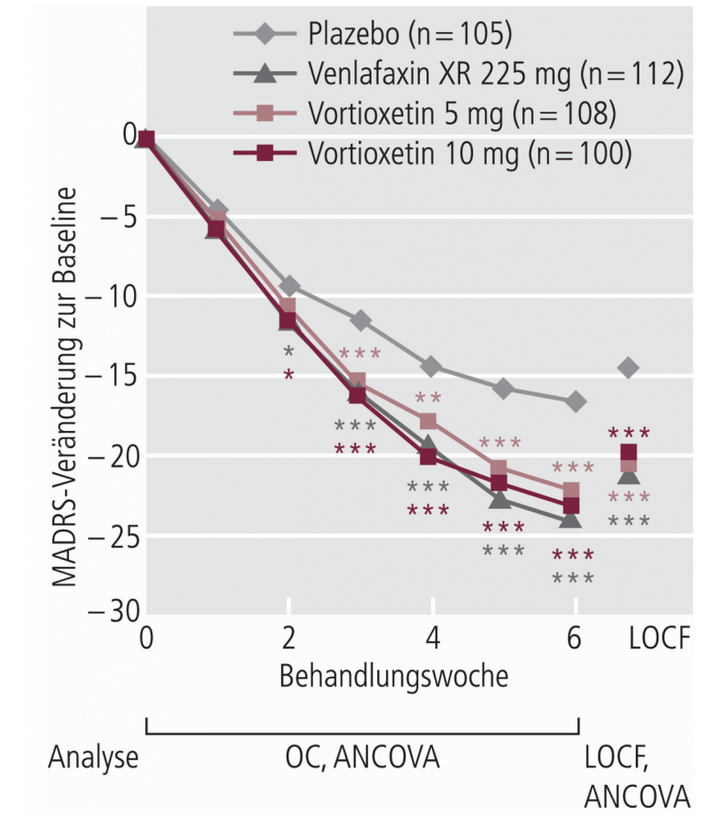
Abb. 1. Mittlere Differenz von Baseline in der Montgomery-Åsberg Depression Rating Scale (MADRS) [2]. Gesamtwert (FAS, OC, over-time) und LOCF (Woche 6). *p<0,05; **p<0,01; ***p<0,001 vs. Plazebo; FAS: full-analysis set; LOCF: last observation carried forward, OC: observed cases; ANCOVA: Kovarianzanalyse
In einer achtwöchigen, randomisierten, doppelblinden Plazebo-kontrollierten Studie (n=776) wurden vier Behandlungsgruppen mit Vortioxetin 2,5 mg/Tag (n=155), 5 mg/Tag (n=159), 10 mg/Tag (n=153) oder mit Duloxetin 60 mg/Tag (n=157) mit Plazebo (n=152) verglichen [5]. Einschlusskriterium war ein Schweregrad der Depression von mindestens 26 Punkten in der MADRS und primärer Endpunkt ebenfalls der Unterschied zum Ausgangswert. Während sich in der ANCOVA (LOCF) keine statistisch signifikanten Unterschiede zwischen allen Verum-Gruppen und Plazebo ergaben, trennten sich hinsichtlich der meisten sekundären Wirksamkeitsendpunkte 5 und 10 mg Vortioxetin sowie Duloxetin vom Plazebo unter Verwendung der OC (observed cases) mit ANCOVA und MMRM (mixed model of repeated measurements) statistisch signifikant. Allerdings konnte in der Analyse der Responder und Remitter ebenfalls für keine Behandlungsgruppe ein signifikanter Unterschied im Vergleich zu Plazebo gefunden werden, sodass es sich um eine sogenannte „failed study“ handelt, das heißt, sowohl die Prüfsubstanz als auch die etablierte Vergleichssubstanz erbrachte keinen statistischen Vorteil im Vergleich zu Plazebo.
In einer weiteren europäischen multizentrischen Studie (n=501, head-to-head; Alter zwischen 18 und 75 Jahren, MADRS bei Einschluss >22) wurde Vortioxetin (10–20 mg/Tag) mit Agomelatin (25–50 mg/Tag) als aktivem Komparator geprüft [17]. Einschlusskriterium war insbesondere, dass die Patienten bereits zuvor eine mindestens sechswöchige Monotherapie mit einem selektiven Serotonin-Wiederaufnahmehemmer (SSRI) oder einem Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRI) in adäquater Dosis erfolglos absolviert hatten. Diese Studie zeigte bei depressiven Patienten eine signifikante Verbesserung durch Vortioxetin gegenüber Agomelatin sowohl hinsichtlich des Ansprechens (Response) als auch hinsichtlich der Vollremission (Abb. 2).
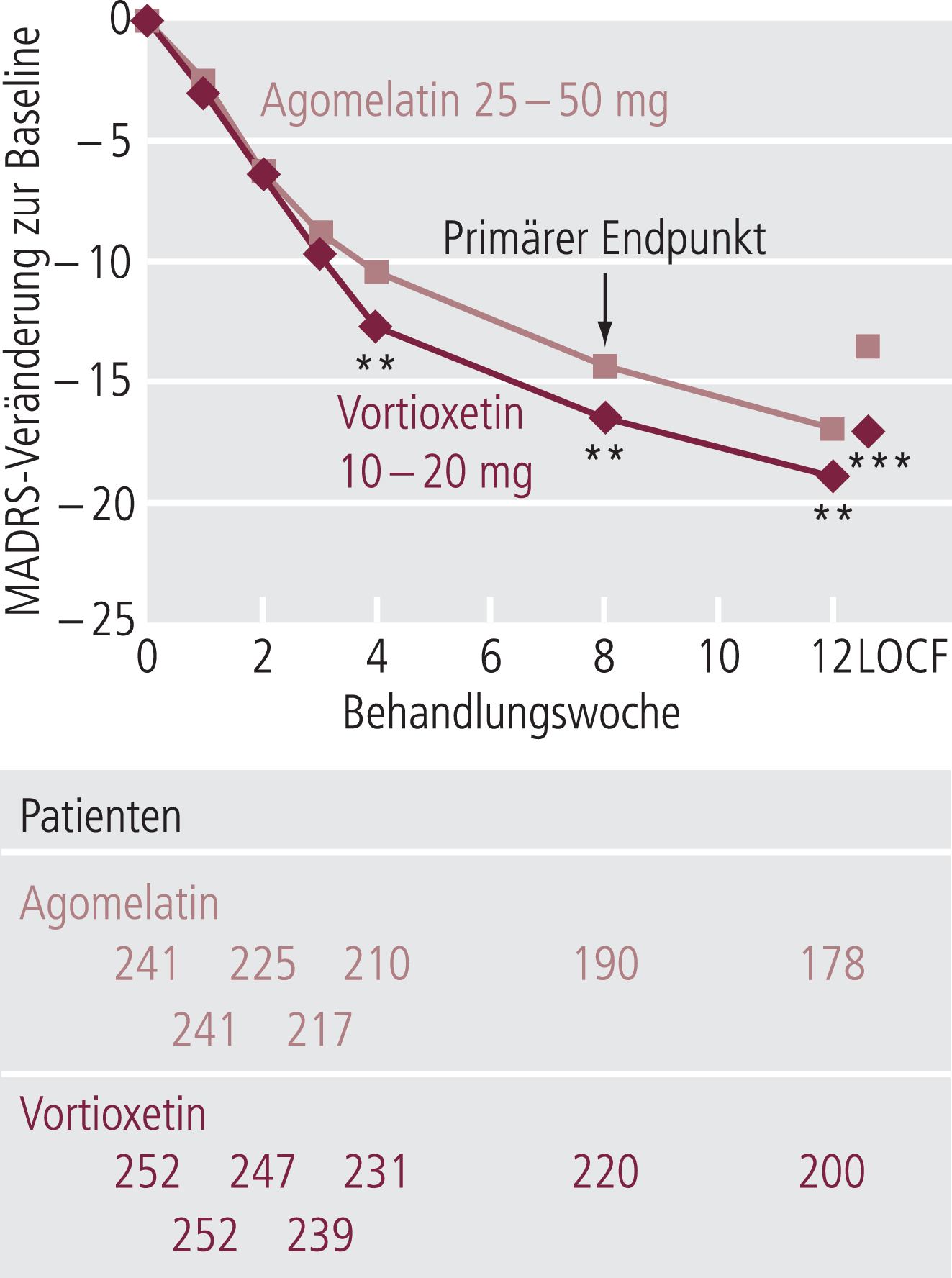
Abb. 2. Vermutete Differenz von Baseline in der Montgomery-Åsberg Depression Rating Scale (MADRS); Gesamtwert von Baseline bis Woche 12 (FAS, MMRM) und LOCF (FAS, ANCOVA) in Woche 12 [17]. FAS: full-analysis set; LOCF: last observation carried forward; MMRM: mixed model repeated measures. Die Anzahl der Patienten bei jedem Besuch ist unter der x-Achse für jede Behandlungsgruppe dargestellt. **p<0,01; ***p<0,001 versus Agomelatin. Der primäre Endpunkt war bei Woche 8 (FAS, MMRM).
Henigsberg et al. führten ebenfalls eine randomisierte, kontrollierte Studie (n=560, je 140 pro Arm) durch, in der Vortioxetin in drei verschiedenen Dosierungen (1 mg/Tag, 5 mg/Tag und 10 mg/Tag) im Vergleich zu Plazebo geprüft wurde [19]. Nach einem Beobachtungszeitraum von acht Wochen schlossen zwischen 87,1 und 92,1% die Studie ab. Gemessen mit der Hamilton-Depressionsskala (HAM-D24) ergaben sich (ausgehend von 32,1–33,1) für alle Dosierungen hochsignifikante Verbesserungen (p<0,001) mit einer Reduktion von 3,52 Punkten (1 mg/Tag), 4,12 Punkten (5 mg/Tag) und 4,93 Punkten (10 mg/Tag), wobei bereits nach zwei Wochen die Überlegenheit der Verum-Gruppen feststellbar war. Die Ansprechraten lagen je nach Dosis zwischen 45,3% und 49,6% (Plazebo 23,0%). Einen HAM-D24-Wert von ≤7 (Vollremission) erreichten nach acht Wochen zwischen 20,9% und 24,5% der Behandelten (Plazebo 11,5%).
Eine weitere sechswöchige, randomisierte, doppelblinde Plazebo-kontrollierte Studie (n=600) prüfte Vortioxetin bei Erwachsenen mit einer schweren Depression im Alter von 18 bis 75 Jahren im ambulanten Setting [26]. Aus der Verum-Gruppe (n=300), die 5 mg Vortioxetin täglich erhalten hatte, beendeten 244 Patienten die Studie. In dieser Untersuchung ließ sich mit dieser Dosierung jedoch kein signifikanter Unterschied im Vergleich zu Plazebo nachweisen.
In der achtwöchigen, Plazebo-kontrollierten Studie von Katona et al. (n=453) wurden die Wirksamkeit, Sicherheit und Verträglichkeit von Vortioxetin (n=156) in einer Dosis von 5 mg/Tag bei Erwachsenen im Alter von ≥65 Jahren mit der Referenzsubstanz Duloxetin (n=151; 60 mg/Tag) anhand der Veränderungen in der Hamilton-Depressionsskala (HAM-D24) verglichen [28]. Hier fanden sich in beiden Behandlungsgruppen nach sechs und nach acht Wochen signifikante Verbesserungen. Aus der Vortioxetin-Gruppe hatten im Beobachtungszeitraum 53,2% auf die Behandlung angesprochen, 29,2% gelangten in eine Vollremission. In der Vergleichsgruppe respondierten 63,3% der Patienten und 34,7% remittierten vollständig. Die Plazebo-Response lag bei 35,2% und die Remission bei 19,3%. Darüber hinaus wurden vermutete kognitive Verbesserungen, die für Duloxetin schon einmal untersucht wurden [53] mit dem Rey Auditory Verbal Learning Test (RAVLT) und dem Digit Symbol Substitution Test (DSST) gemessen. Hier fanden sich in einer Post-hoc-Analyse direkte Behandlungseffekte auf die kognitiven Beeinträchtigungen, die vermutlich unabhängig von den positiven Effekten auf die Depression zu sehen sind und ausgeprägter waren als beim Duloxetin. Während beide Verumgruppen im RAVLT mit Effektstärken von 0,24 bis 0,33 sich signifikant von Plazebo unterschieden, war dies im DSST nur für Vortioxetin der Fall.
Ziel einer weiteren randomisierten, doppelblinden, Plazebo-kontrollierten Untersuchung (n=602) war die Prüfung der Wirksamkeit von Vortioxetin auf kognitive Funktionen bei erwachsenen depressiven Patienten mit Duloxetin als aktiver Referenzsubstanz. Während für Vortioxetin im Vergleich zu Plazebo ein signifikanter Vorteil im DSST gemessen wurde, war dies für Duloxetin nicht der Fall [39].
Eine andere Plazebo-kontrollierte Studie wies eine statistisch signifikante Überlegenheit von Vortioxetin (10–20 mg/Tag) bei depressiven (MADRS ≥26) 18- bis 65-Jährigen in der Verbesserung kognitiver Funktionen nach (primärer Endpunkt), die nicht ausschließlich auf eine Verbesserung der Depression zurückzuführen war, sondern als direkter Effekt von Vortioxetin auf die Kognition angesehen werden kann [42].
Besonders interessant sind auch die Ergebnisse einer doppelblinden, Plazebo-kontrollierten Cross-over-Studie zu kognitiven Funktionen, Psychomotorik und Fahrtauglichkeit, die an 24 gesunden Probanden mit Vortioxetin 10 mg/Tag und Mirtazapin 30 mg/Tag als aktiver Vergleichssubstanz durchgeführt wurde [58]. Beide Antidepressiva wurden an 15 aufeinander folgenden Tagen abends verordnet, worauf an den Tagen 2 und 16 jeweils morgens neuropsychologische Tests durchgeführt wurden. Während die Probanden unter Vortioxetin vergleichbare Testergebnisse aufwiesen wie die Plazebo-Gruppe, waren die Probanden aus der Mirtazapin-Gruppe an Tag 2 in ihrer Kognition, den psychomotorischen Funktionen und in ihrer Fahrtauglichkeit beeinträchtigt. Eine Metaanalyse, die die Ergebnisse von neun Plazebo-kontrollierten Kurzzeitstudien mit mehr als 2000 Verum-behandelten Patienten (Dosis 5–20 mg/Tag) einschließt, zeigt eine gute Wirksamkeit von Vortioxetin, insbesondere im Plazebo-Vergleich bei höherer Dosierung [57].
Langzeitstudien
In einer randomisierten, doppelblinden, Plazebo-kontrollierten Studie zur Rückfallprophylaxe (n=639, Alter 18–75 Jahre, Baseline-MADRS Ø 32,3) erhielten die Patienten zunächst in einer zwölfwöchigen offenen Akutphase 5 mg oder 10 mg Vortioxetin. Zum Ende dieser Akutphase hatten 76% der Patienten auf die Behandlung mit Vortioxetin angesprochen (≥50%ige Verbesserung in der MADRS) und 69% der Patienten hatten eine Vollremission erreicht, das heißt einen MADRS-Wert von ≤10 Punkten. In der sich anschließenden doppelblinden Rückfallverhütungsphase wurden die Patienten (n=400) entweder in derselben Dosis mit Vortioxetin (n=206) oder mit Plazebo (n=194) für 24 bis 64 Wochen weiterbehandelt. Ein Rückfall (Relapse) war definiert als klinischer Wirkungsverlust mit einem MADRS-Wert von ≥22 Punkten. Während in der Plazebo-Gruppe nur 104 Patienten (54,2%) die Studie beendeten und 58 einen Rückfall erlitten, waren es in den beiden Vortioxetin-Gruppen 123 (61,3%), die die Studie beendeten, bei 31 Rückfällen. In der Kaplan-Meier-Analyse zeigte sich, dass das Risiko eines Rückfalls in einem Beobachtungszeitraum von 24 Wochen für die Patienten mit Vortioxetin nur halb so groß war (13%) wie für die Plazebo-Gruppe (26%) (Abb. 3). Zugleich war die Zeit bis zu einer erneuten depressiven Episode signifikant länger (Hazard-Ratio 2,01; p=0,0035). Bei Patienten, die in der zwölfwöchigen Akutphase erfolgreich behandelt werden konnten, hielt die Wirkung auch über weitere 24 Wochen an [10].
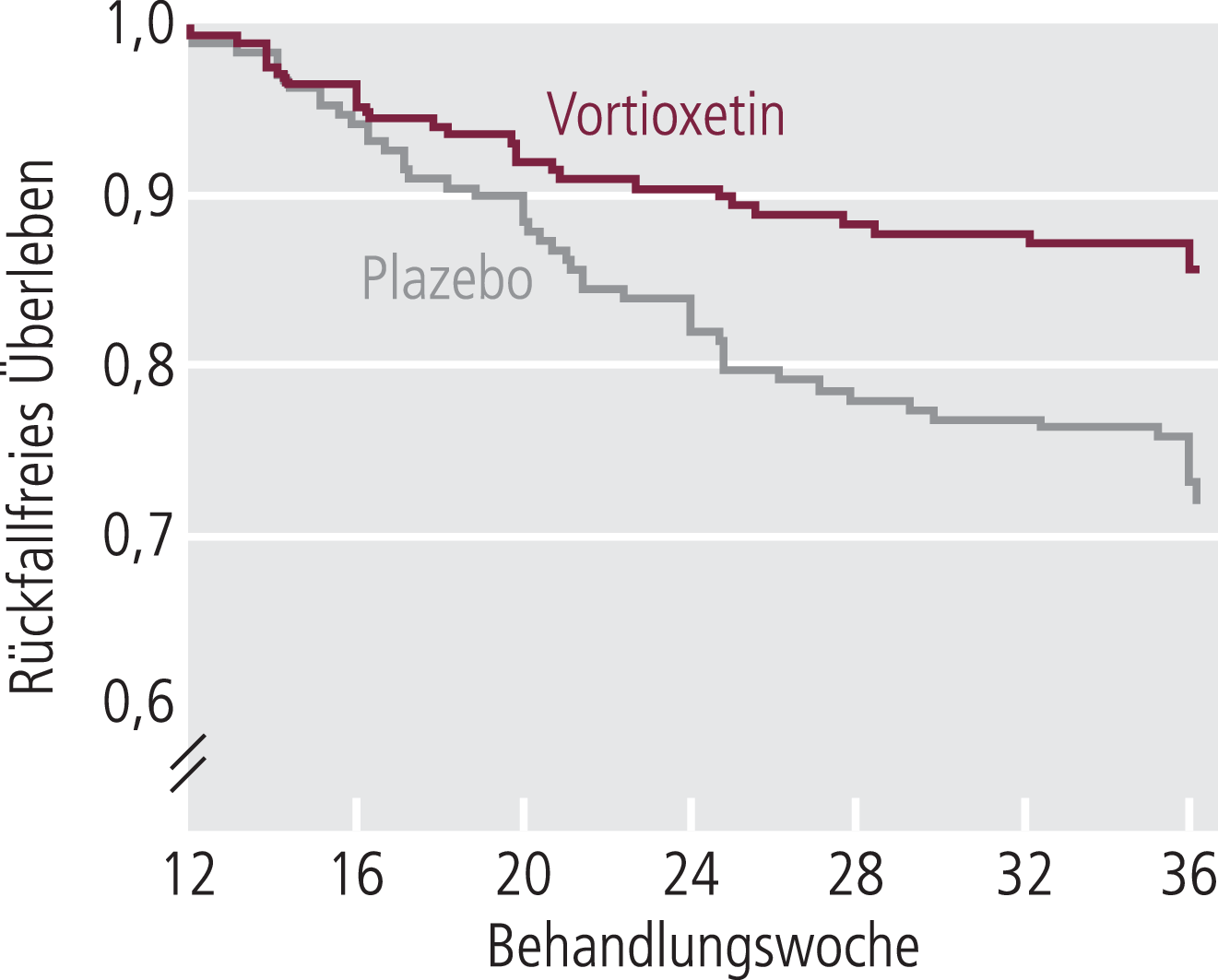
Abb. 3. Kaplan-Meier Überlebensanalyse des Rückfalls über 24 Wochen nach 12-wöchiger offener Behandlungsphase [10]. Die Zeit bis zum Rückfall zeigt signifikante Vorteile für Patienten, die mit Vortioxetin behandelt waren, im Vergleich zu Plazebo (FAS [full anaylsis set], Cox proportional hazard model; p=0,0035).
Unerwünschte Wirkungen
Unerwünschte Ereignisse wurden in allen Studien als mild bis moderat beurteilt. In der Studie von Alvarez et al. trat im Vergleich zu Plazebo Nausea bei beiden Vortioxetin-Gruppen (5 mg: 29,6%; 10 mg: 38,0%) als einziges der 16 erfassten Items hochsignifikant häufiger auf. Schwere unerwünschte Ereignisse wurden unter Plazebo in 4% der Fälle erfasst, unter Vortioxetin 5 mg (3%) und 10 mg (7%) und unter Venlafaxin 12%. In der Venlafaxin-Gruppe waren im Plazebo-Vergleich Nausea (33,6%), Hyperhidrosis (15,0%) und Obstipation (9,7%) signifikant häufiger. Die Quote sexueller Dysfunktionen lag unter Vortioxetin 5 mg und 10 mg auf Plazebo-Niveau, während 12,4% der Behandelten in der Venlafaxin-Gruppe darüber berichteten [2]. Ein ähnliches Resultat zeigte sich in der Studie mit Duloxetin, in der Nausea als einzige unerwünschte Nebenwirkung signifikant häufiger auftrat. Ein Absetzen als Folge von Nebenwirkungen war in Abhängigkeit von der Dosierung in den Vortioxetin-Gruppen bei 6 bis 11% der Behandlungen erforderlich, in der Duloxetin-Gruppe waren es 12% und in der Plazebo-Gruppe 8% [5]. In der Untersuchung von Henigsberg et al. waren Nausea, Kopfschmerzen, Nasopharyngitis und Benommenheit häufigste Nebenwirkungen [19].
Auch in der Langzeitstudie war Nausea bei 8,8% der Betroffenen das einzige unerwünschte Ereignis, das sich signifikant von Plazebo (3,1%) unterschied (Tab. 2). Es wurden keine Absetzphänomene beobachtet, die Abbruchraten betrugen 7,8% unter Vortioxetin und 2,6% unter Plazebo [10]. Sowohl in der offenen zwölfwöchigen Behandlungsperiode (7,7%) als auch in der Langzeitperiode (7,8%) waren die substanzbezogenen Behandlungsunterbrechungen gering.
Tab. 2. Unerwünschte Wirkungen von Vortioxetin in der akuten Behandlungsphase und in der Erhaltungsbehandlung [mod. nach 10]
|
Nebenwirkungen (NW) mit einer Häufigkeit von ≥5% in ≥1 Gruppe [% der Patienten] |
|||
|
Bevorzugte Bezeichnung |
Akute Behandlungsphase (12 Wochen, offen; APTS) |
Rückfallpräventions-Phase (erste 24 Wochen, doppelblind; FAS) |
|
|
Vortioxetin |
Plazebo |
Vortioxetin 5 oder 10 mg (n=204) |
|
|
Patienten mit ≥1 NW |
70,6 |
63,5 |
62,3 |
|
Übelkeit |
25,7 |
3,1 |
8,8* |
|
Kopfschmerzen |
18,3 |
13,0 |
12,3 |
|
Nasopharyngitis |
8,1 |
14,1 |
10,8 |
|
Schwindel |
6,9 |
1,6 |
2,5 |
|
Trockener Mund |
6,4 |
0 |
2,0 |
|
Versehentliche Überdosierung |
5,8 |
7,8 |
7,8 |
|
Insomnie |
5,6 |
0,5 |
1,5 |
|
Erschöpfung |
5,0 |
1,6 |
1,5 |
|
Influenza |
1,1 |
5,2 |
6,9 |
|
Gastroenteritis |
1,9 |
3,1 |
5,4 |
* p<0,05 vs. Plazebo; APTS: all-patients-treated set; FAS: full-analysis set
Sexuelle Dysfunktionen können sowohl im Kontext der depressiven Störung als auch als Folge der Behandlung mit Antidepressiva auftreten. In allen Untersuchungen fand sich eine sehr geringe Inzidenz von sexueller Dysfunktion. In einer achtwöchigen randomisierten, kontrollierten Studie (n=447), in der Vortioxetin (10 oder 20 mg/Tag) mit Escitalopram (10 oder 20 mg/Tag) Head-to-Head im Hinblick auf sexuelle Dysfunktion mit dem CSFQ-14 (Changes in sexual functioning questionnaire short-form) verglichen wurde, war Vortioxetin in allen fünf Dimensionen der CSFQ-14 gegenüber Escitalopram überlegen [24].
In der Studie mit den älteren Patienten zeigte sich wiederum als einzig signifikante Nebenwirkung in 21,8% der Fälle Nausea, während in der Duloxetin-Gruppe neben Nausea auch Mundtrockenheit (21,9%), Obstipation (13,9%) und Schläfrigkeit (10,6%) als signifikante Nebenwirkungen zu verzeichnen waren [28].
Diskussion
Die Depression ist eine chronische, rekurrierende und potenziell lebensbedrohliche Erkrankung, die weltweit bis zu 20% der Bevölkerung betrifft [18, 40, 46] und zu den häufigsten Ursachen für eine erhöhte Morbidität und Mortalität zählt. In der europäischen Erhebung zum Ausmaß und Belastung durch neuropsychiatrische Erkrankungen steht sie mit Abstand an der Spitze [60]. Obgleich die Erkrankung eine hohe Heritabilität aufweist, konnten spezifische Risiko-Gene bislang nicht identifiziert werden. Allerdings stützen große funktionale Studien den Verdacht, dass die Assoziation von genetischen Polymorphismen, die beispielsweise an der Regulation der Stresshormonachse beteiligt sind (z.B. FKPB5 oder HTR2A), mit (früh-)kindlichen Traumata ein erheblich erhöhtes Risiko für eine Depression oder andere affektive Störungen begründet [8, 32, 43]. Obwohl letztlich die Ursache für die psychische Störung, die wir als Depression bezeichnen, ungeklärt ist [21], gibt es große wissenschaftliche Anstrengungen, anhand genetischer und klinischer Befunde die Therapieresponse oder unerwünschte Arzneimittelnebenwirkungen der pharmakologischen Behandlung zu prädizieren [20, 22, 33, 34, 59].
Obwohl weltweit mehr als 50 Substanzen zugelassen sind, die im Rahmen des Zulassungsverfahrens eine antidepressive Wirksamkeit nachgewiesen haben, wird das Ziel einer Vollremission (HAM-D17 ≤7) nach einem ersten Behandlungsversuch nur in etwa 30 bis 40% der Fälle erreicht. Wegen der hohen Quote von Fällen, in denen ein erster medikamentöser Behandlungsversuch, beispielsweise mit monoaminergen Substanzen scheitert und ein Wechsel auf ein anderes Antidepressivum aus derselben Klasse überwiegend ebenfalls erfolglos bleibt [12], kommen verschiedene Switch- oder Augmentierungsstrategien in Betracht, die dann nochmals die Remissionsrate um 20 bis 30 Prozentpunkte auf maximal 70% erhöhen können [55]. So werden häufig Kombinationsbehandlungen, beispielsweise SSRI plus SNRI [9] oder Augmentierungen mit Lithium [7] oder Antipsychotika [45] favorisiert. Man geht davon aus, dass mindestens 30% der behandlungsbedürftigen depressiven Patienten die Kriterien für eine Therapieresistenz erfüllen [35, 47].
Die Tatsache, dass sowohl hochselektive serotonerge und noradrenerge Antidepressiva als auch dual wirksame Substanzen bislang bei einem großen Teil der Betroffenen kein Ansprechen (Response) oder die gewünschte nachhaltige Symptomsuppression (Remission) zur Folge haben, begründet das wissenschaftliche Interesse an multimodalen Substanzen. Vor allem besteht die Erfordernis, nicht nur die affektiven Symptome zu behandeln, sondern insbesondere auch kognitive Dysfunktionen oder depressionsassoziierte Schmerzen. Gleichzeitig muss das Antidepressivum auch eine gute Verträglichkeit besonders im Hinblick auf sexuelle Nebenwirkungen oder Gewicht aufweisen und sicher sein, beispielsweise hinsichtlich der kardialen Funktion. Angesichts dieser unerfüllten klinischen Bedürfnisse wuchs das Interesse daran, Substanzen zu entwickeln, die unter verschiedenen Wirksamkeitsaspekten potenter sein könnten.
Es besteht allgemein Konsens darüber, dass eine Serotonin-Rezeptorbesetzung von etwa 80% durch SSRI oder SNRI zu therapeutischen Effekten führt. Mit Vortioxetin steht nun ein neuartiges, „multimodales“ Antidepressivum zur Verfügung, das die Wiederaufnahme am Serotonin-, Dopamin- und Noradrenalintransporter hemmt und gleichzeitig an G-Protein-Rezeptoren, beispielsweise 5-HT1A, 5-HT1B/D, 5-HT7, und an Ionen-Kanal-Rezeptoren wie 5-HT3 agiert. Da für Vortioxetin eine klinische Wirksamkeit bereits bei einer Rezeptorbesetzung von etwa 50% nachgewiesen werden konnte, wird als eine mögliche Erklärung dafür die Multimodalität dieser Substanz diskutiert [3]. Die Ergebnisse der bisher vorliegenden Studien haben im Vergleich zu Plazebo, aber auch im direkten Vergleich mit etablierten Antidepressiva, wie Agomelatin, eine gute Wirksamkeit in der Behandlung depressiver Episoden nachgewiesen. In den Akutstudien lag die Number needed to treat (NNT) im Vergleich zu Plazebo für das Ansprechen auf die Therapie bei 7 (95%-KI 6–9) und für die Remission bei 11 (95%-KI 8–17). Die Number needed to harm (NNH) für eine Therapieunterbrechung wegen unerwünschter Nebenwirkungen betrug 36 (95%-KI 24–70) [15]. Möglicherweise hat die Substanz aufgrund des besonderen Rezeptorprofils mit einem substanziellen 5-HT3-Antagonismus und der potenziellen Einflussnahme auf Glutamat Eigenschaften, die beeindruckende Hinweise für die Verbesserung kognitiver Dysfunktionen im Rahmen einer Depression zeigen, das heißt einer Verbesserung von Aufmerksamkeit, Lern- und Exekutivfunktionen und Gedächtnisleistung. Vortioxetin weist als Nebenwirkungen Übelkeit (Nausea) und Kopfschmerzen auf, die Verträglichkeit ist aufgrund der aktuellen Datenlage besonders im Hinblick auf sexuelle Nebenwirkungen und weitgehend fehlende Gewichtszunahme günstig.
Interessenkonflikterklärung
TM hat Honorare für die Beratung oder Teilnahme an einem Expertenbeirat sowie Vortragshonorare von Janssen-Cilag, Lundbeck, Otsuka und Trommsdorff erhalten. TM bzw. die Einrichtung, die er vertritt, haben Forschungsbeihilfe durch das MARS-Projekt des MPI und sonstige Unterstützung von Janssen-Cilag, Lilly und Otsuka erhalten.
CG ist Mitarbeiter von Lundbeck.
Vortioxetine – a multimodal antidepressant
Under the trade name Brintellix®, vortioxetine, a novel antidepressant, has been approved for the European market in December 2013. The active substance is assigned to the class of the so-called multimodal antidepressants, because it interacts with various serotonin receptors and also inhibits the serotonin transporter. Placebo-controlled, double-blind short- and long-term studies, some with active reference substance, provided evidence for a good antidepressant efficacy, tolerability and safety. Particularly advantageous are the data for vortioxetine regarding the low incidence of adverse side effects and regarding the improvement of cognitive disorders in the context of depression.
Key words: Depression, antidepressants, multimodal
Literatur
1. Adell A. Lu-AA21004, a multimodal serotonergic agent, for the potential treatment of depression and anxiety. IDrugs 2010;13:900–10.
2. Alvarez E, Perez V, Dragheim M, Loft H, et al. A double-blind, randomized, placebo-controlled, active reference study of Lu AA21004 in patients with major depressive disorder. Int J Neuropsychopharmacol 2012;15:589–600.
3. Areberg J, Luntang-Jensen M, Sogaard B, Nilausen DO. Occupancy of the serotonin transporter after administration of Lu AA21004 and its relation to plasma concentration in healthy subjects. Basic Clin Pharmacol Toxicol 2012;110:401–4.
4. Areberg J, Sogaard B, Hojer AM. The clinical pharmacokinetics of Lu AA21004 and its major metabolite in healthy young volunteers. Basic Clin Pharmacol Toxicol 2012;111:198–205.
5. Baldwin DS, Loft H, Dragheim M. A randomised, double-blind, placebo controlled, duloxetine-referenced, fixed-dose study of three dosages of Lu AA21004 in acute treatment of major depressive disorder (MDD). Eur Neuropsychopharmacol 2012;22:482–91.
6. Bang-Andersen B, Ruhland T, Jorgensen M, Smith G, et al. Discovery of 1-[2-(2,4-dimethylphenylsulfanyl)phenyl]piperazine (Lu AA21004): a novel multimodal compound for the treatment of major depressive disorder. J Med Chem 2011;54:3206–21.
7. Bauer M, Adli M, Bschor T, Pilhatsch M, et al. Lithium‘s emerging role in the treatment of refractory major depressive episodes: augmentation of antidepressants. Neuropsychobiology 2010;62:36–42.
8. Binder EB, Salyakina D, Lichtner P, Wochnik GM, et al. Polymorphisms in FKBP5 are associated with increased recurrence of depressive episodes and rapid response to antidepressant treatment. Nat Genet 2004;36:1319–25.
9. Blier P, Ward HE, Tremblay P, Laberge L, et al. Combination of antidepressant medications from treatment initiation for major depressive disorder: a double-blind randomized study. Am J Psychiatry 2010M;167:281–8.
10. Boulenger JP, Loft H, Florea I. A randomized clinical study of Lu AA21004 in the prevention of relapse in patients with major depressive disorder. J Psychopharmacol 2012;26:1408–16.
11. Boulenger JP, Loft H, Olsen CK. Efficacy and safety of vortioxetine (Lu AA21004), 15 and 20 mg/day: a randomized, double-blind, placebo-controlled, duloxetine-referenced study in the acute treatment of adult patients with major depressive disorder. Int Clin Psychopharmacol 2014;29:138–49.
12. Bschor T, Baethge C. No evidence for switching the antidepressant: systematic review and meta-analysis of RCTs of a common therapeutic strategy. Acta Psychiatr Scand 2010;121:174–9.
13. Busch MA, Maske UE, Ryl L, Schlack R, et al. [Prevalence of depressive symptoms and diagnosed depression among adults in Germany: results of the German Health Interview and Examination Survey for Adults (DEGS1)]. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz 2013;56:733–9.
14. Chen G, Lee R, Hojer AM, Buchbjerg JK, et al. Pharmacokinetic drug interactions involving vortioxetine (Lu AA21004), a multimodal antidepressant. Clin Drug Investig 2013;33:727–36.
15. Citrome L. Vortioxetine for major depressive disorder: a systematic review of the efficacy and safety profile for this newly approved antidepressant – what is the number needed to treat, number needed to harm and likelihood to be helped or harmed? Int J Clin Pract 2014;68:60–82.
16. Godard J, Baruch P, Grondin S, Lafleur MF. Psychosocial and neurocognitive functioning in unipolar and bipolar depression: a 12-month prospective study. Psychiatry Res 2012;196:145–53.
17. Häggström L, Nielsen RZ, Dragheim M. (2013) A randomised, double-blind, active controlled study of vortioxetine (10–20 mg/d) versus agomelatine (25–50 mg/d) in adults with major depressive disorder with inadequate response to antidepressant treatment. Poster P.2.f.029 presented at the 26th ECNP Congress, Barcelona, Spain 5–9 October 2013.
18. Hasler G, Drevets WC, Manji HK, Charney DS. Discovering endophenotypes for major depression. Neuropsychopharmacology 2004;29:1765–81.
19. Henigsberg N, Mahableshwarkar AR, Jacobsen P, Chen Y, et al. A randomized, double-blind, placebo-controlled 8-week trial of the efficacy and tolerability of multiple doses of Lu AA21004 in adults with major depressive disorder. J Clin Psychiatry 2012;73:953–9.
20. Hennings JM, Owashi T, Binder EB, Horstmann S, et al. Clinical characteristics and treatment outcome in a representative sample of depressed inpatients – findings from the Munich Antidepressant Response Signature (MARS) project. J Psychiatr Res 2009;43:215–29.
21. Holsboer F. [The future of depression research]. Nervenarzt 2010;81:1306, 1308,1309–1306,12, Passim.
22. Ising M, Lucae S, Binder EB, Bettecken T, et al. A genomewide association study points to multiple loci that predict antidepressant drug treatment outcome in depression. Arch Gen Psychiatry 2009;66:966–75.
23. Jacobi F, Hofler M, Meister W, Wittchen HU. [Prevalence, detection and prescribing behavior in depressive syndromes. A German federal family physician study]. Nervenarzt 2002;73:651–8.
24. Jacobsen P, Mahableshwarkar A, Chen Y, Chrones L, et al. A randomized, double-blind, head-to-head, flexible-dose study of vortioxetine vs escitalopram on sexual functioning in adults with well-treated major depressive disorder experiencing treatment-emergent sexual dysfunction. Poster presented on CINP, Vancouver 2014.
25 Jacobsen PL, Mahableshwarkar AR, Serenko M, Chan S, Trivedi MH. A randomized, double-blind, placebo-controlled study of the efficacy and safety of vortioxetine 10 mg and 20 mg in adults with major depressive disorder. Poster NR9-06 presented at the 166th American Psychiatric Association Annual Meeting, San Francisco, California, USA, 18–22 May, 2013.
26. Jain R, Mahableshwarkar AR, Jacobsen PL, Chen Y, et al. A randomized, double-blind, placebo-controlled 6-week trial of the efficacy and tolerability of 5 mg vortioxetine in adults with major depressive disorder. Int J Neuropsychopharmacol 2013;16:313–21.
27. Judd LL, Schettler PJ, Solomon DA, Maser JD, et al. Psychosocial disability and work role function compared across the long-term course of bipolar I, bipolar II and unipolar major depressive disorders. J Affect Disord 2008;108:49–58.
28. Katona C, Hansen T, Olsen CK. A randomized, double-blind, placebo-controlled, duloxetine-referenced, fixed-dose study comparing the efficacy and safety of Lu AA21004 in elderly patients with major depressive disorder. Int Clin Psychopharmacol 2012;27:215–23.
29. Kennedy N, Foy K, Sherazi R, McDonough M, et al. Long-term social functioning after depression treated by psychiatrists: a review. Bipolar Disord 2007;9:25–37.
30. Kessler RC, Berglund P, Demler O, Jin R, et al. The epidemiology of major depressive disorder: results from the National Comorbidity Survey Replication (NCS-R). JAMA 2003;289:3095–105.
31. Kessler RC, Birnbaum H, Bromet E, Hwang I, et al. Age differences in major depression: results from the National Comorbidity Survey Replication (NCS-R). Psychol Med 2010;40:225–37.
32. Klengel T, Binder EB. Gene-environment interactions in major depressive disorder. Can J Psychiatry 2013;58:76–83.
33. Licinio J, Wong ML. Pharmacogenomics of antidepressant treatment effects. Dialogues Clin Neurosci 2011;13:63–71.
34. Lucae S, Ising M, Horstmann S, Baune BT, et al. HTR2A gene variation is involved in antidepressant treatment response. Eur Neuropsychopharmacol 2010;20:65–8.
35. Maalouf FT, Atwi M, Brent DA. Treatment-resistant depression in adolescents: review and updates on clinical management. Depress Anxiety 2011;28:946–54.
36. Mahableshwarkar AR, Jacobsen PL, Chen Y. A randomized, double-blind trial of 2.5 mg and 5 mg vortioxetine (Lu AA21004) versus placebo for 8 weeks in adults with major depressive disorder. Curr Med Res Opin 2013; 29:217–26.
37. Mahableshwarkar AR, Jacobsen PL, Serenko M, Chen Y, Trivedi MH. A duloxetine-referenced, fixed-dose study comparing efficacy and safety of 2 vortioxetine doses in the acute treatment of adult MDD patients. Poster NR9-01 presented at the 166th American Psychiatric Association Annual Meeting, San Francisco, California, USA, 18–22 May, 2013.
38. Mahableshwarkar AR, Jacobsen PL, Serenko M, Chen Y, Trivedi MH. A randomized, double-blind, parallelgroup, placebo-controlled, fixed-dose study comparing the efficacy and safety of 2 doses of vortioxetine (Lu AA21004) in acute treatment of adults with major depressive disorder. Poster NR9-02 presented at the 166th American Psychiatric Association Annual Meeting, San Francisco, California, USA, 18–22 May, 2013.
39. Mahableshwarkar A, Zajecka J, Jacobson W, Chen Y, et al. Efficacy of vortioxetine on cognitive function in adult patients with major depressive disorder: results of a randomized, double-blind, active-referenced, placebo-controlled trial. Poster presented on CINP, Vancouver 2014.
40. Manji HK, Drevets WC, Charney DS. The cellular neurobiology of depression. Nat Med 2001;7:541–7.
41. Marazziti D, Consoli G, Picchetti M, Carlini M, et al. Cognitive impairment in major depression. Eur J Pharmacol 2010;626:83–6.
42. McIntyre R, Lophaven S, Olsen CK. Randomized, double-blind, placebo-controlled study of the efficacy of vortioxetine on cognitive function in adult patients with major depressive disorder (MDD). Int J Neuropsychopharmacology 2014. E-pub 30 April 2014.
43. Menke A, Klengel T, Rubel J, Bruckl T, et al. Genetic variation in FKBP5 associated with the extent of stress hormone dysregulation in major depression. Genes Brain Behav 2013;12:289–96.
44. Mork A, Pehrson A, Brennum LT, Nielsen SM, et al. Pharmacological effects of Lu AA21004: a novel multimodal compound for the treatment of major depressive disorder. J Pharmacol Exp Ther 2012;340:666–75.
45. Nelson JC, Papakostas GI. Atypical antipsychotic augmentation in major depressive disorder: a meta-analysis of placebo-controlled randomized trials. Am J Psychiatry 2009;166:980–91.
46. Nestler EJ, Barrot M, DiLeone RJ, Eisch AJ, et al. Neurobiology of depression. Neuron 2002;34:13–25.
47. Nierenberg AA, Katz J, Fava M. A critical overview of the pharmacologic management of treatment-resistant depression. Psychiatr Clin North Am 2007;30:13–29.
48. Nutt DJ. Beyond psychoanaleptics – can we improve antidepressant drug nomenclature? J Psychopharmacol 2009;23:343–5.
49. Paykel ES. Depression: major problem for public health. Epidemiol Psychiatr Soc 2006,15:4–10
50. Paykel ES. Cognitive therapy in relapse prevention in depression. Int J Neuropsychopharmacol 2007;10:131–6.
51. Paykel ES, Brugha T, Fryers T. Size and burden of depressive disorders in Europe. Eur Neuropsychopharmacol 2005;15:411–23.
52. Pehrson AL, Cremers T, Betry C, van der Hart MG, et al. Lu AA21004, a novel multimodal antidepressant, produces regionally selective increases of multiple neurotransmitters – a rat microdialysis and electrophysiology study. Eur Neuropsychopharmacol 2013;23:133–45.
53. Raskin J, Wiltse CG, Siegal A, Sheikh J, et al. Efficacy of duloxetine on cognition, depression, and pain in elderly patients with major depressive disorder: an 8-week, double-blind, placebo-controlled trial. Am J Psychiatry 2007;164:900–9.
54. Reischies FM, Neu P. Comorbidity of mild cognitive disorder and depression – a neuropsychological analysis. Eur Arch Psychiatry Clin Neurosci 2000;250:186–93.
55. Rush AJ, Trivedi MH, Wisniewski SR, Nierenberg AA, et al. Acute and longer-term outcomes in depressed outpatients requiring one or several treatment steps: a STAR*D report. Am J Psychiatry 2006;163:1905–17.
56. Solomon DA, Keller MB, Leon AC, Mueller TI, et al. Multiple recurrences of major depressive disorder. Am J Psychiatry 2000;157:229–33.
57. Thase ME, Mahableshwarkar AR, Dragheim M, Loft H. The efficacy of vortioxetine versus placebo in the treatment of adults with major depressive disorder: Data from 10 short-term studies and a meta-analysis. 52nd Annual Meeting of the American College of Neuropsychopharmacology (ACNP), Hollywood, FL, December 8–12, 2013.
58. Theunissen EL, Street D, Hojer AM, Vermeeren A, et al. A randomized trial on the acute and steady-state effects of a new antidepressant, vortioxetine (Lu AA21004), on actual driving and cognition. Clin Pharmacol Ther 2013;93:493–501.
59. Uhr M, Tontsch A, Namendorf C, Ripke S, et al. Polymorphisms in the drug transporter gene ABCB1 predict antidepressant treatment response in depression. Neuron 2008;57:203–9.
60. Wittchen HU, Jacobi F, Rehm J, Gustavsson A, et al. The size and burden of mental disorders and other disorders of the brain in Europe 2010. Eur Neuropsychopharmacol 2011;21:655–79.
61. Wittchen HU, Pittrow D. Prevalence, recognition and management of depression in primary care in Germany: the Depression 2000 study. Hum Psychopharmacol 2002;17(Suppl 1):S1–11.
Priv.-Doz. Dr. med. Thomas Messer, Danuvius Klinik GmbH, Krankenhausstraße 68, 85276 Pfaffenhofen an der Ilm, E-Mail: thomas.messer@danuviusklinik.de
Dr. med Christoph Goemann, Lundbeck GmbH, Ericusspitze 2, 20457 Hamburg, E-Mail: goem@lundbeck.com
Psychopharmakotherapie 2014; 21(04)
