Markus Schwarz, München, und Christoph Hiemke, Mainz
Der Kostendruck, der in der medizinischen Versorgung immer stärker spürbar wird, hat zur Folge, dass für jede Untersuchung die Indikationsstellung sehr viel kritischer hinterfragt wird als noch vor einigen Jahren. Therapeutisches Drug-Monitoring (TDM), welches häufig als reines Messen der Arzneistoffspiegel im Blut oder anderen Körperflüssigkeiten angesehen wird, wird in Deutschland je nach angewandter Methode und nach Gebührenordnungen mit 21 bis 60 Euro abgerechnet [19]. Verschiedene Untersuchungen haben ein erhebliches Einsparpotenzial durch TDM bei antidepressiver Pharmakotherapie nachgewiesen. Simmons und Mitarbeiter fanden eine verkürzte Zeit bis zur Wiedererlangung der Arbeitsfähigkeit [24], Bengtsson und Mitarbeiter [1, 15, 16] eine Reduktion von Arzneimittelkosten und Ostad Haji und Mitarbeiter [19, 20] eine verkürzte Verweildauer im Krankenhaus. Für das Antipsychotikum Clozapin wurde nachgewiesen, dass ein Absinken oder eine ausgeprägte intraindividuelle Streuung der Blutspiegel einen Rückfall [6] bzw. eine stationäre Wiederaufnahme [25] prädizieren. Trotz dieses offensichtlichen Einsparpotenzials wird TDM häufig aus Kostenüberlegungen auf wenige Indikationen beschränkt, etwa die Überwachung der Lithium-Therapie zur Vermeidung von Intoxikationen. TDM geht jedoch weit über das reine Bestimmen der Arzneistoffkonzentrationen im Blut zur Vermeidung von Intoxikationen hinaus. Ein TDM-Befund, der immer einer pharmakologischen Interpretation bedarf [3, 10, 11], liefert dem behandelnden Arzt wichtige Hinweise für die Therapieoptimierung. Letztlich dient TDM sowohl der Arzneimittelsicherheit als auch der Verbesserung des Ansprechens. Besonders bedeutsam sind dabei die Überprüfung der Zuverlässigkeit der Medikamenteneinnahme (Compliance-Kontrolle) und die Aufklärung pharmakokinetischer Besonderheiten.
Ziel von TDM ist die Optimierung der Psychopharmakotherapie jedes einzelnen Patienten. TDM ist damit in der Psychiatrie die bisher einzige Methode der personalisierten Medizin. Um mit TDM einen maximalen Nutzen zu erzielen, muss allerdings eine klare Indikation für die Messung eines Blutspiegels gegeben sein und das Verfahren muss korrekt angewandt werden. Typische Indikationen für die Risikominimierung sind in Tabelle 1 angegeben.
Tab. 1. Indikationen für TDM zur Risikominimierung der Psychopharmakotherapie
|
Vermeidung von Intoxikationen bei Arzneimitteln mit enger therapeutischer Breite, z.B. Lithium, Clozapin oder trizyklische Antidepressiva |
|
Unerwünschte Arzneimittelwirkung bei empfohlener Dosis |
|
Kombination von Arzneistoffen mit Wechselwirkungspotenzial |
|
Verdacht auf unzuverlässige Einnahme der Arzneimittel, unzureichende Adhärenz |
|
TDM in Pharmakovigilanzprogrammen |
|
Rückfallprävention unter Erhaltungstherapie |
|
Rezidiv unter Erhaltungstherapie bei empfohlener Dosis |
|
Genetische Besonderheit im Arzneistoffmetabolismus |
|
Schwangere oder stillende Patientin |
|
Patient im Kindes- oder Jugendalter (bis 18 Jahre) |
|
Alterspatient (>65 Jahre) |
|
Patient mit verminderter Intelligenz |
|
Patient mit pharmakokinetisch relevanter Komorbidität |
|
Forensischer Patient |
Zusammengestellt nach den Leitlinien der TDM-Gruppe der AGNP (Arbeitsgemeinschaft für Neuropsychopharmakologie und Pharmakopsychiatrie) [10, 11]; TDM: Therapeutisches Drug-Monitoring
2004 wurden von der interdisziplinären TDM-Gruppe der Arbeitsgemeinschaft für Neuropsychopharmakologie und Pharmakopsychiatrie (AGNP) Leitlinien für TDM in der Psychiatrie publiziert [2]. Sie wurden 2011 umfassend überarbeitet [10] und in verschiedene Sprachen, darunter auch Deutsch übersetzt [11]. Die englischen und die deutschen Leitlinien können kostenfrei im Internet heruntergeladen werden (www.ppt-online.de oder www.agnp.de). Das Labor muss eine validierte Methode einsetzen und über einen Zeitraum von zwei Arbeitstagen Ergebnisse mit ausreichender Präzision und Richtigkeit erzeugen. Durch obligate externe Kontrollen (Teilnahme an Ringversuchen) wird erreicht, dass unterschiedliche Labore vergleichbare Werte erzielen. Für die Beurteilung des Befundes sind vollständige Angaben auf dem Anforderungsschein notwendig. Wichtig sind Angaben zur Höhe und Verteilung der täglichen Dosis des Medikaments sowie sämtlicher weiterer Medikamente, die der Patient einnimmt. Weiterhin sollten Angaben zu pharmakokinetisch relevanten besonderen Umständen oder Erkrankungen gemacht werden. In aller Regel (Ausnahme sind Nebenwirkungen) sollte der Steady-State erreicht sein (mindestens 4 Halbwertszeiten des Arzneistoffs), und die Blutentnahme sollte im Talspiegel erfolgen.
Der therapeutische Referenzbereich
Eine wesentliche Zielgröße für eine TDM-geleitete Pharmakotherapie ist der therapeutische Referenzbereich (therapeutisches Fenster). Wenn der Arzneistoffspiegel innerhalb des therapeutischen Referenzbereichs liegt, ist mit höchster Wahrscheinlichkeit mit therapeutischem Ansprechen bei gleichzeitig guter Verträglichkeit zu rechnen. Liegt der Messwert unterhalb des Bereichs, so ist in der Akuteinstellung damit zu rechnen, dass sich die Arzneimittelwirkung nicht von der durch Plazebo unterscheidet. In der Erhaltungstherapie besteht das Risiko eines Rückfalls. Liegen die Arzneistoffkonzentrationen oberhalb des Referenzbereichs, so ist ein erhöhtes Risiko für Unverträglichkeitsprobleme anzunehmen. Bei Medikamenten mit großer therapeutischer Breite, wie den meisten selektiven Serotonin-Wiederaufnahmehemmern (SSRI) [12], besteht bei Überschreitung des Referenzbereichs zwar nur ein geringfügig erhöhtes Risiko für Unverträglichkeit, aber es ist davon auszugehen, dass der Patient eine höhere Dosis einnimmt, als notwendig wäre, und damit unnötige Kosten entstehen. Der therapeutische Referenzbereich ist eine erste Orientierungsgröße. Im Einzelfall kann die individuell optimale Plasmakonzentration auch außerhalb dieses Bereichs liegen. Um den individuell optimalen Blutspiegel zu ermitteln, ist es sinnvoll, eine Blutspiegelmessung durchzuführen, wenn sich ein Patient klinisch deutlich gebessert hat [6].
Der Grund für einen Blutspiegel oberhalb (Risiko: Unverträglichkeit/Intoxikation) oder unterhalb (Risiko: Wirkverlust) des therapeutischen Referenzbereichs kann eine pharmakokinetische Besonderheit sein, die zu einer verminderten oder beschleunigten Clearance des Arzneimittels geführt hat. Bei der Feststellung toxischer Blutspiegel, die oberhalb der Warnschwelle für das Labor liegen, die von der TDM-Gruppe der AGNP neu eingeführt wurde [10, 11], können pharmakokinetische Interaktionen oder pharmakogenetische Auffälligkeiten zugrunde liegen. TDM gibt hier rasch und einfach den oft entscheidenden Hinweis.
Der dosisbezogene Referenzbereich
Zu hohe oder zu niedrige Wirkspiegel können aber auch einfach dadurch verursacht werden, dass eine zu hohe oder zu niedrige Dosis eingenommen wurde. Daher ist es wichtig zu prüfen, ob der gemessene Arzneistoffspiegel (CSS) zur Dosis passt [7]. Im Steady-State korreliert der Blutspiegel mit der Dosis (D), dem Dosierungsintervall (τ), der Bioverfügbarkeit (F) und der Gesamtclearance (CL):
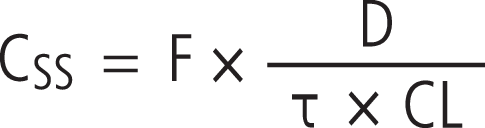
Der durch die Tagesdosis (D / τ) korrigierte Blutspiegel eines Patienten im Steady-State (τ × CSS/D) ist ein Maß für seine individuelle Bioverfügbarkeit und Clearance (τ × CSS/D = F/CL). Es handelt sich um einen einfach zu berechnenden Wert, da Daten zur Bioverfügbarkeit und Clearance aus pharmakokinetischen Untersuchungen für gesunde Probanden oder Patienten vorliegen [7]. Wie man den dosisbezogenen Referenzbereich ausrechnen kann, ist in den aktuellen Konsensus-Leitlinien beschrieben [10, 11]. Innerhalb des Bereichs sollte τ × CSS/D liegen, wenn das Arzneimittel in der verordneten Dosis und zur angegebenen Zeit eingenommen wurde, und das Blut zu Zeiten minimaler Wirkstoffkonzentrationen abgenommen wurde (Talspiegel). Abweichungen vom Normalbereich sind Hinweise auf pharmakokinetische Besonderheiten oder Compliance-Probleme, denen nachgegangen werden sollte. Wenn keine Talspiegel vorliegen, weil beispielsweise die Tagesdosis einmal abends eingenommen wird und morgens Blut abgenommen wurde, dann muss der zu erwartende dosiskorrigierte Talspiegel errechnet werden. Dies ist leicht möglich, wenn man die Dosis, das Dosierungsschema und den Zeitpunkt der Blutabnahme kennt. Von einem Labor, welches TDM anbietet, ist zu fordern, dass es in der Lage ist, solche einfachen pharmakokinetischen Berechnungen durchzuführen.
Miterfassung von Arzneistoffmetaboliten
Um pharmakokinetische Besonderheiten zu erkennen, ist es auch wichtig, Metaboliten des zu überwachenden Arzneimittels zu bestimmen, unabhängig davon, ob diese pharmakologisch aktiv sind oder nicht. Das Verhältnis der Konzentrationen von Metabolit zu Muttersubstanz (Metabolic Ratio, MR) ist ein direktes Maß für die Verstoffwechselung eines Medikaments. Wenn der Abbau bevorzugt über ein distinktes Enzym erfolgt, dann ist das MR ein Maß für die In-vivo-Aktivität dieses Enzyms. Ein MR, das deutlich vom Normalwert abweicht, ist ein Hinweis auf eine genetische Besonderheit oder eine Wechselwirkung [8, 10, 11]. Für Venlafaxin wurde beispielsweise nachgewiesen, dass aus dem MR von O-Desmethylvenlafaxin zu Venlafaxin auf die Aktivität des Cytochrom-P450-Isoenzyms (CYP)2D6 geschlossen werden kann [9, 23]; für Risperidon aus dem MR von 9-Hydroxyrisperidon zu Risperidon [5]. Bei auffälligen MR ist immer auch an eine partielle Non-Compliance zu denken [16, 22].
Praktische Anwendung von TDM
Die Durchführung von TDM ist in den Konsensus-Leitlinien der AGNP beschrieben [10, 11]. Welche Bedingungen dazu einzuhalten sind, ist in Tabelle 2 zusammenfassend dargestellt.
Tab. 2. Einzuhaltende Bedingungen bei Anwendung von TDM in der Psychiatrie
|
Steady-State sollte erreicht sein (Ausnahme Auftreten von Nebenwirkungen), d.h. mindestens 4 Eliminationshalbwertszeiten |
|
Blutentnahme sollte im Talspiegel (üblicherweise vor der ersten Medikamenteneinnahme des Tages) vorgenommen werden |
|
Im Anforderungsschein für das Labor sind Angaben zu Dosis, Dosierungsintervall und Zeitpunkte der letzten Medikamenteneinnahme und der Blutentnahme sowie Komedikation für die Befundinterpretation erforderlich |
|
Zusätzliche Einflüsse wie Zigarettenkonsum oder andere pharmakokinetisch relevante Besonderheiten sollten angegeben werden |
|
Einsatz validierter Methoden mit interner und externer Qualitätskontrolle |
|
Mitteilung der Laborbefunde innerhalb von 48 Stunden nach Eintreffen der Blutprobe |
|
Pharmakologische Befundkommentierung mit Angabe der Referenzbereiche, Hinweisen auf festgestellte oder potenzielle Arzneimittelwechselwirkungen |
|
Bei Bedarf Dosierungsempfehlung |
|
Berechnung der Talspiegel, wenn die Blutprobe nicht zur Zeit minimaler Konzentrationen entnommen wurde |
Neben Blutentnahme zur falschen Zeit oder Nichtbeachtung von Besonderheiten, wie Instabilität der Wirkstoffe nach Blutentnahme oder lange Halbwertszeit, gibt es viele Gründe, die zu fehlerhaften Schlussfolgerungen für die pharmakologische Weiterbehandlung führen können und damit den Patienten sogar gefährden können [17, 18, 27]. Wenn beispielsweise die Blutentnahme vor Erreichen des Steady-State erfolgt, ein niedriger Spiegel gemessen wurde, eine Dosiserhöhung empfohlen und vorgenommen wird, so kann dies zu einer Intoxikation führen.
Individualisierte Risikominimierung durch Anwendung von TDM
Die folgenden Einzelfälle sind Beispiele aus der Anwendung von TDM für die individualisierte Psychopharmakotherapie. Sie zeigen, wie TDM zur Risikominimierung der psychiatrischen und auch nichtpsychiatrischen Pharmakotherapie beitragen kann.
Quetiapin und Clarithromycin – Risiko Intoxikation durch Wechselwirkung
Eine 40-jährige Patientin leidet unter einer paranoiden Schizophrenie und ist zur ersten stationär-psychiatrischen Aufnahme in der Klinik, wo sie seit Wochen mit einer stabilen Dosis von 350 mg/Tag Quetiapin behandelt wird. Nach initialer mittelgradiger Somnolenz zeigt sie ein sehr gutes Ansprechen bei guter Verträglichkeit. Die wöchentlich kontrollierte Serumkonzentration des Quetiapin liegt stabil in einem Bereich zwischen 87 und 102 ng/ml, zuletzt 93 ng/ml (empfohlener therapeutischer Bereich: 100–500 ng/ml; dosisbezogener Referenzbereich: 100–212 ng/ml). Von einem Tag auf den anderen entwickelt die Patientin eine starke, geradezu narkolepsieartige Somnolenz. Das am nächsten Morgen im sicheren Talspiegel durchgeführte TDM zeigt eine Serumkonzentration von 649 ng/ml, was im Vergleich zum Vorwert einer etwa siebenfachen Erhöhung des Quetiapin-Spiegels entspricht und die unerwünschten Arzneimittelwirkungen (UAW) erklärt. Die Recherche ergibt, dass der wegen einer akuten bakteriellen Infektion hinzugerufene Konsiliarius drei Tage vor dem Ereignis Clarithromycin, ein Makrolidantibiotikum, verschrieben hatte. Makrolide sind starke Inhibitoren des Cytochrom-P450-Isoenzyms 3A4/5, welches hauptsächlich für die Verstoffwechselung des Quetiapins verantwortlich ist. Nach Reduktion der Dosis auf 150 mg/Tag normalisierte sich der Quetiapin-Spiegel und die Patientin litt nicht mehr unter der Somnolenz. Im Anschluss an das Absetzen des Makrolids wurde innerhalb von zehn Tagen wieder auf die ursprüngliche Dosis erhöht und die Serumkonzentrationen lagen nach Erreichen des Steady-State wieder zwischen 90 und 100 ng/ml.
Das Beispiel zeigt, dass TDM in der Lage ist eine Wechselwirkung zu erkennen, und darüber hinaus auch geeignet ist, eine gefährliche Kombination, die wegen des Wechselwirkungsrisikos kontraindiziert ist, TDM-geleitet sicher anzuwenden.
Olanzapin – Risiko Rückfall durch mangelhafte Compliance
Ein 32-jähriger Patient mit paranoider Schizophrenie wird im Rahmen seines insgesamt zweiten stationär-psychiatrischen Aufenthalts auf eine medikamentöse Therapie mit 25 mg/Tag Olanzapin eingestellt. Nach Erreichen der Zieldosis liegen über mehrere Wochen hinweg die Medikamentenspiegel stabil bei 49,4 bis 53,6 ng/ml Olanzapin (therapeutischer Referenzbereich 20–80 ng/ml) und 7,0 bis 11,6 ng/ml Desmethylolanzapin; das MR liegt also im für einen Nichtraucher erwarteten Bereich von 0,1 bis 0,3. Der Patient wird schließlich deutlich gebessert entlassen und bei unveränderter Medikation ambulant weiter betreut. Nach etwa zehn Wochen zeigt sich eine zunehmende Verschlechterung der Symptomatik. Das TDM ergibt keine nachweisbaren Spiegel des nach wie vor verschriebenen Olanzapin – ein klarer Hinweis für die Non-Compliance des Patienten. Der Patient wird über die Problematik aufgeklärt, und er verspricht, künftig das verschriebene Antipsychotikum regelmäßig einzunehmen. Beim nächsten Untersuchungszeitpunkt wird wieder TDM durchgeführt und es zeigt sich ein unüblich hoher Olanzapin-Spiegel von 86 ng/ml bei kaum nachweisbarem Desmethylolanzapin (1,4 ng/ml) – wiederum ein deutlicher Hinweis auf partielle Non-Compliance. Diesmal wurde offenbar kurz vor dem Ambulanztermin das Medikament einmalig eingenommen.
Dieses Beispiel illustriert nicht nur, wie hilfreich das TDM beim Erkennen der Non-Compliance ist, sondern auch, wie sinnvoll die gleichzeitige Bestimmung des Hauptmetaboliten ist, denn ohne diese Bestimmung wäre beim zweiten Termin die Non-Compliance unentdeckt geblieben. Durch Ergänzung der für TDM üblichen Einzelblutentnahmen um 2 bis 4 Blutentnahmen im Tagesverlauf kann sehr genau das Adhärenzverhalten nachvollzogen werden [26].
Venlafaxin – Risiko genetische Besonderheit
Eine 63-jährige Patientin mit einer rezidivierenden depressiven Störung leidet gegenwärtig an einer schweren Episode ohne psychotische Symptome und wird bereits seit einigen Wochen ambulant mit 225 mg/Tag Venlafaxin behandelt. Nach stationär-psychiatrischer Aufnahme wird bei unveränderter Dosis TDM durchgeführt. Es fällt das unüblich niedrige Verhältnis von 0,2 zwischen dem Metaboliten O-Desmethylvenlafaxin (67 ng/ml) und der Muttersubstanz Venlafaxin (331 ng/ml) auf, wobei die Summe mit 398 ng/ml im oberen Bereich des empfohlenen therapeutischen Bereiches von 100 bis 400 ng/ml liegt. Das Verhältnis (MR) von O-Desmethylvenlafaxin zur Muttersubstanz Venlafaxin liegt üblicherweise zwischen 0,3 und 5,2 [10, 11]. Das TDM-Labor empfiehlt daraufhin, im sicheren Talspiegel die Blutentnahme zu wiederholen, um auszuschließen, dass der Befund durch eine Medikamenteneinnahme kurz vor der Blutentnahme verfälscht war. Einige Tage später wird kontrolliert vor der morgendlichen Medikamenteneinnahme Blut für TDM abgenommen. Es zeigt sich ein Venlafaxin-Spiegel von 339 ng/ml bei einem Metabolitenspiegel von 73 ng/ml; das MR von 0,2 bestätigt sich damit. In der Summe ergibt sich ein Spiegel, der den empfohlenen therapeutischen Bereich nur marginal übersteigt. Bei Venlafaxin gilt zu beachten, dass der pharmakologisch aktive Metabolit O-Desmethylvenlafaxin verträglicher zu sein scheint als die Muttersubstanz [9, 23]. Das TDM-Labor empfiehlt die Genotypisierung des CYP2D6-Gens, welche den Verdacht auf Poor-Metabolizer-Status bestätigt [13]. Aus den sich daraus ergebenden möglichen Vorgehensweisen, eine Dosisanpassung durchzuführen oder auf ein anderes Medikament umzustellen, wählt der behandelnde Psychiater letztere Alternative.
Das Beispiel zeigt, dass TDM geeignet ist, einen Hinweis auf einen genetisch bedingten Enzymdefekt zu erhalten. Aus dem Befund ergibt sich für den Patienten die Konsequenz, dass Medikamente, die bevorzugt über CYP2D6 abgebaut werden (z.B. Metoprolol, Tolterodin oder Nortriptylin) zwecks Risikominimierung vermieden oder unter strenger TDM-Kontrolle angepasst werden sollten.
Interaktion Bupropion und Tamoxifen – Risiko Therapiegefährdung
Eine 52-jährige Patientin wird im Anschluss an die operative Entfernung eines Mammakarzinoms mit Tamoxifen behandelt. Im weiteren Verlauf entwickelt sie eine behandlungsbedürftige Depression, welche zunächst mit 150 mg/Tag Venlafaxin behandelt wird. Nach Erreichen des Steady-State hat die Patientin einen Venlafaxin-Spiegel von 58 ng/ml und einen O-Desmethylvenlafaxin-Spiegel von 282 ng/ml (Summe: 340 ng/ml, Verhältnis Metabolit : Muttersubstanz, MR =4,9); zwei Wochen später liegen die Spiegel bei gleicher Dosierung in etwa unverändert bei 64 und 310 (Summe 347) ng/ml (MR 4,8). Da diese Monotherapie nicht erfolgreich ist, wird ihr neben Venlafaxin auch Bupropion in einer Dosis von 300 mg/Tag verschrieben. Bei der Anforderung des TDM zwei Wochen später fällt ein deutlicher Anstieg der Venlafaxin-Spiegel auf 243 ng/ml bei 343 ng/ml O- Desmethylvenlafaxin auf (MR 1,4). Die Summe von 586 ng/ml liegt nun deutlich über dem empfohlenen therapeutischen Bereich; das MR hat sich auf 1,4 reduziert. Bupropion ist ein starker Inhibitor des Enzyms CYP2D6, welches für die Verstoffwechselung von Venlafaxin zuständig ist, was die deutlich angestiegenen Venlafaxin-Spiegel erklärt.
Bei der Befundung fällt im TDM-Labor weiterhin die Kombination von Bupropion und Tamoxifen auf. Tamoxifen selbst ist nur die inaktive Vorstufe des eigentlich pharmakologisch aktiven Endoxifen, welches durch Metabolisierung des Tamoxifen über CYP2D6 erfolgt. Da Bupropion ein starker CYP2D6-Inhibitor ist, hemmt es die „Aktivierung“ des Prodrugs Tamoxifen. In diesem Falle traten keine für den behandelnden Arzt sichtbaren UAW auf, aber durch Bupropion wurde die onkologische Therapie maßgeblich beeinträchtigt. Im Anschluss an die pharmakologische Beratung durch das Labor wurde anstelle von Bupropion Mirtazapin, welches keine Interaktion mit CYP2D6 aufweist, verschrieben und damit die Effizienz der onkologischen Therapie wieder sichergestellt. Auch die Venlafaxin-Spiegel stellten sich unter dieser Kombination wieder auf die zuvor gemessenen Werte ein. Dieses Beispiel zeigt, wie wichtig die pharmakokinetische Beurteilung der gesamten Medikamentenkombination eines Patienten ist.
Fazit für die Praxis
Therapeutisches Drug-Monitoring (TDM) ist die praktische Anwendung von pharmakokinetischem Wissen für die Therapie. Es ist ein Instrument zur Verbesserung von Effizienz und Sicherheit einer medikamentösen Therapie. In der Psychiatrie ist es derzeit die einzige Methode der individualisierten Medizin [4, 13, 21]. Am Beispiel von Einzelfällen wurde dargestellt, wie die Anwendung von TDM in der Psychiatrie individualisiert zur Risikominimierung beitragen kann. Um maximalen Nutzen für den Einzelpatienten zu erzielen, ist insbesondere bei widersprüchlich erscheinenden Befunden ein interdisziplinärer Austausch notwendig. Die Leitlinien der AGNP [10, 11] liefern Sachinformationen, in erster Linie pharmakokinetisch relevante Daten, für die Problemlösung. Durch Einbeziehung patientenspezifischer Informationen ergibt sich eine solide Wissensbasis für eine rationale risikominimierende Psychopharmakotherapie.
Literatur
1. Akerblad AC, Bengtsson F, Holgersson M, von Knorring L, Ekselius L. Identification of primary care patients at risk of non-adherence to antidepressant treatment. Patient Prefer Adherence 2008;2:379–86.
2. Baumann P, Hiemke C, Ulrich S, Eckermann G, et al. Arbeitsgemeinschaft für Neuropsychopharmakologie und Pharmakopsychiatrie. The AGNP-TDM expert group consensus guidelines: therapeutic drug monitoring in psychiatry. Pharmacopsychiatry 2004;37:243–65.
3. Bengtsson, F. Therapeutic drug monitoring of psychotropic drugs. TDM “nouveau”. Ther Drug Monit 2004;26,145–51.
4. de Leon J. The future (or lack of future) of personalized prescription in psychiatry. Pharmacol Res 2009;59:81–9.
5. de Leon J, Wynn G, Sandson NB. The pharmacokinetics of paliperidone versus risperidone. Psychosomatics, 2010;51:80–8.
6. Gaertner I, Gaertner HJ, Vonthein R, Dietz K. Therapeutic drug monitoring of clozapine in relapse prevention: a five-year prospective study. J Clin Psychopharmacol 2001;21:305–10.
7. Haen E, Greiner C, Bader W, Wittmann M. Wirkstoffkonzentrationsbestimmungen zur Therapieleitung Ergänzung therapeutischer Referenzbereiche durch dosisbezogene Referenzbereiche. Nervenarzt 2008;79:558–66.
8. Hendset M, Haslemo T, Rudberg I, Refsum H, et al. The complexity of active metabolites in therapeutic drug monitoring of psychotropic drugs. Pharmacopsychiatry 2006;39:121–7.
9. Hermann M, Hendset M, Fosaas K, Hjerpset M, et al. Serum concentrations of venlafaxine and its metabolites O-desmethylvenlafaxine and N-desmethylvenlafaxine in heterozygous carriers of the CYP2D6*3, *4 or *5 allele. Eur J Clin Pharmacol 2008;64:483–7.
10. Hiemke C, Baumann P, Bergemann N, Conca A, et al. AGNP consensus guidelines for therapeutic drug monitoring in psychiatry: update 2011. Pharmacopsychiatry 2011;44:195–235.
11. Hiemke C, Baumann P, Bergemann N, Conca A, et al. AGNP-Konsensus-Leitlinien für therapeutisches Drug-Monitoring in der Psychiatry: update 2011. Phsychopharmakotherapie 2012;19:195–235.
12. Isbister GK, Bowe SJ, Dawson A, Whyte IM. Relative toxicity of selective serotonin reuptake inhibitors (SSRIs) in overdose. J Toxicol Clin Toxicol 2004;42:277–85
13. Jaquenoud Sirot E, van der Velden JW, Rentsch K, Eap CB, et al. Therapeutic drug monitoring and pharmacogenetic tests as tools in pharmacovigilance. Drug Saf 2006;29:735–68.
14. Laib K, Brünen S, Pfeifer P, Vincent P, et al. Serum concentrations of hydroxybupropion for dose optimization of depressed patients treated with bupropion. Ther Drug Monit 2013; im Druck.
15. Lundmark J, Bengtsson F, Nordin C, Reis M, et al. Therapeutic drug monitoring of selective serotonin reuptake inhibitors influences clinical dosing strategies and reduces drug costs in depressed elderly patients. Acta Psychiatr Scand 2000;101:354–9.
16. Lundmark J, Reis M, Bengtsson F. Therapeutic drug monitoring of sertraline: variability factors as displayed in a clinical setting. Ther Drug Monit 2000;22:446–54.
17. Mann K, Hiemke C, Schmidt LG, Bates DW. Appropriateness of therapeutic drug monitoring for antidepressants in routine psychiatric inpatient care. Ther Drug Monit 2006;28:83–8.
18. Müller MJ, Dragicevic A, Fric M, Gaertner I, et al. Therapeutic drug monitoring of tricyclic antidepressants: how does it work under clinical conditions? Pharmacopsychiatry 2003;36:98–104.
19. Ostad Haji E, Mann K, Dragicevic A, Müller MJ, et al. Potential cost-effectiveness of therapeutic drug monitoring for depressed patients treated with citalopram. Ther Drug Monit 2013;35:396–401.
20. Ostad Haji E, Tadic A, Wagner S, Dragicevic A, et al. Association between citalopram serum levels and clinical improvement of patients with major depression. J Clin Psychopharmacol 2011;31:281–6.
21. Pfuhlmann B, Gerlach M, Burger R, Gonska S, et al. Therapeutic drug monitoring of tricyclic antidepressants in everyday clinical practice. J Neural Transm 2007;(Suppl 72):287–96.
22. Reis M, Aberg-Wistedt A, Agren H, Akerblad AC, et al. Compliance with SSRI medication during 6 months of treatment for major depression: an evaluation by determination of repeated serum drug concentrations. J Affect Disord 2004;82:443–6.
23. Shams ME, Arneth B, Hiemke C, Dragicevic A, et al. CYP2D6 polymorphism and clinical effect of the antidepressant venlafaxine. J Clin Pharm Ther 2006;31:493–502.
24. Simmons SA, Perry PJ, Rickert ED, Browne JL. Cost-benefit analysis of prospective pharmacokinetic dosing of nortriptyline in depressed inpatients. J Affect Disord 1985;8:47–53.
25. Stieffenhofer V, Saglam H, Schmidtmann I, Silver H, et al. Clozapine plasma level monitoring for prediction of rehospitalization schizophrenic outpatients. Pharmacopsychiatry 2011;44:55–9.
26. Stieffenhofer V, Hiemke C. Pharmakogenetik, therapeutisches Drug-Monitoring und Non-Compliance. Ther Umsch 2010;67:309–15.
27. Vuille F, Amey M, Baumann P. Use of plasma level monitoring of antidepressants in clinical practice. Towards an analysis of clinical utility. Pharmacopsychiatry 1991;24:190–5.
Prof. Dr. med. Markus Schwarz, Institut für Laboratoriumsmedizin, Klinikum der Universität München, Marchioninistraße 15, 81377 München, E-Mail: Markus.Schwarz@med.uni-muenchen.de
Prof. Dr.rer.nat. Christoph Hiemke, Klinik für Psychiatrie und Psychotherapie, Universitätsmedizin Mainz, Untere Zahlbacher Straße 8, 55131 Mainz
Therapeutic drug monitoring for individualized risk reduction of psychopharmacotherapy
Therapeutic drug monitoring (TDM), which includes measurement of medication concentrations and interpretation of the results, is a valuable tool for tailoring the dosage of a prescribed medication to the individual characteristics of a patient. Uncertain drug adherence, tolerability problems, non-response to therapeutic doses or drug-drug interactions under polypharmacy are typical situations when TDM is helpful for problem solving and risk reduction. Individuals that may predominantly benefit from TDM in psychiatry are elderly patients or patients with known or suspected genetically determined pharmacokinetic abnormalities or individuals with pharmacokinetically relevant comorbidities. Here we present typical cases to demonstrate how TDM may be used in psychiatry for individualized risk reduction.
Key words: Therapeutic drug monitoring, pharmacokinetics, psychorpharmacological treatment, drug safety
Psychopharmakotherapie 2013; 20(04)
