Dr. Ellen Jahn, Bad Homburg
Der rekombinante, monoklonale Antikörper Alemtuzumab, der bis vor Kurzem unter dem Handelsnamen MabCampath zur Behandlung von Patienten mit chronisch-lympatischer B-Zell-Leukämie eingesetzt wurde, gilt für viele als „Hoffnungsträger“ für die Therapie der multiplen Sklerose. Seine Wirkung beruht auf einer gezielten Depletion von Immunzellen: Alemtuzumab bindet an das Oberflächenprotein CD52, das besonders stark auf zirkulierenden B- und T-Lymphozyten exprimiert ist. Nach Bindung des Antikörpers werden diese Zellen relativ rasch zerstört. Damit sind die Immunzellen dieses Typs erst einmal aus dem Blutkreislauf entfernt. Das Immunsystem erholt sich zwar innerhalb eines Jahres, aber dabei wird es nicht 1:1 wiederhergestellt, sondern rekonditioniert. So scheint sich die mit der multiplen Sklerose (MS) einhergehende Imbalance zwischen autoreaktiven T-Effektorzellen und regulatorischen T-Zellen (Treg) zugunsten der Treg zu verschieben [1].
Geringere Behinderungszunahme und weniger Schübe in Phase II
Die klinische Prüfung von Alemtuzumab wird vor allem deshalb mit Spannung verfolgt, weil die bisherigen Studienergebnisse eine Verlangsamung der Behinderungsprogression erkennen lassen. So zeigte sich bereits in der Phase-II-Studie CAMMS223 (Campath in multiple sclerosis) [2] eine beeindruckende Wirkung auf das Fortschreiten der Behinderung. In diese Studie wurden 334 nicht vorbehandelte Patienten mit früher schubförmiger MS eingeschlossen. Die Teilnehmer wurden randomisiert über drei Jahre mit Alemtuzumab (12 oder 24 mg/Tag i.v. jährlich an 5 bzw. 3 aufeinander folgenden Tagen) oder Interferon beta-1a (Rebif®, 44 μg s.c. 3-mal wöchentlich) behandelt. Unter Alemtuzumab war das Risiko einer über sechs Monate anhaltenden Behinderungsprogression (gemessen anhand der Expanded disability status scale [EDSS]) um rund 70% niedriger als in der Kontrollgruppe. Zudem war die Zahl der Schübe unter dem Antikörper um 75% signifikant gegenüber der Interferon-Therapie verringert.
Wirksamkeit in Phase III bestätigt
Die Ergebnisse dieser Studie wurden in zwei randomisierten, doppelblinden Phase-III-Studien (CARE-MS I und II, Comparison of alemtuzumab and Rebif® efficacy in multiple sclerosis) bestätigt.
An der zweijährigen CARE-MS-I-Studie nahmen 581 therapienaive Patienten (mittleres Alter 33 Jahre) mit einer mittleren Krankheitsdauer von 1,7 Jahren und einer geringgradigen Behinderung (mittlerer EDSS-Score 2,0) teil [3]. Sie wurden mit Alemtuzumab (12 mg/Tag an Tag 1–5 im ersten Jahr und an Tag 1–3 im zweiten Jahr) oder Interferon beta-1a (44 μg s.c. 3-mal wöchentlich) behandelt.
Unter der Antikörpertherapie zeigte sich eine signifikant niedrigere adjustierte jährliche Schubrate (0,18 vs. 0,39; p<0,0001; Abb. 1): Gegenüber dem aktiven Komparator reduzierte Alemtuzumab die Schubrate noch einmal um etwa die Hälfte, was angesichts des frühen Krankheitsstadiums einen großen Therapieerfolg darstellt. Der Anteil der Patienten mit einer über sechs Monate anhaltenden Behinderungsprogression (EDSS) war im Alemtuzumab-Arm mit 8% ebenfalls geringer als im Interferon-Arm (11%; p=0,22).
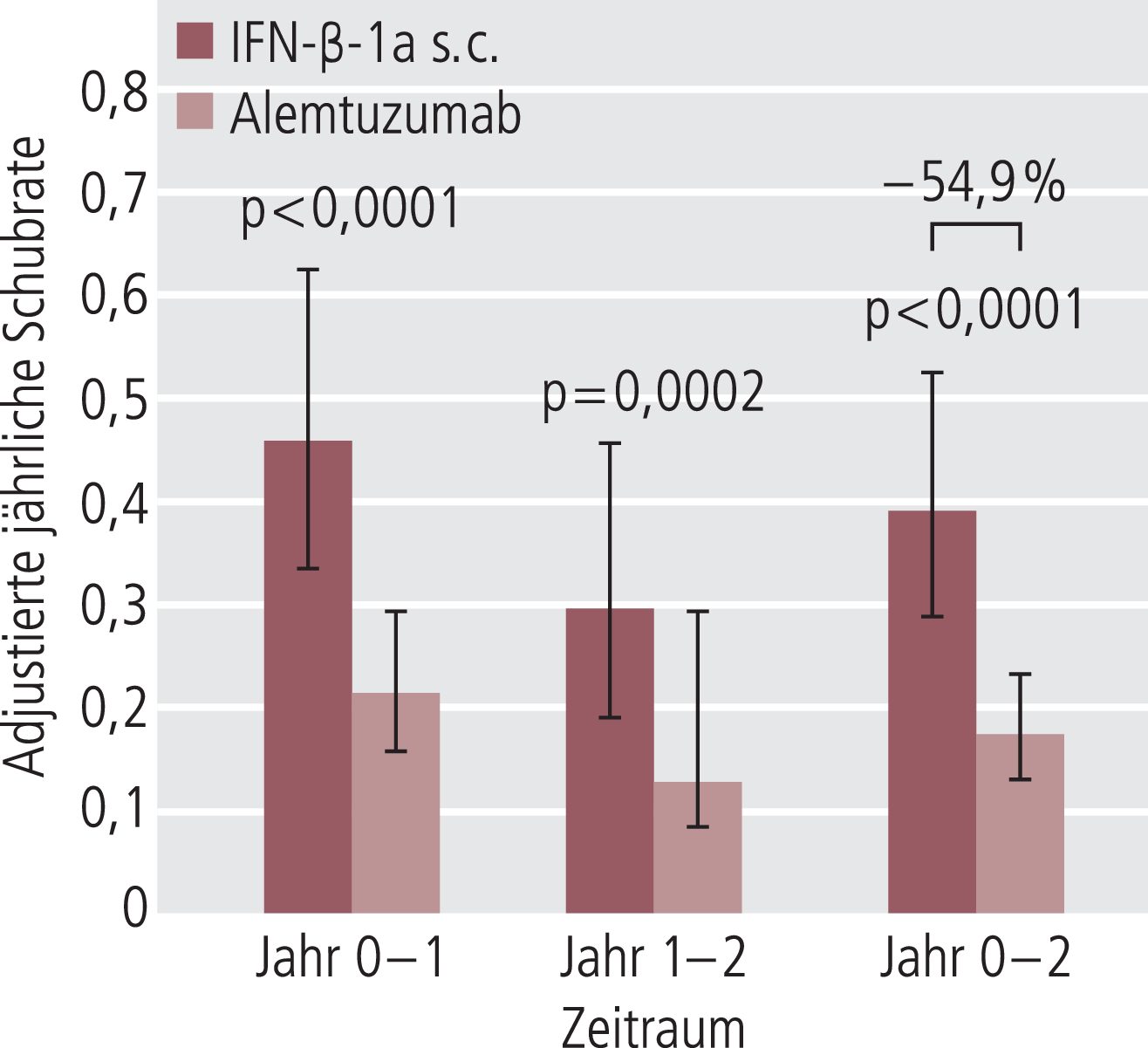
Abb. 1. In der zweijährigen Phase-III-Studie CARE-MS-I senkte Alemtuzumab (i.v. in jährlichen Zyklen zu 12 mg/Tag an 3–5 Tagen) die adjustierte jährliche Schubrate signifikant gegenüber Interferon beta-1a (44 mg s.c. 3-mal wöchentlich) [3]
Die Wirksamkeit des Antikörpers spiegelte sich auch in verschiedenen Surrogat-Parametern wider. So war der Anteil der Patienten mit Gadolinium-aufnehmenden Herden in der Alemtuzumab-Gruppe signifikant geringer als in der Kontroll-Gruppe (27% vs. 15,4%, p = 0,0008). Die Atrophie des Gehirns wurde anhand der Brain Parenchymal Fraction in der Magnetresonanztomographie beurteilt: Hier zeigte sich unter Alemtuzumab eine signifikant geringere Abnahme als unter dem Interferon (–0,87 vs. –1,49; p<0,0001).
Wirksamkeit nach Therapieversagen
Dass Alemtuzumab auch bei Patienten wirkt, die unter einer Ersttherapie bereits einen neuen Schub erlitten haben, zeigen die Daten der CARE-MS-II-Studie: In diese Studie wurden 840 Patienten aufgenommen, die im Mittel seit 3,8 Jahren erkrankt waren und einen mittleren EDSS-Score von 2,7 aufwiesen. Alle Teilnehmer hatten unter einer vorhergehenden Behandlung bereits einen Schub erlitten. Sie wurden wie in der CARE-MS-I- Studie mit Interferon beta-1a oder Alemtuzumab behandelt.
Unter Alemtuzumab verringerte sich die jährliche Schubrate über zwei Jahre um 49% gegenüber dem Interferon (p<0,0001). Gleichzeitig sank das Risiko für eine über sechs Monate anhaltende Behinderungsprogression, gemessen anhand der EDSS, unter dem Antikörper signifikant um 42% gegenüber der Vergleichstherapie (p=0,0084) [4].
Wie sicher ist die Behandlung?
In allen drei Studien traten unter Alemtuzumab leichte bis mäßige Infusionsreaktionen auf, die durch eine Prämedikation und eine symptomorientierte Behandlung gut zu beherrschen waren.
In der CARE-MS-I-Studie waren schwere unerwünschte Ereignisse im Alemtuzumab-Arm nicht signifikant häufiger als im Interferon-Arm (18 vs. 14%), sie führten jedoch seltener zum Behandlungsabbruch als in der Interferon-Gruppe. Infektionen waren in beiden Gruppen häufige unerwünschte Ereignisse, wobei die Inzidenz in der Alemtuzumab-Gruppe höher war als in der Kontrollgruppe (67 vs. 46%). Behandlungsbedingte lebensbedrohliche oder tödliche Infektionen traten in keiner Gruppe auf.
Ausblick
Erste Langzeitdaten lassen erkennen, dass viele Patienten, denen Alemtuzumab in zwei aufeinander folgenden Jahren appliziert wurde, vier Jahre nach der letzten Infusion noch stabil waren, also weniger Schübe und geringere Behinderungsprogression aufwiesen, ohne weitere Infusionszyklen zu benötigen [5]. Alemtuzumab könnte somit das potenteste Therapieprinzip sein, das sich zurzeit in der klinischen Prüfung befindet.
Vieles spricht dafür, dass die Substanz in frühen Krankheitsstadien besonders wirksam ist. Um den Patienten optimal zu helfen, wäre demnach eine frühzeitige Therapie mit Alemtuzumab sinnvoll. Wichtig ist dabei aber ein engmaschiges Monitoring, denn schwerwiegende Ereignisse wie eine thrombozytopenische Purpura oder eine Autoimmunthyreoiditis, die in den Studien bei weniger als 5% der Behandelten auftraten, können durch Laborkontrollen frühzeitig erkannt und so gegebenenfalls rechtzeitig behandelt werden.
Die europäische Zulassung wurde beantragt, eine Entscheidung der European Medicines Agency (EMA) wird 2013 erwartet. Für den Einsatz in der Praxis empfiehlt es sich, zu Patienten, die mit dem neuen Arzneimittel behandelt werden, eine enge Patientenbindung aufzubauen und einen Patientenvertrag abzuschließen, der beispielsweise Blutbildkontrollen im Abstand von zwei Monaten beinhaltet.
Quellen
Priv.-Doz. Dr. med. Mathias Mäurer, Bad Mergentheim, Prof. Dr. med. Heinz Wiendl, Münster, Prof. Dr. med. Peter Rieckmann, Würzburg. Presse-Workshop „Teriflunomid und Alemtuzumab: Neue Perspektiven in der MS-Therapie“, Frankfurt, 21. März 2012, veranstaltet von Genzyme/Sanofi.
1. Klotz L, et al. Immune mechanisms of new therapeutic strategies in multiple sclerosis – A focus on alemtuzumab. Clin Immunol 2012;142:25–30.
2. CAMMS223 Trial Investigators, Coles AJ, et al. Alemtuzumab vs. interferon beta-1a in early multiple sclerosis. N Engl J Med 2008;359:1786–801.
3. Coles AJ, et al. Efficacy and safety results from CARE-MS I: A phase 3 study comparing alemtuzumab and interferon beta-1a ECTRIMS/ACTRIMS Amsterdam, 19.–22. Oktober 2011, P151.
4. Genzyme: Genzyme gibt erfolgreiche Ergebnisse der Phase-III-Studie zu Alemtuzumab bei Multipler Sklerose bekannt. Presseinformation 14. November 2011.
5. Boyko A, et al. Alemtuzumab’s durable efficacy in multiple sclerosis four years after last treatment cycle. ECTRIMS/ACTRIMS Amsterdam, 19.–22. Oktober 2011, P931.
Psychopharmakotherapie 2012; 19(06)
