Priv.-Doz. Dr. Dieter Angersbach, Wolfratshausen
Psychische Symptome, wie Wahnvorstellungen oder Halluzinationen, und Verhaltensauffälligkeiten, wie Aggression und Agitation, treten bei der Alzheimer-Erkrankung häufig auf. Zur Behandlung werden Substanzen unterschiedlicher pharmakologischer Klassen eingesetzt, wie Antidepressiva, Tranquilizer oder Antipsychotika. Die meisten der Studien mit atypischen Antipsychotika waren Kurzzeitstudien mit oft geringem Behandlungserfolg. Die kognitiven Effekte dieser Substanzen wurden aber weitgehend in Schizophreniestudien untersucht.
Mit Alzheimer-Patienten liegen zwei Plazebo-kontrollierte Studien vor, in denen jedoch nur wenige kognitive Tests angewendet wurden und in denen die Patienten keine Verhaltensprobleme hatten: In einer 12-wöchigen Studie wurde eine Verschlechterung auf der MMSE von 0,73 Punkten und in einer 26-wöchigen Studie eine Verschlechterung auf der ADASCog um 4 Punkte gefunden. Die vorliegende Studie (Clinical antipsychotic trials of intervention effectiveness – Alzheimer’s disease study; CATIE – AD) hatte das Ziel, die Effekte atypischer Antipsychotika im Vergleich zu Plazebo auf die kognitiven Funktionen von Patienten mit einer Alzheimer-Erkrankung und Wahnvorstellungen oder aggressivem/agitiertem Verhalten über einen Zeitraum von neun Monaten zu untersuchen.
Studiendesign
Eingeschlossen wurden Patienten mit der Diagnose einer Demenz vom Alzheimer-Typ nach DSM-IV. Weitere Einschlusskriterien waren unter anderen: ambulante Patienten, die zu Hause oder in einem Heim leben; MMSE-Score von 5 bis 26; nahezu täglich Wahnvorstellungen, Halluzinationen, Agitation oder Aggression; ein Score von ≥4 (wenigstens mäßig schwer) bei einem der Items „Zerfall des Denkprozesses“, „Misstrauen, paranoide Inhalte“ oder „Halluzinationen“ der BPRS. Ausgeschlossen waren Patienten, die ein Antidepressivum oder Antikonvulsivum zur Stimmungsstabilisierung einnahmen. Die Einnahme eines Cholinesterasehemmers war erlaubt.
Die 36-wöchige Studienperiode enthielt bis zu vier mögliche Phasen: In Phase 1, beginnend mit dem Einschluss, wurden die Patienten randomisiert einer doppelblinden Behandlung mit Olanzapin, Quetiapin, Risperidon oder Plazebo zugeteilt (Randomisierungsverhältnis 2:2:2:3). Wenn in dieser Phase das zugewiesene Medikament abgesetzt wurde, konnte der Patient in die Phase 2 oder in Phase 4 (offene Behandlung nach Wahl des Arztes) wechseln. In Phase 2 erhielten die Patienten, die bisher ein Antipsychotikum eingenommen hatten, eine doppelblinde Behandlung mit einem der beiden anderen Antipsychotika oder mit Citalopram (3:3:2). Patienten, die in Phase 1 Plazebo erhalten hatten, wurden in Phase 2 randomisiert einer doppelblinden Behandlung mit Citalopram oder einem der Antipsychotika zugeteilt (3:1:1:1).
Nach dem Absetzen der Behandlung in Phase 2 konnte der Patient in der Phase 3 weiterbehandelt werden und erhielt dort in einer offenen Behandlung randomisiert ein Antipsychotikum aus der Studienmedikation, das er bisher noch nicht eingenommen hatte.
Die kognitiven Effekte der Behandlung wurden unter anderen mithilfe folgender Tests beurteilt: MMSE, ADASCog, ADAS-Subskalen „Konzentration/Ablenkbarkeit“, „Zahlen durchstreichen“ und „Arbeitsgedächtnis“, semantischer Sprachkompetenz-Test; Finger-Tapping-Test mit der bevorzugten und der nicht bevorzugten Hand, Trail-Making-Test (Teil A). Die Ergebnisse aller Tests wurden in einem kognitiven Summenscore zusammengefasst. Dazu wurden die Testwerte in einen angepassten z-Score umgewandelt. Eine Abnahme des z-Scores bedeutet in allen Tests eine Abnahme der kognitiven Funktion.
Weiterhin wurde aus den Items „Zerfall des Denkprozesses“ und „Desorientierung“ der BPRS ein kognitiver Dysfunktionsfaktor berechnet, der aber nicht in den kognitiven Summenscore einging.
Ergebnisse
Patienten: Von den 357 Patienten, die ausgewertet werden konnten, erreichten 342 Patienten Woche 12, 320 Patienten Woche 24 und 307 Patienten Woche 36. Das mittlere Alter aller Teilnehmer war 77,6 Jahre und die mittlere Ausbildungsdauer 12,3 Jahre; 64% der Patienten nahmen Cholinesterasehemmer.
Kognitive Funktion. Während der 36-wöchigen Studienperiode zeigte sich eine signifikante Abnahme der kognitiven Fähigkeiten in den meisten Tests (MMSE, ADASCog, ADAS „Konzentration/Ablenkbarkeit“, ADAS „Zahlen durchstreichen“, beide Finger-Tapping-Tests, Trail-Making-Test und kognitiver Summenscore) und dem kognitiven Dysfunktionsfaktor der BPRS. Für einen 77,6 Jahre alten Mann mit einer Ausbildungsdauer von 12,3 Jahren (statistische Mittel der Stichprobe) wurden folgende Abnahmen über 36 Wochen berechnet: der MMSE-Score fiel von 15,6 auf 13,2; der ADASCog-Score verschlechterte sich von 34,2 auf 38,6; der kognitive Summenscore ging von –0,06 auf –0,46 zurück und der kognitive Dysfunktionsfaktor der BPRS verschlechterte sich von 4,6 auf 5,0.
Abbildung 1 zeigt die Abnahme des z-Scores für diese Tests bei der Gesamtpopulation. Der Rückgang des MMSE-, ADASCog- und Summenscores war stärker als der des BPRS-Dysfunktionsfaktors, der mehr das Verhalten beurteilt.
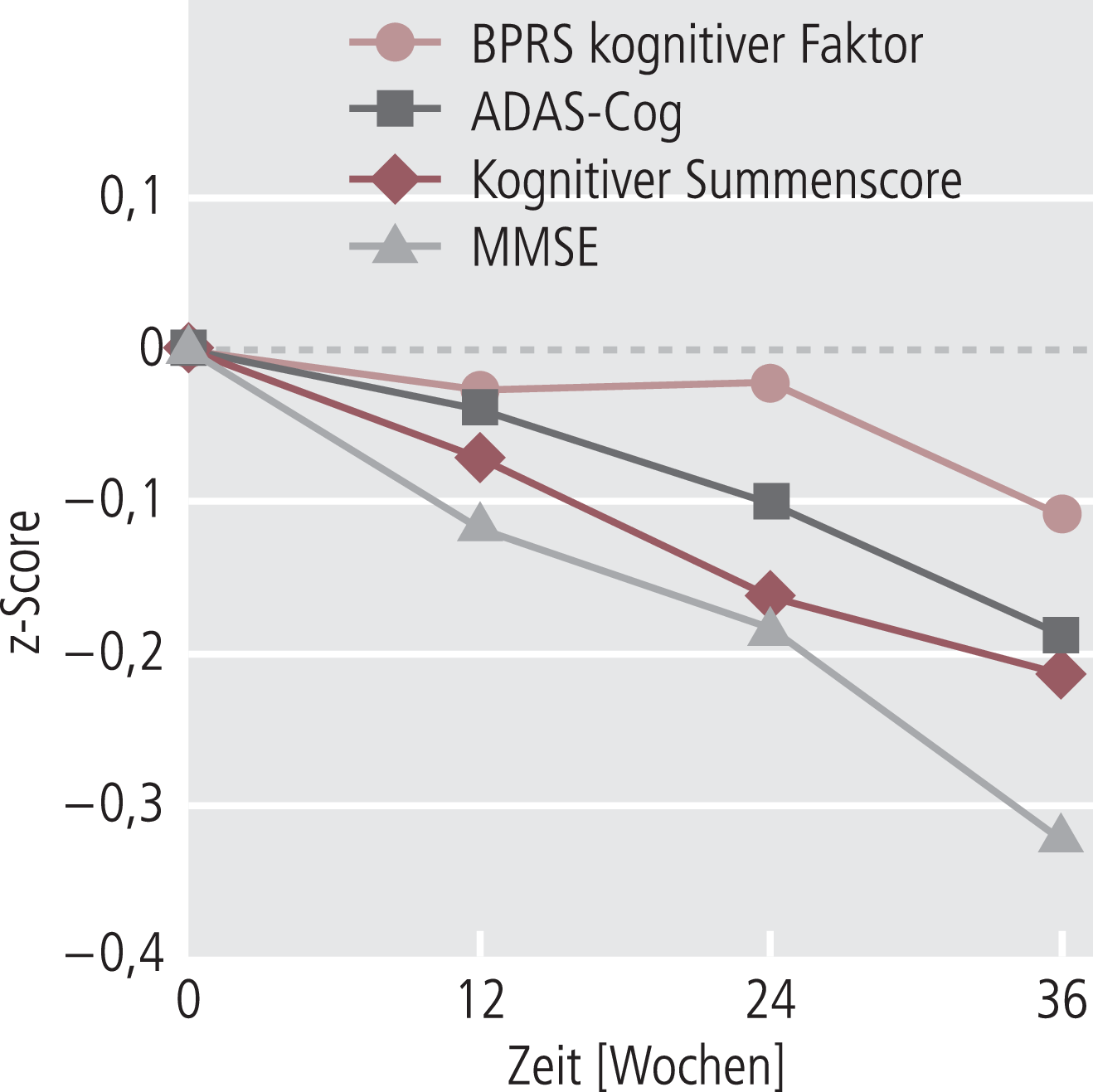
Abb. 1. Der mittlere kognitive Summenscore and die z-Scores kognitiver Tests für die gesamte Studienpopulation
MMSE = Mini-Mental State Examination; ADASCog = Kognitive Subskala der Alzheimer’s Disease Assessment Scale; BPRS kognitiver Faktor = kognitiver Faktor der Brief Psychiatric Rating Scale. z-Score = angepasster Testscore: ein Abfall bedeutet auch für ADASCog und BPRS-Faktor nachlassende kognitive Funktion
Effekte atypischer Antipsychotika. Patienten, die wenigstens für 14 Tage mit einem atypischen Antipsychotikum behandelt wurden, hatten signifikant größere Abfallraten in den kognitiven Tests als Plazebo-Patienten. Dies zeigte sich unter anderen im MMSE (p=0,004), dem kognitiven Dysfunktionsfaktor der BPRS (p≤0,05) und dem kognitiven Summenscore (p=0,004). Der Abfall im MMSE-Score war um 2,46 Punkte höher als unter Plazebo, ein nicht nur statistisch signifikanter, sondern auch klinisch relevanter Unterschied. Bei allen kognitiven Messungen schnitten die Patienten unter atypischen Antipsychotika schlechter ab als mit Plazebo behandelte Patienten, obwohl die Unterschiede nicht alle statistisch signifikant waren. Statistisch signifikante Unterschiede zwischen den Effekten der verschiedenen Substanzen und der einzelnen Substanzen im Vergleich zu Plazebo ließen sich aufgrund der geringen Gruppenstärken nicht zeigen. Die Autoren weisen darauf hin, dass die Größenordnung des Effekts der atypischen Antipsychotika durchaus mit der des Effekts einer Behandlung mit einem Cholinesterasehemmer vergleichbar ist – nur gehen die Effekte in die negative Richtung.
Kommentar
Das wichtigste Resultat dieser Studie, die Abnahme der kognitiven Funktion unter einer Behandlung mit atypischen Antipsychotika, wird durch die Ergebnisse vorheriger Studien gestützt und erscheint ausreichend gesichert. Der behandelnde Arzt würde nun vermutlich gerne erfahren, ob die Antipsychotika die Progression der Erkrankung erhöhen oder ob die beobachtete kognitive Verschlechterung eine Folge unerwünschter Wirkungen dieser Substanzen ist, beispielsweise Sedierung oder Lethargie, die nach dem Absetzen wieder verschwinden. In diesem Zusammenhang würde sich auch die Frage stellen, ob die Verschlechterungen im Verlauf der Behandlung ständig zunehmen oder nach einiger Zeit zum Stillstand kommen. Diese Fragen beantwortet die Studie nicht. Auf die Frage, ob man atypische Antipsychotika überhaupt bei Alzheimer-Patienten einsetzen sollte, meinen die Autoren, dass in einzelnen Fällen bei schweren Störungen eine Behandlung mit diesen Substanzen erforderlich sein kann.
Quelle
Vigen CLP, et al. Cognitive effects of atypical antipsychotic medications in patients with Alzheimer’s disease: Outcomes from CATIE-AD. Am J Psychiatry 2011;168:831–9.
Psychopharmakotherapie 2012; 19(02)
