Priv.-Doz. Dr. Dieter Angersbach, Wolfratshausen
In epidemiologischen Untersuchungen lag die Häufigkeit depressiver Erkrankungen bei Kindern und Jugendlichen zwischen 2 und 8%. Bei etwa 50 bis 75% der Betroffenen treten wiederholt Episoden auf.
Ziel der vorliegenden Studie war die Untersuchung der Wirksamkeit von Fluoxetin im Vergleich zu Plazebo in der Verhinderung von Rückfällen nach einer erfolgreichen Akutbehandlung. Eingeschlossen wurden ambulante Patienten im Alter zwischen 7 und 18 Jahren, bei denen wenigstens vier Wochen vor Screening eine Major Depression diagnostiziert worden war. Weitere Aufnahmekriterien waren unter anderen ein Score von ≥40 auf der Children’s Depression Rating Scale, revidierte Fassung (CDRS-R) und ein Score von ≥4 auf der Clinical Global Impression Scale, Teil: Schweregrad der Erkrankung (CGI-S).
Ausgeschlossen blieben unter anderen Patienten mit einer psychotischen Erkrankung (akut und jemals zuvor), mit einer bipolaren Erkrankung, einer Essstörung, mit Substanz- und Alkoholmissbrauch oder mit einer ernsthaften körperlichen Erkrankung.
Insgesamt wurden 331 Patienten gescreened. Von ihnen wurden 168 in die offene Akutbehandlung eingeschlossen. Davon wiederum eigneten sich 102 Patienten (Fluoxetin: n=50; Plazebo: n=52) für die Aufnahme in die doppelblinde Fortführungsstudie. Geeignet waren remittierte Patienten (CGI-S-Score 1 oder 2 und CDRS-R-Score ≤28) und Patienten, die eine adäquate klinische Response gezeigt hatten (CGI-S-Score 1 oder 2 und Verringerung des CDRS-Scores um ≥50%).
In der offenen Phase erhielten die Patienten in der ersten Woche 10 mg/d Fluoxetin. Danach wurde die Dosis auf 20 mg/d gesteigert. Nach der 6. Behandlungswoche konnte die Dosis auf 30 bis 40 mg/d erhöht werden. Bei Unverträglichkeit konnte die Dosis auf 10 mg/d gesenkt werden. In der doppelblinden Phase erhielten die Fluoxetin-Patienten weiterhin die Dosis, die sie in der offenen Phase eingenommen hatten.
Primäre Wirksamkeitsparameter waren Rückfall und die Zeit bis zum Rückfall. Zwei Schweregrade von Rückfällen wurde ausgewertet:
● Rückfall definiert als einmaliger Anstieg des CDRS-R-Scores auf ≥40 mit einer Verschlechterung depressiver Symptome über wenigsten zwei Wochen
● Kompletter Rückfall definiert als dauerhafter Anstieg des CDRS-R-Scores auf ≥40.
Von den 102 in die Fortführungsphase aufgenommenen Patienten waren 57 Kinder (7–11 Jahre) und 45 Jugendliche (12–18 Jahre). Nahezu drei Viertel der Patienten (74%) waren neu erkrankt, hatten also die erste Episode.
Die mittlere Fluoxetin-Dosis lag bei 26,2 mg/d und war bei den Jugendlichen höher (29,8 mg/d) als bei den Kindern (23,3 mg/d). Alle Teilnehmer nahmen wenigsten 20 mg/d ein. Nur bei einem Kind musste die Dosis wegen ansteigender Hyperaktivität von 20 mg auf 10 mg/d gesenkt werden.
Ergebnisse
Ein Rückfall kam unter Plazebo (69,2% der Patienten) signifikant häufiger vor als unter Fluoxetin (42%). Ebenso deutlich waren die Unterschiede in der Zeit bis zum Rückfall. In der Plazebo-Gruppe war die mediane Zeit von Beginn der Fortführungsphase (Absetzen von Fluoxetin) bis zum Eintreten eines Rückfalls acht Wochen. Für die Fluoxetin-Gruppe konnte die mediane Zeit nicht berechnet werden, da sie innerhalb des Studienzeitraums nicht erreicht wurde.
Abbildung 1 zeigt die Kaplan-Meier-Kurven für Überleben ohne kompletten Rückfall. Auch nach diesem Kriterium war Fluoxetin der Plazebo-Behandlung signifikant überlegen.
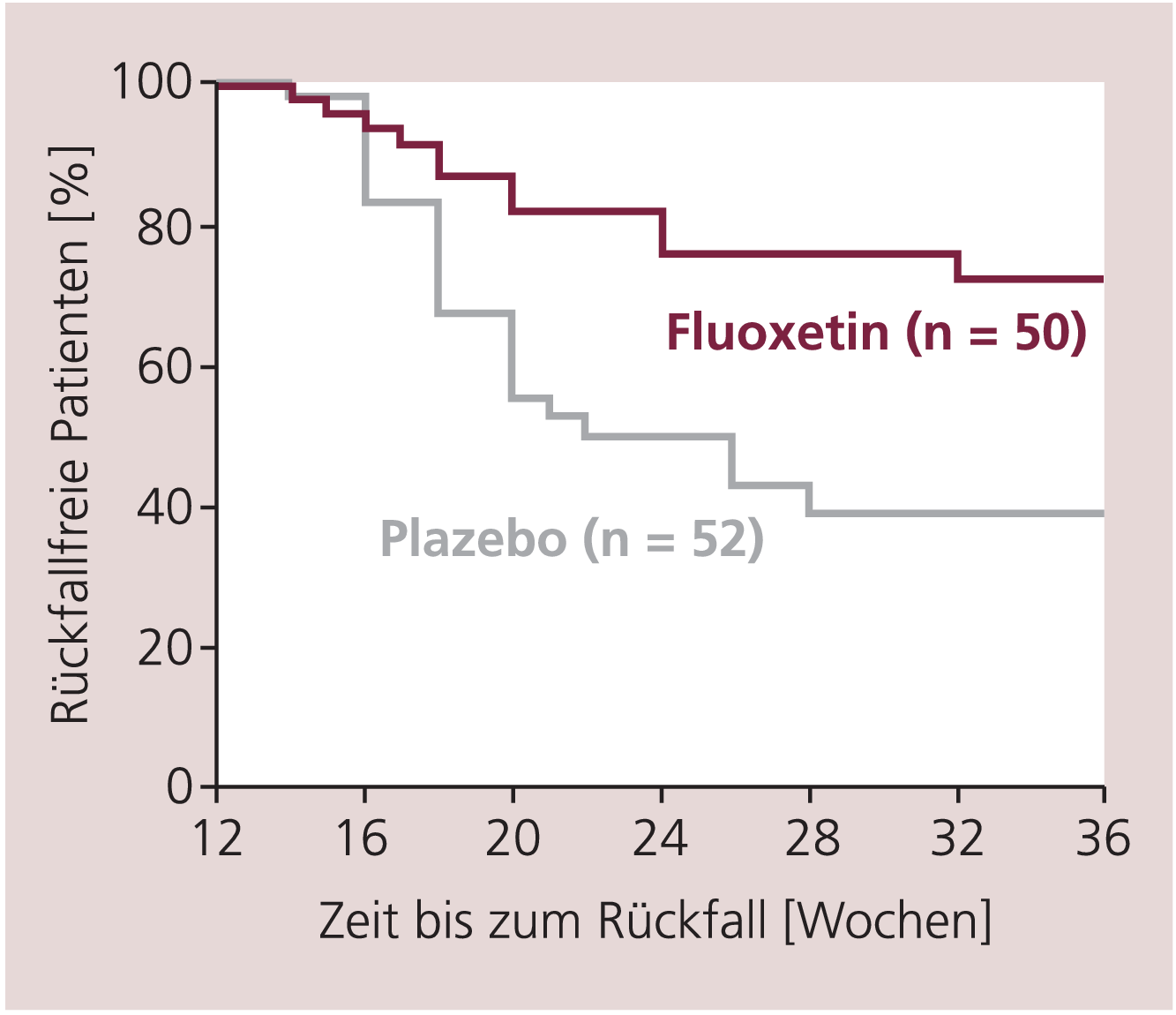
Abb. 1. Die Kaplan-Meier-Überlebenskurven zeigen die Zeit bis zum kompletten Rückfall bei Kindern und Jugendlichen, die nach einer Response in der Akutbehandlung mit Fluoxetin in der Fortführungsbehandlung Fluoxetin oder Plazebo erhalten haben
Am Ende der Akutbehandlung berichteten 52,9% der Patienten über wenigstens ein Residualsymptom. In der Fortführungsphase erlitten signifikant mehr Patienten mit einem Residualsymptom einen Rückfall (46,3%) als Patienten, die ohne Residualsymptome in diese Phase eingetreten waren (22,9%).
Über die Verträglichkeit der Behandlung berichten die Autoren nicht ausführlich. In der offenen Phase brachen 8 (von 168) Patienten die Behandlung wegen unerwünschter Wirkungen ab. In der Fortführungsstudie war die Häufigkeit unerwünschter Wirkungen in beiden Gruppen ähnlich.
Zusammenfassend zeigt die Studie die Überlegenheit von Fluoxetin gegenüber Plazebo in der Rückfallprävention. Ebenso wie bei erwachsenen Patienten sollte die Behandlung nach Remission/klinisch relevanter Response für wenigsten sechs Monate fortgeführt werden, und dies auch bei Patienten mit der ersten depressiven Episode.
Kommentar
Die Bedeutung dieser Studie liegt unter anderem darin, dass sie die ersten Daten zur Wirksamkeit und zum Nutzen einer Fortführungstherapie bei Kindern und Jugendlichen vorstellt. Sie zeigt, dass das zur Akuttherapie zugelassene Antidepressivum Fluoxetin auch in der Rückfallprävention wirksam ist, und gibt Auskunft, bei welcher Dosierung diese Wirksamkeit zu erwarten ist.
Weiterhin macht die Studie auf das Rückfallrisiko bei Residualsymptomen auch bei Kindern und Jugendlichen aufmerksam, ein Risiko das bereits vielfach bei erwachsenen Patienten beschrieben worden ist.
Quelle
Emslie GJ, et al. Fluoxetin versus placebo in preventing relapse of major depression in children and adolescents. Am J Psychiatry 2008;165: 459–67.
Psychopharmakotherapie 2008; 15(04)
