Patrik Stephan und Eveline Jaquenoud Sirot, Brugg (Schweiz)
Fallbericht
Unerwünschte Arzneimittelwirkungen (UAW) werden an unserer Klinik gemäß den Richtlinien der internationalen Arbeitsgemeinschaft für Arzneimittelsicherheit in der Psychiatrie (AMSP, [4]) durch speziell geschultes ärztliches Personal erfasst und dokumentiert. Mit der klinikinternen UAW-Meldung ist eine morgendliche Blutentnahme verbunden, womit Talspiegel der involvierten Pharmaka bestimmt werden können. Bei Polypharmazie erfolgt ein Interaktions-Check mit Hilfe eines Interaktionsprogramms [7].
Die 42-jährige, adipöse (162 cm, 77 kg, BMI 29,3 kg/m2) Patientin mit bekannter Dysthymie (ICD-10 F34.1) bei akzentuierter Persönlichkeit (unreif, selbstunsicher) musste wegen Suizidäußerungen im Rahmen einer depressiven Episode stationär aufgenommen werden (Tag 0). Die seit Monaten etablierte antidepressive Therapie mit einem selektiven Serotonin-Wiederaufnahmehemmer wurde wegen unbefriedigender Wirkung abgesetzt (Tag 3) und auf die Kombination von Venlafaxin (75 mg/d ab Tag 7) mit Mirtazapin (15 mg/d ab Tag 6) umgestellt, die vorbestehende Komedikation (Valproinsäure 1 000 mg/d) weiter gegeben. Anlässlich der Aufnahme durchgeführte Laboruntersuchungen ergaben Normwerte für Creatinin, Leberwerte und Thyreotropin (TSH).
Bei anamnestisch bekannter Polyallergie (Nickel, Kobalt, Parabene) kam es im Verlauf, nachdem sich die depressive Symptomatik unter der erwähnten Therapie gebessert hatte, zu ekzematösen Hautveränderungen im Gesicht, weswegen eine UAW-Meldung ausgelöst (Tag 17) und Blut zur Bestimmung von Talspiegeln der involvierten Pharmaka entnommen wurde (Tab. 1). Das Gesichtsekzem wurde in der Folge vorübergehend (und erfolgreich) mit einem topischen Glucocorticoid behandelt, ohne dass ein Zusammenhang mit der Medikation im Sinne einer UAW postuliert wurde. Pharmakotherapeutisch erfolgte, bei „leicht erhöhtem Venlafaxin-Spiegel und gebessertem Zustandsbild“, eine Reduktion der Tagesdosis von 75 mg/d auf 37,5 mg/d (Tag 27), womit die Patientin – ohne Veränderung der Komedikation – wenig später entlassen werden konnte (Tag 31). Zehn Wochen später musste sie jedoch erneut in mittelschwer depressivem Zustand hospitalisiert werden.
Tab. 1. Blutspiegel Tag 17
|
Substanz |
Dosierung |
Blutspiegel |
Zielbereich [1] |
|
|
Venlafaxin |
75 mg/d |
Venlafaxin (VEN) |
438 ng/ml |
|
|
O-Desmethylvenlafaxin (ODV) |
50 ng/ml |
|||
|
Summe (VEN+ODV) |
488 ng/ml |
195–400 ng/ml |
||
|
Metabolischer Quotient (ODV/VEN) |
0,1 |
|||
|
Mirtazapin |
15 mg/d |
Mirtazapin |
42 ng/ml |
40–80 ng/ml |
|
Valproinsäure |
1000 mg/d |
Valproinsäure |
97 µg/ml |
50–100 µg/ml |
Diskussion
Die Demethylierung von Venlafaxin (VEN) zu seinem aktiven Metaboliten O-Desmethylvenlafaxin (ODV) erfolgt hauptsächlich durch Cytochrom P450 (CYP) 2D6 [3, 8]. CYP3A katalysiert die Metabolisierung von Venlafaxin zu N-Desmethylvenlafaxin (NDV), der Einfluss der CYP3A-Aktivität auf den Venlafaxin-Blutspiegel ist aber vergleichsweise gering [5]. Hingegen konnte wiederholt eine deutliche Abhängigkeit des Venlafaxin-Blutspiegels und des metabolischen Quotienten (metabolic ratio) ODV/VEN vom CYP2D6-Genotyp beziehungsweise der Aktivität dieses Enzyms nachgewiesen werden. In einer neueren Arbeit war beispielsweise ein Quotient ODV/VEN <0,3 ausnahmslos mit dem „poor-metaboliser“ Genotyp (inaktivierende Mutation beider Allele) assoziiert und umgekehrt fanden sich bei einem Quotienten >5,2 immer Gen-Duplikationen („ultrarapid metaboliser“) [10].
Die in Tabelle 1 dargestellten Resultate sind auffällig: Erstens erstaunt der dosiskorreliert relativ hohe Summenspiegel und zweitens besteht ein sehr niedriger Quotient ODV/VEN von 0,1. (Zum Vergleich: In einem größeren, heterogenen Kollektiv fanden sich mittlere Werte zwischen 1,4 und 1,8 [9].) Das Verhältnis von Muttersubstanz (VEN) zum Metaboliten (ODV) ist also stark zu Gunsten der Muttersubstanz verschoben. Mögliche Erklärungen dieses Befunds sind:
1. Heimlicher Beikonsum von Venlafaxin in den Tagen vor der Blutentnahme (überproportionaler Anstieg der Muttersubstanz vor Erreichen des Steady State),
2. eine pharmakokinetische Interaktion (Hemmung) und
3. eine genetisch bedingte Defizienz der Metabolisierung.
In Bezug auf die medikamentöse Compliance fanden sich retrospektiv keine Hinweise für Unregelmäßigkeiten. Die zum Zeitpunkt der Blutentnahme (Tag 17) bestehende Komedikation (Mirtazapin, Valproinsäure) hat keinen relevanten Einfluss auf die CYP2D6-Aktivität [7].
Eine genetisch bedingte Defizienz von CYP2D6 wurde bei der beschriebenen Patientin bereits früher ausgeschlossen (Genotyp CYP2D6 *1/*1 = Wildtyp, untersuchte Allele *3, *4, *6, *XN).
Schlussendlich findet sich die Erklärung im eingangs erwähnten Serotonin-Wiederaufnahmehemmer. Dabei handelte es sich um Fluoxetin (Tagesdosis 40 mg), eine Substanz mit langer Halbwertszeit (4–6 Tage), einem aktiven Metaboliten (Norfluoxetin) mit noch längerer Halbwertszeit (4–16 Tage) und starker Inhibition von CYP2D6. Retrospektiv konnten die Blutspiegel von Fluoxetin und Norfluoxetin zum Zeitpunkt der Bestimmung von Venlafaxin (Tag 17) aus tiefgefrorenem Restserum noch bestimmt werden, wobei – 14 Tage nach Absetzen – immer noch therapeutische Spiegel (Fluoxetin 136 ng/ml, Norfluoxetin 136 ng/ml, empfohlener Zielbereich für Summenspiegel 120–300 ng/ml [1]) vorlagen. In diesem Zusammenhang sei erwähnt, dass wiederholt über einen Anstieg der Eliminationshalbwertszeiten von Fluoxetin und Norfluoxetin bei chronischer Gabe berichtet wurde [2], wobei die in unserem Fallbeispiel gefundenen Werte trotzdem noch vergleichsweise hoch imponieren. Mögliche Erklärungen für diesen Befund wären inhibierende Effekte von Valproinsäure (CYP2C9, CYP3A) und/oder eine genetisch bedingte Defizienz von CYP2C9 und/oder CYP2C19 [6], welche beide relevant zur Metabolisierung von Fluoxetin beitragen. Eine entsprechende Genotypisierung wurde jedoch nicht durchgeführt.
Nach der erwähnten stationären Wiederaufnahme wurde die Patientin weiterhin mit Venlafaxin (ohne Mirtazapin) behandelt, eine Blutspiegelbestimmung unter 150 mg/d (Komedikation Valproinsäure 1 000 mg/d) zeigte dann auch einen dosiskorreliert unauffälligen Summenspiegel und einen deutlich höheren Quotienten ODV/VEN von 1,9 (Abb. 1).
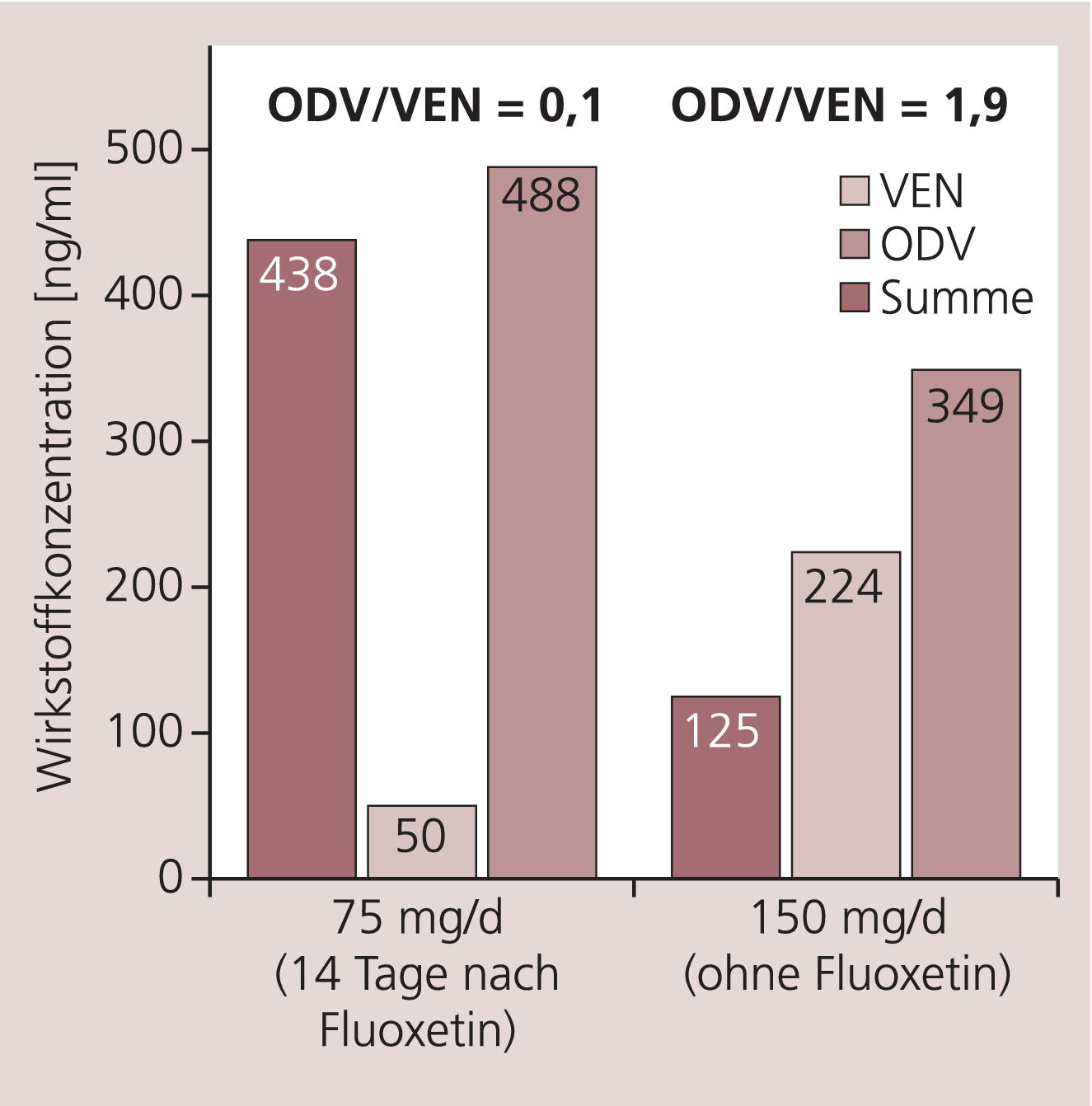
Abb. 1. Vergleich metabolischer Quotient ODV/VEN
Die Interpretation der Blutspiegel von VEN und ODV („leicht erhöht“) führte im beschriebenen Fall, in Unkenntnis des persistierenden Einflusses von Fluoxetin, zu einer Dosisreduktion auf nur 37,5 mg/d. Es ist anzunehmen, dass es im weiteren Verlauf, mit abnehmender Inhibition durch Fluoxetin, zu einem Abfall der Blutspiegel von VEN und ODV in den subtherapeutischen Bereich gekommen ist, was wahrscheinlich den klinischen Verlauf ungünstig beeinflusst hat.
Bei der Beurteilung eines Medikamentenspiegels sollte immer die Frage beantwortet werden, ob der gefundene Wert dosiskorreliert adäquat ist. Werden aktive Metaboliten mitbestimmt, können aus dem Verhältnis von Metabolit zu Muttersubstanz häufig wichtige Zusatzinformationen über die Aktivität involvierter Cytochrome gewonnen werden. Als weitere Beispiele seien hier Clozapin (CYP1A2), Risperidon (CYP2D6) und Amitriptylin (CYP2C19) genannt [11]. Beim Interaktions-Check muss die Medikamenten-Anamnese mit eingeschlossen und speziell Fluoxetin aufgrund seiner pharmakokinetischen Besonderheiten aktiv gesucht werden. Schließlich empfiehlt sich bei Unsicherheiten in der Interpretation die Rücksprache mit dem Laboratorium oder einem Kompetenz-Zentrum mit entsprechender Erfahrung. Neuerdings existiert auch eine entsprechende Online-Beratung [7].
Literatur
1. Baumann P, Hiemke C, Ulrich S, Eckermann G, et al. The AGNP-TDM expert group consensus guidelines: therapeutic drug monitoring in psychiatry. Pharmacopsychiatry 2004;37:243–65.
2. Brunswick DJ, Amsterdam JD, Fawcett J, Quitkin FD, et al. Fluoxetine and norfluoxetine plasma levels after discontinuing fluoxetine therapy. J Clin Psychopharmacol 2001;21:616–8.
3. Fogelman SM, Schmider J, Venkatakrishnan K, von Moltke LL, et al. O- and N-demethylation of venlafaxine in vitro by human liver microsomes from cDNA-transfected cells: effect of metabolic inhibitors and SSRI antidepressants. Neuropsychopharmacology 1999;20:480–90.
4. Grohmann R, Engel RR, Ruther E, Hippius H. The AMSP drug safety program: methods and global results. Pharmacopsychiatry 2004;37(Suppl 1):S4–11.
5. Lindh JD, Annas A, Meurling L, Dahl ML, et al. Effect of ketaconazole on venlafaxine plasma concentrations in extensive and poor metabolisers of debrisoquine. Eur J Clin Pharmacol 2003;59:401–6.
6. Liu ZQ, Cheng ZN, Huang SL, Chen XP, et al. Effect of the CYP2C19 oxidation polymorphism on fluoxetine metabolism in Chinese healthy subjects. Br J Clin Pharmacol 2001;52:96–9.
7. MediQ-Website. MediQ-Interaktionsprogramm: www.mediQ.ch (Stand 01.03.08).
8. Otton SV, Ball SE, Cheung SW, Inaba T, et al. Venlafaxine oxidation in vitro is catalysed by CYP2D6. Br J Clin Pharmacol 1996;41:149–56.
9. Reis M, Lundmark J, Björk H, Bengtsson F. Therapeutic drug monitoring of racemic venlafaxine and its main metabolites in an everyday clinical setting. Ther Drug Monit 2002;24:545–53.
10. Shams M, Arneth B, Hiemke C, Dragicevic A, et al. CYP2D6 polymorphism and clinical effect of the antidepressant venlafaxine. J Clin Pharm Ther 2006;31:493–502.
11. Van der Weide J, van Baalen-Benedek EH, Koostra-Ros JE. Metabolic ratios of psychotropics as indication of cytochrome P450-2D6/2C19 genotype. Ther Drug Monit 2005;27:478–83.
Dr. med. Patrik Stephan, Eveline Jaquenoud Sirot, MSc, Psychiatrische Dienste Aargau AG, Klinik Königsfelden, Postfach 432, 5201 Brugg (Schweiz), E-Mail: patrik.stephan@pdag.ch
Misinterpretation of a venlafaxine blood level
Blood levels of venlafaxine (V) and its active metabolite O-desmethylvenlafaxine (ODV) were measured because of an adverse event. The results showed an unusual high concentration/dose and a very low metabolic ratio ODV/V which lead to a suboptimal dose correction and probably to a depression relapse.
Keywords: Interaction, venlafaxine, fluoxetine
Psychopharmakotherapie 2008; 15(03)
