Branka Knezevic, Patrik L. Stephan, Brugg (Schweiz), Renate Grohmann, München, Detlef Degner, Wolfgang Jordan, Göttingen, und Eveline Jaquenoud Sirot, Brugg (Schweiz)
Unbestrittenermaßen handelt es sich beim metabolischen Syndrom – nicht nur bei psychiatrischen Patienten – um eine Krankheit mit weltweit zunehmender Inzidenz bei relevanter Morbidität und Mortalität [4]. Zur Diagnose wurden im April 2005 von der International Diabetes Federation (IDF) neue Konsensus-Kriterien publiziert (Tab. 1, www.idf.org). Ätiologisch finden sich primär Zusammenhänge mit Qualität und Quantität der Nahrung sowie Bewegungsmangel, wobei in Zwillingsstudien auch Hinweise auf genetische Komponenten identifiziert werden konnten [13]. Die Gewichtszunahme und assoziierte metabolische Störungen sind aber auch eine bekannte unerwünschte Arzneimittelwirkung vieler atypischer und einiger typischer Antipsychotika [2, 14]. Unmedizierte Patienten mit Erstpsychose scheinen sich in Bezug auf Gewicht, Body-Mass-Index (BMI) und Fettverteilung von gesunden Probanden nicht zu unterscheiden [17]. Untersuchungen zum Glucosestoffwechsel zeigten bisher divergierende Resultate [1, 15].
Tab. 1. IDF-Konsensus-Kriterien des metabolischen Syndroms
|
Zentrale Adipositas (Bauchumfang auf Nabelhöhe in Exspiration): |
|
Männer ≥94 cm, Frauen ≥80 cm („Europid“) |
|
Plus mindestens zwei der vier folgenden Kriterien: |
|
Erhöhte Triglyceride: ≥150 mg/dl (1,7 mmol/l), |
|
Vermindertes HDL-Cholesterol: |
|
Erhöhter arterieller Blutdruck: |
|
Erhöhte Nüchternglucose: |
Im AMSP-Projekt wurden in den Jahren 2001 bis 2003 bei 67 von insgesamt 43511 mit Psychopharmaka behandelten Patienten ausgeprägte Gewichtszunahmen (Zunahme des Ausgangsgewichts um ≥10% und BMI >25) dokumentiert. Bei 31 Patienten fand sich eine Gewichtszunahme von über 20% ihres Ausgangsgewichts. Die am häufigsten angeschuldigten Substanzen waren Olanzapin, Risperidon und Mirtazapin. Die Inzidenz für Olanzapin war 0,54%, für Risperidon 0,17%. Erstaunlicherweise wurde nur über zwei Fälle unter Clozapin-Therapie berichtet. Hyperglykämien wurden im AMSP-Projekt im Zeitraum von 1993 bis 2000 bei 86 348 mit Antipsychotika behandelten Patienten mit einer Inzidenz von 0,01% lediglich unter Olanzapin und Clozapin gefunden [10]. In acht der neun Fälle wurde die Monotherapie mit Olanzapin oder Clozapin angeschuldigt; in sechs Fällen war der Anstieg der Nüchternglucose mit einer Gewichtszunahme verbunden. Das mittlere Lebensalter dieser Patienten lag bei 47,7 Jahren, es waren fünf Männer und vier Frauen betroffen. Drei weitere Fälle kamen in den Jahren 2001 bis 2003 hinzu. Insgesamt fanden sich sieben Neumanifestationen und fünf Verschlechterungen eines vorbestehend stabilen Diabetes mellitus.
Kasuistiken
Fall A: Metabolisches Syndrom unter Therapie mit Olanzapin
Bei diesem 1971 geborenen Patienten wurde 1999 eine paranoide Schizophrenie diagnostiziert. Damals – vor Beginn der antipsychotischen Behandlung – war der Patient bereits übergewichtig (BMI 29 kg/m2), Glucose und Lipidstatus aber unauffällig. Die Familienanamnese bezüglich Adipositas war negativ, der (früh verstorbene) Vater habe aber an Diabetes mellitus Typ 2 gelitten. Im Verlauf wurde der Patient ab 2002 mit Zuclopenthixol-Depot behandelt, worunter er Mitte 2004 Spätdyskinesien entwickelte. Während dieser Behandlungsperiode blieb das Körpergewicht mit 93 bis 98 kg stabil, wobei die Nüchternglucose phasenweise leicht erhöht (maximal 6,8 mmol/l) gemessen wurde (Lipide nicht kontrolliert).
Nach dem Wechsel der antipsychotischen Therapie auf Olanzapin 10 mg/Tag wurde – bei unveränderter Komedikation (Diazepam, Biperiden) – innerhalb von 10 Monaten ein kontinuierlicher Gewichtsanstieg von 97 kg auf maximal 114,5 kg (BMI 35,3 kg/m2) festgestellt (max. Bauchumfang 121 cm). Dabei stiegen die Triglyceride auf 8,8 mmol/l, die Nüchternglucose auf maximal 11 mmol/l, sank das HDL-Cholesterol auf 0,83 mmol/l und wurden neu hypertensive Blutdruckwerte gemessen. Zusätzlich fanden sich transient erhöhte Leberwerte im Sinne einer nicht-alkoholischen Fettleber, eine Cholezystolithiasis konnte ausgeschlossen werden.
Maßnahmen. Der Patient musste antihypertensiv (Lisinopril), hinsichtlich Hypertriglyzeridämie (Pravastatin, Bezafibrat) und schließlich auch wegen manifestem Diabetes mellitus (Metformin) medikamentös behandelt werden (Abb. 1). Begleitend erfolgte eine Diätberatung und es wurde versucht, den Patienten zu vermehrter körperlicher Aktivität zu motivieren. Die Olanzapin-Tabletten wurden durch Schmelztabletten ersetzt [5], wobei die Dosis im Verlauf wegen beginnender Zeichen einer psychotischen Dekompensation auf 20 mg/Tag erhöht wurde. Der Patient konnte mit diesen Maßnahmen innerhalb von vier Monaten 6 kg abnehmen.
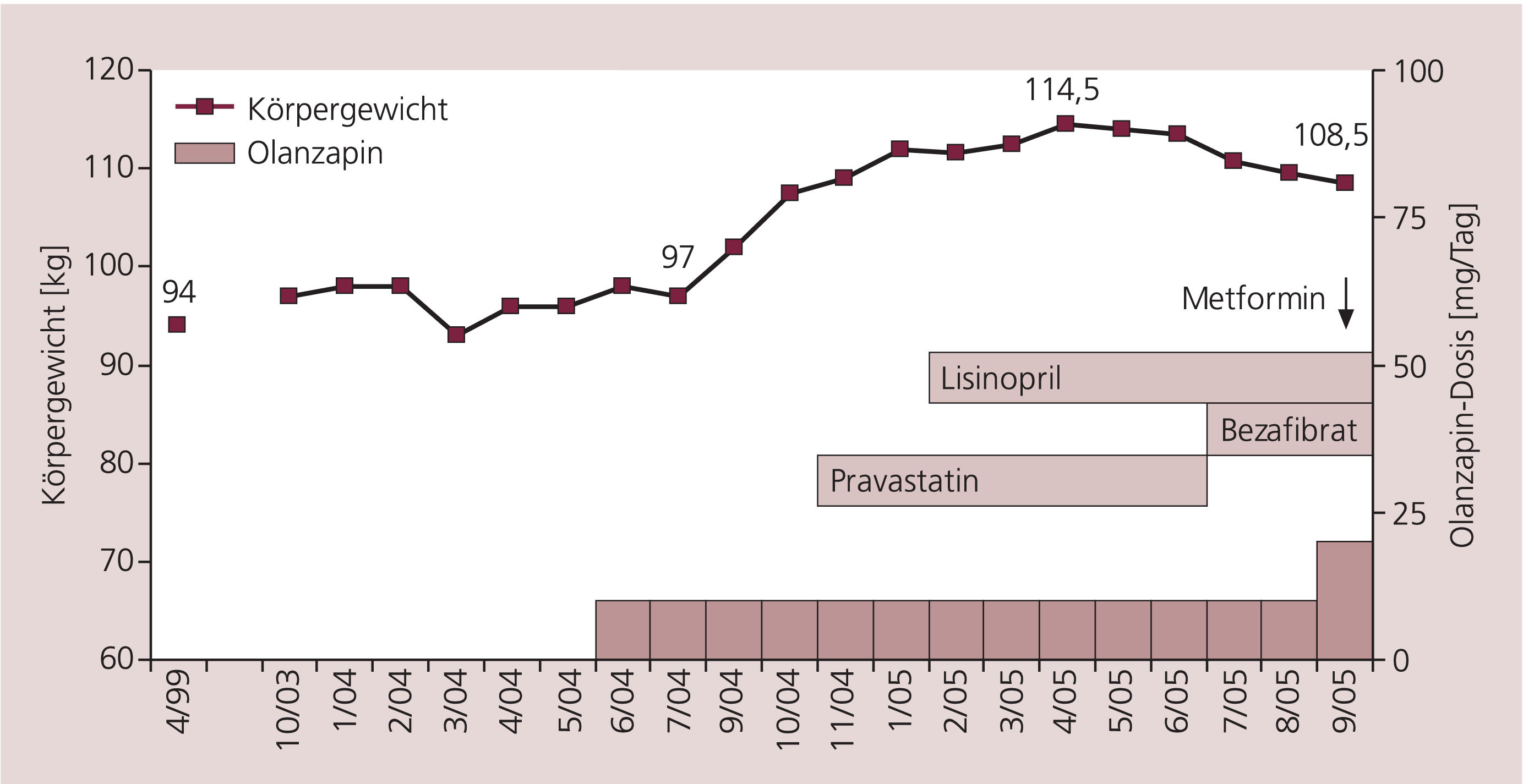
Abb. 1. Metabolisches Syndrom unter Therapie mit Olanzapin (Fall A)
Beurteilung. Bei einem vorbestehend adipösen Patienten mit einer erblichen Belastung in Bezug auf Diabetes mellitus entwickelte sich unter antipsychotischer Monotherapie mit Olanzapin innerhalb von zehn Monaten ein eindrückliches, therapiebedürftiges metabolisches Syndrom (Tab. 1). Bei favorabler Wirkung und fehlender Motivation des Patienten für einen Medikamentenwechsel wurde die Medikation mit Olanzapin beibehalten, aber auf Schmelztabletten gewechselt.
Fall B: Ausgeprägte Gewichtszunahme unter Therapie mit Clozapin
Diese heute 33-jährige Patientin mit chronisch paranoider Schizophrenie wurde seit 1997 vorwiegend mit Clozapin und seit 1999 bis zum aktuellen Zeitpunkt zusätzlich mit Valproinsäure behandelt, wobei 2003 ein vorübergehender (5-monatiger) Wechsel auf Risperidon erfolgte. Therapieversuche mit anderen Antipsychotika (Haloperidol, Zuclopenthixol, Promazin, Penfluridol, Quetiapin, Olanzapin) waren allesamt von kurzer Dauer (<4 Wochen).
Vor der Behandlung mit Clozapin und Valproinsäure betrug das Gewicht der Patientin 76 kg bei einer Größe von 1,80 m (BMI 23,5 kg/m2). Abgesehen von einer Gewichtsabnahme von 4 kg während der Behandlung mit Risperidon nahm die Patientin kontinuierlich zu bis zu einem Gewicht von 120 kg (BMI 37,5, Bauchumfang 132 cm), was einer Zunahme von 58% ihres ursprünglichen Körpergewichts entspricht. Im Verlauf wurden seit 2002 mehrfach hypertensive Blutdruckwerte (syst. max. 160 mmHg, diast. max. 100 mmHg) gemessen, ohne dass eine antihypertensive Therapie notwendig wurde. Auch wurden erhöhte Werte der Triglyceride (max. 2,1 mmol/l) und erniedrigte Werte des HDL-Cholesterols (min. 1,2 mmol/l) registriert bei grenzwertiger Nüchternglucose (4,9–6 mmol/l), womit die Kriterien für ein metabolisches Syndrom erfüllt waren (Tab. 1). Dabei fühlte sich die Patientin in ihrer Lebensqualität zunehmend beeinträchtigt (Mühe beim Gehen, Harninkontinenz).
Maßnahmen. Einzig die vorübergehende Umstellung auf Risperidon führte bisher zu einer Gewichtsreduktion, hatte aber psychopathologisch eine Destabilisierung zur Folge. Allenfalls wäre eine Kombinationstherapie mit Fluvoxamin oder Aripiprazol in Betracht zu ziehen.
Beurteilung. Sowohl Clozapin als auch Valproinsäure können prinzipiell eine Gewichtszunahme verursachen. Der kausale Zusammenhang mit Clozapin ist als sicher zu betrachten, nicht zuletzt wegen einer positiven Reexposition nach dem Wechsel auf Risperidon. Im Rahmen der AMSP-Erfassung wurde zudem Valproinsäure als wahrscheinliche Ursache mit angeschuldigt.
Fall C: Annähernde Verdoppelung des Gewichts unter Therapie mit Clozapin
Ein 1972 geborener Patient mit chronisch paranoider Schizophrenie wurde seit 1989 vorwiegend mit Clozapin, vorübergehend (2002–2004) zusätzlich mit Levomepromazin behandelt. Vor dem Therapiebeginn wog der Patient 67 kg bei einer Größe von 1,84 m (BMI 19,7 kg/m2). In knapp vier Jahren nahm er 25 kg an Gewicht zu und wog 1992 92 kg (BMI 27 kg/m2). Im Verlauf zeigte er bis 2004 eine weitere Gewichtszunahme auf maximal 128 kg (BMI 37,8 kg/m2). Zu diesem Zeitpunkt waren die Blutdruckwerte (syst. max. 153 mmHg, diast. max. 92 mmHg) leicht erhöht, das HDL-Cholesterol (0,9 mmol/l) erniedrigt bei grenzwertigen Triglyceriden (1,7 mmol/l) und Werten der Nüchternglucose um 5 mmol/l.
Maßnahmen. Initial wurde mit Topiramat bis 200 mg/Tag während knapp vier Monaten, dann mit Amisulprid 400 bis 600 mg während drei Monaten kombiniert, was eine kontinuierliche Gewichtsabnahme auf 112 kg bewirkte. Wegen unbefriedigendem Therapieverlauf erfolgte die Umstellung auf die Kombination Clozapin/Fluvoxamin, worunter der Patient weiter an Gewicht abnehmen konnte. Das aktuelle Gewicht beträgt 102 kg (BMI 30,1 kg/m2), der Bauchumfang 119 cm.
Beurteilung. Während einer 16-jährigen Therapie vorwiegend mit Clozapin kam es zu einer annähernden Verdoppelung des Gewichts mit Entwicklung eines metabolischen Syndroms. Verschiedene medikamentöse Strategien kombiniert mit nicht-medikamentösen Maßnahmen führten bei diesem Patienten zu einer markanten Gewichtsreduktion mit Verbesserung der metabolischen Parameter.
Diskussion
Anhand der dargestellten Kasuistiken sollen nachfolgend ausgewählte psychopharmakotherapeutische Interventionen zur Gewichtsreduktion vorgestellt werden. Es handelt sich dabei um eine fallbezogene Selektion. In der Literatur sind zahlreiche weitere Optionen beschrieben: Zentral wirksam sind Sibutramin, Amantadin und Psychostimulanzien, peripher wirken Orlistat, Metformin und Nizatidin (Auswahl).
Topiramat. Bei psychiatrischen Patienten, die mit Topiramat komediziert wurden, konnte eine signifikante Abnahme des Körpergewichts dokumentiert werden [3, 8], dies vor allem bei einer Dosierung von mindestens 200 mg [9]. Topiramat wird auch als Augmentation bei Therapieresistenz unter Atypika diskutiert [16].
Kombination Clozapin und Fluvoxamin. In einer kontrollierten Studie [12] beeinträchtigte die Kombination Clozapin/Fluvoxamin Gewicht, BMI, Triglyceride und Glucose deutlich weniger als die Monotherapie mit Clozapin. Dieser Effekt scheint mit den Norclozapin-Serumspiegeln (5-HT2c-Antagonismus) zu korrelieren. Fluvoxamin führt als potenter Inhibitor von Cytochrom (CYP) 1A2 zu einem deutlichen Anstieg des Clozapin-Spiegels mit relativem Abfall von Norclozapin. Die Kombination muss vorsichtig eingestellt werden unter Kontrolle des Clozapin-Spiegels.
Kombination Clozapin und Aripiprazol. Die Kombination mit Aripiprazol führte in einer Pilotstudie und Einzelfallberichten zu einer signifikanten Abnahme von Körpergewicht, Gesamt-Cholesterol und Triglyceriden [7].
Olanzapin-Schmelztabletten. In einer Pilotstudie führte der Wechsel von herkömmlichen Tabletten auf Schmelztabletten zu einer signifikanten Abnahme von Gewicht und BMI. Als Erklärung wird eine verkürzte Kontaktzeit mit 5-HT-Rezeptor-Subtypen im Magen diskutiert [5].
Die Therapie des metabolischen Syndroms stellt bereits in der psychisch gesunden Normalbevölkerung ein großes Problem dar. Ursachen für dessen erhöhte Inzidenz bei an Schizophrenie Erkrankten sind Bewegungsmangel und Fehlernährung, möglicherweise genetische Faktoren und die Therapie mit Antipsychotika. Körperliche Inaktivität und Fehlernährung können – weit gefasst – auch als Symptome der Krankheit interpretiert werden. Bei deren Ausbruch fehlen, gerade beim jungen Patienten, häufig objektivierbare Zeichen einer Stoffwechselstörung, was dazu führt, dass diesbezügliche Überlegungen bei der Auswahl des Antipsychotikums nicht erfolgen. Im Wissen um erbliche Einflüsse empfiehlt sich hier eine systematische Erhebung der Familienanamnese in Bezug auf kardiovaskuläre Risikofaktoren und Folgekrankheiten (Adipositas, Diabetes mellitus, arterielle Hypertonie, Dyslipidämie, arterielle Verschlusskrankheit). Das Monitoring der Parameter des metabolischen Syndroms sollte erstmals vor Therapiebeginn erfolgen, nach einigen Wochen wiederholt und im Verlauf regelmäßig durchgeführt werden. Durch eine engmaschige Kontrolle des Körpergewichts kann eine entsprechende Zunahme frühzeitig erkannt und können erweiterte Diagnostik und Gegenmaßnahmen rechtzeitig eingeleitet werden [11].
Literatur
1. Arranz B, Rosel P, Ramirez N, Duenas R, et al. Insulin resistance and increased leptin concentrations in noncompliant schizophrenia patients but not in antipsychotic-naive first-episode schizophrenia patients. J Clin Psychiatry 2004;65:1335–42.
2. Baptista T, Kin NM, Beaulieu S, De Baptista EA. Obesity and related metabolic abnormalities during antipsychotic drug administration: Mechanisms, management and research perspectives. Pharmacopsychiatry 2002;35:205–19.
3. Chengappa KN, Chalasani L, Brar JS, Parepally H, et al. Changes in body weight and body mass index among psychiatric patients receiving lithium, valproate, or topiramate: an open-label, nonrandomized chart review. Clin Ther 2002;24:1576–84.
4. Chopra M, Darnton-Hill I. Tobacco and obesity epidemics: not so different after all? BMJ 2004;328:1558–60.
5. de Haan L, Van Amelsvoort T, Rosien K, Linszen D. Weight loss after switching from conventional olanzapine tablets to orally disintegrating olanzapine tablets. Psychopharmacology (Berl) 2004;175:389–90.
6. Fric M, Laux G, Artmann S, Bickmann E, et al. Atypische Antipsychotika und metabolisches Syndrom. Psychopharmakotherapie 2005;12:51–6.
7. Henderson DC, et al. An exploratory open label trial of aripiprazole as an adjuvant to clozapine therapy in chronic schizophrenia. Acta Psychiatr Scand 2005. Im Druck.
8. Kirov G, Tredget J. Add-on topiramate reduces weight in overweight patients with affective disorders: a clinical case series. BMC Psychiatry 2005;5:19.
9. Ko YH, Joe SH, Jung IK, Kim SH. Topiramate as an adjuvant treatment with atypical antipsychotics in schizophrenic patients experiencing weight gain. Clin Neuropharmacol 2005;28:169–75.
10. Kropp S, Grohmann R, Hauser U, Rüther E, et al. Hyperglycemia associated with antipsychotic treatment in a multicenter drug safety project. Pharmacopsychiatry 2004;37(Suppl 1):S79–83.
11. Lieberman JA. Metabolic changes associated with antipsychotic use. Prim Care Companion J Clin Psychiatry 2004;6:8–13.
12. Lu ML, Lane HY, Lin SK, Chen KP, et al. Adjunctive fluvoxamine inhibits clozapine-related weight gain and metabolic disturbances. J Clin Psychiatry 2004;65:766–71.
13. Maes HH, Neale MC, Eaves LJ. Genetic and environmental factors in relative body weight and human adiposity. Behav Genet 1997;27:325–51.
14. Newcomer JW. Second-generation (atypical) antipsychotics and metabolic effects: a comprehensive literature review. CNS Drugs 2005;19(Suppl 1):1–93.
15. Ryan MC, Collins P, Thakore JH. Impaired fasting glucose tolerance in first-episode, drug-naive patients with schizophrenia. Am J Psychiatry 2003;160:284–9.
16. Tiihonen J, Halonen P, Wahlbeck K, Repo-Tiihonen E, et al. Topiramate add-on in treatment-resistant schizophrenia: A randomized, double-blind, placebo-controlled, crossover trial. J Clin Psychiatry 2005;66:1012–5.
17. Zhang ZJ, Yao ZJ, Liu W, Fang Q, et al. Effects of antipsychotics on fat deposition and changes in leptin and insulin levels. Magnetic resonance imaging study of previously untreated people with schizophrenia. Br J Psychiatry 2004;184:58–62.
Eveline Jaquenoud Sirot, MSc, Branka Knezevic MD, Dr. med. Patrik L. Stephan, Psychiatrische Dienste Aargau AG, Postfach 298, 5201 Brugg, Schweiz, E-Mail: Eveline.JaquenoudSirot@ pdag.ch
Dr. Renate Grohmann, Klinik für Psychiatrie der Ludwig-Maximilians-Universität, Nussbaumstraße 7, 80336
München Dr. med. Detlef Degner, Dr. med. Wolfgang Jordan, Klinik für Psychiatrie und Psychotherapie der Georg-August-Universität, von-Siebold-Str. 5, 37075 Göttingen
Psychopharmakotherapie 2005; 12(06)
